文档内容
第二十二、二十三讲 化学能与电能
【基础巩固】
1.港珠澳大桥设计寿命为120年,对桥体钢制构件采用了多种防腐措施,下列防腐措施错误的是( )
A.用导线与石墨相连 B.用导线与电源负极相连
C.钢制构件上焊接锌块 D.表面喷涂分子涂层
【答案】 A
【解析】 A项,石墨、Fe和电解质溶液构成原电池,Fe作负极加速被腐蚀,错误;B项,将铁和电源负
极相连时Fe作阴极而被保护,正确;C项,为牺牲阳极法,正确;D项,为增加防护层,正确。
2.(2023·长治质量检测)一种水性电解液Zn-MnO 离子选择双隔膜电池如图所示[KOH溶液中,Zn2+以
2
Zn(OH)存在]。电池放电时,Ⅱ区的KSO 溶液浓度变大,下列叙述错误的是( )
2 4
A.电池放电时,转移2 mol e-正极质量减少32 g
B.Ⅰ区与Ⅱ区之间的离子交换膜为阴离子交换膜
C.Zn电极反应:Zn+4OH--2e-=Zn(OH)
D.Ⅲ区的K+通过隔膜向Ⅱ区迁移
【答案】 A
【解析】 Zn电极为负极,Zn失电子产物与电解质反应,生成Zn(OH),同时K+透过离子交换膜向Ⅱ区
移动;正极为MnO ,MnO 得电子产物与电解质反应,生成Mn2+等,同时SO透过离子交换膜向Ⅱ区移
2 2
动。A.电池放电时,正极反应为:MnO +4H++2e-=Mn2++2HO,转移2 mol e-,正极质量减轻87 g,A
2 2
错误;B.由分析可知,电极反应发生时,Ⅰ区SO透过离子交换膜向Ⅱ区移动,则Ⅰ区与Ⅱ区之间的离子
交换膜为阴离子交换膜,B正确;C.Zn电极,Zn失电子产物与电解质反应,生成Zn(OH),则电极反应式
为:Zn+4OH--2e-=Zn(OH),C正确;D.由分析可知,电极反应发生时,Ⅲ区的K+透过离子交换膜向Ⅱ
区迁移,D正确。
3.(2023·全国·统考高考真题)室温钠-硫电池被认为是一种成本低、比能量高的能源存储系统。一种室
温钠-硫电池的结构如图所示。将钠箔置于聚苯并咪唑膜上作为一个电极,表面喷涂有硫黄粉末的炭化纤维
资料整理【淘宝店铺:向阳百分百】素纸作为另一电极。工作时,在硫电极发生反应: S+e-→ S , S +e-→S ,2Na++ S +2(1- )e-
8
→NaS
2 x
下列叙述错误的是
A.充电时Na+从钠电极向硫电极迁移
B.放电时外电路电子流动的方向是a→b
C.放电时正极反应为:2Na++ S+2e-→NaS
8 2 x
D.炭化纤维素纸的作用是增强硫电极导电性能
【答案】 A
【解析】 由题意可知放电时硫电极得电子,硫电极为原电池正极,钠电极为原电池负极。A.充电时为
电解池装置,阳离子移向阴极,即钠电极,故充电时,Na+由硫电极迁移至钠电极,A错误;B.放电时Na
在a电极失去电子,失去的电子经外电路流向b电极,硫黄粉在b电极上得电子与a电极释放出的Na+结合
得到NaS,电子在外电路的流向为a→b,B正确;C.由题给的的一系列方程式相加可以得到放电时正极
2 x
的反应式为2Na++ S+2e-→NaS,C正确;D.炭化纤维素纸中含有大量的炭,炭具有良好的导电性,可
8 2 x
以增强硫电极的导电性能,D正确;故答案选A。
4.(2022·潍坊高三检测)某Al-MnO电池原理如图所示,电池总反应的离子方程式为Al+MnO===AlO+
MnO ,下列说法正确的是( )
2
A.电池工作时,K+向负极区移动
B.Al电极发生还原反应
C.正极的电极反应式为MnO+4H++3e-= MnO +2HO
2 2
D.理论上电路中每通过1 mol电子,负极质量减小 9 g
【答案】 D
【解析】 电池工作时,阳离子向正极移动,即K+向正极区移动,A错误;反应中铝为负极,发生氧化反
应,B错误;电解质溶液呈碱性,MnO在正极上发生得电子的还原反应,即MnO+2HO+3e-===MnO+
2 2
4OH-,C错误;理论上电路中每通过1 mol电子,则有 mol铝被氧化,负极质量减少9 g,D正确。
5.有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下:
实验装
置
资料整理【淘宝店铺:向阳百分百】部分实 a极质量减少;b极 b极有气体产生;c d极溶解;c极有气体产 电流从a极流向d
验现象 质量增加 极无变化 生 极
由此可判断这四种金属的活动性顺序是( )
A.a>b>c>d B.b>c>d>a C.d>a>b>c D.a>b>d>c
【答案】 C
【解析】 把四个实验从左到右分别编号为①②③④,则由实验①可知,a作原电池负极,b作原电池正
极,金属活动性:a>b;由实验②可知,活动性:b>c;由实验③可知,d作原电池负极,c作正极,活动
性:d>c;由实验④可知,d极为原电池负极,a极为原电池正极,活动性:d>a。
6.(2023·武汉检测)用石墨作电极电解溶有物质的量之比为 3∶1的NaCl和HSO 的水溶液。根据反应产
2 4
物,电解可明显分为三个阶段,下列叙述不正确的是( )
A.电解的最后阶段为电解水
B.阳极先逸出氯气后逸出氧气
C.阴极逸出氢气
D.电解过程中溶液的pH不断增大,最后pH为7
【答案】 D
【解析】 根据离子放电顺序可知,电解此混合溶液时,在阳极阴离子放电的先后顺序为Cl-、OH-、
SO,先生成Cl 后生成O ,在阴极始终为H+放电,逸出H ,整个电解过程可看成三个阶段:电解HCl溶
2 2 2
液、电解NaCl溶液、电解HO,最后溶液呈碱性,D错误。
2
7.(2023·全国·统考高考真题)用可再生能源电还原 时,采用高浓度的 抑制酸性电解液中的析氢
反应来提高多碳产物(乙烯、乙醇等)的生成率,装置如下图所示。下列说法正确的是
A.析氢反应发生在 电极上
B. 从 电极迁移到 电极
C.阴极发生的反应有:
D.每转移 电子,阳极生成 气体(标准状况)
【答案】 C
资料整理【淘宝店铺:向阳百分百】【解析】 由图可知,该装置为电解池,与直流电源正极相连的IrO -Ti电极为电解池的阳极,水在阳极失
x
去电子发生氧化反应生成氧气和氢离子,电极反应式为2HO-4e—=O ↑+4H+,铜电极为阴极,酸性条件下
2 2
二氧化碳在阴极得到电子发生还原反应生成乙烯、乙醇等,电极反应式为2CO+12H++12e−=C H+4H O、
2 2 4 2
2CO+12H++12e−=C HOH+3H O,电解池工作时,氢离子通过质子交换膜由阳极室进入阴极室。A.析氢
2 2 5 2
反应为还原反应,应在阴极发生,即在铜电极上发生,故A错误;B.离子交换膜为质子交换膜,只允许
氢离子通过,Cl-不能通过,故B错误;C.由分析可知,铜电极为阴极,酸性条件下二氧化碳在阴极得到
电子发生还原反应生成乙烯、乙醇等,电极反应式有2CO+12H++12e−=C H+4H O,故C正确;D.水在阳
2 2 4 2
极失去电子发生氧化反应生成氧气和氢离子,电极反应式为2HO-4e—=O ↑+4H+,每转移1mol电子,生成
2 2
0.25molO,在标况下体积为5.6L,故D错误;答案选C。
2
8.铅酸蓄电池是汽车常用的蓄电池,其构造如图所示。下列说法不正确的是( )
A.电池放电时,负极质量减轻
B.电池放电时,c(H+)减小
C.电池充电时总反应为2PbSO +2HO=Pb+PbO +2HSO
4 2 2 2 4
D.铅酸蓄电池的缺点是笨重、比能量低
【答案】 A
【解析】 放电时,负极Pb失去电子转化为PbSO ,负极质量增加,A项错误;放电过程中消耗HSO ,
4 2 4
溶液中c(H+)减小,B项正确。
9.(2023·北京朝阳·统考三模)某同学利用下列电池装置探究 的氧化性和还原性。电流表显示电子由
铁电极流向石墨电极,石墨电极上未见Fe析出,下列分析不正确的是
A.盐桥中的阳离子进入右侧烧杯溶液中
B.一段时间后两烧杯溶液中 均增大
C.当两烧杯溶液中 相等时,说明反应已达到平衡状态
D.由A、B中的现象可知, 还原性小于Fe、氧化性小于
【答案】 C
资料整理【淘宝店铺:向阳百分百】【解析】 该反应为Fe+2Fe3+=3Fe2+,负极为铁单质失电子生成亚铁离子,正极为铁离子得电子生成亚铁
离子,据此分析下列选项。A.铁电极失电子为负极,石墨电极为正极,阳离子从负极向正极移动,故盐
桥中阳离子进入石墨电极溶液中,A正确;B.负极反应为Fe-2e-=Fe2+,石墨电极上发生的反应为Fe3++e-
=Fe2+,两侧均反应生成亚铁离子,故一段时间后两烧杯溶液中c(Fe2+)均增大,故石墨电极溶液中亚铁离子
浓度增大,B正确;C.负极反应为Fe-2e-=Fe2+,正极反应为2Fe3++2e-=2Fe2+,设两边均为1L溶液,一段
时间后转移电子为2xmol时两极溶液中亚铁离子浓度相等,则0.10+x=2x+0.05,得x=0.05,则右边消耗铁
离子为0.05mol<1mol,则反应仍能继续进行,故不能说明反应达到平衡状态,C错误;D.负极反应为
Fe-2e-=Fe2+,正极反应为2Fe3++2e-=2Fe2+,总反应为Fe+2Fe3+=3Fe2+,反应中氧化剂为Fe3+,还原剂为Fe,
Fe2+既是氧化产物也是还原产物,故Fe2+还原性小于Fe,氧化性小于Fe3+,D正确;故答案选C。
10.(2023·全国·统考高考真题)一种以VO 和Zn为电极、Zn(CF SO ) 水溶液为电解质的电池,其示意
2 5 3 3 2
图如下所示。放电时,Zn2+可插入VO 层间形成ZnxVO·nH O。下列说法错误的是
2 5 2 5 2
A.放电时VO 为正极
2 5
B.放电时Zn2+由负极向正极迁移
C.充电总反应:xZn+V O +nHO = ZnxVO·nH O
2 5 2 2 5 2
D.充电阳极反应:ZnxVO·nH O-2xe-=xZn2++V O +nHO
2 5 2 2 5 2
【答案】 C
【解析】 由题中信息可知,该电池中Zn为负极、VO 为正极,电池的总反应为xZn+V O +nHO =
2 5 2 5 2
ZnxVO·nH O。A.由题信息可知,放电时,Zn2+可插入VO 层间形成ZnxVO·nH O,VO 发生了还原反
2 5 2 2 5 2 5 2 2 5
应,则放电时VO 为正极,A说法正确;B.Zn为负极,放电时Zn失去电子变为Zn2+,阳离子向正极迁
2 5
移,则放电时Zn2+由负极向正极迁移,B说法正确;C.电池在放电时的总反应为xZn+V O
2 5
+nHO=ZnxVO·nH O,则其在充电时的总反应为ZnxVO·nH O=xZn+V O +nHO ,C说法不正确;D.
2 2 5 2 2 5 2 2 5 2
充电阳极上ZnxVO·nH O被氧化为VO,则阳极的电极反应为ZnxVO·nH O-2xe-=xZn2++V O +nHO ,
2 5 2 2 5 2 5 2 2 5 2
D说法正确;综上所述,本题选C。
11.某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指
针发生了偏转。
资料整理【淘宝店铺:向阳百分百】请回答下列问题:
(1)甲池为________(填“原电池”“电解池”或“电镀池”),通入 CHOH 电极的电极反应式为
3
___________________________________________________________________________________________
。
(2)乙池中 A(石墨)电极的名称为________(填“正极”“负极”“阴极”或“阳极”),总反应式为
________________________________________。
(3)当乙池中B极质量增加5.40 g时,甲池中理论上消耗O 的体积为________mL(标准状况下),丙池中
2
________极析出________g铜。
(4)若丙池中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将________(填
“增大”“减小”或“不变”);丙中溶液的pH将________(填“增大”“减小”或“不变”)。
【答案】 (1)原电池 CHOH-6e-+8OH-===CO+6HO
3 2
(2)阳极 4AgNO+2HO=====4Ag+O↑+4HNO (3)280 D 1.60 (4)减小 增大
3 2 2 3
【解析】 (1)甲池为原电池,通入CHOH的电极为负极,电极反应式为CHOH-6e-+8OH-===CO+
3 3
6HO。(2)乙池中电解AgNO 溶液,其中C作阳极,Ag作阴极,总反应式为4AgNO +2HO=====4Ag+
2 3 3 2
O↑+4HNO 。(3)根据各电极上转移的电子数相同,得n(Ag)=4n(O )=2n(Cu),故V(O )=××22.4 L=0.28
2 3 2 2
L=280 mL,m(Cu)=××64 g=1.60 g。(4)若丙中电极不变,将其溶液换成 NaCl溶液,根据丙中总反应
2NaCl+2HO=====2NaOH+H↑+Cl↑,则溶液 pH 增大,而甲中总反应为 2CHOH+3O +
2 2 2 3 2
4KOH===2K CO+6HO,溶液pH减小。
2 3 2
12.(2023·陕西宝鸡·统考一模)硫酸铅(PbSO ),制造铅蓄电池的一种原料;以废旧铅酸电池中的含铅废
4
料(Pb、PbO、PbO 、PbSO 及炭黑等)和HSO 为原料,制备高纯PbO,可实现铅的再生利用。
2 4 2 4
(1)铅蓄电池中需要配制5.3 mol∙L−1的HSO 溶液,需要的仪器有玻璃棒、 (从下列图中选择,
2 4
写出名称)。
(2)工业上以PbS为原料可以制取PbSO ,80℃时浸取,将PbS与盐酸、MnO 和饱和食盐水一起浸取,PbS
4 2
资料整理【淘宝店铺:向阳百分百】反应后生成 和S。
①写出PbS反应的离子方程式: 。
②浸取时应控制盐酸的浓度。其他条件一定,若盐酸浓度过大,铅元素的浸出率反而下降,原因是
。
(3)用废旧铅酸电池中的含铅废料,制备高纯PbO,实现铅的再生利用的过程中,
过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++PbO+4H++ =2Fe3++PbSO+2H O
2 4 2
ii:2Fe3++Pb+ =2Fe2++PbSO
4
下列实验方案可证实上述催化过程。请将实验方案补充完整。
a.向酸化的FeSO 溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO ,溶液变红。
4 2
b. 。
(4)已知:K (PbCO )=1.5×10−13,K (PbSO )=1.8×10−8.在某制备过程中,经检测,过滤出的PbCO 沉淀中混
sp 3 sp 4 3
有PbSO ,则该滤液中 = 。
4
(5)以铅蓄电池为电源,电解二氧化碳酸性溶液可制得丙烯(如图)。
①Y极与电源 (填“正极”或“负极”)相连。
②该离子交换膜为 膜。
资料整理【淘宝店铺:向阳百分百】③X极的电极反应式为 。
【答案】(1)烧杯、量筒
(2) PbS+MnO +4Cl-+4H+= +S+Mn2++2HO 盐酸浓度过大,盐酸与MnO 发生氧化还原
2 2 2
反应,部分MnO 被盐酸消耗,导致与PbS反应的MnO 的量减少
2 2
(3)取a中红色溶液少量,加入过量Pb,充分反应后,红色褪去 (4)1.2×105
(5) 正极 质子 3CO+18e-+18H+=CHCH=CH+6HO
2 3 2 2
【解析】(1)配制5.3 mol∙L−1的HSO 溶液,需要的仪器有玻璃棒、量筒、胶头滴管、烧杯、一定规格的
2 4
容量瓶,不用托盘天平、圆底烧瓶、漏斗;故答案为:烧杯、量筒。(2)①将PbS与盐酸、MnO 和饱和
2
食盐水一起浸取,PbS反应后生成 和S,MnO 发生还原反应生成Mn2+,反应的离子方程式为PbS+
2
MnO +4Cl-+4H+= +S+Mn2++2HO;故答案为:PbS+MnO +4Cl-+4H+= +S+
2 2 2
Mn2++2HO。②MnO 能与浓盐酸反应,则盐酸浓度过大,部分MnO 被盐酸消耗,导致与PbS反应的
2 2 2
MnO 的量减少,铅元素的浸出率会下降;故答案为:盐酸浓度过大,盐酸与MnO 发生氧化还原反应,部
2 2
分MnO 被盐酸消耗,导致与PbS反应的MnO 的量减少。(3)过程Ⅰ中Fe2+作催化剂,在反应i中作反应
2 2
物,转化为Fe3+,设计的实验方案为:向酸化的FeSO 溶液中加入KSCN溶液,溶液几乎无色,再加入少
4
量PbO ,溶液变红;要证明Fe2+在反应ii中作生成物,Fe3+转化为Fe2+,可取a中红色溶液,加入过量Pb
2
粉,若充分反应后红色褪去,即可说明Fe3+又转化为Fe2+;故答案为:取a中红色溶液少量,加入过量
Pb,充分反应后,红色褪去。(4)过滤出的PbCO 沉淀中混有PbSO ,则PbCO 、PbSO 共存体系中
3 4 3 4
;故答案为:1.2×105。(5)①该电解池
中,Y极中水失电子生成O,为阳极,与电源正极相连;故答案为:正极。②阳极反应式为2HO−4e﹣=
2 2
O↑+4H+,阴极反应式为3CO+18e-+18H+=CHCH=CH+6HO,电解质溶液呈酸性,则离子交换膜为
2 2 3 2 2
质子交换膜;故答案为:质子。③X电极为阴极,阴极上CO 得电子生成丙烯,电极反应式为3CO+18e
2 2
-+18H+=CHCH=CH+6HO;故答案为:3CO+18e-+18H+=CHCH=CH+6HO。
3 2 2 2 3 2 2
【拔高练习】
1.(2022·济南模拟)四个电解装置都以Pt做电极,它们分别装有如下电解质溶液,电解一段时间后,测定其
pH变化,所记录的结果正确的是( )
资料整理【淘宝店铺:向阳百分百】选项 A B C D
电解质溶液 HCl CuSO KOH BaCl
4 2
pH变化 减小 增大 增大 不变
【答案】 C
【解析】 电解盐酸,溶质HCl的量减少,溶剂的量不变,所以酸性减弱,pH增大,A项错误;电解
CuSO 溶液生成硫酸、金属铜和氧气,溶液酸性增强,pH减小,B项错误;电解氢氧化钾溶液的实质是电
4
解水,溶质的量不变,溶剂减少,碱性增强,pH增大,C项正确;电解氯化钡溶液得到氢氧化钡、氢气和
氯气,溶液碱性增强,pH增大,D项错误。
2.(2022·全国·统考高考真题) 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科
学家研究了一种光照充电 电池(如图所示)。光照时,光催化电极产生电子 和空穴 ,驱动阴极
反应 和阳极反应(Li O+2h+=2Li++O )对电池进行充
2 2 2
电。下列叙述错误的是
A.充电时,电池的总反应
B.充电效率与光照产生的电子和空穴量有关
C.放电时,Li+从正极穿过离子交换膜向负极迁移
D.放电时,正极发生反应
【答案】 C
【解析】 充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应
(LiO+2h+=2Li++O ),则充电时总反应为LiO=2Li+O ,结合图示,充电时金属Li电极为阴极,光催化
2 2 2 2 2 2
电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。A.光照时,光催化电极产生
电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应
为LiO=2Li+O ,A正确;B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反
2 2 2
应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;C.放电时,金属Li电极为负极,
光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;D.放电时总反应为2Li+O=Li O,
2 2 2
正极反应为O+2Li++2e-=Li O,D正确。
2 2 2
3.(2022·四川绵阳模拟)1,5-戊二胺( )是生物法制备尼龙材料的重要原料,利用双极膜
资料整理【淘宝店铺:向阳百分百】(BPM)电渗析产碱技术可将生物发酵液中的1,5-戊二胺硫酸盐(含 和SO)转换为1,5-
戊二胺,实现无害化提取,工作原理如图所示。下列说法错误的是( )
A.a极的电势比b极的低
B.m膜为阳离子交换膜,n膜为阴离子交换膜
C.电解过程中,HSO 极室溶液的pH逐渐减小
2 4
D.b极区每生成11.2 L气体(标准状况),理论上可生成2 mol 1,5-戊二胺
【答案】 D
【解析】 根据题意,将生物发酵液中的1,5-戊二胺硫酸盐转换为1,5-戊二胺,则生物发酵液中的SO应
通过n膜进入HSO 溶液, 应通过m膜进入产品室,与BPM表面产生的OH-反应生成
2 4
水和 。阳离子向a极移动,a极是阴极,则b极是阳极,阳极电势比阴极电势高,A正
确;电解过程中SO进入HSO 极室,生成HSO ,溶液pH逐渐减小,C正确;b极区是阳极区,电渗析
2 4 2 4
过程生成 O ,每生成 11.2 L气体(标准状况)转移的电子为×4=2 mol,而1 mol 生成
2
转移2 mol电子,故理论上可生成1 mol 1,5-戊二胺,D错误。
4.(2023·河南·校联考三模)近日,中国科学院大连化学物理研究所团队利用固体氧化物(γ–Al O)电解质
2 3
实现了乙烷电化学脱氢制乙烯,其工作原理如图所示。下列说法正确的是
A.a为电源的负极
B.M极电极反应式为C H+2e-=C H+2H+
2 6 2 4
C.每生成0.5molC H,N极消耗标准状况下11.2LCO
2 4 2
D.每生成56gCO,电路中转移电子的物质的量为2mol
【答案】C
【解析】A.M电极乙烷发生氧化反应生成乙烯,M为阳极,a为电源的正极,故A错误;B.M极乙烷失
电子发生氧化反应生成乙烯,反应式为C H-2e-+O2-=C H+2H O,故B错误;C.阳极发生反应C H-2e-
2 6 2 4 2 2 6
资料整理【淘宝店铺:向阳百分百】+O2-=C H+2H O,阴极发生反应CO+2e-=CO+O2-,每生成0.5molC H,转移1mol电子,N极消耗
2 4 2 2 2 4
0.5molCO,标准状况下的体积为11.2LCO,故C正确;D.阴极发生反应CO+2e-=CO+O2-,每生成
2 2 2
56gCO,电路中转移电子的物质的量为 ,故D错误;选C。
5.(2023·河南郑州·统考三模)一种利用电化学进行“大气固碳”的装置如图所示。该电池放电时正极生
成C和LiCO,充电时通过催化剂的选择性控制,只有LiCO 是阳极反应物。下列说法正确的是
2 3 2 3
A.该电池放电时的正极反应式为CO+4e-=C+2O2-
2
B.图中Li+移动方向是电池充电时的移动方向
C.充电时,阳极反应式为2LiCO-4e-=4Li++2CO ↑+O ↑
2 3 2 2
D.该电池放电、充电过程中转移电子相同时,消耗与生成CO 的量相等
2
【答案】 C
【解析】 由图可知,放电时,负极:Li-e-=Li+,正极:3CO+4e-+4Li+=2Li CO+C,总反应为:4Li+
2 2 3
3CO=2Li CO+C。充电时只有LiCO 发生氧化:阳极:2LiCO-4e-=4Li+ +2CO ↑+O ↑,阴极:4Li++4e-
2 2 3 2 3 2 3 2 2
=4Li,总反应为:2LiCO=4Li+2CO ↑+O ↑,依据此分析解答。A.由分析可知,该电池放电时的正极反应
2 3 2 2
式为3CO+4e-+4Li+=2Li CO+C,故A错误;B.由分析可知,充电时,电极A为阴极,电极B为阳极,
2 2 3
Li+移动方向是由阳极移向阴极,图中Li+移动方向不是电池充电时的移动方向,故B错误;C.由分析可
知,充电时,阳极反应式为2LiCO-4e-=4Li++2CO ↑+O ↑,故C正确;D.该电池放电时的正极反应式为
2 3 2 2
3CO+4e-+4Li+=2Li CO+C,充电时阳极电极方程式为:2LiCO-4e-=4Li+ +2CO ↑+O ↑,该电池放电、充电
2 2 3 2 3 2 2
过程中转移电子相同时,消耗与生成CO 的量不相等,故D错误;故选C。
2
6.用如图所示装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中各项所列对应关系均正确的
一项是( )
资料整理【淘宝店铺:向阳百分百】选项 X极 实验前U形管中液体 通电后现象及结论
A 正极 NaSO 溶液 U形管两端滴入酚酞后,a管中呈红色
2 4
b管中电极反应式是4OH--4e-===O ↑+
2
B 正极 AgNO 溶液
3
2HO
2
C 负极 CuCl 溶液 b管中有气体逸出
2
D 负极 NaOH溶液 溶液pH降低
【答案】 C
【解析】 电解NaSO 溶液时,阳极上是OH-发生失电子的氧化反应,即a管中OH-放电,酸性增强,
2 4
酸遇酚酞不变色,即a管中呈无色,A错误;电解AgNO 溶液时,阴极上是Ag+发生得电子的还原反应,
3
即b管中电极反应是析出金属Ag的反应,B错误;电解CuCl 溶液时,阳极上是Cl-发生失电子的氧化反
2
应,即b管中Cl-放电,产生Cl ,C正确;电解NaOH溶液时,实际上电解的是水,导致NaOH溶液的浓
2
度增大,碱性增强,pH升高,D错误。
7.(2023·陕西西安·陕西师大附中校考模拟预测)利用光伏电池与膜电解法制备Ce(SO) 溶液的装置如下
4 2
图所示,下列说法不正确的是
A.电解池中阴极的电极反应式为
B.该离子交换膜为阴离子交换膜, 由左池向右池迁移
资料整理【淘宝店铺:向阳百分百】C.该光伏电池的N电极为负极
D.电路中有0.1mol电子通过时,阳极室生成33.2g Ce(SO )
4 2
【答案】 B
【解析】 光伏电池内负电荷向N极移动,则N极为负极,P电极为正极,电解池中纯铜为阴极,石墨为
阳极。A.由分析可知,纯铜为阴极,阴极发生还原反应,电极反应式为 ,故A正确;B.
Ce3+在石墨极发生反应后变为Ce4+,发生了氧化反应,Ce4+与 结合变为Ce(SO) 而流出,消耗了硫酸根
4 2
离子,因此右池中的 向左池迁移,不断进行补充,故B错误;C.光伏电池内负电荷向N极移动,则
N极为负极,故C正确;D.由电路中有0.1mol电子通过时,根据电极反应: 可知,阳极
室生成 即 ,故D正确;故答案选B。
8.(2023·陕西宝鸡·统考二模)海泥细菌通过消耗海底沉积层中的有机物获得营养,同时产生电子。科学
家利用这一原理设计了海泥细菌电池,该技术可在海底加速石油污染物降解速率,其中海泥代谢产物显酸
性,电池工作原理如图所示。下列说法错误的是
A.负极的电极反应式为:CHO-4e-+H O=CO+4H+
2 2 2
B.工作时B电极附近溶液pH减小
C.海水和海泥含有电解质,导电性高,有利于输出电能
D.A电极消耗标况下O5.6L,有1mol质子通过海底沉积层和海水层交接面
2
【答案】 A
【解析】 由图可知,A极氧气得到电子发生还原生成水,为正极, ;B电极HS-失去
电子发生氧化反应生成硫单质,为负极, ;A.由分析可知,负极反应为
资料整理【淘宝店铺:向阳百分百】,A错误; B.工作时B电极附近生成氢离子,酸性增强,溶液pH减小,B正确;C.海水和海泥含有电
解质,导电性高,有利于形成闭合电路输出电能,C正确; D.A电极反应为 ,消耗
标况下O5.6L,为0.25mol氧气,根据电子守恒可知,有1mol质子通过海底沉积层和海水层交接面,D正
2
确;故选A。
9.(2023·陕西咸阳·统考一模)某课题组以纳米Fe O 作为电极材料制备锂离子电池(另一极为金属锂和石
2 3
墨的复合材料),通过在室温条件下对锂离子电池进行循环充放电,成功地实现了对磁性的可逆调控(见右
图),下列说法不正确的是
A.充电时,Fe O 对应电极连接充电电源的负极
2 3
B.该电池的正极的电极反应式:Fe O+6Li++6e−=3Li O+2Fe
2 3 2
C.该电池不能使用氢氧化钠溶液作为电解液
D.该电池工作的原理:放电时,Fe O 作为电池正极被还原为Fe,电池被磁铁吸引
2 3
【答案】 A
【解析】 据图可知放电时,Li被氧化Li+,所以金属锂和石墨的复合材料为负极,纳米Fe O 为正极。A.
2 3
放电时Fe O 对应电极为正极,则充电时为阳极,与电源正极相连,A错误;B.放电时Fe O 对应电极为
2 3 2 3
正极,Fe O 被还原为Fe,O元素转化为LiO,根据电子守恒、元素守恒可得电极反应式为Fe O+6Li+
2 3 2 2 3
+6e−=3Li O+2Fe,B正确;C.Li为活泼金属,会与氢氧化钠溶液中的水反应,C正确;D.据图可知,该
2
电池工作时,Fe O 为正极,被还原为Fe,使电池被磁铁吸引,D正确;综上所述答案为A。
2 3
10.(2023·河北·校联考三模)磷酸铁锂( )电池应用广泛,放电后,电池的正极材料主要含有
、Al、石墨以及少量难溶性的杂质。已知 易溶于 溶液,难溶于 溶液,从放电
后正极材料中回收金属锂的流程如图所示。下列说法错误的是
资料整理【淘宝店铺:向阳百分百】A.向“滤液”中滴加稀盐酸至过量,先产生白色沉淀,后沉淀逐渐溶解
B.“酸浸氧化”时可以用 溶液代替 溶液
C.“酸浸氧化”时检验是否完全氧化,可用 溶液
D.“沉锂”时主要反应的离子方程式为
【答案】 B
【解析】 正极材料主要含有 、Al、石墨以及少量难溶性的杂质,加入NaOH溶液除去Al,滤渣
加入HO 和硝酸过滤除去铁、石墨和难溶性杂质,溶液加入NaHCO 溶液沉锂,最后得到碳酸锂。A.滤
2 2 3
液中含有 ,在滴加稀盐酸至过量过程中,先后发生离子反应 、
,A项正确;B.依据题给信息, 易溶于 溶液,难溶于
溶液,若用 溶液代替 溶液,则 溶于其中,难以通过过滤除去,对后续回收锂产
生影响,B项错误;C. 溶液和 溶液氧化 ,生成 ,若未完全氧化,则溶液中存
在 ,可使用 溶液检验,观察是否有蓝色沉淀生成,C项正确;D.沉锂过程中发生的主
要反应的离子方程式为 ,D项正确;答案选B。
11.(2023·河北·校联考三模)科学家开发了一种可循环使用的太阳能水电池,该装置绿色环保,有广泛
的研究前景,其工作原理如图所示。下列说法错误的是
资料整理【淘宝店铺:向阳百分百】A.光充电时, 电极附近溶液的酸性增强
B.放电时, 电极为正极
C.光充电时, 向 电极迁移
D.放电时,Pt电极反应式:
【答案】 B
【解析】光充电时是电解池, 电极有电子流出,发生氧化反应,是阳极;放电时是原电池, 电
极有电子流出,发生氧化反应,故 电极为负极,Pt电极为正极,据此作答;A.太阳能水电池光充电
过程中, 电极有电子流出,发生氧化反应,电极反应式为 ,故 电极附
近溶液的酸性增强,A正确;B.放电时, 电极有电子流出,发生氧化反应,故 电极为负极,Pt
电极为正极, B错误;C.充电时, 电极为阴极, 向阴极迁移,C正确;D.放电时,Pt电极为
正极,Pt电极附近有光充电产生的大量 ,故Pt电极反应式为 ,D正确; 故选
B。
12. 某化学兴趣小组的同学用如下图所示装置研究有关电化学的问题。当闭合 K时,观察到电流表的指针
发生了偏移。
资料整理【淘宝店铺:向阳百分百】请回答下列问题:
(1)乙装置的名称是________;Zn为________极。
(2)写出电极反应:Cu极:_________________________________________;
石墨棒极:_________________________________________________________。
(3)当甲中产生0.1 mol气体时,乙中产生的气体在标准状况下的体积应为________。
(4)若乙中溶液不变,将其电极都换成铜电极,闭合K一段时间后,乙中溶液的颜色________(填“变深”
“变浅”或“不变”)。
(5)若乙中电极不变,将其溶液换成NaCl溶液,闭合K一段时间后,甲中溶液的pH将________(填“增
大”“减小”或“不变”,下同);乙中溶液的pH将________。
(6)若乙中电极不变,将其溶液换成饱和NaSO 溶液,闭合K一段时间,当阴极上有a mol气体生成时,
2 4
同时有ω g Na SO ·10H O析出,假设温度不变,剩余溶液中溶质的质量分数应为________________(用含
2 4 2
ω、a的表达式表示,不必化简)。
【答案】 (1)电解池 负 (2)2H++2e-===H ↑
2
Cu2++2e-===Cu (3)2.24 L (4)不变
(5)增大 增大 (6)×100%
【解析】 (1)乙中Pt、石墨棒都是惰性电极,甲中Zn和Cu都是活性电极,则甲是原电池,Zn是负极,
Cu是正极;乙是电解池,Pt是阳极,石墨棒是阴极。(2)甲中电解液是稀硫酸,Cu极的电极反应式为2H+
+2e-===H ↑;石墨棒阴极上Cu2+发生还原反应,电极反应式为 Cu2++2e-===Cu。(3)甲中Cu电极产生
2
H ,产生0.1 mol气体时,电路中通过0.2 mol电子;乙中Pt电极反应式为2Cl--2e-===Cl↑,则转移0.2
2 2
mol 电子时生成0.1 mol Cl ,在标准状况下的体积为2.24 L。(4)铜电极是活性电极,乙为电镀池,电解液
2
中c(Cu2+)不变,则乙中溶液的颜色不变。(5)甲中电池总反应为Zn+2H+===Zn2++H↑,溶液的pH增大;
2
乙中电极不变,将其溶液换成NaCl溶液,电池总反应为2NaCl+2HO=====2NaOH+H↑+Cl↑,反应生
2 2 2
成NaOH,溶液的pH增大。(6)利用惰性电极电解饱和NaSO 溶液,电池总反应式为2HO=====2H↑+
2 4 2 2
O↑,阴极上析出H ,则阴极上有a mol气体生成时,消耗a mol H O,同时有ω g Na SO ·10H O析出,
2 2 2 2 4 2
剩余溶液仍为饱和 NaSO 溶液,故 a mol H O 和 ω g Na SO ·10H O 也形成饱和 NaSO 溶液,ω g
2 4 2 2 4 2 2 4
资料整理【淘宝店铺:向阳百分百】NaSO ·10H O中含有NaSO 的质量为 g,因此剩余溶液中溶质的质量分数为(g)/(ω g+18a g)×100%=
2 4 2 2 4
×100%。
13.(2022·德阳三模)铝的阳极氧化是一种重要的表面处理技术,其原理是用电化学方法处理铝件表面,优化
氧化膜结构,增强铝件的抗腐蚀性,同时便于表面着色。取铝片模拟该实验,并测定氧化膜厚度,操作步
骤如下:
(1)铝片预处理
铝片表面除去油垢后,用2 mol/LNaOH溶液在60~70 ℃下洗涤,除去铝表面薄氧化膜,离子方程式为:
________________________________________;
再用10%(质量分数)的HNO 溶液对铝片表面进行化学抛光。若取一定体积68%(质量分数)的浓硝酸配制该
3
化学抛光液,需要用到的玻璃仪器有________、________、玻璃棒和胶头滴管。
(2)电解氧化
取预处理过的铝片和铅做电极,控制电流恒定为0.06 A,用直流电源在5~6 mol/L硫酸中电解。其中铝片
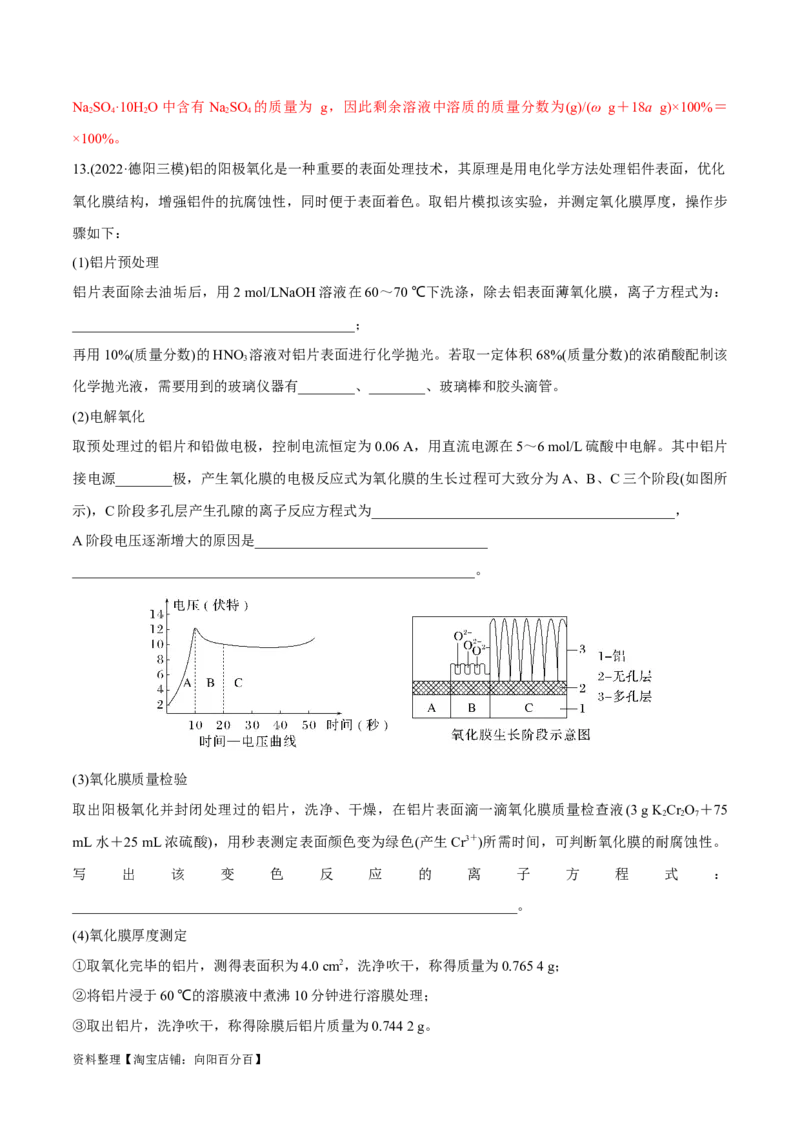
接电源________极,产生氧化膜的电极反应式为氧化膜的生长过程可大致分为A、B、C三个阶段(如图所
示),C阶段多孔层产生孔隙的离子反应方程式为___________________________________________,
A阶段电压逐渐增大的原因是_________________________________
_________________________________________________________。
(3)氧化膜质量检验
取出阳极氧化并封闭处理过的铝片,洗净、干燥,在铝片表面滴一滴氧化膜质量检查液(3 g K Cr O +75
2 2 7
mL水+25 mL浓硫酸),用秒表测定表面颜色变为绿色(产生Cr3+)所需时间,可判断氧化膜的耐腐蚀性。
写 出 该 变 色 反 应 的 离 子 方 程 式 :
_______________________________________________________________。
(4)氧化膜厚度测定
①取氧化完毕的铝片,测得表面积为4.0 cm2,洗净吹干,称得质量为0.765 4 g;
②将铝片浸于60 ℃的溶膜液中煮沸10分钟进行溶膜处理;
③取出铝片,洗净吹干,称得除膜后铝片质量为0.744 2 g。
资料整理【淘宝店铺:向阳百分百】已知氧化膜的密度为2.7 g/cm3,可以计算得出氧化膜厚度为________μm(1 μm=1×10-4cm)。
【答案】 (1)AlO +2OH-=2AlO+HO 烧杯 量筒 (2)正 2Al-6e-+3HO=Al O +6H+、Al O +6H
2 3 2 2 2 3 2 3
+=Al3++3HO 电流不变时,氧化膜覆盖阳极表面,电阻增大 (3)2Al+ Cr O+14H+=2Cr3++2Al3++
2 2
7HO
2
(4)19.6
【解析】 (1)铝片表面除去油垢后,用2 mol/L NaOH溶液在60~70 ℃下洗涤,除去铝表面薄氧化膜,即
Al O 与NaOH溶液反应的离子方程式为:Al O +2OH-===2AlO+HO,用浓硝酸配制一定量的10%(质量
2 3 2 3 2
分数)的HNO 溶液,需要的实验步骤为:计算、量取、稀释、装瓶,需要用到的玻璃仪器有量筒、烧杯、
3
玻璃棒和胶头滴管;(2)本电解的目的是将铝片电解氧化生成致密的氧化物保护膜,电解池中阳极发生氧化
反应,则其中铝片接电源正极,产生氧化膜的生长过程可大致分为A、B、C三个阶段(如图所示),C阶段
多孔层产生孔隙即生成有Al O 保护膜,同时又被生成的H+消耗掉一部分Al O ,从而形成多孔层产生空
2 3 2 3
隙,该过程的离子反应方程式为2Al-6e-+3HO===AlO +6H+、Al O +6H+===Al3++3HO,随着电解
2 2 3 2 3 2
的进行氧化膜覆盖阳极表面厚度加厚,电阻增大,则为了保持电流不变,则 A阶段电压需逐渐增大;(3)该
变色反应即KCr O 转化为了Cr3+,被还原,即Al参与该反应转化为Al3+,根据氧化还原反应配平可得,
2 2 7
该反应的离子方程式为:2Al+Cr O+14H+===2Cr3++2Al3++7HO;(4)由题干可知,氧化膜的质量为:
2 2
0.765 4 g-0.744 2 g=0.021 2 g,则氧化膜的体积为:=0.007 85 cm3,则氧化膜的厚度为:=0.001 96 cm
=19.6 μm。
资料整理【淘宝店铺:向阳百分百】