文档内容
第22讲 水的电离与溶液的 pH
1.25 ℃时,水的电离达到平衡:HO H++OH-。下列叙述错误的是( )
2
A.向水中通入氨气,平衡逆向移动,c(OH-)增大
B.向水中加入少量稀硫酸,c(H+)增大,K 不变
w
C.将水加热,平衡正向移动,K 变大
w
D.升高温度,平衡正向移动,c(H+)增大,pH不变
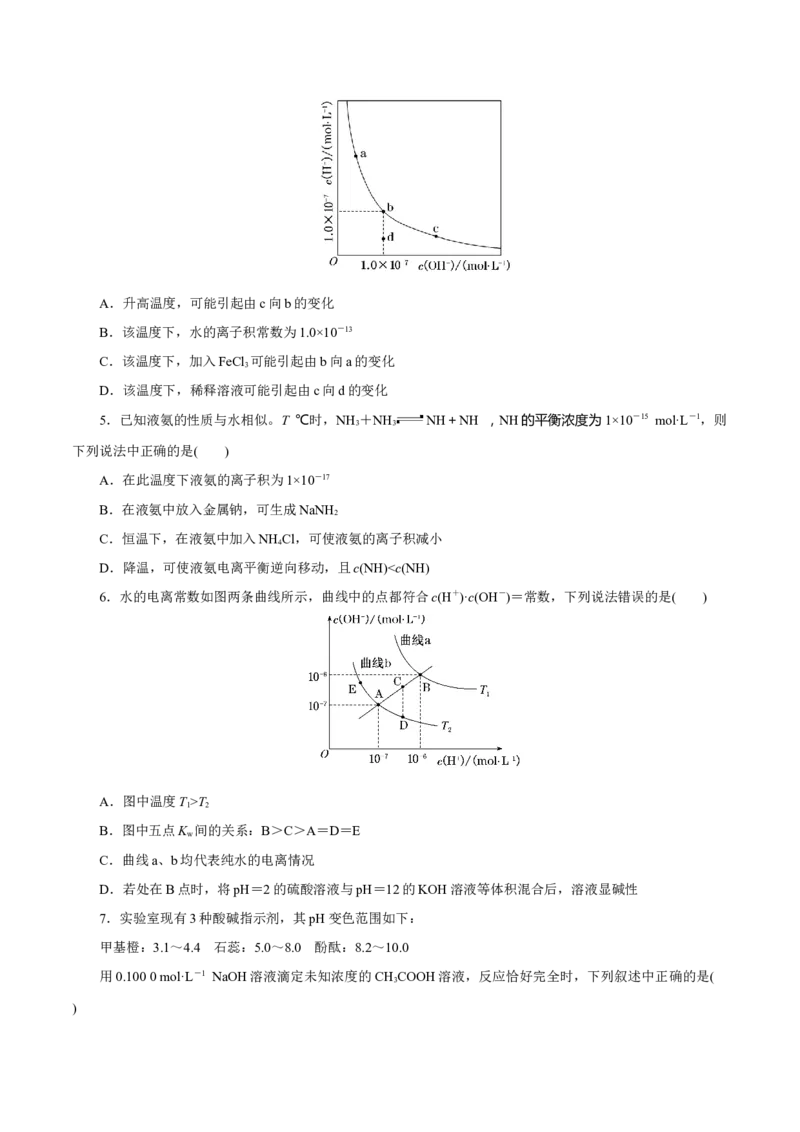
2.HSO 是一种弱酸,实验室欲用 0.01 mol·L-1的 NaSO 溶液滴定 I 溶液,发生的反应为 I +
2 2 3 2 2 3 2 2
2NaSO===2NaI+NaSO,下列说法合理的是( )
2 2 3 2 4 6
A.该滴定可用甲基橙作指示剂
B.NaSO 是该反应的还原剂
2 2 3
C.该滴定可选用如图所示装置
D.该反应中每消耗2 mol NaSO,转移电子数为4 mol
2 2 3
3.一定温度下,水存在HO H++OH- ΔH>0的平衡,下列叙述一定正确的是( )
2
A.向水中滴入少量稀盐酸,平衡逆向移动,K 减小
w
B.将水加热,K 增大,pH减小
w
C.向水中加入少量固体CHCOONa,平衡逆向移动,c(H+)降低
3
D.向水中加入少量固体硫酸钠,c(H+)=10-7 mol·L-1,K 不变
w
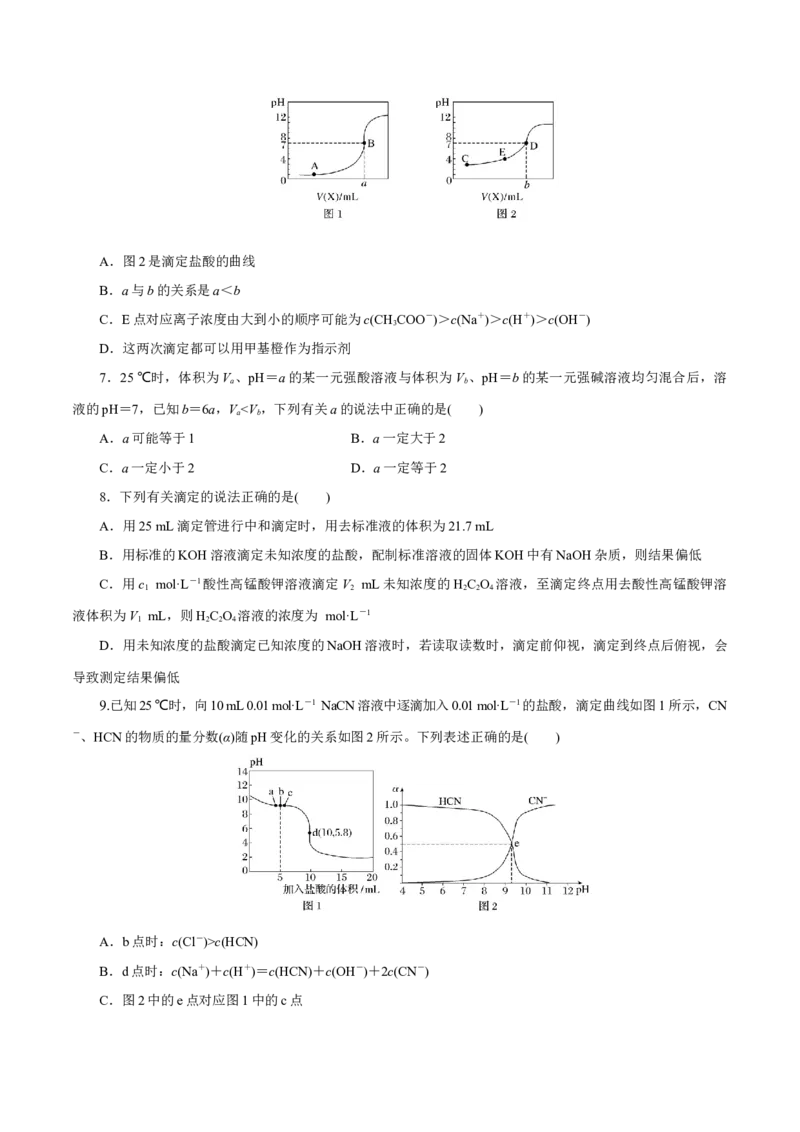
4.一定温度下,水溶液中H+和OH-的浓度变化曲线如图。下列说法正确的是( )A.升高温度,可能引起由c向b的变化
B.该温度下,水的离子积常数为1.0×10-13
C.该温度下,加入FeCl 可能引起由b向a的变化
3
D.该温度下,稀释溶液可能引起由c向d的变化
5.已知液氨的性质与水相似。T ℃时,NH+NH NH+NH ,NH的平衡浓度为1×10-15 mol·L-1,则
3 3
下列说法中正确的是( )
A.在此温度下液氨的离子积为1×10-17
B.在液氨中放入金属钠,可生成NaNH
2
C.恒温下,在液氨中加入NHCl,可使液氨的离子积减小
4
D.降温,可使液氨电离平衡逆向移动,且c(NH)T
1 2
B.图中五点K 间的关系:B>C>A=D=E
w
C.曲线a、b均代表纯水的电离情况
D.若处在B点时,将pH=2的硫酸溶液与pH=12的KOH溶液等体积混合后,溶液显碱性
7.实验室现有3种酸碱指示剂,其pH变色范围如下:
甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0
用0.100 0 mol·L-1 NaOH溶液滴定未知浓度的CHCOOH溶液,反应恰好完全时,下列叙述中正确的是(
3
)A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
8.常温下,0.1 mol·L-1某一元酸(HA)溶液中=1×10-8,下列叙述正确的是( )
A.该一元酸溶液的pH=1
B.该溶液中由水电离出来的c(H+)=1×10-11 mol·L-1
C.该溶液中水的离子积常数为1×10-22
D.用pH=11的NaOH溶液V L和V L 0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V
1 2 1
<V
2
9.用已知浓度的NaOH溶液测定某HSO 溶液的浓度,参考下图,从下表中选出正确的指示剂和仪器(
2 4
)
10.在某温度时,测得0.01 mol·L-1NaOH溶液的pH为11。
(1)该温度下水的离子积常数K =________。
w
(2)在此温度下,将pH=a的NaOH溶液V L与pH=b的硫酸V L混合。
a b
①若所得混合液为中性,且a=12,b=2,则V∶V=________。
a b
②若所得混合液为中性,且a+b=12,则V∶V=________。
a b
1.常温下,关于溶液稀释的说法正确的是( )
A.将1 L 0.1 mol·L-1的Ba(OH) 溶液加水到体积为2 L,pH=13
2
B.pH=3的醋酸溶液加水稀释到原浓度的,pH=5
C.pH=4的HSO 溶液加水稀释到原浓度的,溶液中由水电离产生的c(H+)=1×10-6 mol·L-1
2 4
D.pH=8的NaOH溶液加水稀释到原浓度的,其pH=6
2.实验室用标准盐酸测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准盐酸润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
3.室温下,pH=11的某溶液中水电离出的c(OH-)为( )
①1.0×10-7 mol·L-1 ②1.0×10-6 mol·L-1
③1.0×10-3 mol·L-1 ④1.0×10-11 mol·L-1
A.③ B.④
C.①或③ D.③或④
4.在T ℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12。向该溶
液中逐滴加入pH=c的盐酸(T ℃),测得混合溶液的部分pH如下表所示:
序号 NaOH溶液体积/mL 盐酸体积/mL 溶液pH
① 20.00 0.00 8
② 20.00 20.00 6
假设溶液混合前后的体积变化忽略不计,则c为( )
A.1 B.4
C.5 D.6
5.若往20 mL 0.01 mol·L-1 CHCOOH溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如
3
图所示,下列有关说法不正确的是( )
A.c点时,水的电离程度最大,溶液呈碱性
B.若b点混合溶液显酸性,则2c(Na+)=c(CHCOO-)+c(CHCOOH)
3 3
C.混合溶液中水的电离程度:b>c>d
D.由图可知,该反应的中和热保持不变
6.常温下,用0.10 mol·L-1 NaOH溶液分别滴定20.00 mL 0.10 mol·L-1 HCl溶液和20.00 mL 0.10 mol·L-1
CHCOOH溶液,得到两条滴定曲线,如图所示,则下列说法正确的是( )
3A.图2是滴定盐酸的曲线
B.a与b的关系是a<b
C.E点对应离子浓度由大到小的顺序可能为c(CHCOO-)>c(Na+)>c(H+)>c(OH-)
3
D.这两次滴定都可以用甲基橙作为指示剂
7.25 ℃时,体积为V 、pH=a的某一元强酸溶液与体积为V 、pH=b的某一元强碱溶液均匀混合后,溶
a b
液的pH=7,已知b=6a,Vc(HCN)
B.d点时:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-)
C.图2中的e点对应图1中的c点D.选用酚酞试剂比选用甲基橙试剂作指示剂误差更小
10.亚硝酸钠(NaNO)是一种无色、无味晶体,具有防腐和抗氧化作用,常用作食品添加剂。
2
已知:HNO 是一种弱酸,酸性比醋酸略强,性质不稳定,易分解生成 NO和NO;能被常见强氧化剂氧化;
2 2
但在酸性溶液中它也是一种氧化剂,如能把I-氧化成I。
2
为了测定某样品中NaNO 的含量,某同学进行如下实验:①称取样品a g,加水溶解,配制成100 mL溶液;
2
②取25.00 mL溶液于锥形瓶中,用0.020 0 mol·L-1 KMnO 标准溶液(酸性)进行滴定,滴定结束后消耗KMnO
4 4
溶液V mL。
(1)上述实验①所需玻璃仪器除玻璃棒、胶头滴管之外还有___________________。
(2)在进行滴定操作时,KMnO 溶液盛装在__________(填“酸式”或“碱式”)滴定管中。当滴入最后一滴
4
溶液,________________________________________________时到达滴定终点。
(3)滴定过程中发生反应的离子方程式是_____________________________;测得该样品中NaNO 的质量分
2
数为________。
(4)若滴定过程中刚出现颜色变化就停止滴定,则测定结果________________。(填“偏大”“偏小”或“无
影响”)
1.(2020·浙江卷)下列说法不正确的是( )
A.2.0×10-7 mol·L-1的盐酸中c(H+)=2.0×10-7 mol·L-1
B.将KCl溶液从常温加热至80 ℃,溶液的pH变小但仍保持中性
C.常温下,NaCN溶液呈碱性,说明HCN是弱电解质
D.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大