文档内容
第 2 讲 物质的分离、提纯
课 程 标 准 知 识 建 构
1.掌握常见物质分离与提纯的常用方法。
2.掌握过滤、分液、蒸馏等操作的步骤及要求。
一、分离提纯的物理方法
1.分离、提纯的含义
(1)物质的分离
将混合物的各组分分离开来,获得几种纯净物的过程。
(2)物质的提纯
将混合物中的杂质除去而得到纯净物的过程,又叫物质的净化或除杂。
2.物质分离与提纯的常见实验装置
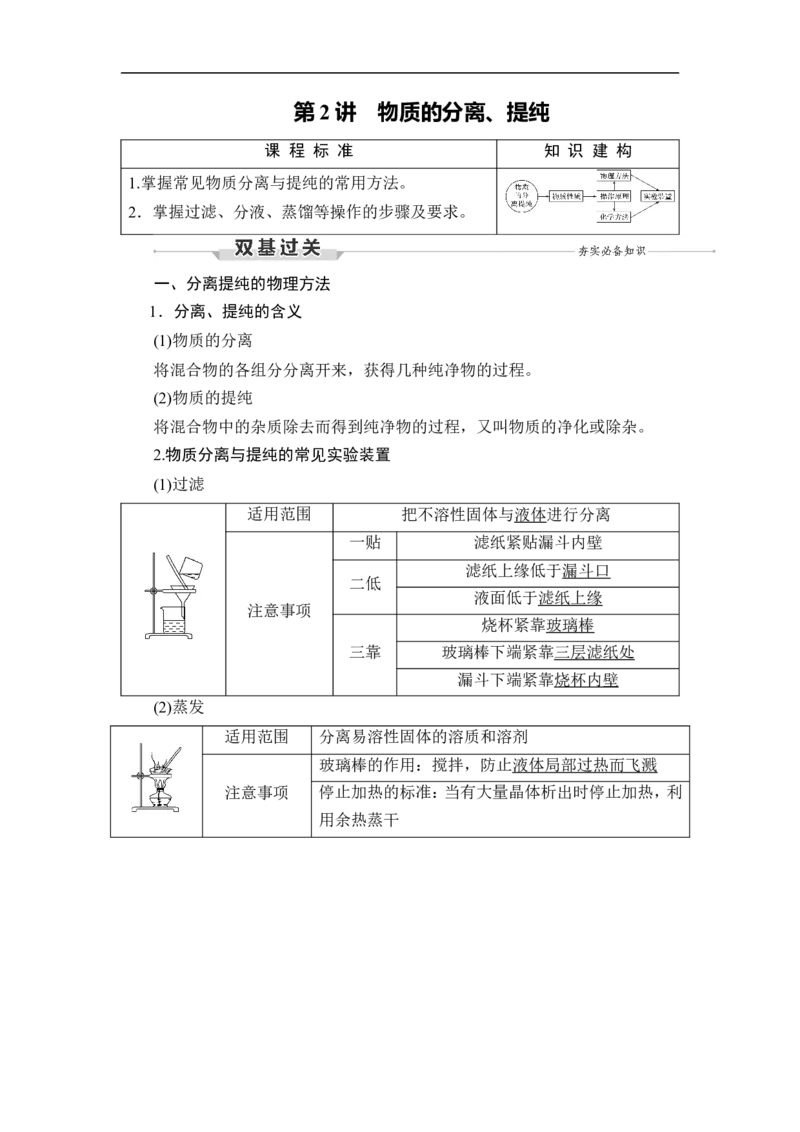
(1)过滤
适用范围 把不溶性固体与液体进行分离
一贴 滤纸紧贴漏斗内壁
滤纸上缘低于漏斗口
二低
液面低于滤纸上缘
注意事项
烧杯紧靠玻璃棒
三靠 玻璃棒下端紧靠三层滤纸处
漏斗下端紧靠烧杯内壁
(2)蒸发
适用范围 分离易溶性固体的溶质和溶剂
玻璃棒的作用:搅拌,防止液体局部过热而飞溅
注意事项 停止加热的标准:当有大量晶体析出时停止加热,利
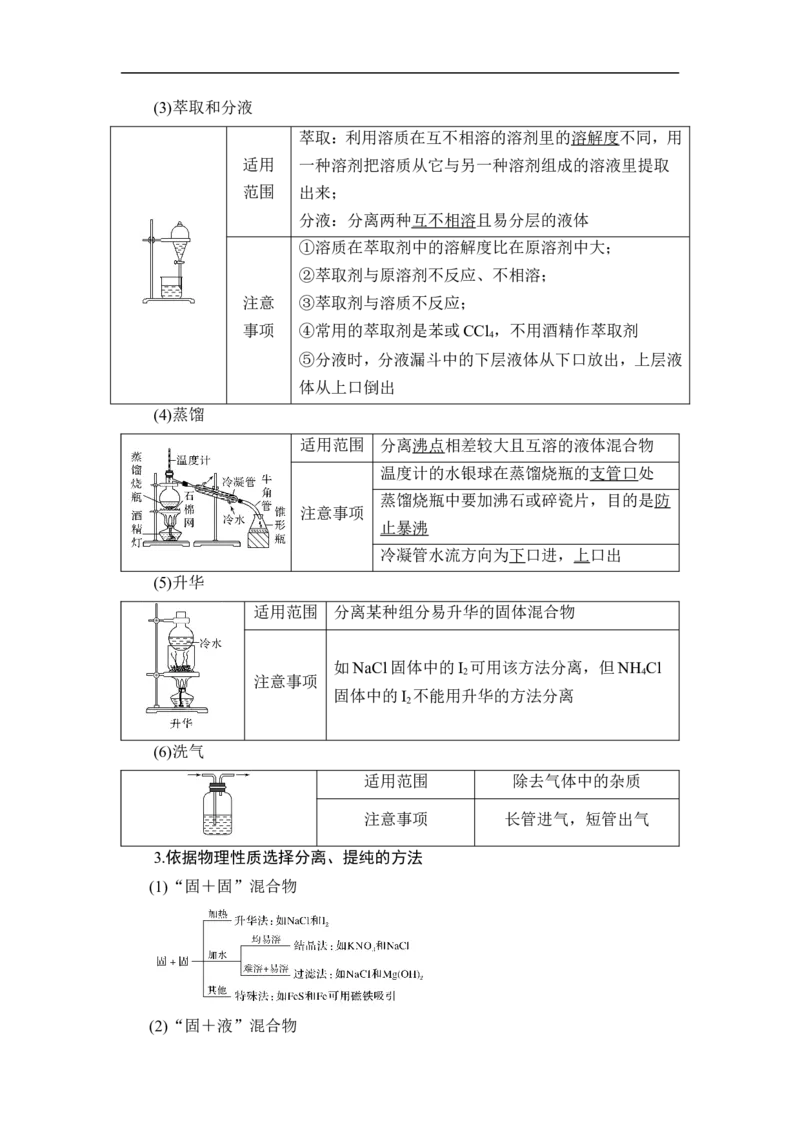
用余热蒸干(3)萃取和分液
萃取:利用溶质在互不相溶的溶剂里的溶解度不同,用
适用 一种溶剂把溶质从它与另一种溶剂组成的溶液里提取
范围 出来;
分液:分离两种互不相溶且易分层的液体
①溶质在萃取剂中的溶解度比在原溶剂中大;
②萃取剂与原溶剂不反应、不相溶;
注意 ③萃取剂与溶质不反应;
事项 ④常用的萃取剂是苯或CCl ,不用酒精作萃取剂
4
⑤分液时,分液漏斗中的下层液体从下口放出,上层液
体从上口倒出
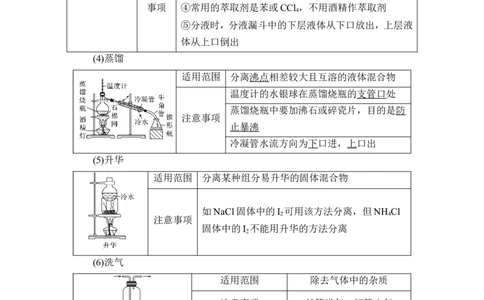
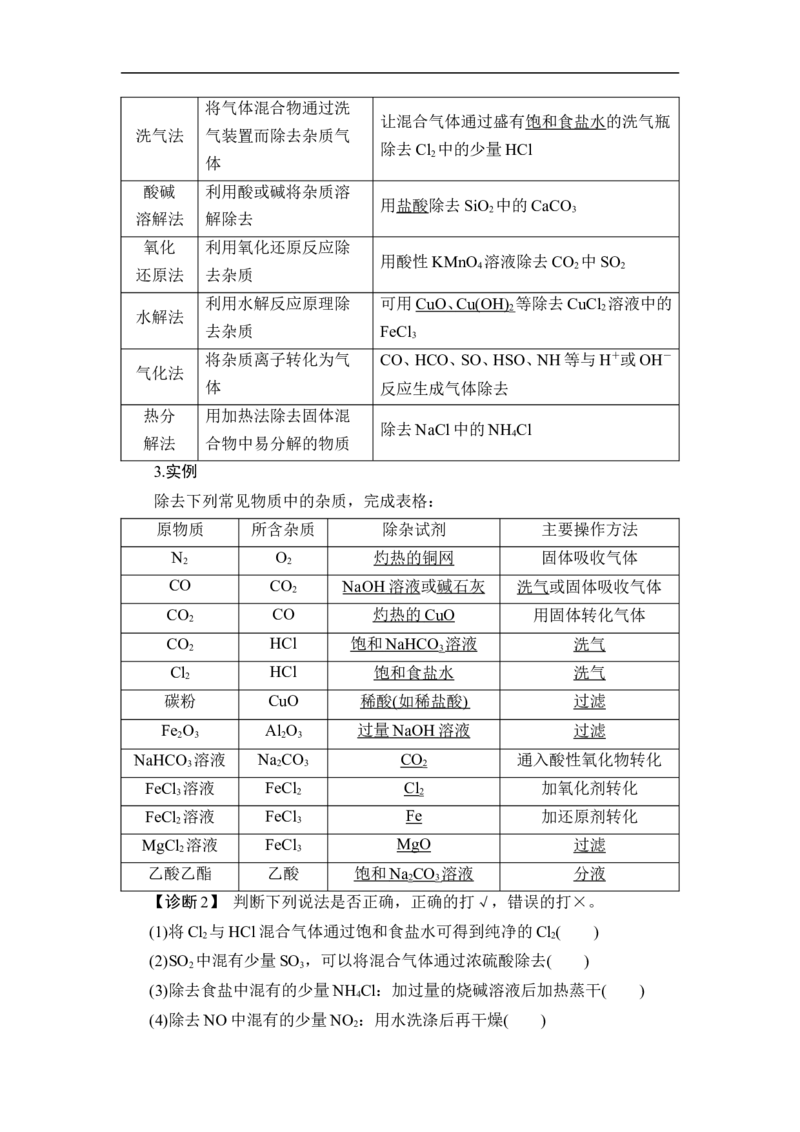
(4)蒸馏
适用范围 分离沸点相差较大且互溶的液体混合物
温度计的水银球在蒸馏烧瓶的支管口处
蒸馏烧瓶中要加沸石或碎瓷片,目的是防
注意事项
止暴沸
冷凝管水流方向为下口进,上口出
(5)升华
适用范围 分离某种组分易升华的固体混合物
如NaCl固体中的I 可用该方法分离,但NH Cl
2 4
注意事项
固体中的I 不能用升华的方法分离
2
(6)洗气
适用范围 除去气体中的杂质
注意事项 长管进气,短管出气
3.依据物理性质选择分离、提纯的方法
(1)“固+固”混合物
(2)“固+液”混合物(3)“液+液”混合物
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)过滤时,为加快过滤速度,应用玻璃棒不断搅拌漏斗中液体( )
(2)从溶液中获取NaCl晶体,用蒸发结晶的方法,其操作应使混合物中的水
分完全蒸干后,再停止加热( )
(3)根据食用油和汽油的密度不同,可选用分液的方法分离( )
(4)用乙醇萃取出溴水中的溴,再用蒸馏的方法分离溴与乙醇( )
(5)蒸馏时温度计的水银球应插入液体中( )
(6)在蒸馏过程中,若发现忘加沸石,应停止加热立即补加( )
(7)利用加热的方法分离NH Cl和I 的固体混合物( )
4 2
(8)蒸馏中,冷却水应从冷凝管的下口通入,上口流出( )
答案 (1)× (2)× (3)× (4)× (5)× (6)× (7)× (8)√
二、分离提纯的化学方法
1.分离、提纯物质遵循的“四原则”“三必须”
2.分离提纯常用的化学方法
方法 原理 举例说明
利用电解原理分离和 电解精炼铜,将含杂质的粗铜作阳极,精
电解法
提纯物质 铜作阴极,电解液为含铜离子的溶液
Cl-、SO、CO及能形成弱碱的金属阳离子
将杂质离子转化为沉
沉淀法 可加入适当的沉淀剂,使离子生成沉淀,
淀
过滤除去将气体混合物通过洗
让混合气体通过盛有饱和食盐水的洗气瓶
洗气法 气装置而除去杂质气
除去Cl 中的少量HCl
2
体
酸碱 利用酸或碱将杂质溶
用盐酸除去SiO 中的CaCO
2 3
溶解法 解除去
氧化 利用氧化还原反应除
用酸性KMnO 溶液除去CO 中SO
4 2 2
还原法 去杂质
利用水解反应原理除 可用 CuO 、 Cu(OH) 等除去CuCl 溶液中的
2 2
水解法
去杂质 FeCl
3
将杂质离子转化为气 CO、HCO、SO、HSO、NH等与H+或OH-
气化法
体 反应生成气体除去
热分 用加热法除去固体混
除去NaCl中的NH Cl
4
解法 合物中易分解的物质
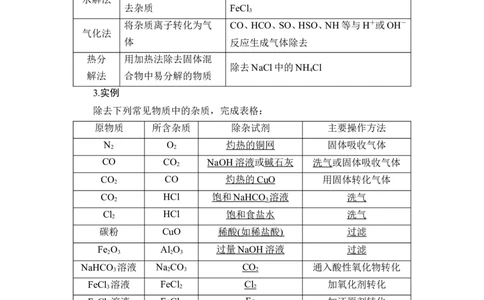
3.实例
除去下列常见物质中的杂质,完成表格:
原物质 所含杂质 除杂试剂 主要操作方法
N O 灼热的铜网 固体吸收气体
2 2
CO CO NaOH 溶液 或碱石灰 洗气或固体吸收气体
2
CO CO 灼热的 CuO 用固体转化气体
2
CO HCl 饱和 NaHCO 溶液 洗气
2 3
Cl HCl 饱和食盐水 洗气
2
碳粉 CuO 稀酸 ( 如稀盐酸 ) 过滤
Fe O Al O 过量 NaOH 溶液 过滤
2 3 2 3
NaHCO 溶液 Na CO CO 通入酸性氧化物转化
3 2 3 2
FeCl 溶液 FeCl Cl 加氧化剂转化
3 2 2
FeCl 溶液 FeCl Fe 加还原剂转化
2 3
MgCl 溶液 FeCl MgO 过滤
2 3
乙酸乙酯 乙酸 饱和 N a CO 溶液 分液
2 3
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)将Cl 与HCl混合气体通过饱和食盐水可得到纯净的Cl ( )
2 2
(2)SO 中混有少量SO ,可以将混合气体通过浓硫酸除去( )
2 3
(3)除去食盐中混有的少量NH Cl:加过量的烧碱溶液后加热蒸干( )
4
(4)除去NO中混有的少量NO :用水洗涤后再干燥( )
2答案 (1)× (2)√ (3)× (4)√
考点一 分离与提纯的常用装置及物理方法
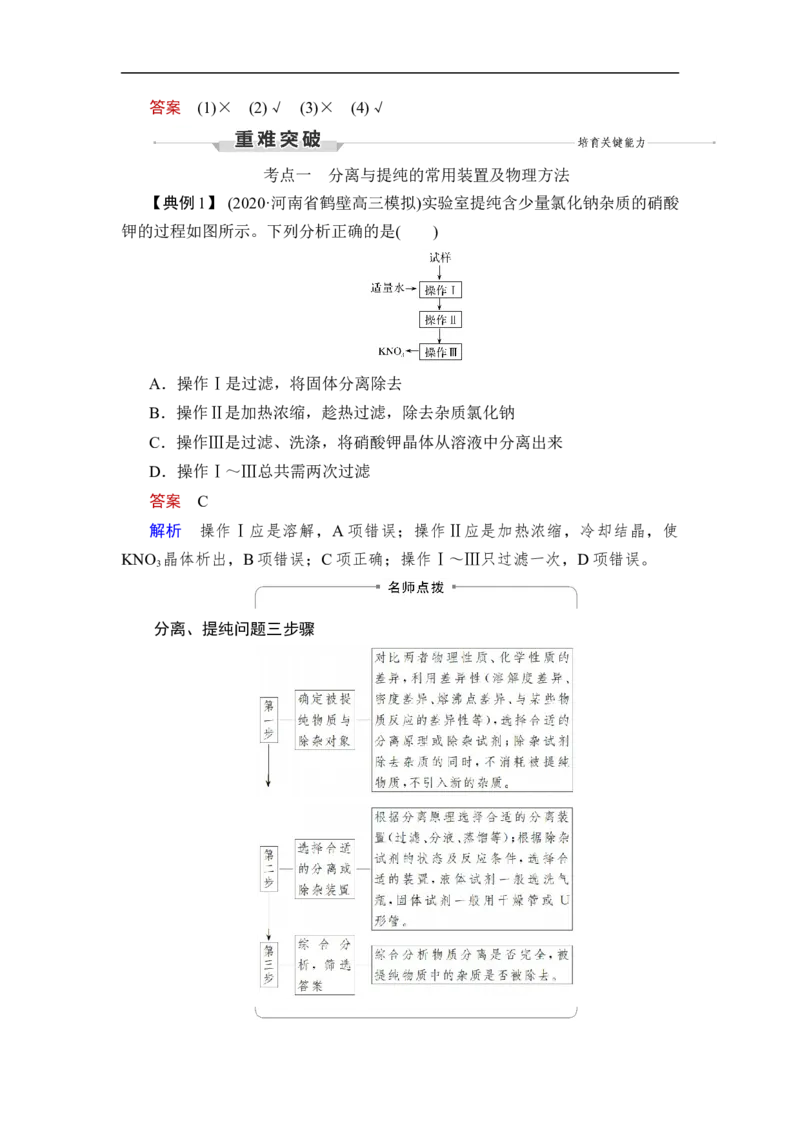
【典例1】 (2020·河南省鹤壁高三模拟)实验室提纯含少量氯化钠杂质的硝酸
钾的过程如图所示。下列分析正确的是( )
A.操作Ⅰ是过滤,将固体分离除去
B.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
C.操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D.操作Ⅰ~Ⅲ总共需两次过滤
答案 C
解析 操作Ⅰ应是溶解,A项错误;操作Ⅱ应是加热浓缩,冷却结晶,使
KNO 晶体析出,B项错误;C项正确;操作Ⅰ~Ⅲ只过滤一次,D项错误。
3
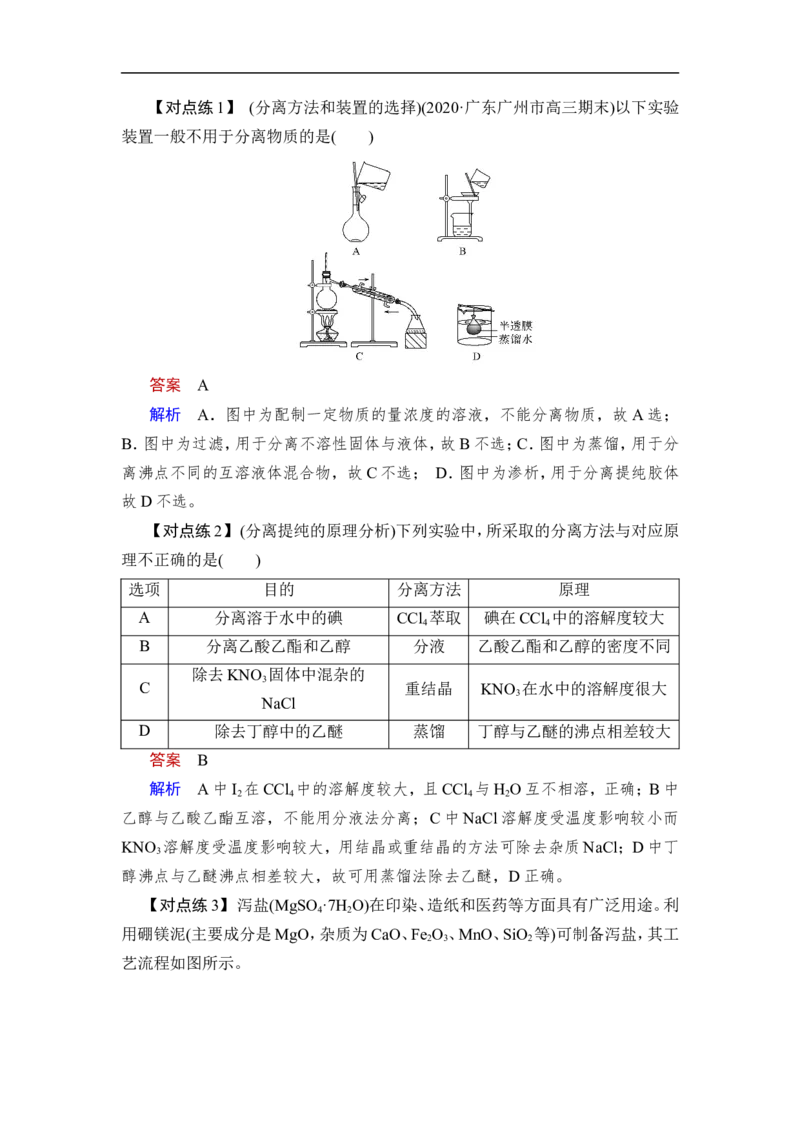
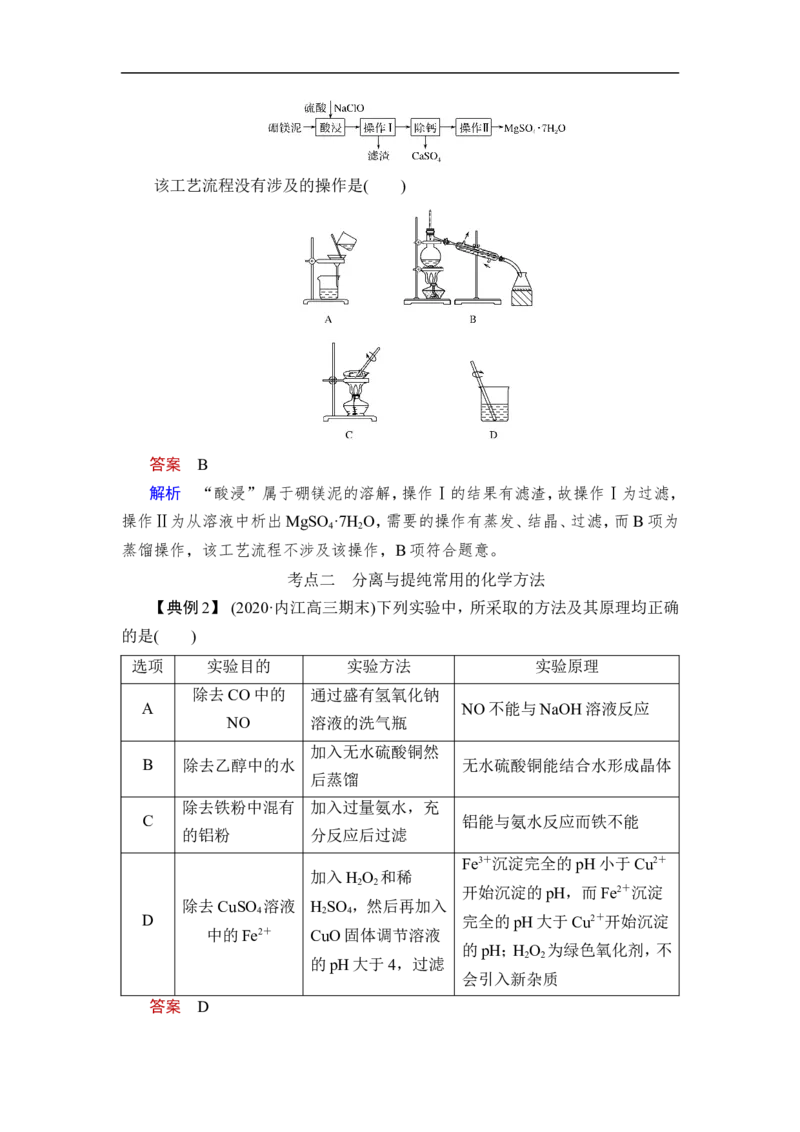
分离、提纯问题三步骤【对点练1】 (分离方法和装置的选择)(2020·广东广州市高三期末)以下实验
装置一般不用于分离物质的是( )
答案 A
解析 A.图中为配制一定物质的量浓度的溶液,不能分离物质,故A选;
B.图中为过滤,用于分离不溶性固体与液体,故B不选;C.图中为蒸馏,用于分
离沸点不同的互溶液体混合物,故C不选; D.图中为渗析,用于分离提纯胶体
故D不选。
【对点练2】 (分离提纯的原理分析)下列实验中,所采取的分离方法与对应原
理不正确的是( )
选项 目的 分离方法 原理
A 分离溶于水中的碘 CCl 萃取 碘在CCl 中的溶解度较大
4 4
B 分离乙酸乙酯和乙醇 分液 乙酸乙酯和乙醇的密度不同
除去KNO 固体中混杂的
3
C 重结晶 KNO 在水中的溶解度很大
3
NaCl
D 除去丁醇中的乙醚 蒸馏 丁醇与乙醚的沸点相差较大
答案 B
解析 A中I 在CCl 中的溶解度较大,且CCl 与H O互不相溶,正确;B中
2 4 4 2
乙醇与乙酸乙酯互溶,不能用分液法分离;C中NaCl溶解度受温度影响较小而
KNO 溶解度受温度影响较大,用结晶或重结晶的方法可除去杂质NaCl;D中丁
3
醇沸点与乙醚沸点相差较大,故可用蒸馏法除去乙醚,D正确。
【对点练3】 泻盐(MgSO ·7H O)在印染、造纸和医药等方面具有广泛用途。利
4 2
用硼镁泥(主要成分是MgO,杂质为CaO、Fe O 、MnO、SiO 等)可制备泻盐,其工
2 3 2
艺流程如图所示。该工艺流程没有涉及的操作是( )
答案 B
解析 “酸浸”属于硼镁泥的溶解,操作Ⅰ的结果有滤渣,故操作Ⅰ为过滤,
操作Ⅱ为从溶液中析出MgSO ·7H O,需要的操作有蒸发、结晶、过滤,而B项为
4 2
蒸馏操作,该工艺流程不涉及该操作,B项符合题意。
考点二 分离与提纯常用的化学方法
【典例2】 (2020·内江高三期末)下列实验中,所采取的方法及其原理均正确
的是( )
选项 实验目的 实验方法 实验原理
除去CO中的 通过盛有氢氧化钠
A NO不能与NaOH溶液反应
NO 溶液的洗气瓶
加入无水硫酸铜然
B 除去乙醇中的水 无水硫酸铜能结合水形成晶体
后蒸馏
除去铁粉中混有 加入过量氨水,充
C 铝能与氨水反应而铁不能
的铝粉 分反应后过滤
Fe3+沉淀完全的pH小于Cu2+
加入H O 和稀
2 2
开始沉淀的pH,而Fe2+沉淀
除去CuSO 溶液 H SO ,然后再加入
4 2 4
D 完全的pH大于Cu2+开始沉淀
中的Fe2+ CuO固体调节溶液
的pH;H O 为绿色氧化剂,不
2 2
的pH大于4,过滤
会引入新杂质
答案 D解析 NO不与NaOH溶液发生反应,A项错误;乙醇中的水加CaO再蒸馏
可除去,B项错误;Al、Fe均不能与氨水反应,C项错误。
【对点练4】 (除杂方案的判断)下列实验中,所采取的分离方法与对应原理都
正确的是( )
选项 实验目的 分离方法 原理
通入饱和Na CO 溶 HCl与Na CO 溶
2 3 2 3
A 除去CO 中的HCl
2
液洗气 液反应生成CO
2
乙醇和乙酸钙的
B 除去乙醇中少量的乙酸 加入足量生石灰蒸馏
沸点相差较大
冷却热饱和溶液进行 NaCl在水中的溶
C 除去KNO 固体中的NaCl
3
重结晶 解度很大
乙酸乙酯和乙醇
D 分离乙酸乙酯和乙醇 分液
的密度不同
答案 B
解析 饱和Na CO 溶液可吸收CO ,A项错误;用重结晶法除去KNO 固体
2 3 2 3
中的NaCl是因为KNO 在水中的溶解度受温度的影响大,C项错误;乙酸乙酯和
3
乙醇互溶,不能采取分液的方法分离,D项错误。
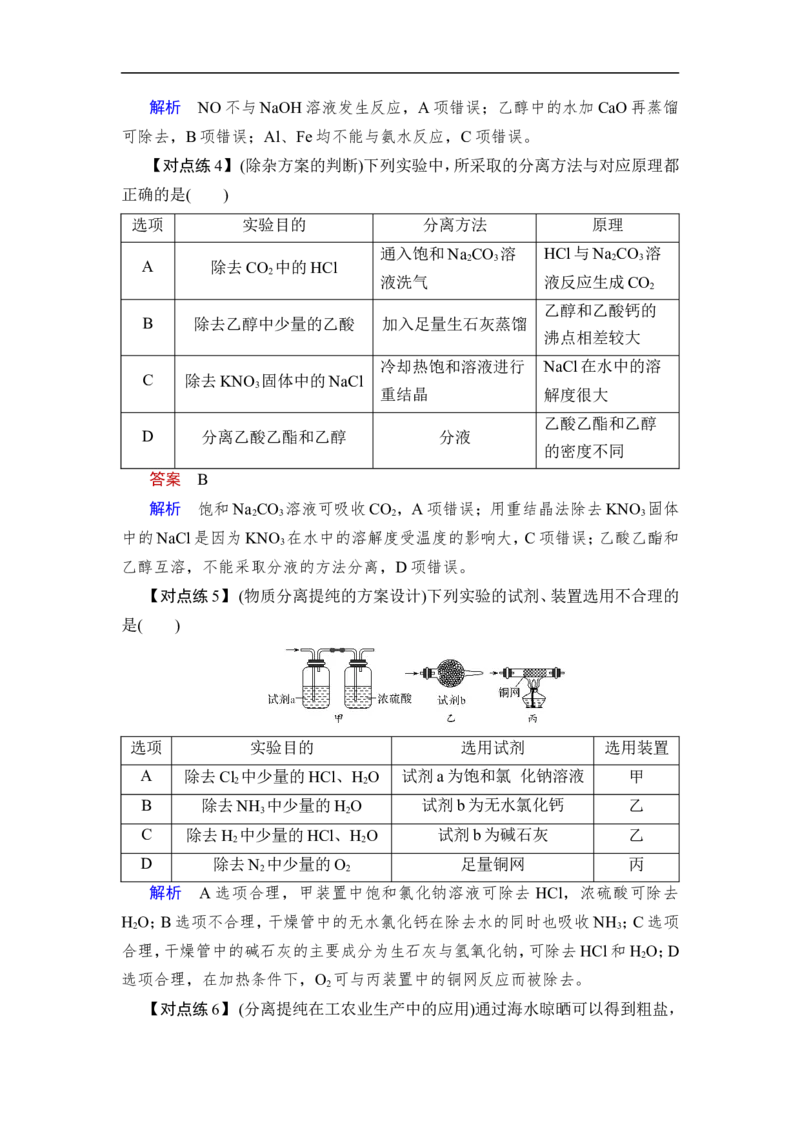
【对点练5】 (物质分离提纯的方案设计)下列实验的试剂、装置选用不合理的
是( )
选项 实验目的 选用试剂 选用装置
A 除去Cl 中少量的HCl、H O 试剂a为饱和氯 化钠溶液 甲
2 2
B 除去NH 中少量的H O 试剂b为无水氯化钙 乙
3 2
C 除去H 中少量的HCl、H O 试剂b为碱石灰 乙
2 2
D 除去N 中少量的O 足量铜网 丙
2 2
解析 A选项合理,甲装置中饱和氯化钠溶液可除去 HCl,浓硫酸可除去
H O;B选项不合理,干燥管中的无水氯化钙在除去水的同时也吸收NH ;C选项
2 3
合理,干燥管中的碱石灰的主要成分为生石灰与氢氧化钠,可除去HCl和H O;D
2
选项合理,在加热条件下,O 可与丙装置中的铜网反应而被除去。
2
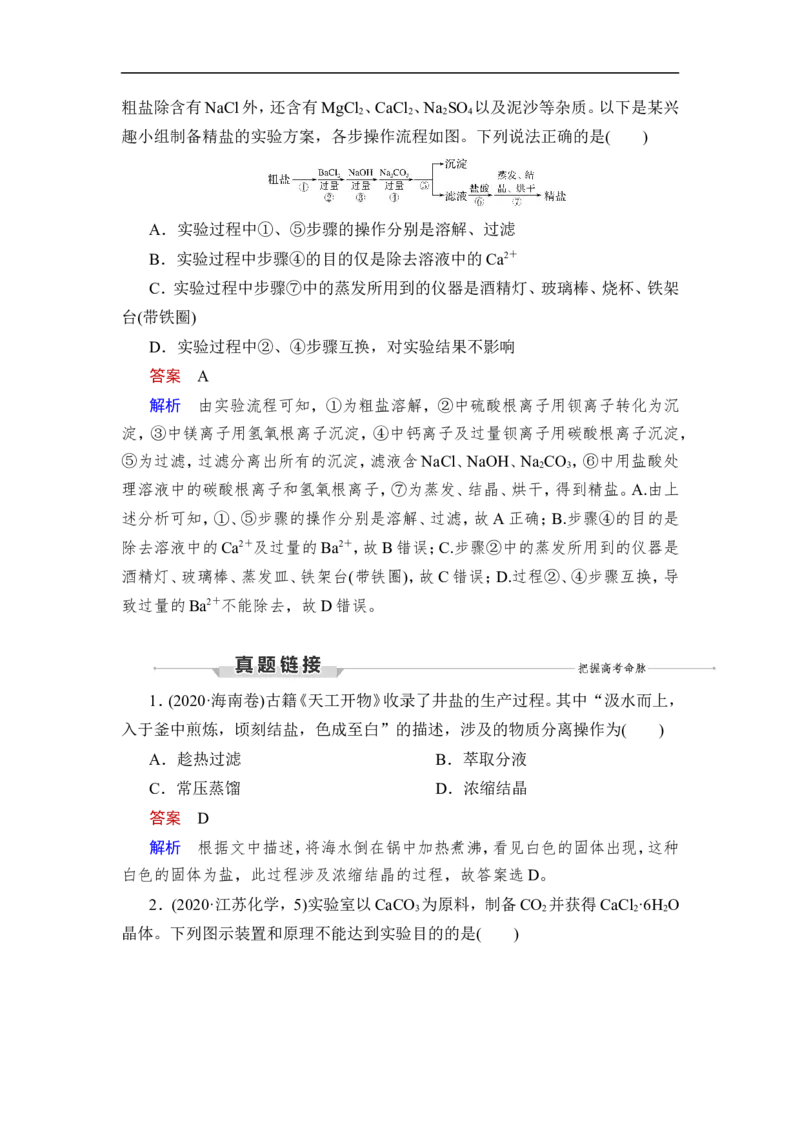
【对点练6】 (分离提纯在工农业生产中的应用)通过海水晾晒可以得到粗盐,粗盐除含有NaCl外,还含有MgCl 、CaCl 、Na SO 以及泥沙等杂质。以下是某兴
2 2 2 4
趣小组制备精盐的实验方案,各步操作流程如图。下列说法正确的是( )
A.实验过程中①、⑤步骤的操作分别是溶解、过滤
B.实验过程中步骤④的目的仅是除去溶液中的Ca2+
C.实验过程中步骤⑦中的蒸发所用到的仪器是酒精灯、玻璃棒、烧杯、铁架
台(带铁圈)
D.实验过程中②、④步骤互换,对实验结果不影响
答案 A
解析 由实验流程可知,①为粗盐溶解,②中硫酸根离子用钡离子转化为沉
淀,③中镁离子用氢氧根离子沉淀,④中钙离子及过量钡离子用碳酸根离子沉淀,
⑤为过滤,过滤分离出所有的沉淀,滤液含NaCl、NaOH、Na CO ,⑥中用盐酸处
2 3
理溶液中的碳酸根离子和氢氧根离子,⑦为蒸发、结晶、烘干,得到精盐。A.由上
述分析可知,①、⑤步骤的操作分别是溶解、过滤,故A正确;B.步骤④的目的是
除去溶液中的Ca2+及过量的Ba2+,故B错误;C.步骤②中的蒸发所用到的仪器是
酒精灯、玻璃棒、蒸发皿、铁架台(带铁圈),故C错误;D.过程②、④步骤互换,导
致过量的Ba2+不能除去,故D错误。
1.(2020·海南卷)古籍《天工开物》收录了井盐的生产过程。其中“汲水而上,
入于釜中煎炼,顷刻结盐,色成至白”的描述,涉及的物质分离操作为( )
A.趁热过滤 B.萃取分液
C.常压蒸馏 D.浓缩结晶
答案 D
解析 根据文中描述,将海水倒在锅中加热煮沸,看见白色的固体出现,这种
白色的固体为盐,此过程涉及浓缩结晶的过程,故答案选D。
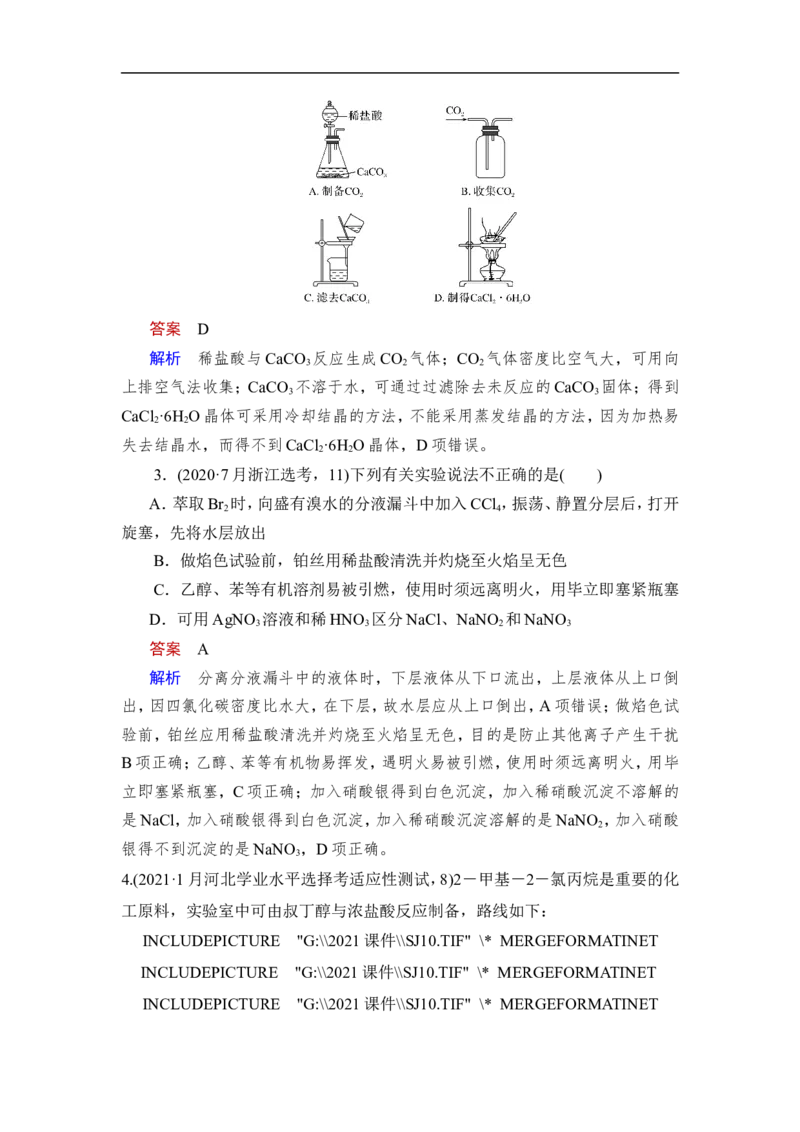
2.(2020·江苏化学,5)实验室以CaCO 为原料,制备CO 并获得CaCl ·6H O
3 2 2 2
晶体。下列图示装置和原理不能达到实验目的的是( )答案 D
解析 稀盐酸与CaCO 反应生成CO 气体;CO 气体密度比空气大,可用向
3 2 2
上排空气法收集;CaCO 不溶于水,可通过过滤除去未反应的CaCO 固体;得到
3 3
CaCl ·6H O晶体可采用冷却结晶的方法,不能采用蒸发结晶的方法,因为加热易
2 2
失去结晶水,而得不到CaCl ·6H O晶体,D项错误。
2 2
3.(2020·7月浙江选考,11)下列有关实验说法不正确的是( )
A.萃取Br 时,向盛有溴水的分液漏斗中加入CCl ,振荡、静置分层后,打开
2 4
旋塞,先将水层放出
B.做焰色试验前,铂丝用稀盐酸清洗并灼烧至火焰呈无色
C.乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞
D.可用AgNO 溶液和稀HNO 区分NaCl、NaNO 和NaNO
3 3 2 3
答案 A
解析 分离分液漏斗中的液体时,下层液体从下口流出,上层液体从上口倒
出,因四氯化碳密度比水大,在下层,故水层应从上口倒出,A项错误;做焰色试
验前,铂丝应用稀盐酸清洗并灼烧至火焰呈无色,目的是防止其他离子产生干扰
B项正确;乙醇、苯等有机物易挥发,遇明火易被引燃,使用时须远离明火,用毕
立即塞紧瓶塞,C项正确;加入硝酸银得到白色沉淀,加入稀硝酸沉淀不溶解的
是NaCl,加入硝酸银得到白色沉淀,加入稀硝酸沉淀溶解的是NaNO ,加入硝酸
2
银得不到沉淀的是NaNO ,D项正确。
3
4.(2021·1月河北学业水平选择考适应性测试,8)2-甲基-2-氯丙烷是重要的化
工原料,实验室中可由叔丁醇与浓盐酸反应制备,路线如下:
INCLUDEPICTURE "G:\\2021课件\\SJ10.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\SJ10.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\SJ10.TIF" \* MERGEFORMATINET下列说法错误的是( )
A.由叔丁醇制备2-甲基-2-氯丙烷的反应类型为取代反应
B.用5% Na CO 溶液洗涤分液时,有机相在分液漏斗的下层
2 3
C.无水CaCl 的作用是除去有机相中残存的少量水
2
D.蒸馏除去残余反应物叔丁醇时,产物先蒸馏出体系
答案 B
解析 对比反应前后有机物的结构可知,Cl原子取代了—OH,所以反应类型为
取代反应,A项正确;叔丁醇与浓盐酸反应后的体系中有机物主要为2-甲基-2
-氯丙烷,其密度小于水,则用5% Na CO 溶液洗涤分液时,有机相在分液漏斗
2 3
的上层,B错误;无水CaCl 是干燥剂,可以除去有机相中残存的少量水,C项正
2
确;2-甲基-2-氯丙烷比叔丁醇的沸点低,所以产物先蒸馏出体系,D项正确。
5.(2019·课标全国Ⅱ,28)咖啡因是一种生物碱(易溶于水及乙醇,熔点234.5
℃,100 ℃以上开始升华),有兴奋大脑神经和利尿等作用。茶叶中含咖啡因约1%
~5%、单宁酸(K 约为10-6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素
a
等。实验室从茶叶中提取咖啡因的流程如图所示。
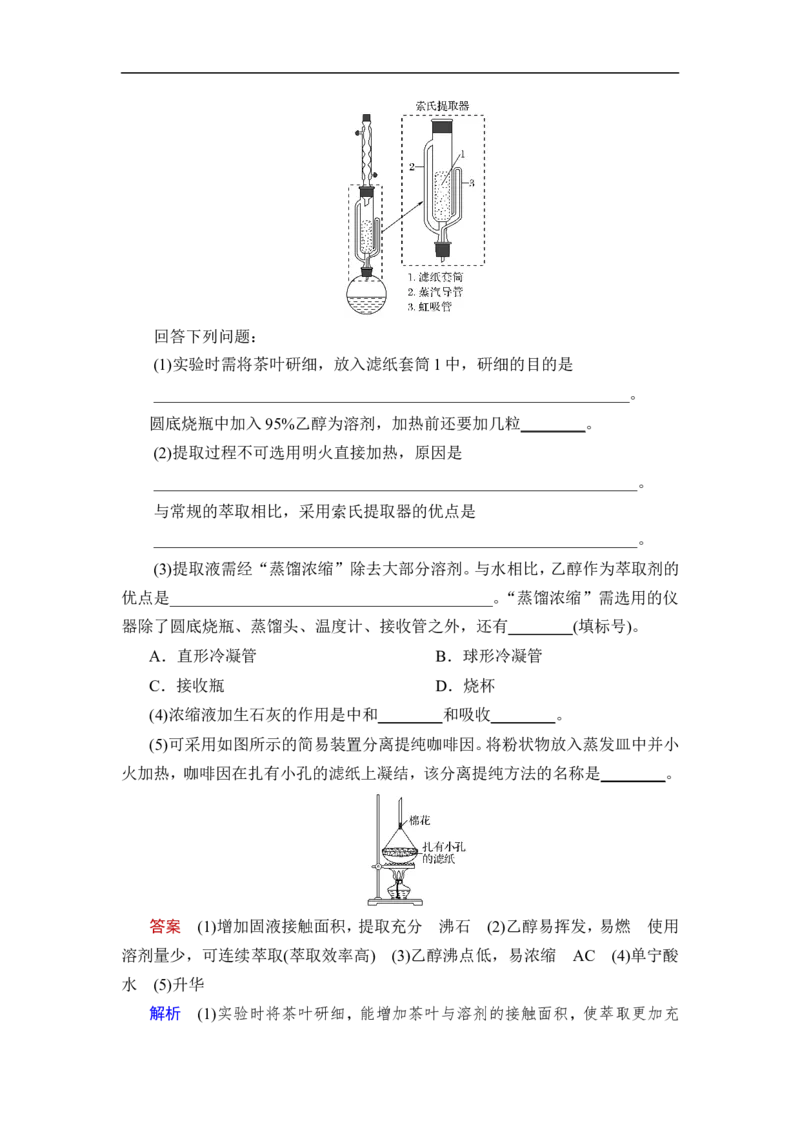
索氏提取装置如图所示。实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上
升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。萃取液液
面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。回答下列问题:
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是
___________________________________________________________。
圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒________。
(2)提取过程不可选用明火直接加热,原因是
____________________________________________________________。
与常规的萃取相比,采用索氏提取器的优点是
____________________________________________________________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。与水相比,乙醇作为萃取剂的
优点是________________________________________。“蒸馏浓缩”需选用的仪
器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有________(填标号)。
A.直形冷凝管 B.球形冷凝管
C.接收瓶 D.烧杯
(4)浓缩液加生石灰的作用是中和________和吸收________。
(5)可采用如图所示的简易装置分离提纯咖啡因。将粉状物放入蒸发皿中并小
火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是________。
答案 (1)增加固液接触面积,提取充分 沸石 (2)乙醇易挥发,易燃 使用
溶剂量少,可连续萃取(萃取效率高) (3)乙醇沸点低,易浓缩 AC (4)单宁酸
水 (5)升华
解析 (1)实验时将茶叶研细,能增加茶叶与溶剂的接触面积,使萃取更加充分。乙醇为溶剂,为防止加热时暴沸,需在加热前向乙醇中加入几粒沸石。(2)由于
溶剂乙醇具有挥发性和易燃性,因此在提取过程中不可用明火直接加热。本实验
中采用索氏提取器的优点是溶剂乙醇可循环使用,能减少溶剂用量,且萃取效率
高。(3)提取液需经“蒸馏浓缩”除去大部分溶剂,与水相比,乙醇作为萃取剂具
有沸点低和易浓缩的优点。“蒸馏浓缩”需选用的仪器除了所给仪器外,还有直
形冷凝管和接收瓶(如锥形瓶)。(4)向浓缩液中加入生石灰能中和单宁酸并吸收水
分。(5)结合分离提纯咖啡因的装置及将粉状物放入蒸发皿并小火加热,咖啡因凝
结在扎有小孔的滤纸上,可知该分离提纯的方法为升华。
一、选择题(每小题只有一个选项符合题意)
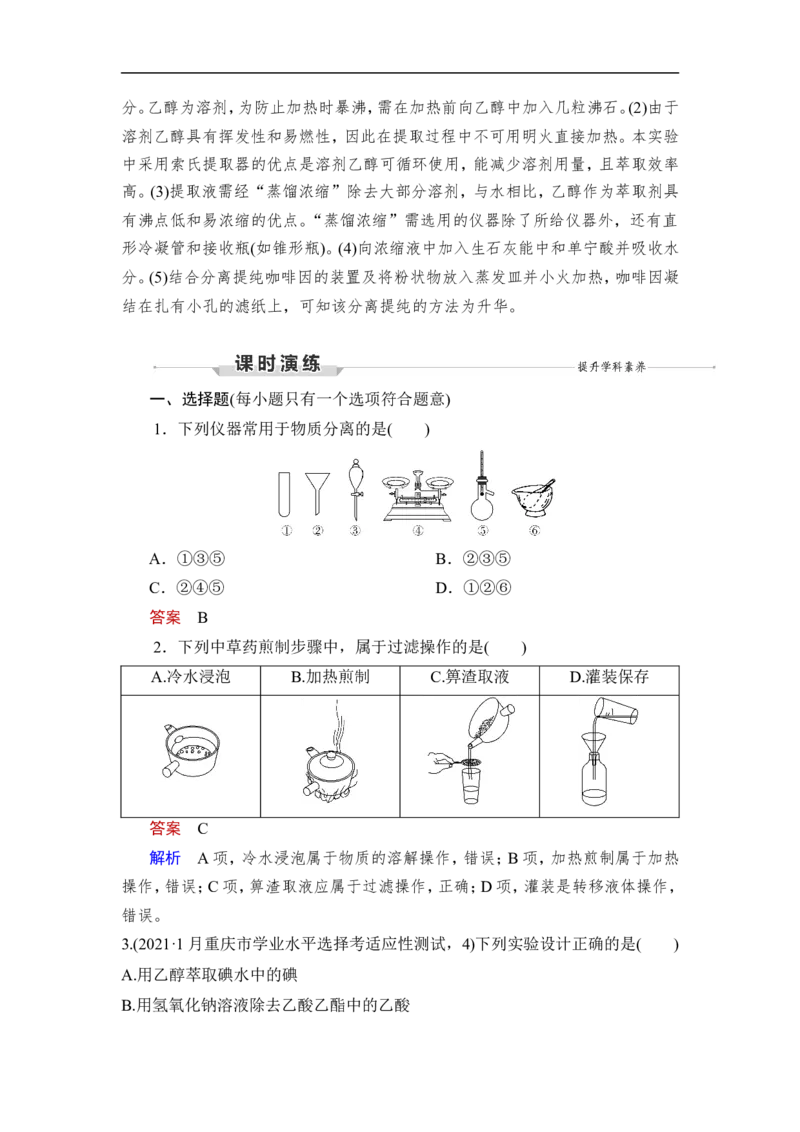
1.下列仪器常用于物质分离的是( )
A.①③⑤ B.②③⑤
C.②④⑤ D.①②⑥
答案 B
2.下列中草药煎制步骤中,属于过滤操作的是( )
A.冷水浸泡 B.加热煎制 C.箅渣取液 D.灌装保存
答案 C
解析 A项,冷水浸泡属于物质的溶解操作,错误;B项,加热煎制属于加热
操作,错误;C项,箅渣取液应属于过滤操作,正确;D项,灌装是转移液体操作,
错误。
3.(2021·1月重庆市学业水平选择考适应性测试,4)下列实验设计正确的是( )
A.用乙醇萃取碘水中的碘
B.用氢氧化钠溶液除去乙酸乙酯中的乙酸C.向乙醇和乙酸中分别加入钠,比较其官能团的活泼性
D.向蔗糖和稀硫酸共热后的溶液中加入少量银氨溶液,检验生成的葡萄糖
答案 C
解析 A项,乙醇与水互溶,不用作碘水中碘的萃取剂,错误;B项,乙酸乙酯
在NaOH溶液中水解,错误;C项,钠在乙酸中反应速率快,说明羧基中羟基的活
泼性强于乙醇中羟基的活泼性,正确;D项,银镜反应需要在碱性条件下进行,因
此在加银氨溶液前,先加NaOH中和稀硫酸,错误。
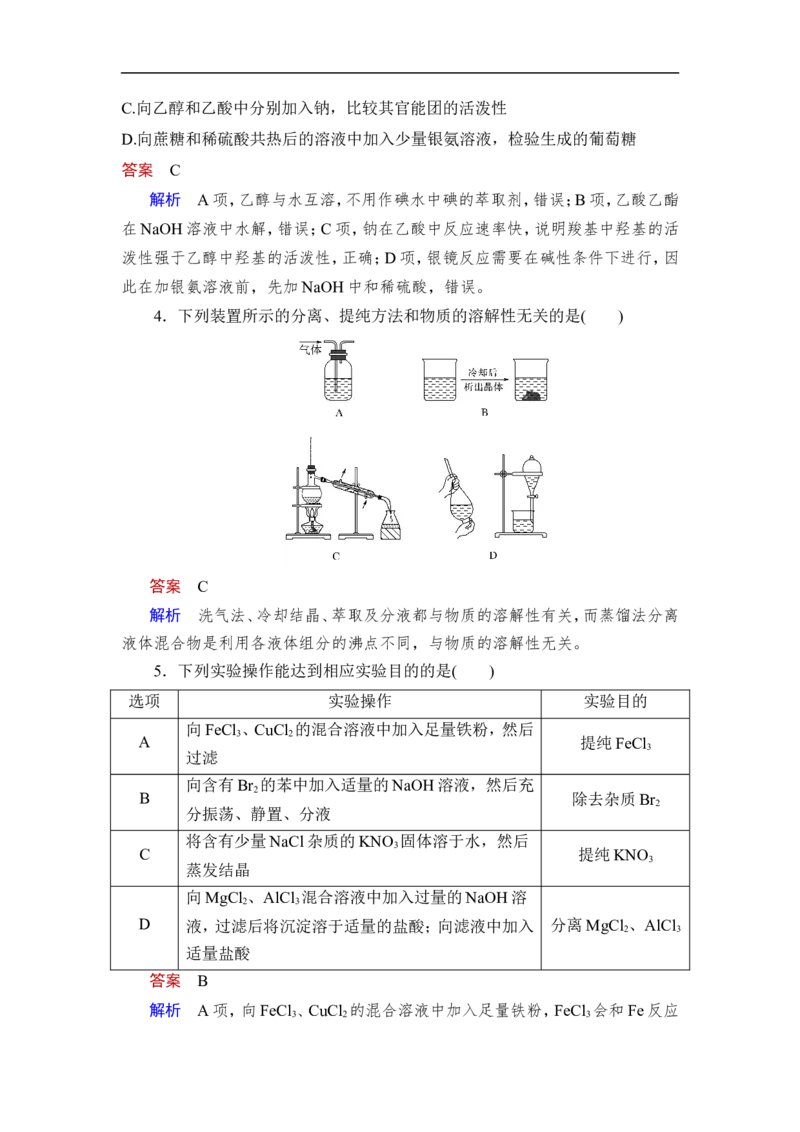
4.下列装置所示的分离、提纯方法和物质的溶解性无关的是( )
答案 C
解析 洗气法、冷却结晶、萃取及分液都与物质的溶解性有关,而蒸馏法分离
液体混合物是利用各液体组分的沸点不同,与物质的溶解性无关。
5.下列实验操作能达到相应实验目的的是( )
选项 实验操作 实验目的
向FeCl 、CuCl 的混合溶液中加入足量铁粉,然后
3 2
A 提纯FeCl
3
过滤
向含有Br 的苯中加入适量的NaOH溶液,然后充
2
B 除去杂质Br
2
分振荡、静置、分液
将含有少量NaCl杂质的KNO 固体溶于水,然后
3
C 提纯KNO
3
蒸发结晶
向MgCl 、AlCl 混合溶液中加入过量的NaOH溶
2 3
D 液,过滤后将沉淀溶于适量的盐酸;向滤液中加入 分离MgCl 、AlCl
2 3
适量盐酸
答案 B
解析 A项,向FeCl 、CuCl 的混合溶液中加入足量铁粉,FeCl 会和Fe反应
3 2 3生成FeCl ,错误;B项,Br 和NaOH溶液反应生成易溶于水的NaBr和NaBrO,
2 2
充分振荡、静置、分液可以除去杂质Br ,正确;C项,KNO 的溶解度随温度升高
2 3
变化较大,而NaCl的溶解度受温度影响不大,要提纯KNO ,将含有少量NaCl杂
3
质的KNO 固体溶于水,蒸发浓缩、冷却结晶,然后过滤即可得较纯净的KNO ,
3 3
错误;D项,滤液中含有NaCl,得不到纯净的AlCl 溶液,错误。
3
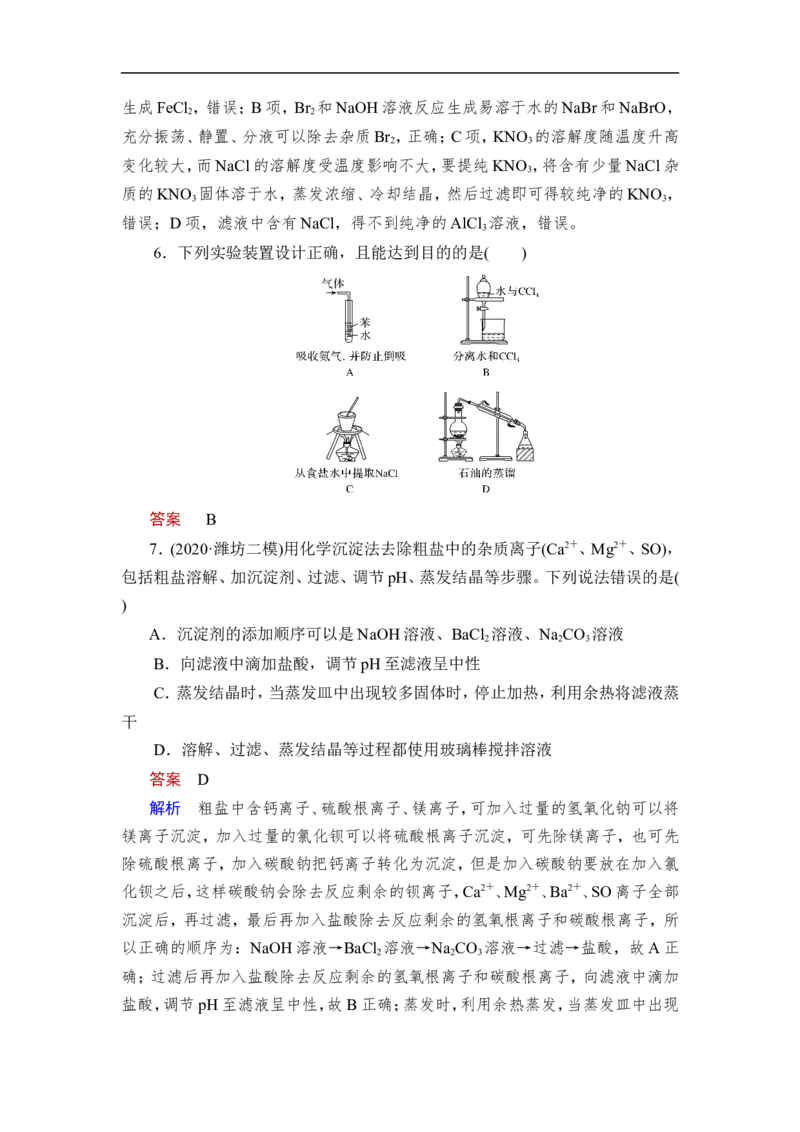
6.下列实验装置设计正确,且能达到目的的是( )
答案 B
7.(2020·潍坊二模)用化学沉淀法去除粗盐中的杂质离子(Ca2+、Mg2+、SO),
包括粗盐溶解、加沉淀剂、过滤、调节pH、蒸发结晶等步骤。下列说法错误的是(
)
A.沉淀剂的添加顺序可以是NaOH溶液、BaCl 溶液、Na CO 溶液
2 2 3
B.向滤液中滴加盐酸,调节pH至滤液呈中性
C.蒸发结晶时,当蒸发皿中出现较多固体时,停止加热,利用余热将滤液蒸
干
D.溶解、过滤、蒸发结晶等过程都使用玻璃棒搅拌溶液
答案 D
解析 粗盐中含钙离子、硫酸根离子、镁离子,可加入过量的氢氧化钠可以将
镁离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,可先除镁离子,也可先
除硫酸根离子,加入碳酸钠把钙离子转化为沉淀,但是加入碳酸钠要放在加入氯
化钡之后,这样碳酸钠会除去反应剩余的钡离子,Ca2+、Mg2+、Ba2+、SO离子全部
沉淀后,再过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所
以正确的顺序为:NaOH溶液→BaCl 溶液→Na CO 溶液→过滤→盐酸,故A正
2 2 3
确;过滤后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,向滤液中滴加
盐酸,调节pH至滤液呈中性,故B正确;蒸发时,利用余热蒸发,当蒸发皿中出现较多固体时,停止加热,故C正确;过滤操作中玻璃棒是引流作用,不能搅拌,故
D错误。
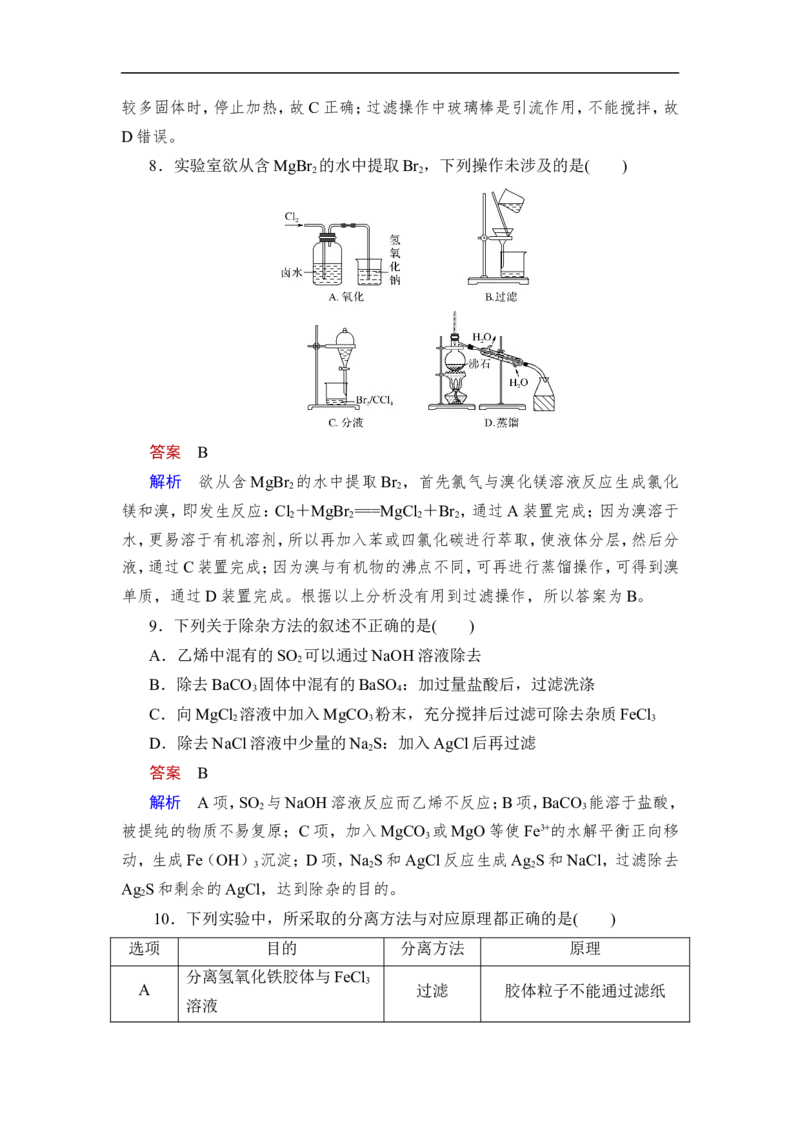
8.实验室欲从含MgBr 的水中提取Br ,下列操作未涉及的是( )
2 2
答案 B
解析 欲从含MgBr 的水中提取Br ,首先氯气与溴化镁溶液反应生成氯化
2 2
镁和溴,即发生反应:Cl +MgBr ===MgCl +Br ,通过A装置完成;因为溴溶于
2 2 2 2
水,更易溶于有机溶剂,所以再加入苯或四氯化碳进行萃取,使液体分层,然后分
液,通过C装置完成;因为溴与有机物的沸点不同,可再进行蒸馏操作,可得到溴
单质,通过D装置完成。根据以上分析没有用到过滤操作,所以答案为B。
9.下列关于除杂方法的叙述不正确的是( )
A.乙烯中混有的SO 可以通过NaOH溶液除去
2
B.除去BaCO 固体中混有的BaSO :加过量盐酸后,过滤洗涤
3 4
C.向MgCl 溶液中加入MgCO 粉末,充分搅拌后过滤可除去杂质FeCl
2 3 3
D.除去NaCl溶液中少量的Na S:加入AgCl后再过滤
2
答案 B
解析 A项,SO 与NaOH溶液反应而乙烯不反应;B项,BaCO 能溶于盐酸,
2 3
被提纯的物质不易复原;C项,加入MgCO 或MgO等使Fe3+的水解平衡正向移
3
动,生成Fe(OH)沉淀;D项,Na S和AgCl反应生成Ag S和NaCl,过滤除去
3 2 2
Ag S和剩余的AgCl,达到除杂的目的。
2
10.下列实验中,所采取的分离方法与对应原理都正确的是( )
选项 目的 分离方法 原理
分离氢氧化铁胶体与FeCl
3
A 过滤 胶体粒子不能通过滤纸
溶液B 用乙醇提取碘水中的碘 萃取 碘在乙醇中的溶解度较大
用MgCl 溶液制备无水
2
C 蒸发 MgCl 受热不分解
2
MgCl 固体
2
D 除去丁醇中的乙醚 蒸馏 丁醇与乙醚的沸点相差较大
答案 D
解析 分离氢氧化铁胶体与FeCl 溶液,应用渗析的方法而不能使用过滤的
3
方法,因为胶体粒子能透过滤纸,不能透过半透膜,A项错误;乙醇与水互溶,不
能用作萃取碘水中的碘的萃取剂,B项错误;用MgCl 溶液制备无水MgCl 固体,
2 2
需要在HCl氛围中加热,目的是抑制Mg2+的水解,直接蒸发得不到无水MgCl
2
固体,C项错误;丁醇和乙醚互溶,但丁醇分子间形成氢键,沸点较高,二者沸点
相差较大,因此可用蒸馏的方法分离二者,D项正确。
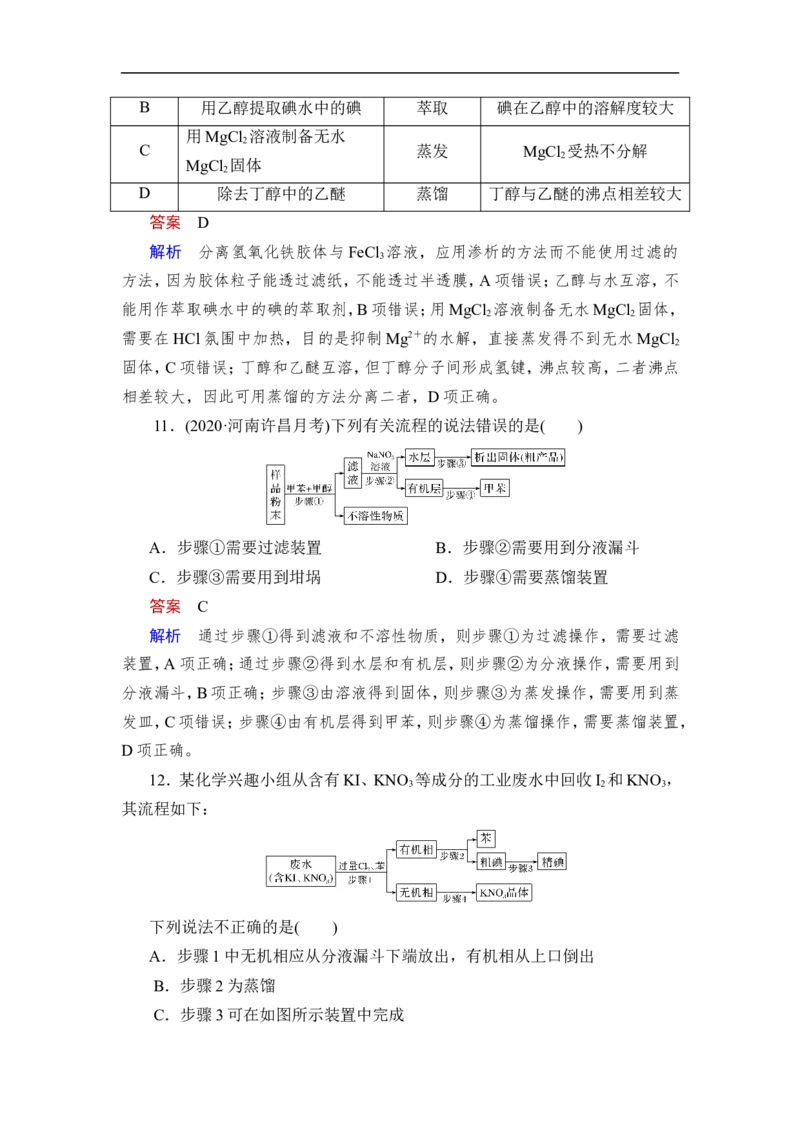
11.(2020·河南许昌月考)下列有关流程的说法错误的是( )
A.步骤①需要过滤装置 B.步骤②需要用到分液漏斗
C.步骤③需要用到坩埚 D.步骤④需要蒸馏装置
答案 C
解析 通过步骤①得到滤液和不溶性物质,则步骤①为过滤操作,需要过滤
装置,A项正确;通过步骤②得到水层和有机层,则步骤②为分液操作,需要用到
分液漏斗,B项正确;步骤③由溶液得到固体,则步骤③为蒸发操作,需要用到蒸
发皿,C项错误;步骤④由有机层得到甲苯,则步骤④为蒸馏操作,需要蒸馏装置,
D项正确。
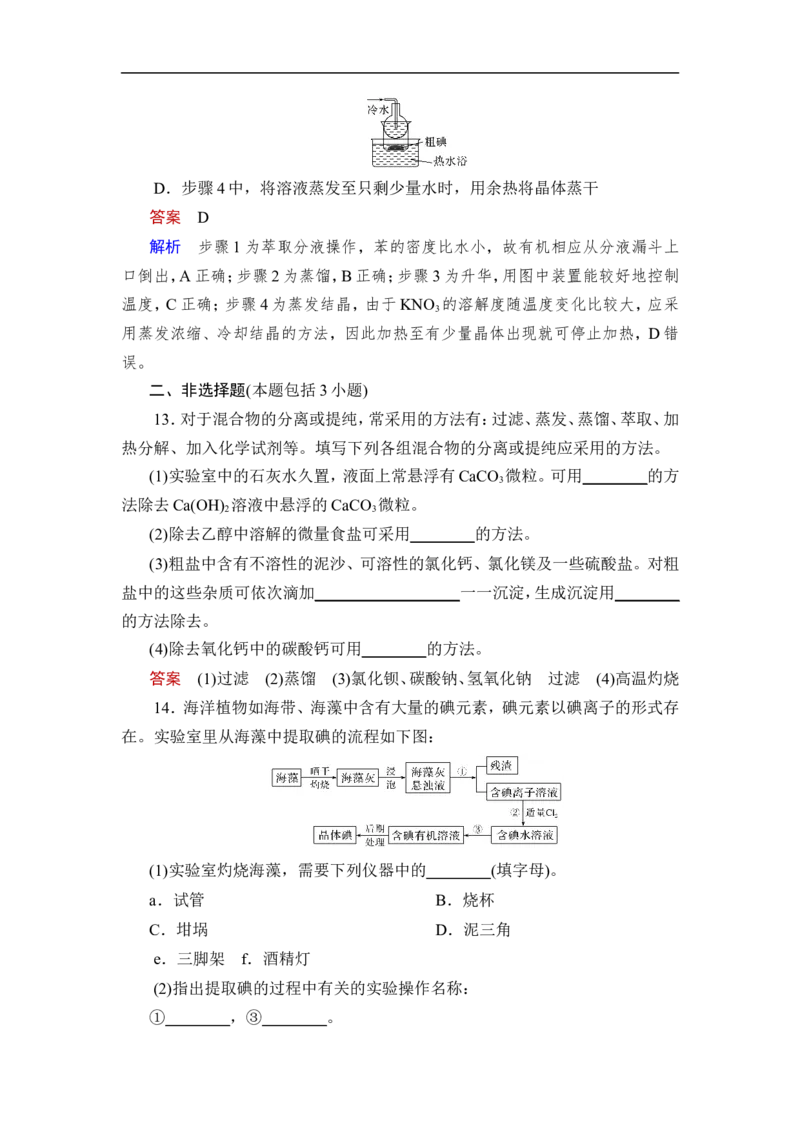
12.某化学兴趣小组从含有KI、KNO 等成分的工业废水中回收I 和KNO ,
3 2 3
其流程如下:
下列说法不正确的是( )
A.步骤1中无机相应从分液漏斗下端放出,有机相从上口倒出
B.步骤2为蒸馏
C.步骤3可在如图所示装置中完成D.步骤4中,将溶液蒸发至只剩少量水时,用余热将晶体蒸干
答案 D
解析 步骤1为萃取分液操作,苯的密度比水小,故有机相应从分液漏斗上
口倒出,A正确;步骤2为蒸馏,B正确;步骤3为升华,用图中装置能较好地控制
温度,C正确;步骤4为蒸发结晶,由于KNO 的溶解度随温度变化比较大,应采
3
用蒸发浓缩、冷却结晶的方法,因此加热至有少量晶体出现就可停止加热,D错
误。
二、非选择题(本题包括3小题)
13.对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、加
热分解、加入化学试剂等。填写下列各组混合物的分离或提纯应采用的方法。
(1)实验室中的石灰水久置,液面上常悬浮有CaCO 微粒。可用________的方
3
法除去Ca(OH) 溶液中悬浮的CaCO 微粒。
2 3
(2)除去乙醇中溶解的微量食盐可采用________的方法。
(3)粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐。对粗
盐中的这些杂质可依次滴加__________________一一沉淀,生成沉淀用________
的方法除去。
(4)除去氧化钙中的碳酸钙可用________的方法。
答案 (1)过滤 (2)蒸馏 (3)氯化钡、碳酸钠、氢氧化钠 过滤 (4)高温灼烧
14.海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存
在。实验室里从海藻中提取碘的流程如下图:
(1)实验室灼烧海藻,需要下列仪器中的________(填字母)。
a.试管 B.烧杯
C.坩埚 D.泥三角
e.三脚架 f.酒精灯
(2)指出提取碘的过程中有关的实验操作名称:
①________,③________。(3)提取碘的过程中,可选择的有机试剂是________(填字母)。
A.甲苯、酒精 B.四氯化碳、苯
C.汽油、乙酸 D.汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气
瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪
器有________、________。
(5)某小组同学用CCl 萃取碘水中的碘,在图中的分液漏斗中,下层液体呈
4
________色。
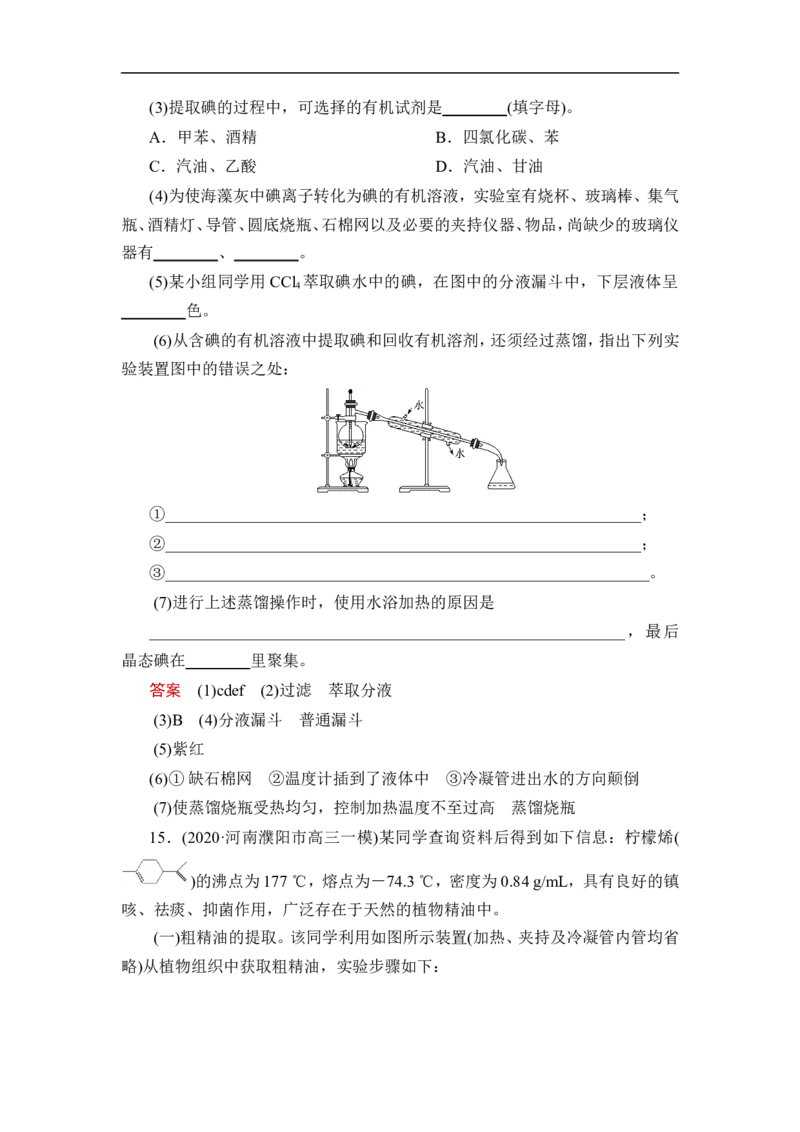
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下列实
验装置图中的错误之处:
①___________________________________________________________;
②___________________________________________________________;
③____________________________________________________________。
(7)进行上述蒸馏操作时,使用水浴加热的原因是
___________________________________________________________,最后
晶态碘在________里聚集。
答案 (1)cdef (2)过滤 萃取分液
(3)B (4)分液漏斗 普通漏斗
(5)紫红
(6)①缺石棉网 ②温度计插到了液体中 ③冷凝管进出水的方向颠倒
(7)使蒸馏烧瓶受热均匀,控制加热温度不至过高 蒸馏烧瓶
15.(2020·河南濮阳市高三一模)某同学查询资料后得到如下信息:柠檬烯(
)的沸点为177 ℃,熔点为-74.3 ℃,密度为0.84 g/mL,具有良好的镇
咳、祛痰、抑菌作用,广泛存在于天然的植物精油中。
(一)粗精油的提取。该同学利用如图所示装置(加热、夹持及冷凝管内管均省
略)从植物组织中获取粗精油,实验步骤如下:i.将几片桔子皮剪成细碎的碎片,投入乙装置中,加入约30 mL水;
ii.打开活塞K,加热甲至K处的支管口有大量水蒸气冒出时旋紧,再打开冷
凝水,水蒸气蒸馏即开始进行。可观察到在馏出液的水面上有一层很薄的油层。
(1)甲中长导管的作用是________。蒸馏结束时,应先将________,再停止加
热。
(2)冷凝管的内管应是________(填“蛇”“球”或“直”)形的。若冷却水从
b口进入,则对提取到精油量的影响情况是__________________________。
(二)柠檬烯的提取。
i.将馏出液加入到仪器A中,然后加入适量的CH Cl (沸点为40 ℃)萃取3次,
2 2
最后将萃取液置于干燥的锥形瓶中,并加入适量的试剂A干燥半个小时。
ii.将干燥好的溶液加入蒸馏烧瓶中,通过一系列操作,最后烧瓶中剩下的橙
黄色液体就是柠檬烯。
(3)仪器A是________,试剂A可以是________(写出两种)。若将一定量的橙
黄色液体滴入溴的 CCl 溶液中,溶液褪色,由此现象可得出的恰当结论是
4
____________________________________________________________。
(4)若桔皮总质量为a g,最后得到V mL柠檬烯,实验过程中柠檬烯的总损失
率为b% ,则桔皮中柠檬烯的质量分数为________%。
答案 (1)平衡压强 乙中的导气管从溶液中移出
(2)直 收集到的精油量减少
(3)分液漏斗 无水Na SO 、无水CaCl 柠檬烯中含有碳碳不饱和键
2 4 2
(4)
解析 (1)甲中长的玻璃导管一端与空气相通,其作用是安全管,能起到平衡
压强的作用;蒸馏结束时为防止倒吸现象的发生,应先将乙中的导气管从溶液中
移出液面;
(2)因蒸馏实验中冷凝管是倾斜的,为减少蒸馏液的积留,冷凝管内管应是直
形。若冷却水从b口进入,会导致冷凝效果较差,会有少量精油不能液化而损失
掉,这样会导致收集到的精油量减少;
(3)加入CH Cl 的目的是进行萃取作用,故操作应在分液漏斗中进行,仪器A
2 2
是分液漏斗。干燥的目的是除去残留的水分,故试剂A可以是无水CaCl 或无水
2Na SO 等。将一定量的橙黄色液体滴入溴的CCl 溶液中,溶液褪色,由此可知发
2 4 4
生了加成反应,故可证明柠檬烯中含有碳碳不饱和键;
(4)柠檬烯密度为0.84 g/mL收集到的柠檬烯体积为V mL,则其质量为0.84V
g,设桔子皮中柠檬烯的质量分数为x,
则ax(1-b%)=0.84V,解得x=×100%=%。
微专题40 有关沉淀洗涤的过程分析与规范解答
1.洗涤沉淀的目的
(1)若滤渣是所需的物质,洗涤的目的是除去其表面的可溶性杂质,得到更纯
净的沉淀物。
(2)若滤液是所需的物质,洗涤的目的是洗涤过滤所得到的滤渣,把有用的物
质如目标产物尽可能洗出来。
2.常用洗涤剂
(1)蒸馏水:主要适用于除去沉淀吸附的可溶性杂质。
(2)冷水:除去沉淀的可溶性杂质,降低沉淀在水中的溶解度而减少沉淀损失
(3)沉淀的饱和溶液:减小沉淀的溶解。
(4)有机溶剂(酒精、乙醚等):适用于易溶于水的固体,既减少了固体溶解,又
利用有机溶剂的挥发性,除去固体表面的水分,产品易干燥。
3.三套答题模板
(1)检验沉淀是否完全的答题模板
静置,取上层清液→加沉淀剂→有无沉淀→结论。
(2)沉淀洗涤的答题模板:
注洗涤液(沿玻璃棒向漏斗中注入洗涤液)
↓
标准(使洗涤液完全浸没沉淀或晶体)
↓
重复(待洗涤液流尽后,重复操作2~3次)
(3)检验沉淀是否洗净的答题模板:
取样(取少量最后一次洗涤液于一洁净的试管中)↓
加试剂[加入××试剂(必要时加热,如检验NH)]
↓
现象(不产生××沉淀、溶液不变××色或不产生××气体)
↓
结论(说明沉淀已经洗涤干净)
【典例】 硫酸亚铁是一种重要的食品和饲料添加剂。实验室通过如下实验由
废铁屑制备FeSO ·7H O晶体:
4 2
①将5%的Na CO 溶液加入盛有一定量废铁屑的烧杯中,加热数分钟,用倾
2 3
析法除去Na CO 溶液,然后将废铁屑用水洗涤2~3遍;
2 3
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80 ℃之间至铁
屑耗尽;
③________,将滤液转入密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO ·7H O晶体放在一个小广口瓶中,密闭保存。
4 2
请回答下列问题:
(1)实验步骤①的目的是__________________________________________。
(2)写出实验步骤②中的化学方程式:______________________________。
(3)补全实验步骤③的操作名称:________。
(4)实验步骤④中用少量冰水洗涤晶体,其目的是
______________________________________________________________。
(5)乙同学认为甲的实验方案中存在明显的不合理之处,乙同学判断的理由
是________________________________________________________________。
答案 (1)去除油污(或利用碳酸钠水解呈碱性的性质除去铁屑表面油污)
(2)Fe+H SO =====FeSO +H ↑
2 4 4 2
(3)趁热过滤
(4)洗去杂质,降低洗涤过程中FeSO ·7H O的损耗
4 2
(5)过量硫酸使铁粉耗尽,不能防止Fe2+被氧化
1.食盐是日常生活的必需品,也是重要的化工原料。粗食盐常含有少量K+、
Ca2+、Mg2+、Fe3+、SO等杂质离子,实验室提纯NaCl的流程如下:提供的试剂:饱和Na CO 溶液、饱和K CO 溶液、NaOH溶液、BaCl 溶液、
2 3 2 3 2
Ba(NO ) 溶液、75%乙醇、四氯化碳。选择最好的试剂洗涤除去NaCl晶体表面附
3 2
带的少量KCl,洗涤的操作为________________________________。
答案 沿玻璃棒向漏斗中注入75%乙醇,使溶液完全浸没NaCl晶体,待溶液
流尽后,重复操作2~3次
2.氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含
有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:
工 业 ZnO――→ 浸 出 液 ――――――――――――→――→ 滤
液――→――→滤液――→――→滤饼――→ZnO
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO 。
2
回答下列问题:
反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是
___________________________________________________________。
答案 取少量最后一次洗涤液于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡
溶液,若无白色沉淀生成,则说明沉淀已经洗涤干净