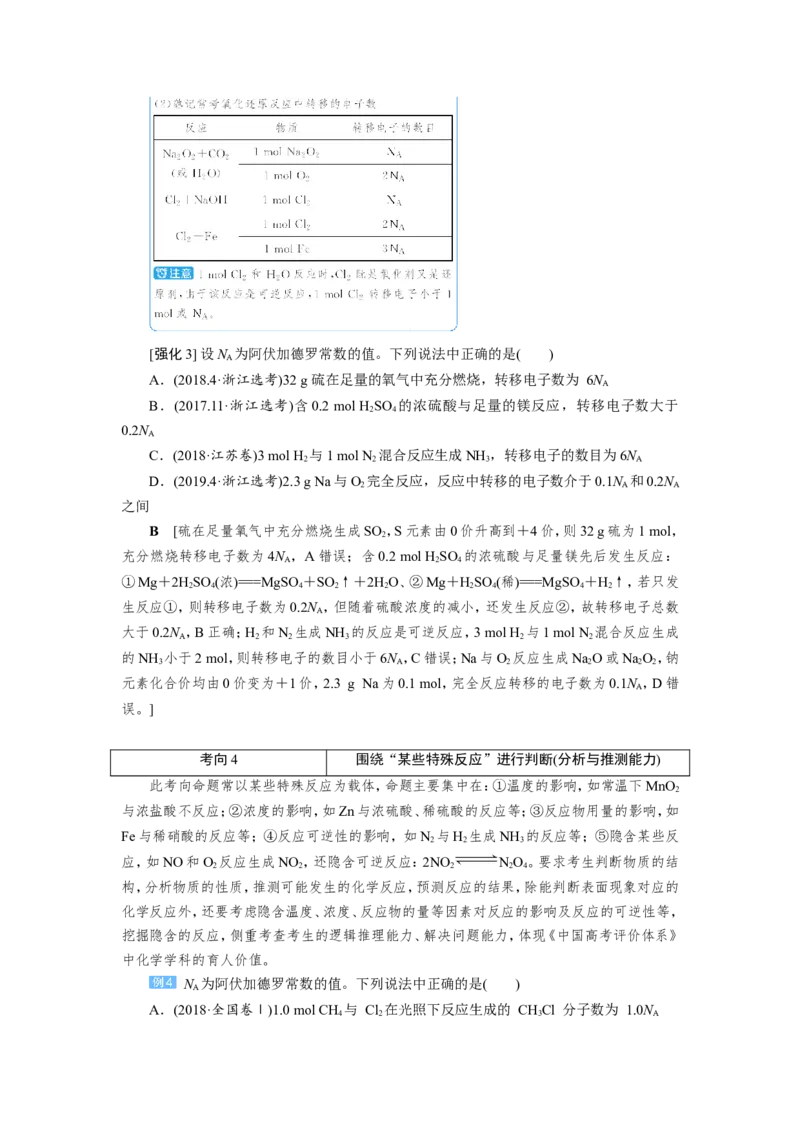
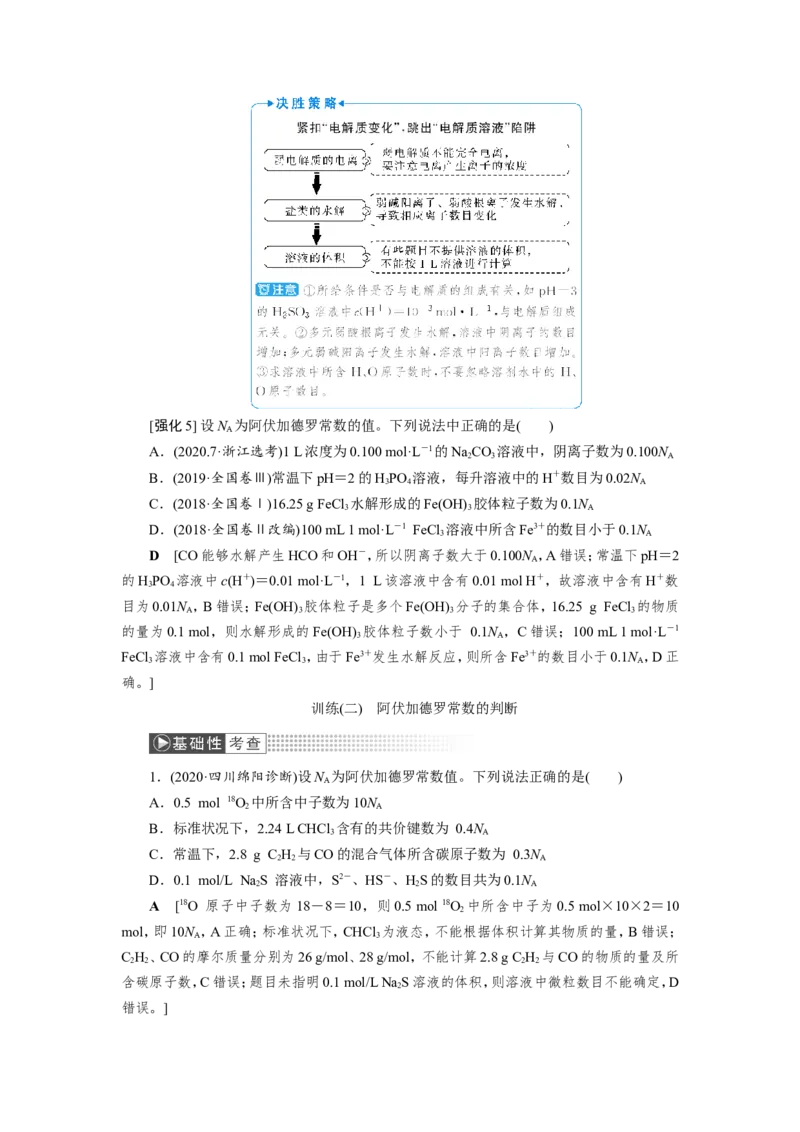
文档内容
第2课时 关键能力——阿伏加德罗常数的判断
阿伏加德罗常数问题是高考常考题型之一,此类试题以阿伏加德罗常数为核心,以中学
所学过的一些重要物质为载体,将微观粒子(原子、分子、离子等)数目与物质的量、摩尔质量、
气体的体积(标准状况)、物质的量浓度等联系起来,突出考查考生的理解与辨析能力、分析与
推测能力,要求考生掌握基础知识、辨析基本概念、获取有关信息,并在此基础上判断物质结
构、分析物质性质、推断反应结果、处理转化数据等。
计算N(微粒数)的基本思路如下图所示:
—————————————————————————————————————
————————————————
考向1 围绕“V =22.4 L·mol-1” 的使用条件进行判断(理解与辨析能力)
m
此考向设置错误的两种常见方式:一是给出标准状况这一条件,但提供物质呈液态或固
态;二是提供物质是气体,但处于常温常压下或不提供气体所处的状况(温度和压强)。要求考
生掌握基础知识(阿伏加德罗常数、气体摩尔体积、阿伏加德罗定律等),判断物质结构(无机
物或有机物),根据物质的性质推测反应结果,确定物质所含分子数、原子数、共价键数、转移
电子数等,并能融会贯通,解决简单化学问题。
设N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.(2020·全国卷Ⅲ)22.4 L(标准状况)氮气中含有7 N 个中子
A
B.(2018·全国卷Ⅰ)22.4 L(标准状况)氩气含有的质子数为18 N
A
C.(2018·全国卷Ⅲ)常温常压下,124 g P 中所含 P-P 键数目为4 N
4 A
D.(2017·全国卷Ⅱ)标准状况下,2.24 L N 和O 的混合气体中分子数为0.2 N
2 2 A
B [标准状况下,22.4 L氮气的物质的量为1 mol,一个氮气分子中含有14个中子,故1
mol氮气中含有14N 个中子,A错误;标准状况下22.4 L氩气为1 mol, 1个氩气分子含有18
A个质子,则含有的质子数为 18N ,B正确;1个P 分子(白磷,分子结构为 )含有6个
A 4
P—P键,124 g P 的物质的量为1 mol,则所含P—P 键数目为6N ,C错误;标准状况下,
4 A
2.24 L N 和O 的混合气体的总物质的量为0.1 mol,则含有的分子数为0.1N ,D错误。]
2 2 A
[强化1] 设N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.常温常压下,11.2 L NH 中含有的氢原子数为1.5N
3 A
B.常温常压下,16 g O 和O 的混合气体中所含氧原子数为N
2 3 A
C.标准状况下,22.4 L水含有的分子数为N
A
D.2.24 L CO和CO 混合气体中含有的碳原子数目为0.1N
2 A
B [常温常压下,V 不等于22.4 L·mol-1,则11.2 L NH 的物质的量不是0.5 mol,故
m 3
含有的氢原子数不是1.5N ,A项错误;16 g O 和O 的混合气体所含氧原子的物质的量为
A 2 3
16 g/(16 g·mol-1)=1 mol,则所含氧原子数为N ,B项正确;标准状况下水是非气体,22.4
A
L HO的物质的量远大于1 mol,则含有的分子数远大于N ,C项错误;题目未指明2.24 L
2 A
CO和CO 混合气体所处的状况(温度和压强),无法根据其体积计算物质的量,D项错误。]
2
考向2 围绕“物质的组成与结构”进行判断(分析与推测能力)
此考向涉及试题中常考内容:①物质中所含的微粒数目,如原子数、分子数、离子数、质
子数、中子数、电子数等,考查核素及质量数、质子数和中子数之间关系的题目较多;②物质
中存在化学键的数目,主要是共价键。要求考生掌握基础知识(教材中常见物质的组成及结
构),分析物质的组成与结构,推测物质所含分子数、原子数、共价键数、转移电子数等,同时
要求考生能够透过现象看到本质,能够从多个视角观察、思考同一个问题。
设N 为阿伏加德罗常数的值。下列说法中不正确的是( )
A
A.(2020·全国卷Ⅲ)1 mol重水比1 mol水多N 个质子
A
B.(2020·全国卷Ⅲ)12 g石墨烯和12 g金刚石均含有N 个碳原子
A
C.(2019·全国卷Ⅱ)3 g 3He含有的中子数为1N
A
D.(2019·全国卷Ⅱ)48 g正丁烷和10 g异丁烷的混合物中共价键数目为13N
AA [一个重水分子和一个普通水分子都是由2个氢原子和1个氧原子构成的,所含质子
数都是10,故1 mol重水和1 mol水所含质子数相等,A错误;石墨烯和金刚石都是碳元素形
成的单质,12 g石墨烯和12 g金刚石中都含有1 mol碳原子,B正确;3He的质子数为2,中
子数为1,3 g 3He为1 mol,中子数为1 mol,C正确;正丁烷和异丁烷互为同分异构体,1分
子的正丁烷和异丁烷含有的共价键数均为13,混合物中含有的共价键数为×13+×13=13
mol,D正确。]
[强化2] N 为阿伏加德罗常数的值。下列说法中不正确的是( )
A
A.(2018·海南卷)12 g金刚石中含有化学键的数目为4N
A
B.(2018.11·浙江选考)2 g由HO和2HO组成的物质中含有的质子数为N
2 2 A
C.(2019.4·浙江选考)1 mol CH ===CH 分子中含有的共价键数为6 N
2 2 A
D.(2019.4·浙江选考)30 g HCHO与CHCOOH混合物中含C原子数为N
3 A
A [金刚石中每个碳原子形成4个C—C键,每个C—C键被两个碳原子共用,实际上
每个碳原子相当于形成2个共价键,12 g金刚石中含有1 mol碳,则含有化学键的数目为
2N ,A项错误;1个HO分子和1个2HO分子均含有10个质子,HO和2HO的摩尔质量均
A 2 2 2 2
为20 g·mol-1,则2 g由HO和2HO组成物质的总物质的量为0.1 mol,故含有的质子数为
2 2
N ,B项正确;1个CH===CH 分子含有6个共价键(碳碳双键看作2个共价键),则1 mol
A 2 2
CH===CH 分子中含有的共价键数为6N ,C项正确;30 g HCHO的物质的量为1 mol,含
2 2 A
C原子数为N ,而30 g CHCOOH 的物质的量为0.5 mol,含C原子数为N ,故30 g
A 3 AHCHO与CHCOOH混合物中含C原子数为N ,D项正确。]
3 A
考向3 围绕“氧化还原反应中转移电子数目”进行判断(分析与推测能力)
此考向命题主要集中在某些特殊氧化还原反应上,常考点有:①“歧化反应”中转移电
子数目,如Cl 与NaOH溶液的反应、NaO 与CO 或HO(g)的反应等;②变价金属单质与氧
2 2 2 2 2
化性酸反应,如Fe与硝酸反应时,HNO 足量生成Fe3+,HNO 不足生成Fe2+;③变价金属单
3 3
质与不同氧化剂的反应,如Cu与Cl、S的反应等。要求考生基于对化学反应规律的认识,根
2
据物质的结构特征、化学原理,推测简单反应的过程、机理及反应结果,从微观角度(电子转
移)认识化学反应的本质,体现物质观、微粒观、变化观等基本观念。
N 为阿伏加德罗常数的值。下列说法中不正确的是( )
A
A.(2020.7·浙江选考)4MnO+5HCHO+12H+===4Mn2++5CO↑+11HO,1 mol
2 2
[4MnO+5HCHO]完全反应转移的电子数为20N
A
B.(2020.7·浙江选考)用电解粗铜的方法精炼铜,当电路中通过的电子数为N 时,阳极应
A
有32g Cu转化为Cu2+
C.(2020.1·浙江选考)Cr O+14H++ne-===2Cr3++7HO,则每生成1 mol Cr3+转移电子
2 2
数为3N
A
D.(2019·全国卷Ⅱ)1 mol K Cr O 被还原为Cr3+转移的电子数为6N
2 2 7 A
B [该反应转移20个电子,即1 mol[4MnO+5HCHO]完全反应转移电子数为20N ,A
A
正确;电解精炼铜的装置中,阳极首先是比铜活泼的Fe、Zn等金属放电,所以当通过的电子
数为N 时,阳极发生反应的Cu可能少于32 g,B错误;铬元素由+6价降低到+3价,则生成
A
1 mol Cr3+转移电子数为3N ,C正确;KCr O 被还原为Cr3+时,Cr元素由+6价降低到+3
A 2 2 7
价,则1 mol K Cr O 被还原为Cr3+转移的电子数为6N ,D 正确。]
2 2 7 A[强化3] 设N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.(2018.4·浙江选考)32 g 硫在足量的氧气中充分燃烧,转移电子数为 6N
A
B.(2017.11·浙江选考)含0.2 mol H SO 的浓硫酸与足量的镁反应,转移电子数大于
2 4
0.2N
A
C.(2018·江苏卷)3 mol H 与1 mol N 混合反应生成NH ,转移电子的数目为6N
2 2 3 A
D.(2019.4·浙江选考)2.3 g Na与O 完全反应,反应中转移的电子数介于0.1N 和0.2N
2 A A
之间
B [硫在足量氧气中充分燃烧生成SO ,S元素由0价升高到+4价,则32 g硫为1 mol,
2
充分燃烧转移电子数为4N ,A错误;含0.2 mol HSO 的浓硫酸与足量镁先后发生反应:
A 2 4
①Mg+2HSO (浓)===MgSO +SO ↑+2HO、②Mg+HSO (稀)===MgSO +H↑,若只发
2 4 4 2 2 2 4 4 2
生反应①,则转移电子数为0.2N ,但随着硫酸浓度的减小,还发生反应②,故转移电子总数
A
大于0.2N ,B正确;H 和N 生成NH 的反应是可逆反应,3 mol H 与1 mol N 混合反应生成
A 2 2 3 2 2
的NH 小于2 mol,则转移电子的数目小于6N ,C错误;Na与O 反应生成NaO或NaO,钠
3 A 2 2 2 2
元素化合价均由0价变为+1价,2.3 g Na为0.1 mol,完全反应转移的电子数为0.1N ,D错
A
误。]
考向4 围绕“某些特殊反应”进行判断(分析与推测能力)
此考向命题常以某些特殊反应为载体,命题主要集中在:①温度的影响,如常温下MnO
2
与浓盐酸不反应;②浓度的影响,如Zn与浓硫酸、稀硫酸的反应等;③反应物用量的影响,如
Fe与稀硝酸的反应等;④反应可逆性的影响,如N 与H 生成NH 的反应等;⑤隐含某些反
2 2 3
应,如NO和O 反应生成NO ,还隐含可逆反应:2NO NO。要求考生判断物质的结
2 2 2 2 4
构,分析物质的性质,推测可能发生的化学反应,预测反应的结果,除能判断表面现象对应的
化学反应外,还要考虑隐含温度、浓度、反应物的量等因素对反应的影响及反应的可逆性等,
挖掘隐含的反应,侧重考查考生的逻辑推理能力、解决问题能力,体现《中国高考评价体系》
中化学学科的育人价值。
N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.(2018·全国卷Ⅰ)1.0 mol CH 与 Cl 在光照下反应生成的 CHCl 分子数为 1.0N
4 2 3 AB.(2018·全国卷Ⅱ)密闭容器中,2 mol SO 和 1 mol O 催化反应后分子总数为2N
2 2 A
C.(2017·全国卷Ⅱ)0.1 mol H 和0.1 mol I 于密闭容器中充分反应后,其分子总数为0.2
2 2
N
A
D.(2018.11·浙江选考)标准状况下,11.2 L Cl 溶于水,溶液中Cl-、ClO-和HClO的微
2
粒数之和为N
A
C [CH 与 Cl 在光照下发生取代反应生成CHCl、CHCl、CHCl 、CCl 等一系列取代
4 2 3 2 2 3 4
产物,故1.0 mol CH 反应生成的 CHCl 分子数小于 1.0N ,A错误;SO 和O 生成SO 的反
4 3 A 2 2 3
应是可逆反应,该反应不能正向进行到底,故2 mol SO 和 1 mol O 催化反应后分子总数大
2 2
于2N
A
,B错误;H
2
和I
2
在密闭容器中发生反应:H
2
(g)+I
2
(g)⇌2HI(g),该反应前后气体总分
子数不变,故0.1 mol H 和0.1 mol I 充分反应后,分子总数为0.2N ,C正确;标准状况下11.2
2 2 A
L Cl 为0.5 mol,若与水完全反应,溶液中Cl-、ClO-和HClO的微粒数之和为N ,但该反应
2 A
是可逆反应,故三种微粒之和小于N ,D错误。]
A
[强化4] N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.标准状况下,0.1 mol Cl 溶于水,转移的电子数目为0.1N
2 A
B.5.6 g 铁和6.4 g铜分别与足量单质硫充分反应,转移的电子数均为0.2N
A
C.1 mol N 和3 mol H 混合反应,当生成0.1 mol NH 时,转移电子数目为0.3N
2 2 3 A
D.标准状况下,11.2 L HCl和11.2 L NH 充分混合后含有的分子数为N
3 A
C [Cl 与HO的反应是可逆反应,将0.1 mol Cl 通入水中,Cl 并非完全与水反应,故
2 2 2 2
转移电子的数目小于0.1N ,A错误;5.6 g 铁和6.4 g铜均为0.1 mol,与足量单质硫充分反
A应分别生成FeS、Cu S,前者转移电子数为0.2N ,后者转移电子数为0.1N ,B错误;合成氨
2 A A
反应中,N元素由0价降低到-3价,故生成0.1 mol NH 时,转移电子数目为0.3N ,C正
3 A
确;标准状况下,11.2 L HCl和11.2 L NH 的物质的量均为0.5 mol,二者充分混合反应生
3
成0.5 mol NH Cl,而NH Cl是离子化合物,不存在分子,故充分混合后含有的分子数为0,D
4 4
错误。]
考向5 围绕“电解质溶液中粒子数目”进行判断(理解与辨析能力)
此考向主要考查电解质在水溶液中的变化,命题集中在:①弱电解质的电离,涉及弱酸
溶液中所含的H+数目、弱碱溶液中所含的OH-数目、水电离出的H+(或OH-)等;②盐类的
水解,涉及强酸弱碱盐溶液中所含的阳离子数,强碱弱酸盐溶液中所含弱酸根的离子数、胶
体粒子数等。要求考生在掌握基础知识(物质的量浓度、电离平衡、盐类水解等)的前提下,辨
析基本概念,明确电离平衡和盐类水解的特点,获取题目提供的关键信息,从微观角度认识
物质发生的变化及规律;合理运用化学学科的思维方法,有效地组织整合学科的相关知识,
调动运用学科的相关能力,高质量地认识问题、分析问题和解决问题。
N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.(2020·全国卷Ⅲ)1 L 1 mol·L-1NaCl溶液含有28N 个电子
A
B.(2020.7·浙江选考)常温下,pH=9的CHCOONa溶液中,水电离出的H+数为10-5N
3 A
C.(2019·全国卷Ⅱ)1 L 0.1 mol·L-1 磷酸钠溶液含有的PO数目为0.1N
A
D.(2019.4·浙江选考)500 mL 0.5 mol·L-1 的NaCl溶液中微粒数大于0.5N
A
D [1 L 1 mol·L-1NaCl溶液中含有1 mol NaCl和大量的水,1 mol NaCl中就含有28
mol电子,再加上溶剂水中的电子,则溶液中的电子数大于28N ,A错误;题目未指明
A
CHCOONa溶液的体积,无法计算水电离出的H+数目,B错误;NaPO 是强碱弱酸盐,1 L
3 3 4
0.1 mol·L-1 磷酸钠溶液含有0.1 mol Na PO ,由于PO发生水解反应,故溶液含有的PO数
3 4
目小于0.1N ,C错误;500mL 0.5 mol/L NaCl溶液中含有0.25 mol NaCl,由于还含有水分子,
A
故溶液中微粒数大于0.5N ,D正确。]
A[强化5] 设N 为阿伏加德罗常数的值。下列说法中正确的是( )
A
A.(2020.7·浙江选考)1 L浓度为0.100 mol·L-1的NaCO 溶液中,阴离子数为0.100N
2 3 A
B.(2019·全国卷Ⅲ)常温下pH=2的HPO 溶液,每升溶液中的H+数目为0.02N
3 4 A
C.(2018·全国卷Ⅰ)16.25 g FeCl 水解形成的Fe(OH) 胶体粒子数为0.1N
3 3 A
D.(2018·全国卷Ⅱ改编)100 mL 1 mol·L-1 FeCl 溶液中所含Fe3+的数目小于0.1N
3 A
D [CO能够水解产生HCO和OH-,所以阴离子数大于0.100N ,A错误;常温下pH=2
A
的HPO 溶液中c(H+)=0.01 mol·L-1,1 L该溶液中含有0.01 mol H+,故溶液中含有H+数
3 4
目为0.01N ,B错误;Fe(OH) 胶体粒子是多个Fe(OH) 分子的集合体,16.25 g FeCl 的物质
A 3 3 3
的量为0.1 mol,则水解形成的Fe(OH) 胶体粒子数小于 0.1N ,C错误;100 mL 1 mol·L-1
3 A
FeCl 溶液中含有0.1 mol FeCl ,由于Fe3+发生水解反应,则所含Fe3+的数目小于0.1N ,D正
3 3 A
确。]
训练(二) 阿伏加德罗常数的判断
1.(2020·四川绵阳诊断)设N 为阿伏加德罗常数值。下列说法正确的是( )
A
A.0.5 mol 18O 中所含中子数为10N
2 A
B.标准状况下,2.24 L CHCl 含有的共价键数为 0.4N
3 A
C.常温下,2.8 g C H 与CO的混合气体所含碳原子数为 0.3N
2 2 A
D.0.1 mol/L NaS 溶液中,S2-、HS-、HS的数目共为0.1N
2 2 A
A [18O 原子中子数为18-8=10,则0.5 mol 18O 中所含中子为0.5 mol×10×2=10
2
mol,即10N ,A正确;标准状况下,CHCl 为液态,不能根据体积计算其物质的量,B错误;
A 3
C H、CO的摩尔质量分别为26 g/mol、28 g/mol,不能计算2.8 g C H 与CO的物质的量及所
2 2 2 2
含碳原子数,C错误;题目未指明0.1 mol/L Na S溶液的体积,则溶液中微粒数目不能确定,D
2
错误。]2.(2021·安徽“江南十校”联考)假定N 为阿伏加德罗常数的值。下列说法正确的是(
A
)
A.常温下,46 g乙醇中含C—H键的数目为6N
A
B.1 mol/L的KSO 溶液中含K+的数目为2N
2 4 A
C.标准状况下,22.4 L氦气中含质子的数目为4N
A
D.1 mol HNO 被还原为NO转移电子的数目为3N
3 A
D [乙醇的结构简式为CHCHOH,46 g乙醇为1 mol,则含C—H键的数目为5N ,A
3 2 A
错误;题目未指明1 mol/L的KSO 溶液的体积,无法确定所含K+数目,B错误;1个He原子
2 4
含有2个质子,标准状况下22.4 L氦气(He)为1 mol,则含质子的数目为2N ,C错误;HNO
A 3
被还原为NO,N元素由+5价降低到+2价,则1 mol HNO 被还原为NO转移电子的数目为
3
3N ,D正确。]
A
3.(2021·安徽宣城模拟)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.1 mol Na与O 完全反应,转移的电子数目大于N
2 A
B.标准状况下,11.2 L 2HO中含有的中子数目为5N
A
C.8.0 g CuO和Cu S的混合物中含有铜原子的数目为0.1N
2 A
D.25 ℃时,1 L pH=1的稀硫酸中含有的氢离子数目大于0.1N
A
C [Na与O 完全反应时被氧化生成Na+,故1 mol Na反应时转移电子数为N ,A错误;
2 A
标准状况下2HO为非气体,11.2 L 2HO的物质的量远大于0.5 mol,故所含中子数远大于
2 2
5N ,B错误; 8.0 g CuO为0.1 mol,含有0.1 mol Cu原子,而8.0 g Cu S为0.05 mol,含有0.1
A 2
mol Cu原子,故8.0 g CuO和Cu S的混合物中含有铜原子的数目为0.1N ,C正确; 25℃时,
2 A
1 L pH=1的稀硫酸中n(H+)=1 L×0.1 mol/L=0.1 mol,故所含H+离子数目为0.1N ,D错
A
误。]
4.(2021·陕西榆林一模)设N 为阿伏加德罗常数的数值,下列说法正确的是( )
A
A.22.4 L乙烷中所含的极性共价键数目为7N
A
B.某温度下,将 1 mol SO 通入足量水中生成的HSO 分子数为N
2 2 3 A
C.常温常压下,3.0 g含葡萄糖的冰醋酸中含有的原子总数为0.4N
A
D.室温下,1 L pH为13的NaOH 溶液和Ba(OH) 混合溶液中含 OH-个数为 0.01N
2 A
C [题目未指明22.4 L乙烷是否处于标准状况下,无法计算其物质的量及所含共价键
数目,A错误;SO 与水的反应是可逆反应,1 mol SO 不能与水完全反应,故生成的HSO 分
2 2 2 3
子数小于N ,B错误;葡萄糖和冰醋酸的最简式均为CHO,3.0 g含葡萄糖的冰醋酸中含
A 2
“CHO”为0.1 mol,则含有的原子总数为0.4N ,C正确;室温下,1 L pH为13的NaOH 溶
2 A
液和Ba(OH) 混合溶液中含OH-为1 L×0.1 mol/L=0.1 mol,故含 OH-个数为 0.1N ,D错
2 A
误。]
5.(2021·辽宁丹东一模)用N 表示阿伏加德罗常数值,下列叙述中正确的是( )
A
A.0.4 mol NH 与0.6 mol O 在催化剂的作用下充分反应,得到NO的分子数为0.4N
3 2 A
B.C 和石墨的混合物共1.8 g,含碳原子数目为0.15N
60 AC.1 L 0.1 mol/L NH Al(SO ) 溶液中阳离子总数小于0.2N
4 4 2 A
D.5.6 g铁在足量的O 中燃烧,转移的电子数为0.3N
2 A
B [NH 与O 发生催化氧化反应:4NH +5O 4NO+6HO,0.4 mol NH 与0.6
3 2 3 2 2 3
mol O 反应生成0.4 mol NO,且剩余0.1 mol O,剩余的O 与NO反应生成NO ,故得到NO
2 2 2 2
的分子数小于0.4 N ,A错误;C 和石墨都是碳元素形成的单质,1.8 g二者混合物含有碳原
A 60
子的物质的量为1.8 g/(12 g·mol-1)=0.15 mol,故含碳原子数目为0.15N ,B正确;1 L 0.1
A
mol/L NH Al(SO ) 溶液中含有0.1 mol NH和0.1 mol Al3+,二者均发生水解,由于1个Al3+
4 4 2
水解生成3个H+,故阳离子总数大于0.2N ,C错误;5.6 g Fe为0.1 mol,在O 中燃烧生成
A 2
Fe O,则转移电子数约为0.267N ,D错误。]
3 4 A
6.(2021·山东聊城模拟)设N 为阿伏加德罗常数的值,下列叙述中正确的是( )
A
A.等物质的量的NaO和NaO 中所含阴离子数均为N
2 2 2 A
B.电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2N
A
C.4.6 g C HO的分子中含有C—H键数目一定为0.5N
2 6 A
D.1 mol Mg在空气中完全燃烧生成MgO和MgN,转移电子数为2N
3 2 A
D [Na O 由Na+和O构成,NaO由Na+和O2-构成,则等物质的量的NaO 和NaO所
2 2 2 2 2 2
含阴离子数相等,但不一定是N ,A错误;电解精炼铜时,阳极上铁、锌杂质先放电,且Fe的
A
摩尔质量小于64 g·mol-1,Zn的摩尔质量大于64 g·mol-1,则阳极减少6.4 g,转移的电子的
物质的量不一定为0.2 mol,B错误;C HO可能是CHCHOH或CHOCH 4.6 g C HO的
2 6 3 2 3 3, 2 6
物质的量为0.1 mol,则含有C—H键数目介于0.5N ~0.6N 之间, C错误; MgO和MgN
A A 3 2
中镁元素的化合价都是+2价,0.1 mol镁完全反应失去0.2 mol电子,则转移的电子数为
0.2N ,D正确。]
A
7.(2021·山东济南联考)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.17 g由HS与PH 组成的混合气体中含有的质子数为9N
2 3 A
B.90 g果糖(C H O,分子中无环状结构和碳碳双键)中含有的非极性键数目为3N
6 12 6 A
C.1 mol由乙醇与二甲醚(CH—O—CH)组成的混合物中含有的羟基数目为N
3 3 A
D.已知Ra→X+He,则0.5 mol X中含有的中子数为34N
A
A [1个HS和1个PH 分子均含18个质子,二者摩尔质量均为34 g/mol,17 g由HS
2 3 2
与PH 组成混合气体的总物质的量为0.5 mol,故含有的质子数为9N ,A正确;1个果糖分子
3 A
含有5个非极性键(C—C键),90 g果糖为0.5 mol,则含有非极性键的数目为0.25N ,B错误;
A
二甲醚不含羟基,只有乙醇中含羟基,故含有羟基数目介于0~N 之间,C错误;据质量守恒
A
和电荷守恒推知,X应为X,1个X含有136 个中子,则0.5 mol X含有的中子数为68N ,D错
A
误。]
8.(2020·吉林长春二模)设N 为阿伏加德罗常数的值。下列有关叙述正确的是( )
A
A.常温下,1 L 0.5 mol/L CHCOONH 溶液的pH=7,则溶液中CHCOO-与NH的
3 4 3数目均为0.5N
A
B.10 g质量分数为46%的乙醇溶液含有氢原子的数目为0.6N
A
C.16 g氨基(-NH )中含有的电子数为7N
2 A
D.在密闭容器中将2 mol SO 和1 mol O 混合反应后,体系中的原子数为8N
2 2 A
D [1 L 0.5 mol/L CH COONH 溶液中含0.5 mol CH COONH,CHCOO-、NH都发生
3 4 3 4 3
水解反应,则溶液中CHCOO-与NH的数目均小于0.5N ,A错误;乙醇溶液中乙醇和水都
3 A
含氢原子,故含有氢原子的数目大于0.6N ,B错误;1个氨基(-NH )含有9个电子,16 g氨
A 2
基(-NH )为1 mol,则含有的电子数为9N ,C错误;SO 和O 的反应是可逆反应,但遵循质
2 A 2 2
量守恒定律,反应前后原子总数不变,则体系中的原子数为8N ,D正确。]
A
9.(2020·山东济南三模)N 表示阿伏加德罗常数的值。下列说法正确的是( )
A
A.标准状况下,560 mL氯气溶于水,共转移0.025N 个电子
A
B.1 L 0.1 mol·L-1氨水中,NH 、NH ·H O、NH的总数为0.1N
3 3 2 A
C.向FeBr 溶液中加入酸性KMnO 溶液,当有1 mol Fe2+被氧化时,转移3N 个电子
2 4 A
D.35 g乙烯和丙烯组成的混合气体中含有N 个碳原子
A
B [标准状况下,560 mL Cl 为0.025 mol,由于Cl 与水的反应是可逆反应,Cl 不能完
2 2 2
全反应,故转移电子数小于0.025N ,A错误;1 L 0.1 mol/L 氨水中含有NH 为0.1 mol,由于
A 3
氨水中存在平衡:NH
3
+H
2
O⇌NH
3
·H
2
O⇌NH+OH-,故NH
3
、NH
3
·H
2
O、NH的总数为
0.1N ,B正确;由于Fe2+的还原性大于Br-,有1 mol Fe2+被氧化时,Br-未被氧化,则转移电
A
子数为N ,C错误;乙烯和丙烯的最简式均为CH,35 g二者混合物中含“CH”的物质的
A 2 2
量为35 g/(14 g·mol-1)=2.5 mol,则含有碳原子数为2.5 N ,D错误。]
A
10.(2021·广东韶关一模)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.反应3H(g)+N(g) 2NH (g) ΔH=-92 kJ/mol,当放出9.2 kJ热量时,转移电
2 2 3
子为0.6N
A
B.向FeI 溶液中通入适量Cl,当有1 mol Fe2+被氧化时,共转移的电子数目为N
2 2 A
C.1 mol/L氯化铜溶液中,若Cl-的数目为2N ,则Cu2+的数目为N
A A
D.标准状况下,NO和O 各11.2 L混合充分反应,所得气体的分子总数为0.75N
2 A
A [放出9.2 kJ热量时,反应生成0.2 mol NH ,则转移电子为0.6N ,A正确;I-的还原
3 A
性强于Fe2+,有1 mol Fe2+被氧化时,至少有2mol I-被氧化,故转移电子的数目大于3N ,B
A
错误;Cu2+发生水解反应,Cl-的数目为2N ,则Cu2+的数目小于N ,C错误;标准状况下,
A A
11.2 L NO和11.2 L O 均为0.5 mol,二者发生反应:2NO+O===2NO ,由于存在平衡:
2 2 2
2NO 2⇌N
2
O
4
,故所得气体的总分子数小于0.75N
A
,D错误。]