文档内容
专题 12 化学反应与电能
第 36 练 金属的腐蚀与防护
1.下列有关金属腐蚀的说法中正确的是( )
A.金属腐蚀指不纯金属与接触到的电解质溶液进行化学反应而损耗的过程
B.电化学腐蚀指在外加电流的作用下不纯金属发生化学反应而损耗的过程
C.钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈
D.金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生
【答案】D
【解析】金属腐蚀的本质,主要是金属原子失电子被氧化,腐蚀的内因是金属的化学性质比较活泼,
外因是金属与空气、水和其他腐蚀性的物质接触,腐蚀主要包括化学腐蚀和电化学腐蚀,所以 A错误;电
化学腐蚀指不纯金属与电解质溶液接触时发生原电池反应而损耗的过程,不需要外加电流,所以 B错误;
钢铁腐蚀最普遍的是吸氧腐蚀,正极吸收氧气,而不是负极吸收氧气,所以C错误。
2.下列关于钢铁腐蚀说法正确的是( )
A.电化学腐蚀是造成钢铁腐蚀的主要原因
B.钢铁腐蚀的负极为Fe-3e-=Fe3+
C.弱酸性条件下钢铁发生析氢腐蚀
D.镀锡铁器破损时镀层金属仍可以保护铁器
【答案】A
【解析】A项,不纯的金属(或合金)跟电解质溶液接触时,会发生原电池反应,比较活泼的金属失去
电子而被氧化,这种腐蚀叫做电化学腐蚀。由于钢铁直接接触化学物质而发生化学腐蚀的机会并不多,而
接触电解质溶液的机会却比较多,且钢铁本身又是铁碳合金。因此,易于形成原电池而发生电化学腐蚀,
故A正确;B项,钢铁腐蚀的负极为Fe-2e-=Fe2+,故B错误;C项,弱酸性或中性条件下钢铁发生吸氧腐
蚀,强酸性条件下钢铁发生析氢腐蚀,故C错误;D项,由于铁比锡活泼,镀锡铁器破损时,铁做负极,
被腐蚀,镀层金属不能保护铁器,故D错误;故选A。
3.下列有关镀锌钢管(锌盐溶液作电解质溶液)的说法正确的是( )
A.电镀时,钢管作阳极,锌棒作阴极
B.钢管镀锌过程中,阴阳两极的质量变化一定不相等
C.镀锌的目的是在钢管表面形成Fe—Zn合金,增强钢管的耐腐蚀能力D.钢管镀锌过程中,阴极的电极反应式为Zn2++2e-=Zn
【答案】D
【解析】A项,电镀时镀层金属作阳极,待镀金属作阴极,故钢管镀锌时,锌棒作阳极,钢管作阴极,
A项错误;B项,钢管镀锌过程中,阳极的电极反应式为Zn-2e-=Zn2+,阴极的电极反应式为Zn2++2e-=Zn,
电镀过程中阴阳极转移的电子数相等,故阴阳两极的质量变化一定相等,B项错误;C项,钢管镀锌的目
的是美观、保护钢管等,而不是为了在钢管表面形成Fe—Zn合金,C项错误。D项,钢管镀锌过程中,阳
极的电极反应式为Zn-2e-=Zn2+,阴极的电极反应式为Zn2++2e-=Zn,D项正确;故选 D。
4.化学与生活、生产有着密切关系,下列叙述中正确的是( )
A.钢铁发生析氢腐蚀时,H+得电子释放出H,钢铁被腐蚀
2
B.钢铁发生吸氧腐蚀时,OH-失电子释放出O,钢铁被腐蚀
2
C.船底镶嵌锌块,锌发生还原反应而被消耗,以保护船体
D.外加电源的正极连接在海水中的钢铁闸门上,可保护闸门
【答案】A
【解析】发生吸氧腐蚀时正极反应式是 O +2HO+4e-===4OH-,整个过程是吸收O 而不是释放出
2 2 2
O ,B错误;选项C中是牺牲阳极的阴极保护法,金属锌发生氧化反应,C错;选项D中是外加电流的阴
2
极保护法,钢铁闸门应与外加电源的负极相连,D错。
5.某地下了一场酸雨,在这种环境中的铁制品极易被腐蚀。对该条件下铁制品发生电化学腐蚀的叙
述正确的是( )
A.该电化学腐蚀是析氢腐蚀 B.正极反应式:O +4e-=2O2-
2
C.原电池反应减缓了铁制品的腐蚀 D.负极反应式:Fe-3e-=Fe3+
【答案】A
【解析】A项,铁制品中含有铁和碳,酸雨使水膜呈酸性,构成了原电池,会发生析氢腐蚀,故A正
确;B项,酸性环境中发生析氢腐蚀,正极反应为氢离子得电子生成氢气:2H++2e-=H ↑,故B错误;C项,
2
原电池反应会加快铁制品的腐蚀,故C错误;D项,发生电化学腐蚀时金属铁被氧化为Fe2+,负极反应式
为︰Fe-2e-=Fe2+,故D错误;故选A。
6.如图所示的钢铁腐蚀中,下列说法正确的是( )
A.碳表面发生还原反应B.钢铁被腐蚀的最终产物为FeO
C.生活中钢铁制品的腐蚀以图①所示为主
D.图②中,正极反应式为O+4e-+2H O═4OH-
2 2
【答案】D
【解析】A项,碳是正极,表面发生还原反应,A正确;B项,钢铁被腐蚀的最终产物为氧化铁,B
错误;C项,图①为析氢腐蚀,电解质溶液呈酸性,生活中钢铁制品的腐蚀以图②吸氧腐蚀为主,C错误;
D项,图②为吸氧腐蚀,正极反应式为O+4e-+2H O=4OH-,D正确。故选 D。
2 2
7.如图装置中,小试管内为红墨水,具支试管内盛有pH=4的久置的雨水和生铁片。实验时观察到:
开始时导管内液面下降,一段时间后导管内液面回升,略高于小试管内液面。下列说法正确的是( )
A.生铁片中的碳是原电池的阳极,发生还原反应
B.雨水酸性较强,生铁片仅发生析氢腐蚀
C.墨水回升时,碳电极反应式为O+2HO+4e-===4OH-
2 2
D.具支试管中溶液pH逐渐减小
【答案】C
【解析】生铁片中的碳是原电池的正极,A错;雨水酸性较强,开始时铁片发生析氢腐蚀,产生氢气,
导管内液面下降,一段时间后铁片发生吸氧腐蚀,吸收氧气,导管内液面回升,B错;墨水回升时,铁片
发生吸氧腐蚀,碳极为正极,电极反应为O +2HO+4e-===4OH-,C对;铁片无论是发生析氢腐蚀还是
2 2
吸氧腐蚀,具支试管内溶液pH均增大,D错。
8.下列现象与电化学腐蚀无关的是( )
A.埋在潮湿土壤里的铁管比埋在干燥土壤中的铁管更容易被腐蚀
B.在空气中,生铁比纯铁芯,(几乎是纯铁)更容易生锈
C.马口铁(镀锡)上的金属镀层损坏时,铁更容易被腐蚀
D.纯银饰品戴久后,银表面会变暗甚至有一层黑色物质生成
【答案】D
【解析】A项,铁管在潮湿的环境下容易形成原电池,加快铁的腐蚀,与电化学腐蚀有关,故A不选;
B项,生铁中金属铁、碳、潮湿的空气能构成原电池,金属铁为负极,易被腐蚀而生锈,和电化学腐蚀有
关,故B不选;C项,镀锡铁皮的镀层损坏后,会形成原电池,金属铁是负极,容易腐蚀,故C不选;D
项,金属银在空气中能够生成黑色的硫化银而变黑,此过程属于普通化学腐蚀,与电化学腐蚀无关,故D
符合题意。故选D。
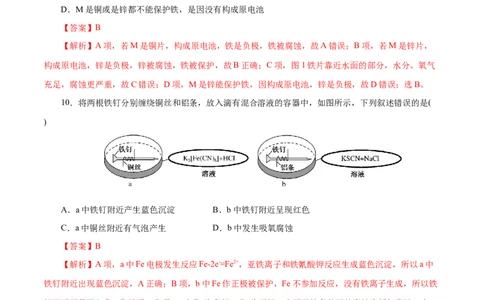
9.如图是研究铁被海水腐蚀的实验装置。图2中M是某种与铁片紧贴的金属,下列说法正确的是( )A.若M是铜片,可保护铁
B.若M是锌片,可保护铁
C.图1铁片靠近烧杯底部的部分,腐蚀更严重
D.M是铜或是锌都不能保护铁,是因没有构成原电池
【答案】B
【解析】A项,若M是铜片,构成原电池,铁是负极,铁被腐蚀,故A错误;B项,若M是锌片,
构成原电池,锌是负极,锌被腐蚀,铁被保护,故B正确;C项,图1铁片靠近水面的部分,水分、氧气
充足,腐蚀更严重,故C错误;D项,M是锌能保护铁,因构成原电池,锌是负极,故D错误;选B。
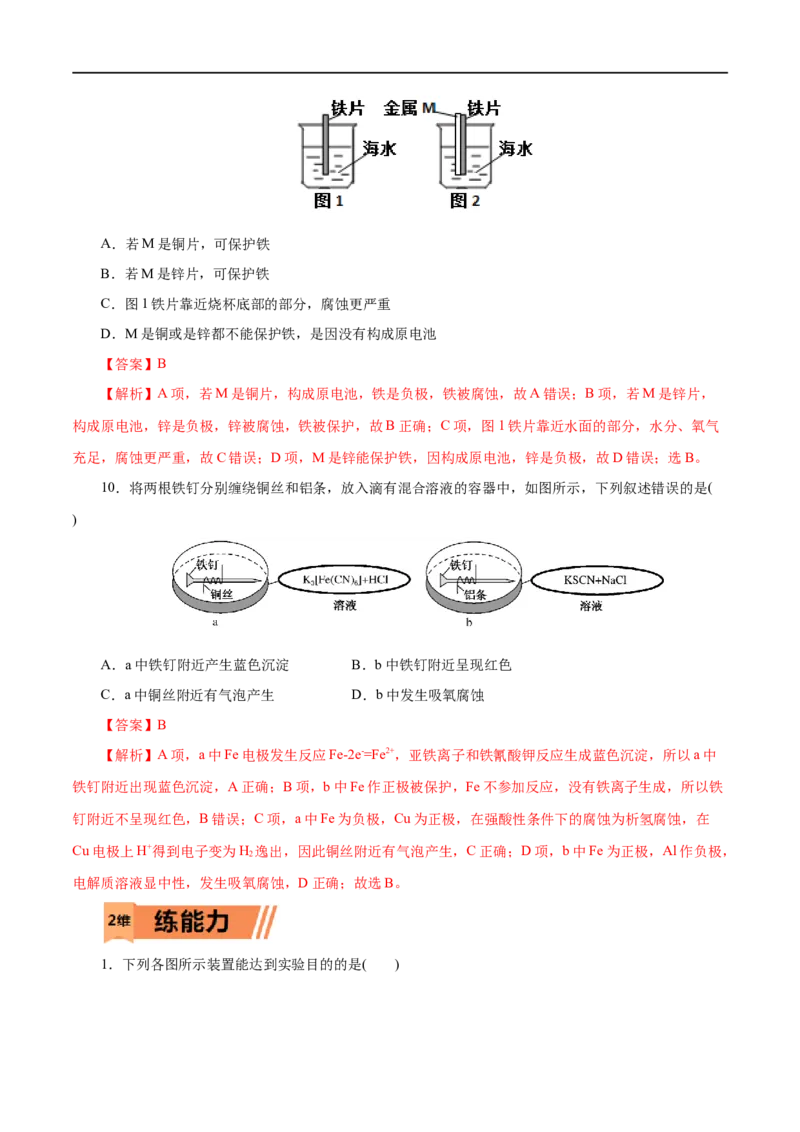
10.将两根铁钉分别缠绕铜丝和铝条,放入滴有混合溶液的容器中,如图所示,下列叙述错误的是(
)
A.a中铁钉附近产生蓝色沉淀 B.b中铁钉附近呈现红色
C.a中铜丝附近有气泡产生 D.b中发生吸氧腐蚀
【答案】B
【解析】A项,a中Fe电极发生反应Fe-2e-=Fe2+,亚铁离子和铁氰酸钾反应生成蓝色沉淀,所以a中
铁钉附近出现蓝色沉淀,A正确;B项,b中Fe作正极被保护,Fe不参加反应,没有铁离子生成,所以铁
钉附近不呈现红色,B错误;C项,a中Fe为负极,Cu为正极,在强酸性条件下的腐蚀为析氢腐蚀,在
Cu电极上H+得到电子变为H 逸出,因此铜丝附近有气泡产生,C正确;D项,b中Fe为正极,Al作负极,
2
电解质溶液显中性,发生吸氧腐蚀,D正确;故选B。
1.下列各图所示装置能达到实验目的的是( )A.图甲,验证铁的吸氧腐蚀
B.图乙,牺牲阳极的阴极保护法
C.图丙,在铁制品表面镀锌
D.图丁,测定盐酸的pH
【答案】A
【解析】A项,图甲,在酸性条件下铁发生析氢腐蚀,在中性或碱性条件下发生吸氧腐蚀,该图是中
性条件,发生吸氧腐蚀,A能达到实验目的;B项,图乙,铁比碳活泼,形成原电池时,铁为负极发生氧
化反应被腐蚀,故不能用此装置保护水体中的钢铁设备,B不能达到实验目的;C项,图丙,锌比铁活泼,
Fe2+得电子能力比Zn2+强,则在阴极上,Fe2+得电子生成铁单质,无法在铁电极上镀锌,应使用硫酸锌做电
解液,C不能达到实验目的;D项,图丁,pH试纸不能润湿,D不能达到实验目的;故选 A。
2.铜板上铁铆钉的吸氧腐蚀原理如图所示。下列说法正确的是( )
A.正极电极反应式为2H++2e-===H↑
2
B.此过程中还涉及反应4Fe(OH) +2HO+O===4Fe(OH)
2 2 2 3
C.此过程中Fe、Cu均被腐蚀
D.此过程中电流从Fe流向Cu
【答案】B
【解析】铁铆钉吸氧腐蚀的正极电极反应式为O+2HO+4e-===4OH-,铜作正极不被腐蚀,电子从
2 2
负极通过导线流向正极。
3.如图是自来水表的常见安装方式。下列有关说法不正确的是( )
A.该安装方式的水表更容易被腐蚀
B.发生腐蚀过程中,电子从接头流向水表
C.腐蚀时水表发生的电极反应为2HO+O+4e−===4OH−
2 2
D.腐蚀过程还涉及反应:4Fe(OH) + O +2H O ===4Fe(OH)
2 2 2 3
【答案】A
【解析】构成原电池,腐蚀铁,保护铜,所以该安装方式的水表不易被腐蚀,故A不正确;电子由铁
流向铜,即电子从接头流向水表,故B正确;水表发生了吸氧腐蚀,氧气在水表的表面得电子,电极反应
式为2HO+O+4e−===4OH−,故C正确;负极放电产生的Fe2+与正极产生的OH−结合成 Fe(OH) ,Fe(OH)
2 2 2 2被空气中的氧气氧化生成氢氧化铁,所以腐蚀过程还涉及反应:4Fe(OH) +2H O+O===4Fe(OH) ,故D正
2 2 2 3
确。
4.港珠澳大桥设计使用寿命120年,需对桥体钢构件采取防腐措施。下列说法错误的是( )
A.采用外加电流保护钢构件时,需在钢构件上焊接锌块
B.防腐主要避免发生的反应是:2Fe+O +2H O=2Fe(OH)
2 2 2
C.钢构件表面喷涂环氧树脂涂层是为了隔绝空气、海水等
D.钢构件可多采用不锈钢材料以减缓腐蚀速率
【答案】A
【解析】A项,采用外加电流保护钢构件时,需附加一个石墨电极。钢构件与外接电源的负极连接,
作阴极,石墨电极与外接电源的正极连接,作阳极,A错误;B项,在钢铁的原电池反应中,Fe为负极,
失去电子发生氧化反应,Fe-2e-=Fe2+;杂质C为正极,O 在正极上得到电子被还原,O+4e-+2H O=4OH-,
2 2 2
根据电子守恒,可得总反应方程式为:2Fe+O +2H O=2Fe(OH) ,B正确;C项,钢构件表面喷涂环氧树脂
2 2 2
涂层能够隔绝空气、海水等,避免由于接触发生造成铁腐蚀损耗,C正确;D项,钢构件可多采用不锈钢
材料,由于其抗腐蚀能力增强,不容易被氧气氧化,因而可以减缓腐蚀速率,D正确;故选A。
5.我国有多条高压直流电线路的瓷绝缘子出现铁帽腐蚀现象,在铁帽上加锌环能有效防止铁帽的腐
蚀,防护原理如图所示。下列说法错误的是( )
A.通电时,锌环是阳极,发生氧化反应
B.通电时,阴极上的电极反应为2HO+2e-===H ↑+2OH-
2 2
C.断电时,锌环上的电极反应为Zn2++2e-===Zn
D.断电时,仍能防止铁帽被腐蚀
【答案】C
【解析】锌环与电源的正极相连,为阳极,A项正确;断电时,Zn比铁活泼,作负极,电极反应为
Zn-2e-===Zn2+,C项错误。
6. “雪龙2号”从深圳启航,执行中国第36次南极科考任务。下列有关科考船的说法正确的是(
)
A.外壳镶嵌一些铅块可提高科考船的抗腐蚀能力
B.停靠期间可将电源正极与船体相连保护船体
C.利用牺牲阳极的阴极保护法保护船体时,正极反应式为O+4e-+2H O=4OH-
2 2D.科考船只采用电化学保护法提高船体抗腐蚀能力
【答案】C
【解析】A项,在船壳上镶嵌铅块,船壳金属比铅活泼构成原电池时,作负极加快其腐蚀,不能减慢
船体的腐蚀,A项错误;B项,与电源正极相连,作阳极,加快船体的腐蚀,B项错误;C项,利用牺牲
阳极的阴极保护法保护船体时,船体作正极被保护,正极是氧气得电子生成氢氧根离子,正极反应式为
O+4e-+2H O=4OH-,C项正确;D项,还可以在船体表面涂上保护层等方法,提高其抗腐蚀能力,D项错
2 2
误;故选 C。
7.在城市地下常埋有纵横交错的管道和运输电线路,有些地面上还铺有地铁或城铁的铁轨,当有电
流泄漏入潮湿的土壤中,并与金属管道或铁轨形成回路时,就会引起金属管道、铁轨的腐蚀。原理简化如
图所示。则下列有关说法不正确的是( )
A.溶液中铁丝左端电极反应式为:Fe−2e−=Fe2+
B.如在NaCl溶液中加入酚酞,右边Fe电极附近溶液变红
C.地下管线被腐蚀,不易发现,也不便维修,故应将埋在地下的金属管道表面涂绝缘膜(或油漆等),
也可以使用外加电流阴极保护法
D.原理图可理解为两个串联电解装置
【答案】A
【解析】A项, 由装置图可知,左边铁与正极相连为阳极,发生Fe−2e−═Fe2+,铁丝左边应为阴极,
反应式为2H++2e−═H ↑,故A错误;B项,根据装置图,铁丝左边应为阴极,反应式为2H++2e−═H ↑,消
2 2
耗氢离子导致碱性增强,阴离子OH-移向阳极,故右边Fe电极附近溶液变红,故B正确;C项,为了保护
地下管线被腐蚀,故应将埋在地下的金属管道表面涂绝缘膜,也可以使用外加电流阴极保护法,故C正确;
D项, 由装置图可知,左边铁与正极相连为阳极,铁丝左边应为阴极,形成电解装置,铁丝右边为阳极,
右边的铁为阴极又组成电解装置,所以可理解为两个串联电解装置,故D正确;故选A。
8.某实验小组利用下列装置探究电解质溶液的浓度对金属腐蚀的影响:装置
现象 电流计指针不发生偏转 电流计指针发生偏转
下列有关说法正确的是( )
A.装置Ⅰ中的铁片均不会发生任何腐蚀
B.铁片d上可能发生的电极反应为:Fe-3e-=Fe3+
C.利用K[Fe(CN) ]溶液可确定装置Ⅱ中的正、负极
3 6
D.铁片a、c所处的NaCl溶液的浓度相等,二者腐蚀速率相等
【答案】C
【解析】A项,装置Ⅰ中因为两烧杯中NaCl溶液的浓度相等,两边电势相等,所以电流计指针不发生
偏转,但铁片a、b仍可发生普通的化学腐蚀,A项错误;B项,铁片d上Fe发生反应生成Fe2+,B项错误;
C 项,装置Ⅱ中负极发生反应:Fe-2e-===Fe2+,Fe2+遇 K[Fe(CN) ]溶液生成蓝色沉淀,故可利用
3 6
K[Fe(CN) ]溶液确定装置Ⅱ中的正、负极,C项正确;D项,装置Ⅱ中明显产生了电流,电化学腐蚀比化
3 6
学腐蚀要快得多,故铁片a、c的腐蚀速率不同,D项错误;故选C。
1.(2022•广东选择性考试)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁
片放入酸化的3%NaCl溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
A.加入AgNO 溶液产生沉淀 B.加入淀粉碘化钾溶液无蓝色出现
3
C.加入KSCN溶液无红色出现 D.加入K[Fe(CN) ]溶液无蓝色沉淀生成
3 6
【答案】D
【解析】镀层有破损的镀锌铁片被腐蚀,则将其放入到酸化的3%NaCl溶液中,会构成原电池,由于
锌比铁活泼,作原电池的负极,而铁片作正极,溶液中破损的位置会变大,铁也会继续和酸化的氯化钠溶
液反应产生氢气,溶液中会有亚铁离子生成。A项,氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液
后,不管铁片是否被腐蚀,均会出现白色沉淀,故A不符合题意;B项,淀粉碘化钾溶液可检测氧化性物
质,但不论铁片是否被腐蚀,均无氧化性物质可碘化钾发生反应,故B不符合题意;C项,KSCN溶液可检测铁离子的存在,上述现象中不会出现铁离子,所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红
色出现,故C不符合题意;D项,K[Fe(CN) ]是用于检测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会
3 6
生成亚铁离子,则加入K[Fe(CN) ]溶液就不会出现蓝色沉淀,故D符合题意。故选D。
3 6
2.(2020年江苏卷)将金属M连接在钢铁设施表面,可减缓水体中钢铁设施的腐蚀。在题图所示的情
境中,下列有关说法正确的是( )
A.阴极的电极反应式为
B.金属M的活动性比Fe的活动性弱
C.钢铁设施表面因积累大量电子而被保护
D.钢铁设施在河水中的腐蚀速率比在海水中的快
【答案】C
【解析】A项,阴极的钢铁设施实际作原电池的正极,正极金属被保护不失电子,故A错误;B项,
阳极金属M实际为原电池装置的负极,电子流出,原电池中负极金属比正极活泼,因此M活动性比Fe的
活动性强,故B错误;C项,金属M失电子,电子经导线流入钢铁设备,从而使钢铁设施表面积累大量电
子,自身金属不再失电子从而被保护,故C正确;D项,海水中的离子浓度大于河水中的离子浓度,离子
浓度越大,溶液的导电性越强,因此钢铁设施在海水中的腐蚀速率比在河水中快,故D错误;故选C。
3.全世界每年因钢铁锈蚀造成巨大损失,钢铁吸氧腐蚀原理如图所示。下列说法正确的是( )
A.钢铁腐蚀过程不只发生化学能与电能的转化
B.钢铁腐蚀的正极反应为:Fe-2e-=Fe2+
C.电解质溶液浓度可影响钢铁腐蚀的速率
D.将地下铁管与铜块连接,可保护铁管
【答案】C【解析】A项,钢铁腐蚀过程不仅发生化学能与电能的转化,钢铁的锈蚀过程属于缓慢氧化,还放出
热量,所以还发生化学能与热能的转化,A正确;B项,钢铁发生的腐蚀为吸氧腐蚀,负极上金属铁失电
子,发生氧化反应,正极上氧气得到电子,发生还原反应,电极反应为:2HO+O+4e-=4OH-,B错误;C
2 2
项,因为反应速率与离子浓度正相关,所以电解质溶液浓度可影响钢铁腐蚀的速率, C正确; D项,将
地下铁管与铜块连接会构成原电池,铁作负极,铜作正极,所以不能保护铁管,反而会加快铁管的腐蚀,
D错误;故选 C。
4.支撑海港码头基础的钢管桩,常用采用如图所示的方法进行防腐,其中高硅铸铁为惰性辅助阳极。
下列有关表述不正确的是( )
A.该保护方法叫做外加电流保护法,高硅铸铁的作用是传递电流
B.钢管桩被迫成为阴极而受到保护,其表面的腐蚀电流接近于零
C.通电后,调整外加电压,外电路中的电子被强制从钢管桩流向高硅铸铁
D.石墨能导电且化学性质不活泼,可用石墨代替高硅铸铁作辅助阳极
【答案】C
【解析】依图示,该防腐利用了外接直流电源,属于外加电流法防腐,高硅铸铁为惰性辅助阳极起到
传递电流作用,A正确;外接直流电源的负极与钢管桩连接,钢管桩被迫成为阴极而受到保护,其表面的
腐蚀电流接近于零,B正确;外电路中的电子被强制从外接直流电源的负极流向钢管桩,高硅铸铁上海水
中阴离子失去电子流向外接直流电源的正极,与海水中离子的移动构成整个防腐电流回路,C错误;高硅
铸铁为惰性辅助阳极起到传递电流作用,也可用石墨代替,D正确;故选C。
5.如图是实验室研究海水对铁闸不同部位腐蚀情况的剖面示意图。下列说法正确的是( )A.铁闸主要发生的是吸氢腐蚀
B.将铁闸与石墨相连可保护铁闸
C.铁腐蚀时的电极反应式:Fe-3e−=Fe3+
D.图中生成铁锈最多的是乙区域
【答案】D
【解析】A项,海水溶液为弱碱性,发生吸氧腐蚀,A错误;B项,将铁闸与石墨相连,铁比碳活泼,
铁作负极失电子,可以加快海水对铁闸的腐蚀,B错误;C项,铁腐蚀时作负极失电子生成亚铁离子,电
极反应式:Fe-2e−=Fe2+,C错误;D项, 在乙处,海水与氧气接触,与Fe最易形成原电池,发生的吸氧
腐蚀的程度最大,生成铁锈最多,故D正确;故选D。
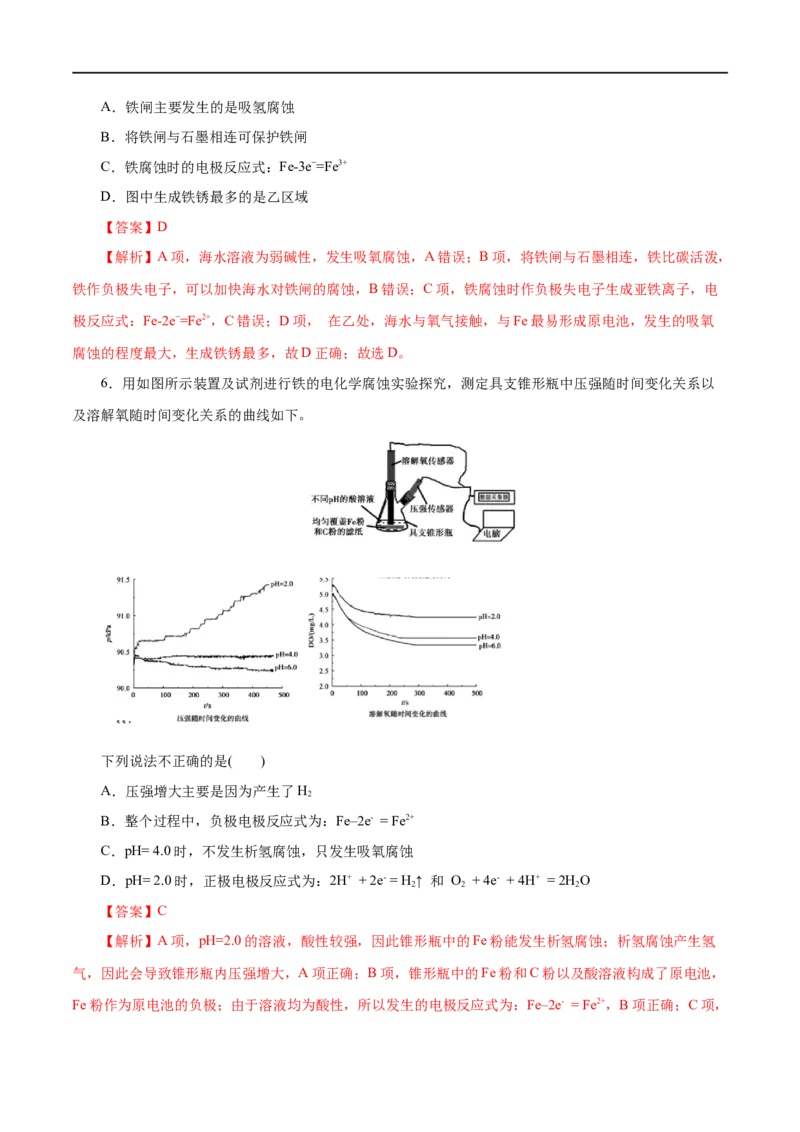
6.用如图所示装置及试剂进行铁的电化学腐蚀实验探究,测定具支锥形瓶中压强随时间变化关系以
及溶解氧随时间变化关系的曲线如下。
下列说法不正确的是( )
A.压强增大主要是因为产生了H
2
B.整个过程中,负极电极反应式为:Fe–2e- = Fe2+
C.pH= 4.0时,不发生析氢腐蚀,只发生吸氧腐蚀
D.pH= 2.0时,正极电极反应式为:2H+ + 2e- = H ↑ 和 O + 4e- + 4H+ = 2H O
2 2 2
【答案】C
【解析】A项,pH=2.0的溶液,酸性较强,因此锥形瓶中的Fe粉能发生析氢腐蚀;析氢腐蚀产生氢
气,因此会导致锥形瓶内压强增大,A项正确;B项,锥形瓶中的Fe粉和C粉以及酸溶液构成了原电池,
Fe粉作为原电池的负极;由于溶液均为酸性,所以发生的电极反应式为:Fe–2e- = Fe2+,B项正确;C项,若pH=4.0时只发生吸氧腐蚀,那么锥形瓶内的压强会有下降;而图中pH=4.0时,锥形瓶内的压强几乎不
变,说明除了吸氧腐蚀,Fe粉还发生了析氢腐蚀;消耗氧气的同时也产生了氢气,因此锥形瓶内压强几乎
不变,C项错误;D项,由图可知,pH=2.0时,锥形瓶内的溶解氧减少,说明有消耗氧气的吸氧腐蚀发生;
同时锥形瓶内的气压增大,说明有产生氢气的析氢腐蚀发生;因此,正极反应式有:2H+ + 2e- = H ↑ 和
2
O + 4e- + 4H+ = 2H O,D项正确;故选C。
2 2
7.下列根据实验操作及现象进行的分析和推断中,不正确的是( )
操作
一段时间后:①中,铁钉裸露在外的附近区域变红;
现象
②中……
A.NaCl的琼脂水溶液为离子迁移的通路
B.①中变红是因为发生反应2H++2e-=H↑,促进了水的电离
2
C.②中可观察到铁钉裸露在外的附近区域变蓝,铜丝附近区域变红
D.①和②中发生的氧化反应均可表示为M—2e-=M2+(M代表锌或铁)
【答案】B
【解析】A项,NaCl的琼脂水溶液能够让离子自由运动,所以其为离子迁移的通路,A正确;B项,
①中变红是因为发生反应O+4e-+2H O==4OH-,OH-使酚酞变红,B不正确;C项,反应生成的Fe2+与
2 2
[Fe(CN) ]3-反应生成蓝色沉淀,使②中铁钉裸露在外的附近区域变蓝,因生成OH-使酚酞变红,而使铜丝附
6
近区域变红,C正确;D项,①中发生的氧化反应为Zn-2e- ==Zn2+,②中发生的氧化反应为Fe-2e- ==Fe2+,
均可表示为M—2e-=M2+(M代表锌或铁),D正确;故选B。
8.考古发掘出的古代青铜器(含铜锡等金属)表面经常出现小孔腐蚀,这是一种电化学腐蚀现象。小孔
腐蚀的过程及铜腐蚀产物(铜锈)的成份如下图所示:
已知:2CuCl+H O Cu O+2HCl。下列分析不正确的是( )
2 2
A.氧气是正极反应物 B.铜锈的成份与氧气浓度、pH有关C.图2中,Cl-从小孔内向小孔外移动 D.青铜中的锡也会发生电化学腐蚀
【答案】C
【解析】A项,青铜器中含铜锡等金属,也含有其它金属及非金属杂质,由于物质活动性不同,周围
有电解质溶液,形成了原电池,Cu为原电池的负极,失去电子发生氧化反应,由于电解质溶液为中性,发
生吸氧腐蚀,正极上氧气得到电子,变为OH-,因此氧气是正极反应物,A正确;B项,根据图2可知:
在锈蚀小孔外物质成分为Cu (OH) CO、Cu (OH) Cl,Cu元素化合价为+2价;在小孔附近物质是Cu O,
2 2 3 2 3 2
小孔内壁物质成分是CuCl,Cu元素化合价为+1价,小孔外氧气浓度大,Cu元素价态高,小孔内氧气浓度
小,Cu元素价态低,物质成分与氧气浓度有关;在溶液酸性较强时可逆反应2CuCl+H O
2
Cu O+2HCl的平衡逆向移动,物质成分主要是CuCl,若溶液酸性弱,,平衡正向移动,物质成分主要是
2
Cu O,可见物质成分也与溶液的pH有关,B正确;C项,溶液中微粒Cl-总是向低洼处流动,因此会从小
2
孔外向小孔内移动,与氧气浓度较小时的+1价Cu形成难溶性固体CuCl, C错误;D项,由于Sn是比较
活泼的金属,因此也会与活动性比Sn弱的金属构成原电池,Sn为负极,被氧化而引起电化学腐蚀,D正
确;故选C。
9.碳钢广泛应用在石油化工设备管道等领域,随着深层石油天然气的开采,石油和天然气中含有的
CO 及水引起的腐蚀问题(俗称二氧化碳腐蚀)引起了广泛关注。深井中二氧化碳腐蚀的主要过程如下所示:
2
负极:Fe(s)+ 2HCO - (aq) -2e- = FeCO (s)+H CO(aq)(主要)
3 3 2 3
正极:2HCO(aq) +2e- = H ↑+2HCO- ( aq)(主要)
2 3 2 3
下列说法不正确的是
A.钢铁在CO 水溶液中的腐蚀总反应可表示为CO+H O +Fe= FeCO +H
2 2 2 3 2
B.深井中二氧化碳对碳钢的腐蚀主要为化学腐蚀
C.碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含量高腐蚀速率会加快
D.腐蚀过程表明含有CO 的溶液其腐蚀性比相同pH 值的 HCl溶液腐蚀性更强
2
【答案】B
【解析】A项,由深井中二氧化碳腐蚀的主要过程的电极反应式:负极:Fe(s)+2HCO -(aq)-2e-
3
═FeCO (s)+HCO(aq);正极:2HCO(aq)+2e-═H ↑+2HCO-(aq),因此总反应可表示为
3 2 3 2 3 2 3
CO+H O+Fe═FeCO +H ,故A正确;B项,深井中二氧化碳对碳钢的腐蚀涉及原电池原理,故主要为电
2 2 3 2
化学腐蚀,不是化学腐蚀,故B错误;C项,碳钢管道在深井中的腐蚀与油气层中盐份含量有关,盐份含
量越高,溶液中离子浓度越大,导电能力越强,腐蚀速率越快,故C正确;D项,碳酸是弱酸,盐酸是强
酸,等pH值的CO 的溶液与HCl溶液相比,HCO(aq)的浓度要大得多,故腐蚀性比相同pH值的HCl溶
2 2 3
液腐蚀性更强,故D正确;故选B。10.化学科技工作者对含有碳杂质的金属铝的腐蚀与溶液酸碱性的关系进行了研究,在 25 ℃时得出
溶液pH值对铝的腐蚀影响关系如图所示,下列说法正确的是( )
A.金属铝在浓硫酸中的腐蚀速率大于盐酸中的腐蚀速率
B.金属铝在中性环境中不易被腐蚀
C.金属铝在pH=8.5的NaCO 溶液中会发生电化学腐蚀析出氧气
2 3
D.不能用电解的方法在金属铝的表面生成致密的氧化物薄膜
【答案】B
【解析】A项,铝在浓硫酸中钝化,错误;B项,由图可知在5