文档内容
第 3 讲 化学键 分子结构与性质
课 程 标 准 知 识 建 构
1.能说出微粒间作用(离子键、共价键、配位键和分子间
作用力等)的主要类型、特征和实质;能比较不同类型
的微粒间作用的联系与区别;能说明典型物质的成键
类型。
2.能利用电负性判断共价键的极性,能根据共价分子
的结构特点说明简单分子的某些性质;能运用离子键、
配位键、金属键等模型,解释离子化合物、配合物、金属
等物质的某些典型性质;能说明分子间作用力(含氢键)
对物质熔、沸点等性质的影响,能列举含有氢键的物质
及其性质特点。
3.能根据给定的信息分析常见简单分子的空间结构,
能利用相关理论解释简单的共价分子的空间结构;能
根据分子结构特点和键的极性来判断分子的极性,并
据此对分子的一些典型性质及其应用做出解释。
一、化学键 电子式
1.化学键
(1)概念:相邻的原子之间强烈的相互作用。
(2)分类
2.离子键、共价键的比较
共价键
离子键
非极性键 极性键
阴、阳离子通过静
概念 电作用形成的化学 原子间通过共用电子对所形成的化学键
键
成键粒子 阴、阳离子 原子
成键实质 阴、阳离子的静电 共用电子对不偏向 共用电子对偏向一作用 任何一方原子 方原子
活泼金属与活泼非
金属经电子得失,
同种元素原子之间 不同种元素原子之
形成条件 形成离子键;或者
成键 间成键
铵根离子与酸根离
子之间
非金属单质(稀有
形成的 气体除外);某些共 共价化合物或某些
离子化合物
物质 价化合物或离子化 离子化合物
合物
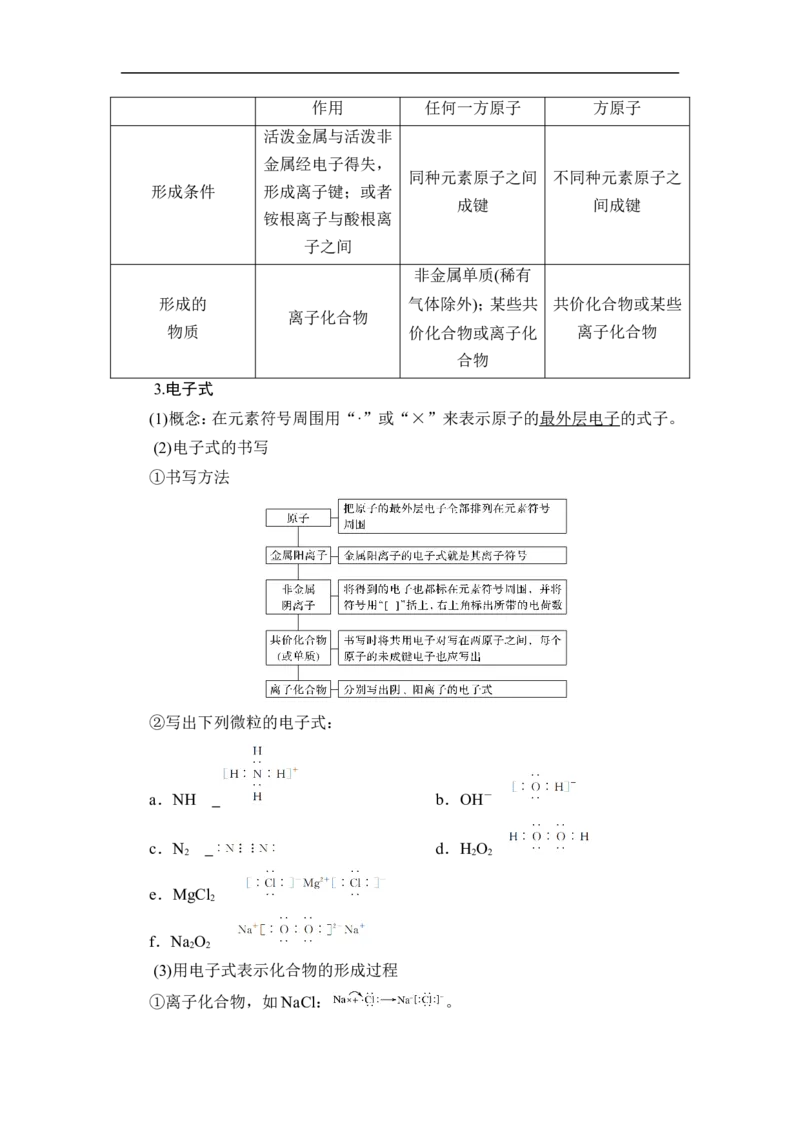
3.电子式
(1)概念:在元素符号周围用“·”或“×”来表示原子的最外层电子的式子。
(2)电子式的书写
①书写方法
②写出下列微粒的电子式:
a.NH b.OH-
c.N d.H O
2 2 2
e.MgCl
2
f.Na O
2 2
(3)用电子式表示化合物的形成过程
①离子化合物,如NaCl: 。②共价化合物,如HCl: 。
4.化学键与物质类别的关系
(1)化学键与物质类别的关系
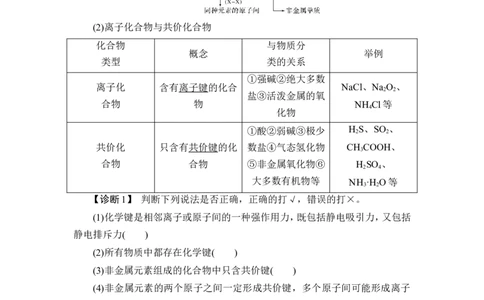
(2)离子化合物与共价化合物
化合物 与物质分
概念 举例
类型 类的关系
①强碱②绝大多数
离子化 含有离子键的化合 NaCl、Na O 、
2 2
盐③活泼金属的氧
合物 物 NH Cl等
4
化物
①酸②弱碱③极少 H S、SO 、
2 2
共价化 只含有共价键的化 数盐④气态氢化物 CH COOH、
3
合物 合物 ⑤非金属氧化物⑥ H SO 、
2 4
大多数有机物等 NH ·H O等
3 2
【诊断1】 判断下列说法是否正确,正确的打√,错误的打×。
(1)化学键是相邻离子或原子间的一种强作用力,既包括静电吸引力,又包括
静电排斥力( )
(2)所有物质中都存在化学键( )
(3)非金属元素组成的化合物中只含共价键( )
(4)非金属元素的两个原子之间一定形成共价键,多个原子间可能形成离子
键( )
(5)由活泼金属元素与活泼非金属元素形成的化学键都是离子键( )
(6)最外层只有一个电子的元素原子跟卤素原子结合时,所形成的化学键一
定是离子键( )
(7)离子化合物中可能含有共价键,共价化合物中一定不含离子键( )
答案 (1)√ (2)× (3)× (4)√ (5)× (6)× (7)√
二、共价键及其参数1.本质和特征
共价键的本质是在原子之间形成共用电子对(电子云重叠),特征是具有饱和
性和方向性。
2.分类
分类依据 类型
σ 键 原子轨道“头碰头”重叠
原子轨道的重叠方式
π 键 原子轨道“肩并肩”重叠
极性键 共用电子对发生偏移
共用电子对是否偏移 非极性
共用电子对不发生偏移
键
单键 原子间有一对共用电子对
原子间共用电子对的数目 双键 原子间有两对共用电子对
三键 原子间有三对共用电子对
3.键参数
(1)概念
(2)键参数对分子性质的影响
①键能越大,键长越短,分子越稳定。
②
【特别提醒】
只有元素的电负性相差不大时,原子间才能形成共用电子对而形成共价键,
当元素电负性相差较大(大于1.7)时,不能形成共用电子对,而形成离子键。
【诊断2】 判断下列说法是否正确,正确的打√,错误的打×。
(1)共价键是成键原子之间的强相互作用 ( )
(2)在任何情况下σ键都比π键强度大( )
(3)共价键的成键原子只能是非金属原子( )
(4)σ键和π键都能单独形成( )
(5)σ键可以绕键轴旋转,π键一定不能绕键轴旋转( )(6)碳碳三键和碳碳双键的键能分别是碳碳单键键能的3倍和2倍( )
答案 (1)√ (2)× (3)× (4)× (5)√ (6)×
三、价层电子对互斥理论和杂化轨道理论、配位键
1.价层电子对互斥理论
(1)理论要点
①价层电子对在空间上彼此相距最远时,排斥力最小,体系的能量最低。
②孤电子对的排斥力较大,孤电子对越多,排斥力越强,键角越小。
(2)分子中的中心原子上的价层电子对数的计算
其中:a是中心原子的价电子数(阳离子要减去电荷数、阴离子要加上电荷数),
b是与中心原子结合的原子最多能接受的电子数,x是与中心原子结合的原子数。
(3)示例分析
价层电 σ键电 孤电子 VSEPR 分子立
实例
子对数 子对数 对数 模型名称 体构型
2 2 0 直线形 直线形 CO
2
3 0 平面三角形 BF
3
3 三角形
2 1 V 形 SO
2
4 0 正四面体形 CH
4
4 3 1 四面体形 三角锥形 NH
3
2 2 V 形 H O
2
2.杂化轨道理论
(1)理论要点
①原子成键时,原子的价电子轨道相互混杂,形成与原轨道数目相等且能量
相同的杂化轨道。
②杂化轨道数不同,轨道间的夹角不同,形成分子的空间结构不同。
(2)杂化轨道的类型(3)杂化轨道与分子立体构型的关系
杂化 杂化轨 杂化轨道
分子立体构型 实例
类型 道数目 间夹角
sp 2 180° 直线形 BeCl
2
sp2 3 120° 平面三角形 BF
3
sp3 4 109°28′ 四面体形 CH
4
3.配位键
(1)孤电子对
分子或离子中没有跟其他原子共用的电子对称孤电子对。
(2)配位键
①配位键的形成:成键原子一方提供孤电子对,另一方提供空轨道形成共价
键。
②配位键的表示:常用“ A → B ”来表示配位键,箭头指向接受孤电子对的原
子,如NH可表示为 ,在NH中,虽然有一个N—H键形成过程与其他
3个N—H键形成过程不同,但是一旦形成之后,4个共价键完全相同。
(3)配合物:如[Cu(NH ) ]SO
3 4 4
(4)配位键的形成条件:
①配体有孤电子对,如H O、NH 、CO、F-、Cl-、CN-等。
2 3
②中心原子有空轨道,如Fe3+、Cu2+、Zn2+、Ag+等。
【诊断3】 判断下列说法是否正确,正确的打√,错误的打×。
(1)价层电子对互斥理论中,π键的电子对数不计入中心原子的价层电子对数
( )
(2)分子中的中心原子若通过sp3杂化轨道成键,则该分子一定为正四面体结
构( )
(3)NH 分子为三角锥形,N原子发生sp2杂化( )
3
(4)只要分子构型为平面三角形,中心原子均为sp2杂化( )
(5)中心原子是sp杂化的,其分子构型不一定为直线形( )
(6)杂化轨道只用于形成σ键或用于容纳未参与成键的孤电子对( )答案 (1)√ (2)× (3)× (4)√ (5)× (6)√
四、分子间作用力和分子性质
1.分子间作用力
(1)概念:物质分子之间普遍存在的相互作用力。
(2)分类:范德华力和氢键。
(3)强弱:范德华力<氢键<化学键。
(4)范德华力
①一般来说,组成和结构相似的物质,随着相对分子质量的增加,范德华力逐
渐增大。
②范德华力主要影响物质的熔点、沸点、硬度等物理性质。范德华力越强,物
质的熔点、沸点越高,硬度越大。
(5)氢键
①形成:已经与电负性很强的原子形成共价键的氢原子(该氢原子几乎为裸
露的质子)与另一个分子中电负性很强的原子之间的作用力,称为氢键。
②表示方法: A—H … B 。
③特征:具有一定的方向性和饱和性。
④分类:氢键包括分子内氢键和分子间氢键两种。
⑤分子间氢键对物质性质的影响
主要表现为使物质的熔、沸点升高,对电离和溶解度等产生影响。
2.分子的性质
(1)分子的极性
类型 非极性分子 极性分子
正电中心和负电中心重合 正电中心和负电中心不重
形成原因
的分子 合的分子
存在的
非极性键或极性键 非极性键或极性键
共价键
分子内
对称 不对称
原子排列
(2)物质的溶解性
①“相似相溶”的规律:非极性溶质一般能溶于非极性溶剂,极性溶质一般
能溶于极性溶剂。若溶剂和溶质分子之间可以形成氢键,则溶质的溶解度增大。
②随着溶质分子中憎水基个数的增多,溶质在水中的溶解度减小。如甲醇、乙
醇和水以任意比互溶,而戊醇在水中的溶解度明显减小。3.分子的手性
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像
却在三维空间里不能重叠,互称手性异构体。具有手性异构体的分子叫手性分子
4.无机含氧酸分子的酸性
对于同一种元素的无机含氧酸来说,该元素的化合价越高,其含氧酸的酸性
越强。如果把含氧酸的通式写成(HO) RO ,R相同时,n值越大,酸性越强。如酸
m n
性:H SO >H SO ,HNO >HNO ,HClO >HClO >HClO >HClO。
2 4 2 3 3 2 4 3 2
【诊断4】 判断下列说法是否正确,正确的打√,错误的打×。
(1)范德华力是短程作用力,分子之间距离太远可忽略 ( )
(2)乙醇分子和水分子间只存在范德华力( )
(3)氢键具有方向性和饱和性,属于化学键的一种( )
(4)H O 分子间存在氢键( )
2 2
(5)卤素单质、卤素氢化物的熔、沸点均随着相对分子质量的增大而增大(
)
(6)氢键的存在一定能使物质的熔、沸点升高( )
(7)H O比H S稳定是因为水分子间存在氢键( )
2 2
答案 (1) √ (2)× (3)× (4)√ (5)× (6)× (7)×
考点一 共价键类型的判断及应用
【典例1】 有下列十种物质:①CH ②CH CH OH
4 3 2
③N ④HCl ⑤CO ⑥CH CH ⑦C H ⑧C H
2 2 3 3 2 4 2 2
⑨H O ⑩HCHO
2 2
请按要求回答下列问题(填写编号):
(1)只有σ键的有________,既有σ键又有π键的有________。
(2)只含有极性键的化合物有________,既含有极性键,又含有非极性键的化
合物有________。
(3)含有双键的有________,含有三键的有________。
答案 (1)①②④⑥⑨ ③⑤⑦⑧⑩
(2)①④⑤⑩ ②⑥⑦⑧⑨
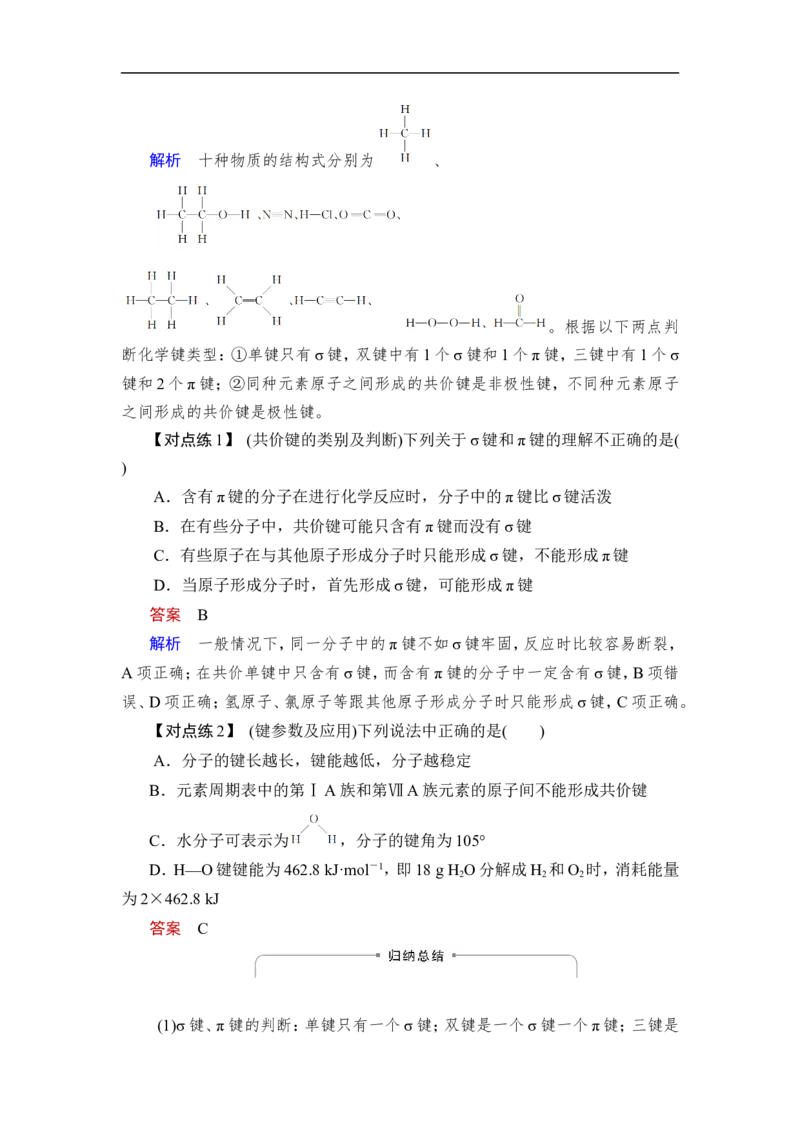
(3)⑤⑦⑩ ③⑧解析 十种物质的结构式分别为 、
。根据以下两点判
断化学键类型:①单键只有σ键,双键中有1个σ键和1个π键,三键中有1个σ
键和2个π键;②同种元素原子之间形成的共价键是非极性键,不同种元素原子
之间形成的共价键是极性键。
【对点练1】 (共价键的类别及判断)下列关于σ键和π键的理解不正确的是(
)
A.含有π键的分子在进行化学反应时,分子中的π键比σ键活泼
B.在有些分子中,共价键可能只含有π键而没有σ键
C.有些原子在与其他原子形成分子时只能形成σ键,不能形成π键
D.当原子形成分子时,首先形成σ键,可能形成π键
答案 B
解析 一般情况下,同一分子中的π键不如σ键牢固,反应时比较容易断裂,
A项正确;在共价单键中只含有σ键,而含有π键的分子中一定含有σ键,B项错
误、D项正确;氢原子、氯原子等跟其他原子形成分子时只能形成σ键,C项正确。
【对点练2】 (键参数及应用)下列说法中正确的是( )
A.分子的键长越长,键能越低,分子越稳定
B.元素周期表中的第ⅠA族和第ⅦA族元素的原子间不能形成共价键
C.水分子可表示为 ,分子的键角为105°
D.H—O键键能为462.8 kJ·mol-1,即18 g H O分解成H 和O 时,消耗能量
2 2 2
为2×462.8 kJ
答案 C
(1)σ键、π键的判断:单键只有一个σ键;双键是一个σ键一个π键;三键是一个σ键两个π键。
(2)成键原子半径越大,越难形成π键,如Si等难形成双键。
(3)σ键与π键由于原子轨道的重叠程度不同从而导致了两者的稳定性不同,
一般σ键比π键稳定,但N 中π键较稳定。
2
(4)并不是所有的共价键都有方向性,如s-s σ键没有方向性。
(5)原子形成共价键时优先形成σ键。
(6)配位键也属于σ键。
考点二 分子(离子)立体结构的判断
【典例2】 (2020·湖北江夏模拟)下列分子中,各分子的立体构型和中心原子
的杂化方式均正确的是( )
A.NH 平面三角形 sp3杂化
3
B.CCl 正四面体 sp2杂化
4
C.H O V形 sp3杂化
2
D.CO 三角锥形 sp3杂化
答案 C
解析 NH 分子中中心原子的价层电子对数=3+(5-3×1)=4,N的杂化方
3
式为sp3,含有一对孤电子对,分子的立体构型为三角锥形,选项A错误;B.CCl
4
分子中中心原子的价层电子对数=4+ (4-4×1)=4,C的杂化方式为sp3,没有
孤电子对,分子的立体构型为正四面体,选项B错误;H O分子中中心原子的价
2
层电子对数=2+ (6-2×1)=4,O的杂化方式为sp3,含有两对孤电子对,分子
的立体构型为V形,选项C正确; CO离子中中心原子的价层电子对数=3+ (4
+2-3×2)=3,C的杂化方式为sp2,没有孤电子对,分子的立体构型为平面三角
形,选项D错误。
杂化类型的判断方法
(1)根据杂化轨道的空间分布构型判断
①若杂化轨道在空间的分布为正四面体形或三角锥形,则分子的中心原子发
生sp3杂化。
②若杂化轨道在空间的分布呈平面三角形,则分子的中心原子发生sp2杂化。
③若杂化轨道在空间的分布呈直线形,则分子的中心原子发生sp杂化。
(2)根据杂化轨道之间的夹角判断
若杂化轨道之间的夹角为109°28′,则分子的中心原子发生sp3杂化;若杂化轨道之间的夹角为120°,则分子的中心原子发生sp2杂化;若杂化轨道之间的夹
角为180°,则分子的中心原子发生sp杂化。
(3)根据中心原子的价层电子对数判断
如中心原子的价层电子对数为4,是sp3杂化,为3是sp2杂化,为2是sp杂化
(4)根据分子或离子中有无π键及π键数目判断
如没有π键为sp3杂化,含一个π键为sp2杂化,含两个π键为sp杂化。
(5)根据等电子原理判断
如CO 是直形线分子,CNS-、N与CO 互为等电子体,所以立体构型均为直
2 2
线形,中心原子均采用sp杂化。
【对点练3】 (价层电子对互斥理论、杂化轨道理论的理解应用)根据价层电子
对互斥理论填空:
(1)OF 分子中,中心原子上的 σ 键电子对数为________,孤电子对数为
2
________,价层电子对数为________,中心原子的杂化方式为________杂化,
VSEPR模型为________,分子的立体构型为________。
(2)BF 分子中,中心原子上的 σ 键电子对数为________,孤电子对数为
3
________,价层电子对数为________,中心原子的杂化方式为________杂化,
VSEPR模型为________,分子的立体构型为________。
(3)SO 分子中,中心原子上的 σ 键电子对数为________,孤电子对数为
________,价层电子对数为________,中心原子的杂化方式为________杂化,
VSEPR模型为________,分子的立体构型为________。
答案 (1)2 2 4 sp3 四面体形 V形
(2)3 0 3 sp2 平面三角形 平面三角形
(3)4 0 4 sp3 正四面体形 正四面体形
解析 (1)OF 分子中,中心原子O的价层电子对数为2+×(6-2×1)=2+2
2
=4,中心原子的杂化方式为sp3杂化,VSEPR模型为四面体形,分子的立体构型
为V形。
(2)BF 分子中,中心原子B的价层电子对数为3+×(3-3×1)=3,中心原子
3
的杂化方式为sp2杂化,VSEPR模型为平面三角形,分子的立体构型为平面三角
形。
(3)SO离子中,中心原子为S原子,其价层电子对数为4+×(6+2-4×2)=
4,中心原子的杂化方式为sp3杂化,VSEPR模型为正四面体形,分子的立体构型
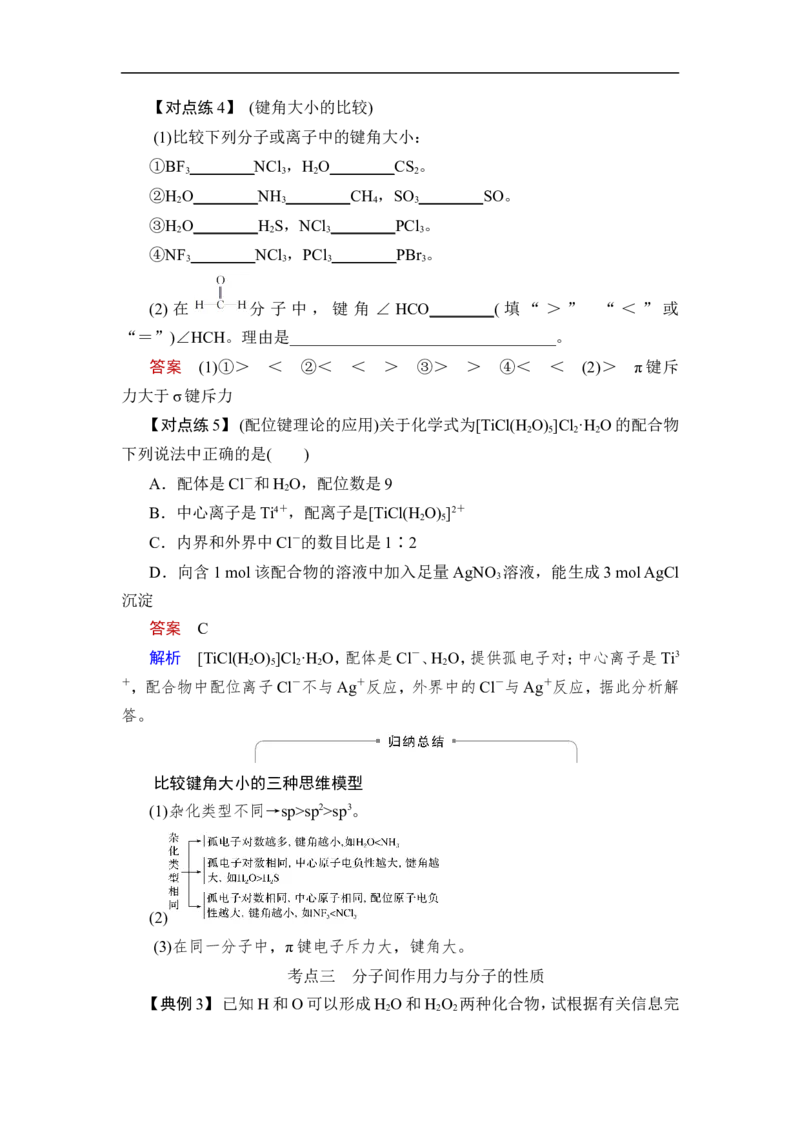
为正四面体形。【对点练4】 (键角大小的比较)
(1)比较下列分子或离子中的键角大小:
①BF ________NCl ,H O________CS 。
3 3 2 2
②H O________NH ________CH ,SO ________SO。
2 3 4 3
③H O________H S,NCl ________PCl 。
2 2 3 3
④NF ________NCl ,PCl ________PBr 。
3 3 3 3
(2) 在 分 子 中 , 键 角 ∠ HCO________( 填 “ > ” “ < ” 或
“=”)∠HCH。理由是_________________________________。
答案 (1)①> < ②< < > ③> > ④< < (2)> π键斥
力大于σ键斥力
【对点练5】 (配位键理论的应用)关于化学式为[TiCl(H O) ]Cl ·H O的配合物
2 5 2 2
下列说法中正确的是( )
A.配体是Cl-和H O,配位数是9
2
B.中心离子是Ti4+,配离子是[TiCl(H O) ]2+
2 5
C.内界和外界中Cl-的数目比是1∶2
D.向含1 mol该配合物的溶液中加入足量AgNO 溶液,能生成3 mol AgCl
3
沉淀
答案 C
解析 [TiCl(H O) ]Cl ·H O,配体是Cl-、H O,提供孤电子对;中心离子是Ti3
2 5 2 2 2
+,配合物中配位离子Cl-不与Ag+反应,外界中的Cl-与Ag+反应,据此分析解
答。
比较键角大小的三种思维模型
(1)杂化类型不同→sp>sp2>sp3。
(2)
(3)在同一分子中,π键电子斥力大,键角大。
考点三 分子间作用力与分子的性质
【典例3】 已知H和O可以形成H O和H O 两种化合物,试根据有关信息完
2 2 2成下列问题:
(1)水是维持生命活动所必需的一种物质。
①1 mol冰中有________mol氢键。
②用球棍模型表示的水分子结构是________。
(2)已知H O 分子的结构如图所示:H O 分子不是直线形的,两个氢原子犹如
2 2 2 2
在半展开的书的两面上,两个氧原子在书脊位置上,书页夹角为93°52′,而两个
O—H键与O—O键的夹角均为96°52′。
试回答:
① H O 分 子 的 电 子 式 是 ________________ , 结 构 式 是
2 2
________________________。
②H O 分子是含有________键和________键的________(填“极性”或“非
2 2
极性”)分子。
③H O 难溶于CS ,简要说明理由:__________________________。
2 2 2
④H O 中氧元素的化合价是________,简要说明原因
2 2
______________________________。
答案 (1)①2 ②B
(2)① H—O—O—H ②极性 非极性 极性 ③H O 为极
2 2
性分子,而CS 为非极性溶剂,根据“相似相溶”规律,H O 难溶于CS ④-1
2 2 2 2
价 因O—O键为非极性键,而O—H键为极性键,共用电子对偏向氧,故氧为-
1价
解析 (1)在冰中,每个水分子与周围的4个水分子形成4个氢键,按“均摊
法”计算,相当于每个水分子有2个氢键;水分子为V形结构。
(2)由H O 的立体构型图可知,H O 是极性分子,分子内既有极性键,又有非
2 2 2 2
极性键,而CS 为非极性分子,根据“相似相溶”规律,H O 难溶于CS 。
2 2 2 2
【对点练6】 (分子的结构与性质)下列说法不正确的是( )
①N H 分子中既含极性键又含非极性键 ②若R2-和M+的电子层结构相同
2 4
则原子序数:R>M ③ F 、Cl 、Br 、I 熔点随相对分子质量增大而升高
2 2 2 2④NCl 、PCl 、CO 、CS 分子中各原子均达到8e-稳定结构 ⑤固体融化成液体
3 3 2 2
的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦Na O 固体中的阴离子和阳离子个数比是1∶2
2 2
⑧由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
A.②⑤⑥⑧ B.①③④⑤
C.②④⑤⑦ D.③⑤⑦⑧
答案 A
解析 ①N H 分子中N原子和N原子之间形成非极性键,N原子和H原子
2 4
之间形成极性键,①正确;②R2-和M+的电子层结构相同,则离子的核外电子数
相等,且M处于R相邻的下一周期,所以原子序数:M>R,②错误;③F 、Cl 、
2 2
Br 、I 是组成和结构相似的分子,熔点随相对分子质量增大而升高,③正确;
2 2
④NCl 、PCl 、CO 、CS 分子中各原子均达到8e-稳定结构,④正确;⑤固体融化
3 3 2 2
成液体的过程是物理变化,也可能破坏化学键,例如氢氧化钠熔融时离子键被破
坏,⑤错误;⑥HF分子很稳定,是因为H—F键键能大,稳定,跟氢键无关,⑥错
误;⑦Na O 固体中的阴离子和阳离子分别是O、Na+,个数比是1∶2,⑦正确;⑧
2 2
氢化物的酸性与元素的非金属性无关,酸性:HCl<HBr<HI,⑧错误。
【对点练7】 (分子极性的判断)下列叙述正确的是( )
A.NH 是极性分子,N原子处在3个H原子所组成的三角形的中心
3
B.CCl 是非极性分子,C原子处在4个Cl原子所组成的正方形的中心
4
C.H O是极性分子,O原子不处在2个H原子所连成的直线的中央
2
D.CO 是非极性分子,C原子不处在2个O原子所连成的直线的中央
2
答案 C
解析 NH 是极性分子,N原子处在三角锥形的顶点,3个H原子处于锥底,
3
A项错误;CCl 是非极性分子,四个Cl原子构成的是正四面体结构,C原子处在4
4
个Cl原子所组成的四面体的中心,B项错误;H O是极性分子,是V形分子,O原
2
子不处在2个H原子所连成直线的中央,C项正确;CO 是非极性分子,三个原子
2
在一条直线上,C原子处在2个O原子所连成的直线的中央,D项错误。
键的极性、分子空间结构与分子极性的关系
类型 实例 键的极性 空间构型 分子极性
X 2 H 、N 非极性键 直线形 非极性分子
2 2XY HCl、NO 极性键 直线形 极性分子
CO 、CS 极性键 直线形 非极性分子
2 2
XY
2
SO 极性键 V形 极性分子
2
(X Y)
2
H O、H S 极性键 V形 极性分子
2 2
BF 极性键 平面三角形 非极性分子
3
XY
3
NH 极性键 三角锥形 极性分子
3
XY CH 、CCl 极性键 正四面体形 非极性分子
4 4 4
微专题19 分子结构类简答题的规范解答
一、答题角度与化学键有关的简答
1.两种三角锥形气态氢化物PH 和NH 的键角分别为93.6°和107°,试分析
3 3
PH 的键角小于NH 的原因_____________________________。
3 3
答案 N电负性强于P,且原子半径小于P,NH 中成键电子对离中心原子更
3
近,成键电子对间距离更小,致使其成键电子对间斥力大,键角更大
2.TiCl 稳定性比CCl 差,极易水解,试从结构分析其原因:
4 4
_________________________________________________________________
_______。
答案 Ti—Cl键比C—Cl键的键长大、键能小,易断裂
3.ZnF 不溶于有机溶剂而ZnCl 、ZnBr 、ZnI 能够溶于乙醇、乙醚等有机溶剂
2 2 2 2
原 因 是
_____________________________________________________________________
___。
答案 ZnF 为离子化合物,ZnCl 、ZnBr 、ZnI 的化学键以共价键为主、极性
2 2 2 2
较小
二、答题角度与化学键、分子间作用力和氢键的区别有关的简答
4 . 沸 点 高 低 : 乙 酸 钠 > 乙 酸 > 乙 醛 , 这 是 因 为
_____________________________________________________________________
____。
答案 乙酸钠是离子晶体,乙酸和乙醛是分子晶体,乙酸分子间存在氢键
三、答题角度与氢键的类别、数目有关的简答
5.邻羟基苯甲酸(又名水杨酸, )和对羟基苯甲酸( )都是 二 元 酸 。 二 者 沸 点 相 差 较 大 的 理 由 是
_____________________________________________________________________
___。
答案 对羟基苯甲酸只在分子间形成氢键,邻羟基苯甲酸只在分子内形成氢
键,所以前者沸点高于后者
6.氮的一种氢化物 N H 是一种良好的火箭发射燃料,其熔点、沸点分别为
2 4
1.4 ℃、113.5 ℃,氨气的熔点、沸点分别为-77.7 ℃、-33.5 ℃。肼与氨气熔点、
沸 点 差 异 最 主 要 的 原 因 是
_____________________________________________________________________
___。
答案 N H 分子间氢键数目多于NH 分子间氢键数目
2 4 3
解析 N H 、NH 都是分子晶体,在分子之间都存在分子间作用力,由于都含
2 4 3
有N—H键,N元素的非金属性强、原子半径小,所以二者的分子之间还都存在氢
键,增加了分子间作用力,但由于N H 分子间氢键数目多于NH 分子间氢键数目
2 4 3
所以克服氢键和分子间作用力使物质熔化、汽化需要较高的能量,因此肼的熔点
沸点比氨气高。
1.(1)(2020·全国卷Ⅰ)磷酸根离子的空间构型为________,其中P的价层电子
对数为________、杂化轨道类型为________。
(2)(2020·全国卷Ⅱ)有机碱CH NH中,N原子的杂化轨道类型是________;
3
CaTiO 的组成元素的电负性大小顺序是________________。
3
(3)(2020·全国卷Ⅲ)①NH BH 分子中,N—B化学键称为________键,其电子
3 3
对由________提供。氨硼烷在催化剂作用下水解释放氢气:
3NH BH +6H O===3NH+B O+9H ↑
3 3 2 3 2
B O的结构为 。在该反应中,B原子的杂化轨道类型由________
3
变为________。
②NH BH 分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈
3 3
负电性(Hδ-),电负性大小顺序是________。与NH BH 原子总数相等的等电子体
3 3
是________(写分子式),其熔点比NH BH ___________ (填“高”或“低”),原
3 3
因是在NH BH 分子之间,存在_________________________,也称“双氢键”。
3 3
答案 (1)正四面体 4 sp3 (2)sp3 O>Ti>Ca(3)①配位 N sp3 sp2 ②N>H>B CH CH 低 Hδ+与Hδ-的静电引力
3 3
解析 (1)PO的中心原子P的价层电子对数为4,孤电子对数为0,中心原子
P为sp3杂化,故PO的空间构型为正四面体。
(2)CH NH中N原子与2个H原子、1个C原子形成三个共价键,与H+形成
3
一个配位键,故N原子的杂化轨道类型为sp3;O为非金属元素,其电负性在三种
元素中最大,Ca和Ti同为第四周期元素,金属性Ca大于Ti,故电负性大小顺序
为O>Ti>Ca。
(3)①NH BH 中N有孤对电子,B有空轨道,N和B形成配位键,电子对由N
3 3
提供。NH BH 中B形成四个σ键,为sp3杂化,B O中B形成3个σ键,为sp2杂化。
3 3 3
②电负性用来描述不同元素的原子对键合电子吸引力的大小。与 N原子相连的
H呈正电性,与B原子相连的H呈负电性,故电负性N>H>B。原子数相同、价电
子总数相同的微粒互称为等电子体,与NH BH 互为等电子体的分子为CH CH 。
3 3 3 3
带相反电荷的微粒能形成静电引力,NH BH 分子间存在Hδ+与Hδ-的静电引力,
3 3
也称为“双氢键”,“双氢键”能改变物质的熔沸点,而 CH CH 分子间不存在
3 3
“双氢键”,熔沸点较低。
2.(2020·江苏化学,21)以铁、硫酸、柠檬酸、双氧水、氨水等为原料可制备柠
檬酸铁铵[(NH ) Fe(C H O ) ]。
4 3 6 5 7 2
(1)[Fe(H O) ]2+中与Fe2+配位的原子是________(填元素符号)。
2 6
(2)NH 分子中氮原子的轨道杂化类型是________。
3
(3)柠檬酸的结构简式见图。1 mol柠檬酸分子中碳原子与氧原子形成的σ键
的数目为________ mol。
答案 (1)O (2)sp3 (3)7
解析 (1)[Fe(H O) ]2+中,H O是配体,H O分子中的O原子有孤对电子,是
2 6 2 2
配位原子。(2)NH 分子中N原子有1对孤对电子,3个成键电子对,所以N原子以
3
sp3方式杂化。(3)单键都是σ键,双键中有一个σ键,则1 mol柠檬酸分子中碳原
子与氧原子形成7 mol σ键。
3.(2020·山东学业水平等级考试)CdSnAs 是一种高迁移率的新型热电材料,
2
回答下列问题:
(1)NH 、PH 、AsH 的沸点由高到低的顺序为________________(填化学式,下
3 3 3
同),还原性由强到弱的顺序为________________,键角由大到小的顺序为________________。
(2)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形
成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1 mol该配合物中通过
螯合作用形成的配位键有________ mol,该螯合物中N的杂化方式有________种
(3)(2020·天津高考)Fe、Co、Ni三种元素二价氧化物的晶胞类型相同,其熔点
由高到低的顺序为______________________________。
答案 (1)NH 、AsH 、PH AsH 、PH 、NH NH 、PH 、AsH (2)6 1
3 3 3 3 3 3 3 3 3
(3)NiO>CoO>FeO
解析 (1)NH 中存在分子间氢键,导致其沸点比与N元素同主族的P、As元
3
素的氢化物PH 、AsH 的沸点要高,而PH 、AsH 中均不存在分子间氢键,故影响
3 3 3 3
PH 、AsH 沸点的因素为范德华力,相对分子质量越大,沸点越高,则沸点由高到
3 3
低的顺序为NH 、AsH 、PH 。通常同主族元素随着原子序数的递增,气态氢化物
3 3 3
的还原性逐渐增强,则还原性由强到弱的顺序是AsH 、PH 、NH 。同主族元素,随
3 3 3
着原子序数的递增,电负性逐渐减弱,则其气态氢化物中的成键电子对逐渐远离
中心原子,致使成键电子对的排斥力降低,键角逐渐减小,故键角由大到小的顺
序是NH 、PH 、AsH 。(2)该螯合物中Cd2+与5个N原子、2个O原子形成化学键,
3 3 3
其中与1个O原子形成的为共价键,另外的均为配位键,故1 mol该配合物中通
过螯合作用形成6 mol配位键。该螯合物中无论是硝基中的N原子,还是NO中
的N原子,还是六元环中的N原子,N均为sp2杂化,即N只有1种杂化方式。(3)
因为Fe、Co、Ni的二价氧化物是离子化合物,Fe2+、Co2+、Ni2+半径依次减小,晶
体的晶格能依次增大,熔点依次升高,故熔点顺序是NiO>CoO>FeO。
4.(高考组合题)化学键的判断和分子的性质。
(1)(2018·全国卷Ⅰ)LiAlH 是有机合成中常用的还原剂,LiAlH 中,存在
4 4
________(填标号)。
A.离子键 B.σ键
C.π键 D.氢键
(2)[2018·全国卷Ⅱ,35(4)节选]气态三氧化硫以单分子形式存在,其中共价键的类型有________种。
(3)[2018·全国卷Ⅱ,35(3)改编]如图为S 的结构,其熔点和沸点要比二氧化硫
8
的熔点和沸点高很多,主要原因为____________________。
(4)(2019·全国卷Ⅲ)FeCl 中的化学键具有明显的共价性,蒸汽状态下以双聚
3
分子存在的FeCl 的结构式为________________,其中Fe的配位数为________。
3
(5)苯胺( )的晶体类型是________。苯胺与甲苯( )的相对分
子质量相近,但苯胺的熔点(-5.9 ℃)、沸点(184.4 ℃)分别高于甲苯的熔点(-
95.0 ℃)、沸点(110.6 ℃),原因是______________________________。
(6)NH H PO 中,电负性最高的元素是________;P的________杂化轨道与O
4 2 4
的2p轨道形成________键。
(7)NH H PO 和LiFePO 属于简单磷酸盐,而直链的多磷酸盐则是一种复杂
4 2 4 4
磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为_____________________ (用n代
表P原子数)。
答案 (1)AB (2)2 (3)S 相对分子质量大,分子间范德华力强
8
(4)
(5)分子晶体 苯胺分子之间存在氢键
(6)O sp3 σ (7)(P O )(n+2)-
n 3n+1
一、选择题(每小题只有一个选项符合题意)
1.下列关于σ键和π键的说法不正确的是( )
A.σ键能单独形成,π键不能单独形成
B.σ键可以绕键轴旋转,π键不能绕键轴旋转
C.双键中一定有一个σ键,一个π键,三键中一定有一个σ键,两个π键
D.CH —CH 、CH ===CH 、CH≡CH中的σ键都是C—C键,所以键能都相
3 3 2 2
同答案 D
解析 单键都是σ键,双键中有1个σ键、1个π键,三键中有1个σ键、2个
π键,所以σ键能单独形成、π键不能单独形成,故A、C正确;σ键通过头碰头形
成,而π键通过肩并肩形成,σ键可以绕键轴旋转,π键不能绕键轴旋转,故B正
确;CH —CH 、CH ===CH 、CH≡CH中的C—H键、C—C键都是σ键,故D错误
3 3 2 2
2.徐光宪在《分子共和国》一书中介绍了许多明星分子,如H O 、CO 、BF 、
2 2 2 3
CH COOH等。下列说法正确的是( )
3
A.H O 分子中O原子为sp2杂化
2 2
B.CO 分子中C原子为sp杂化
2
C.BF 分子中B原子为sp3杂化
3
D.CH COOH分子中C原子均为sp2杂化
3
答案 B
解析 杂化轨道只能用于形成σ键或容纳未参与成键的孤电子对。H O 的分
2 2
子结构为H—O—O—H,每个O原子形成2个σ键,每个O原子含2对孤电子对,
则O原子采取sp3杂化,A错误;CO 的结构式为O===C===O,C原子形成2个σ
2
键和2个π键,则C原子采取sp杂化,B正确;BF 中B原子形成3个σ键,不含
3
孤电子对,则B原子采取sp2杂化,C错误;CH COOH分子中甲基中C原子采取
3
sp3杂化,—COOH中C原子采取sp2杂化,D错误。
3.下列说法中错误的是( )
A.卤化氢中,HF的沸点最高,是由于HF分子间存在氢键
B.邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
C.H O的沸点比HF的沸点高,是由于水中氢键键能大
2
D.氨气极易溶于水与氨气分子和水分子间形成氢键有关
答案 C
解析 HF分子之间存在氢键,故熔、沸点相对较高,故A正确;能形成分子
间氢键的物质熔、沸点较高,邻羟基苯甲醛容易形成分子内氢键,对羟基苯甲醛
易形成分子间氢键,所以邻羟基苯甲醛的沸点比对羟基苯甲醛的沸点低,故B正
确;H O分子最多与周围H O分子形成4个氢键,而HF分子最多与周围HF分子
2 2
形成两个氢键,氢键越多,熔、沸点越高,所以H O熔、沸点高,故C错误;氨气分
2
子和水分子间形成氢键,导致氨气极易溶于水,故D正确。4.毒奶粉主要是奶粉中含有有毒的三聚氰胺( )。下列关于三聚氰
胺分子的说法中正确的是( )
A.所有氮原子均采取sp3杂化
B.一个三聚氰胺分子中共含有15个σ键
C.属于极性分子
D.三聚氰胺分子中同时含有极性键和非极性键
答案 B
解析 C===N键中N原子采取sp2杂化,—NH 中N原子采取sp3杂化,A错
2
误;1个三聚氰胺分子中含有6个N—H键、6个C—N键和3个C===N键,每个
双键中含有1个σ键,故1个三聚氰胺分子中含有15个σ键,B正确;由三聚氰
胺的结构简式可知,该分子结构对称,是非极性分子,C错误;三聚氰胺分子中只
含有极性键,不含非极性键,D错误。
5.(2020·枣庄模拟)镍能形成多种配合物如正四面体形的Ni(CO) 和正方形的
4
[Ni(CN) ]2-、正八面体形的[Ni(NH ) ]2+等。Ni(CO) 常温下为液态,易溶于CCl 、
4 3 6 4 4
苯等有机溶剂。下列说法正确的是( )
A.NH 的键角大于CCl
3 4
B.固态Ni(CO) 属于离子晶体
4
C.Ni(CO) 和[Ni(CN) ]2-中,镍元素均是sp3杂化
4 4
D.Ni(CO) 分子内σ键和π键个数之比为1∶1
4
答案 D
解析 A.NH 是三角锥形,键角为107°,CCl 是正四面体,键角为109°28′,
3 4
所以NH 的键角小于CCl ,故A错误;B.Ni(CO) 常温下为液态,易溶于有机溶剂,
3 4 4
属于分子晶体,不是离子晶体,故B错误;C.[Ni(CN) ]2-为正方形,Ni(CO) 为正
4 4
四面体形,故杂化方式不同,故C错误;D.配位键中有1个σ键,CO分子内含有1
个σ键和2个π键,Ni(CO) 分子内σ键和π键个数之比为1∶1,故D正确。
4
6.(2020·平度模拟)氯化亚砜(SOCl )是一种很重要的化学试剂,可以作为氯化
2
剂和脱水剂。下列关于氯化亚砜分子的几何构型和中心原子(S)采取杂化方式的
说法正确的是( )
A.三角锥形、sp3 B.V形、sp2
C.平面三角形、sp2 D.三角锥形、sp2答案 A
解析 根据价层电子对互斥理论确定微粒的空间构型,SOCl 中S原子成2
2
个S-Cl键,1个S===O,价层电子对个数=σ键个数+孤电子对个数=3+=4,
杂化轨道数是4,故S原子采取sp3杂化,含一对孤电子,分子形状为三角锥形。
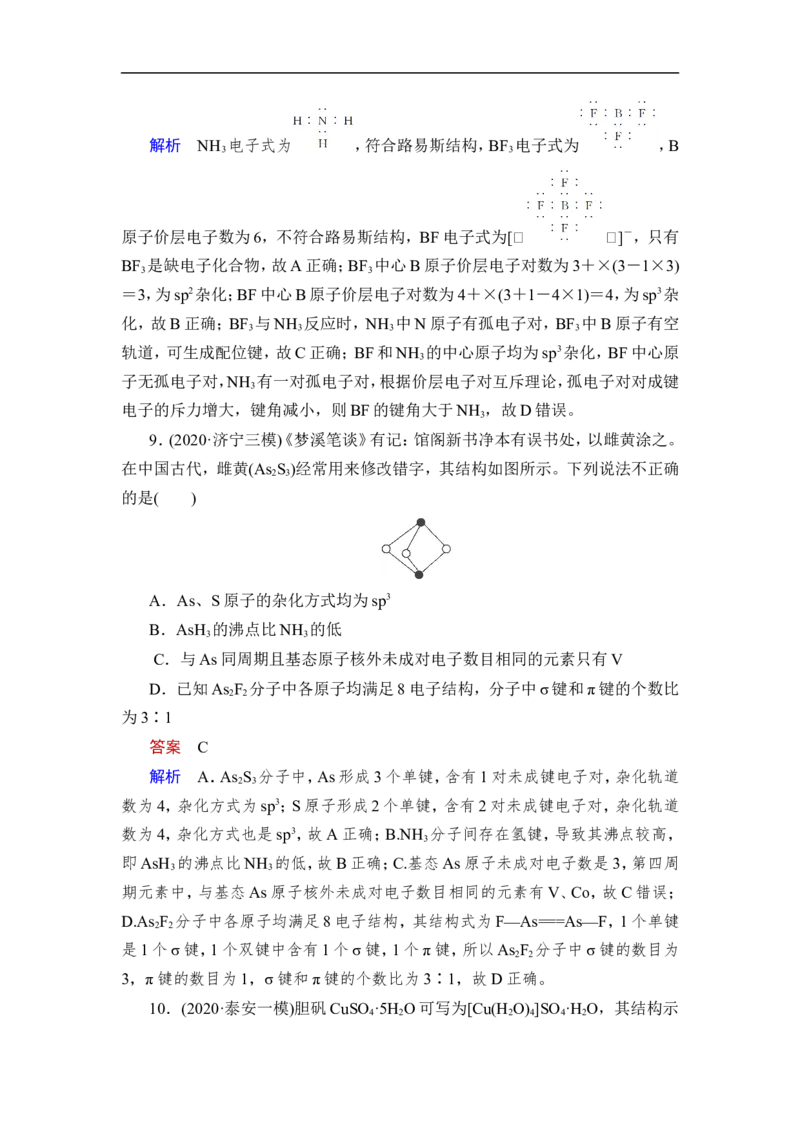
7.(2020·威海二模)“冰面为什么滑?”,这与冰层表面的结构有关(如图)。下
列有关说法错误的是( )
A.由于氢键的存在,水分子的稳定性好,高温下也很难分解
B.第一层固态冰中,水分子间通过氢键形成空间网状结构
C.第二层“准液体”中,水分子间形成氢键的机会比固态冰中少
D.当高于一定温度时,“准液体”中的水分子与下层冰连接的氢键断裂,产
生“流动性的水分子”,使冰面变滑
答案 A
解析 A.水分子的稳定性好,是由水分子内氢氧共价键的键能决定的,与分
子间形成的氢键无关,故A错误;B.固态冰中,1个水分子与周围的4个水分子通
过氢键相连接,从而形成空间网状结构,故B正确;C.“准液体”中,水分子间的
距离不完全相等,所以1个水分子与少于4个的水分子间距离适合形成氢键,形
成氢键的机会比固态冰中少,故C正确;D.当温度达到一定数值时,“准液体”
中的水分子与下层冰连接的氢键被破坏,使一部分水分子能够自由流动,从而产
生“流动性的水分子”,造成冰面变滑,故D正确。
8.(2020·山东模考)缺电子化合物是指电子数不符合路易斯结构(一个原子通
过共享电子使其价层电子数达到8,H原子达到2所形成稳定分子结构)要求的一
类化合物。下列说法错误的是( )
A.NH 、BF 、BF中只有BF 是缺电子化合物
3 3 3
B.BF 、BF中心原子的杂化方式分别为sp2、sp3
3
C.BF 与NH 反应时有配位键生成
3 3
D.BF的键角小于NH
3
答案 D解析 NH 电子式为 ,符合路易斯结构,BF 电子式为 ,B
3 3
原子价层电子数为6,不符合路易斯结构,BF电子式为[ ]-,只有
BF 是缺电子化合物,故A正确;BF 中心B原子价层电子对数为3+×(3-1×3)
3 3
=3,为sp2杂化;BF中心B原子价层电子对数为4+×(3+1-4×1)=4,为sp3杂
化,故B正确;BF 与NH 反应时,NH 中N原子有孤电子对,BF 中B原子有空
3 3 3 3
轨道,可生成配位键,故C正确;BF和NH 的中心原子均为sp3杂化,BF中心原
3
子无孤电子对,NH 有一对孤电子对,根据价层电子对互斥理论,孤电子对对成键
3
电子的斥力增大,键角减小,则BF的键角大于NH ,故D错误。
3
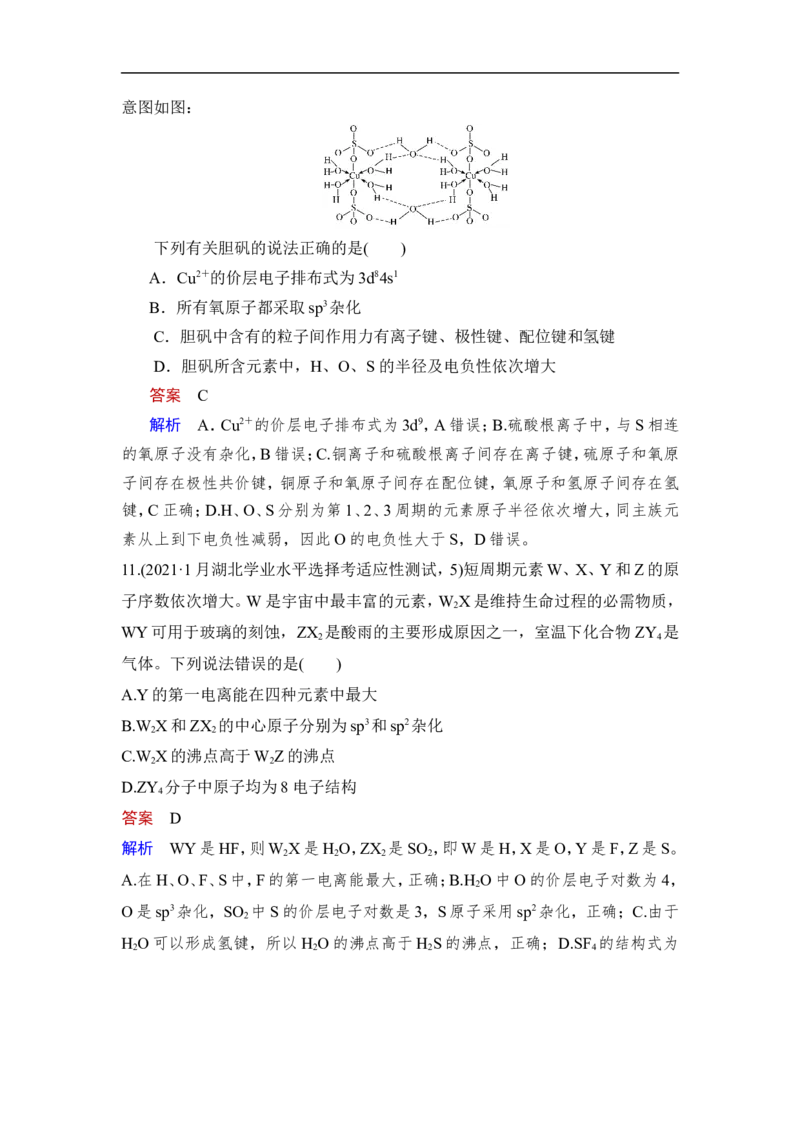
9.(2020·济宁三模)《梦溪笔谈》有记:馆阁新书净本有误书处,以雌黄涂之。
在中国古代,雌黄(As S )经常用来修改错字,其结构如图所示。下列说法不正确
2 3
的是( )
A.As、S原子的杂化方式均为sp3
B.AsH 的沸点比NH 的低
3 3
C.与As同周期且基态原子核外未成对电子数目相同的元素只有V
D.已知As F 分子中各原子均满足8电子结构,分子中σ键和π键的个数比
2 2
为3∶1
答案 C
解析 A.As S 分子中,As形成3个单键,含有1对未成键电子对,杂化轨道
2 3
数为4,杂化方式为sp3;S原子形成2个单键,含有2对未成键电子对,杂化轨道
数为4,杂化方式也是sp3,故A正确;B.NH 分子间存在氢键,导致其沸点较高,
3
即AsH 的沸点比NH 的低,故B正确;C.基态As原子未成对电子数是3,第四周
3 3
期元素中,与基态As原子核外未成对电子数目相同的元素有V、Co,故C错误;
D.As F 分子中各原子均满足8电子结构,其结构式为F—As===As—F,1个单键
2 2
是1个σ键,1个双键中含有1个σ键,1个π键,所以As F 分子中σ键的数目为
2 2
3,π键的数目为1,σ键和π键的个数比为3∶1,故D正确。
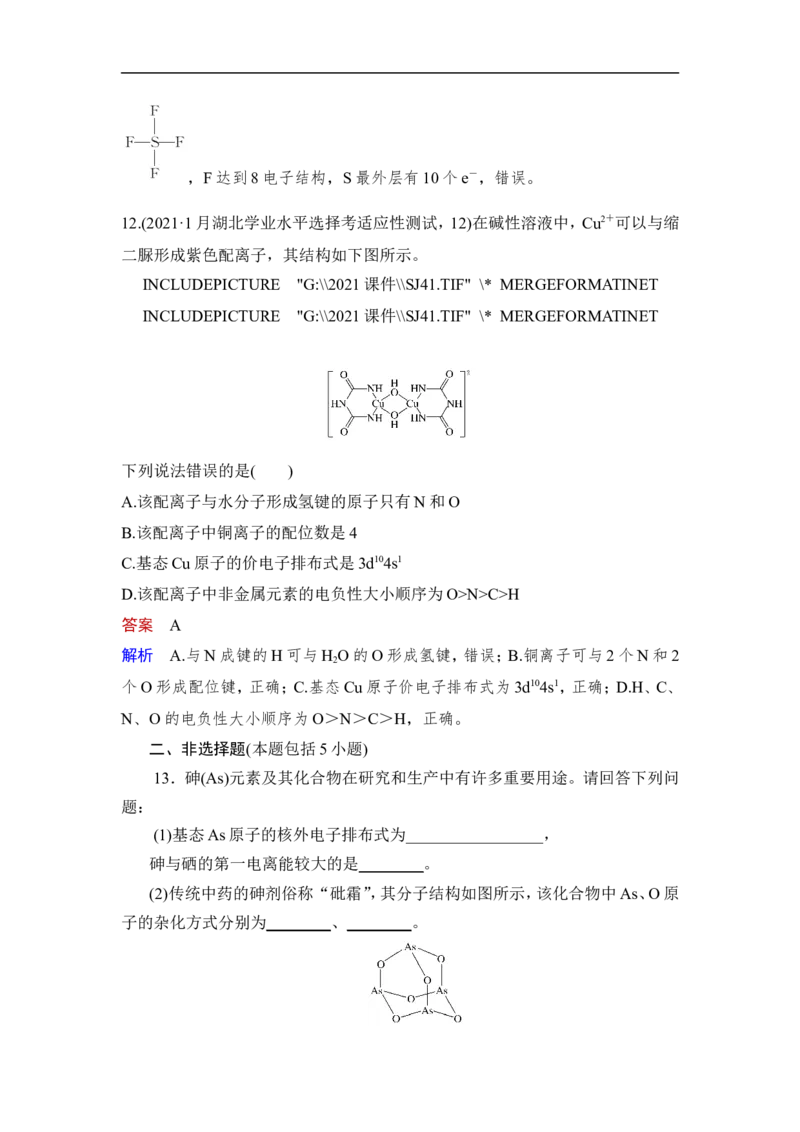
10.(2020·泰安一模)胆矾CuSO ·5H O可写为[Cu(H O) ]SO ·H O,其结构示
4 2 2 4 4 2意图如图:
下列有关胆矾的说法正确的是( )
A.Cu2+的价层电子排布式为3d84s1
B.所有氧原子都采取sp3杂化
C.胆矾中含有的粒子间作用力有离子键、极性键、配位键和氢键
D.胆矾所含元素中,H、O、S 的半径及电负性依次增大
答案 C
解析 A.Cu2+的价层电子排布式为3d9,A错误;B.硫酸根离子中,与S相连
的氧原子没有杂化,B错误;C.铜离子和硫酸根离子间存在离子键,硫原子和氧原
子间存在极性共价键,铜原子和氧原子间存在配位键,氧原子和氢原子间存在氢
键,C正确;D.H、O、S分别为第1、2、3周期的元素原子半径依次增大,同主族元
素从上到下电负性减弱,因此O的电负性大于S,D错误。
11.(2021·1月湖北学业水平选择考适应性测试,5)短周期元素W、X、Y和Z的原
子序数依次增大。W是宇宙中最丰富的元素,W X是维持生命过程的必需物质,
2
WY可用于玻璃的刻蚀,ZX 是酸雨的主要形成原因之一,室温下化合物 ZY 是
2 4
气体。下列说法错误的是( )
A.Y的第一电离能在四种元素中最大
B.W X和ZX 的中心原子分别为sp3和sp2杂化
2 2
C.W X的沸点高于W Z的沸点
2 2
D.ZY 分子中原子均为8电子结构
4
答案 D
解析 WY是HF,则W X是H O,ZX 是SO ,即W是H,X是O,Y是F,Z是S。
2 2 2 2
A.在H、O、F、S中,F的第一电离能最大,正确;B.H O中O的价层电子对数为4,
2
O是sp3杂化,SO 中S的价层电子对数是3,S原子采用sp2杂化,正确;C.由于
2
H O可以形成氢键,所以H O的沸点高于H S的沸点,正确;D.SF 的结构式为
2 2 2 4,F达到8电子结构,S最外层有10个e-,错误。
12.(2021·1月湖北学业水平选择考适应性测试,12)在碱性溶液中,Cu2+可以与缩
二脲形成紫色配离子,其结构如下图所示。
INCLUDEPICTURE "G:\\2021课件\\SJ41.TIF" \* MERGEFORMATINET
INCLUDEPICTURE "G:\\2021课件\\SJ41.TIF" \* MERGEFORMATINET
下列说法错误的是( )
A.该配离子与水分子形成氢键的原子只有N和O
B.该配离子中铜离子的配位数是4
C.基态Cu原子的价电子排布式是3d104s1
D.该配离子中非金属元素的电负性大小顺序为O>N>C>H
答案 A
解析 A.与N成键的H可与H O的O形成氢键,错误;B.铜离子可与2个N和2
2
个O形成配位键,正确;C.基态Cu原子价电子排布式为3d104s1,正确;D.H、C、
N、O的电负性大小顺序为O>N>C>H,正确。
二、非选择题(本题包括5小题)
13.砷(As)元素及其化合物在研究和生产中有许多重要用途。请回答下列问
题:
(1)基态As原子的核外电子排布式为_________________,
砷与硒的第一电离能较大的是________。
(2)传统中药的砷剂俗称“砒霜”,其分子结构如图所示,该化合物中As、O原
子的杂化方式分别为________、________。(3)Na AsO 可作杀虫剂。AsO的立体构型为________,与其互为等电子体的
3 4
分子的化学式为________(任写一种)。
答案 (1)1s22s22p63s23p63d104s24p3 或[Ar]3d104s24p3 As 或砷 (2)sp3 杂化
sp3杂化
(3)正四面体形 CF (或SiF 、CCl 、SiCl ,合理即可)
4 4 4 4
解析 (1)砷由于4p轨道为半充满状态,结构稳定,第一电离能比Se大。(2)
该化合物中As有一个孤电子对,杂化类型为sp3杂化,O有两个孤电子对,杂化
类型为sp3杂化。(3)AsO中As无孤电子对,立体构型为正四面体形,与AsO互为
等电子体的分子有CF 、SiF 、CCl 、SiCl 等。
4 4 4 4
14.芦笋中的冬天酰胺(结构如下图)和微量元素硒、铬、锰等,具有提高身体
免疫力的功效。
(1)天冬酰胺所含元素中,________(填元素名称)元素基态原子核外未成对电
子数最多。
(2)天冬酰胺中碳原子的杂化轨道类型有________种。
(3)H S和H Se的参数对比见下表。
2 2
化学式 键长/nm 键角 沸点/℃
H S 1.34 92.3° -60.75
2
H Se 1.47 91.0° -41.50
2
①H Se分子中含有共价键类型为________。
2
②H S的键角大于H Se的原因可能为______________________________。
2 2
答案 (1)氮 (2)2 (3)①极性键 ②S的电负性强于Se,形成的共用电子
对斥力大,键角大
解析 (3)①H S和H Se的熔、沸点均较低,为分子晶体,不同种元素原子形
2 2
成的为极性键。②S的电负性强于Se,形成的共用电子对斥力大,故H S键角大。
2
15.1985年,Rousssin研究发现了第一个金属原子簇类配位化合物,其结构
如图所示,金属原子簇类化合物与金属原子表面性质相似,具有良好的催化活性
等功能。请回答下列问题:
(1)硫可以形成SOCl 化合物,则该化合物的立体构型为________。
2
(2)除了氮的氧化物之外,氮还可以形成 NO。请写出氮原子的杂化方式
________。
(3)上述原子簇类配合物,中心原子铁的配位原子是________________。
(4)配合物Fe(CO) 的熔点为-20 ℃,沸点103 ℃。可用于制备纯铁。Fe(CO)
5 5
的结构如下图所示。下列关于Fe(CO) 说法正确的是________(填字母)。
5
A.Fe(CO) 是非极性分子,CO是极性分子
5
B.Fe(CO) 中Fe原子以sp3杂化方式与CO成键
5
C.1 mol Fe(CO) 含有10 mol配位键
5
D.Fe(CO) ===Fe+5CO反应中没有新化学键生成
5
答案 (1)三角锥形 (2)sp (3)S、N (4)AC
解析 (1)对于SOCl 其等电子体为SO,二者结构相似,根据VSEPR理论,价
2
电子对数为3+×(6-2×3+2)=4,则其立体构型为三角锥形。(2)对于NO,根据
VSEPR理论,价电子对数为2+×(5-2×2-1)=2,根据杂化轨道理论,则中心
N原子为sp杂化。(3)直接与中心原子成键的为配位原子,所以中心原子铁的配位
原子是:N、S。(4)A项,Fe(CO) 对称是非极性分子,CO不对称是极性分子,正确;
5
B项,铁的杂化轨道数为5,Fe(CO) 分子不是正四面体构型,Fe(CO) 中Fe原子
5 5
不是以sp3杂化方式与CO成键,错误;C项,碳与氧、铁与碳之间形成配位键,1
mol Fe(CO) 含有10 mol 配位键,正确;D项,反应生成金属键,错误。
5
16.Fe、C、N、O、H可以组成多种物质。回答下列问题:
(1)N≡N键的键能为942 kJ·mol-1,N—N单键的键能为247 kJ·mol-1,计算说
明N 中的________键比________键稳定(填“σ”或“π”)。
2
(2)配合物Fe(CO) 会使合成氨等生产过程中的催化剂中毒。
5
CO分子中σ键与π键数目之比为________。
(3)(CN) 分子中所有原子最外层都满足8电子,请写出其结构式:________。
2(CN) 分子为________(填“极性”或“非极性”)分子。
2
(4)H O+中H—O—H的键角比 H O中H—O—H的键角________(填“大”
3 2
或“小”),原因是___________________。
(5)血红素分子结构如图所示。
①血红素分子间存在的作用力有________(填名称)。
②血红素分子中 C 原子的杂化方式为________,N 原子的杂化方式为
________。
③与Fe通过配位键结合的氮原子的编号是________。
答案 (1)π σ (2)1∶2 (3)N≡C—C≡N 非极性
(4)大 H O中O原子有2对孤对电子,而H O+中O原子只有1对孤对电子,
2 3
排斥力较小
(5)①范德华力、氢键 ②sp2、sp3 sp2、sp3 ③1和3
解析 (1)N≡N键中σ键的键能为247 kJ·mol-1,π键的平均键能为 kJ·mol-1
=347.5 kJ·mol-1,故π键比σ键稳定。(2)由N 的结构式类推CO中C、O之间为
2
三键,含有1个σ键、2个π键。(3)(CN) 的结构式为N≡C—C≡N,为直线形分子,
2
属于非极性分子。(4)H O中O原子有2对孤对电子,而H O+中O原子只有1对
2 3
孤对电子,排斥力较小,故H O+中H—O—H的键角比H O中H—O—H的键角
3 2
大。(5)①血红素分子间存在范德华力,血红素分子中存在羧基,能形成氢键。②
血红素分子中形成4个单键的C为sp3杂化,形成2个单键和1个双键的C为sp2
杂化;形成3个单键的N为sp3杂化,形成2个单键和1个双键的N为sp2杂化。
③2、4号N原子形成3个单键,达到8电子稳定结构,而1、3号N形成2个单键、
1个双键,其中有一个单键为配位键。
17.已知A、B、C、D、E、F为元素周期表前四周期原子序数依次增大的六种
元素,其中A的一种同位素原子中无中子,B的一种核素在考古时常用来鉴定一
些文物的年代,D与E同主族,且E的原子序数是D的2倍,F元素在地壳中的含
量位于金属元素的第二位。试回答下列问题:(1)关于B A 的下列说法中正确的是________。
2 2
①B A 中的所有原子都满足8电子稳定结构
2 2
②B A 是由极性键和非极性键形成的非极性分子
2 2
③每个B A 分子中σ键和π键数目比为1∶1
2 2
④B A 分子中的A—B键属于s-sp σ键
2 2
(2)B 、 C 、 D 三 种 元 素 中 与 BD 互 为 等 电 子 体 的 分 子 式 为
2
________________________(用元素符号表示)。
(3)A E分子中心原子的杂化类型为_____________________________。
2
比较A D与A E分子的沸点,其中沸点较高的原因为
2 2
_________________________________________________________________
_______。
元素D可形成两种同素异形体,其中在水中溶解度更大的是________(填分
子式)。
(4)已知ClO为角形,中心氯原子周围有四对价层电子。ClO中心氯原子的杂
化轨道类型为________,写出一个ClO的等电子体____________________。
答案 (1)②④ (2)N O (3)sp3 H O分子之间存在氢键 O
2 2 3
(4)sp3 Cl O或OF
2 2
解析 A的一种同位素原子中无中子,则A为H元素;B的一种核素在考古
时常用来鉴定一些文物的年代,则B为C元素;D与E同主族,且E的原子序数
是D的2倍,则D为O元素、E为S元素;C的原子序数介于碳、氧之间,应为N
元素;F元素在地壳中的含量位于金属元素的第二位,则F为Fe元素。
(1)①H原子核外不满足8电子稳定结构;③C H 分子的结构式为H—C≡C
2 2
—H,一个分子中有3个σ键、2个π键,错误;④C H 分子中C原子采取sp杂化,
2 2
所以H、C之间形成的是s-sp σ键,正确。
(2)与CO 互为等电子体的为N O。
2 2
(3)H S中S形成2个σ键,孤电子对数==2,为sp3杂化;O 分子为V形结构
2 3
与水相似,易溶于水。
(4)由中心氯原子周围有四对价层电子可知为sp3杂化。