文档内容
第 18 讲 铜 金属材料 金属冶炼
[复习目标] 1.了解铜单质及其重要化合物的性质、用途。2.理解含铜重要化合物的制备原
理及过程。3.了解金属冶炼的原理和方法。
考点一 铜及其化合物
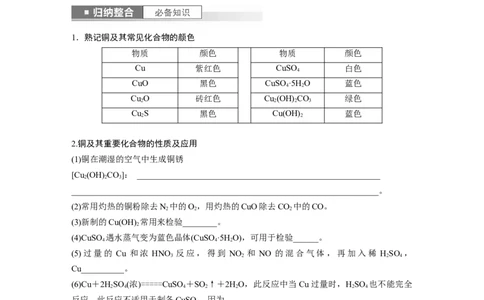
1.熟记铜及其常见化合物的颜色
物质 颜色 物质 颜色
Cu 紫红色 CuSO 白色
4
CuO 黑色 CuSO ·5H O 蓝色
4 2
Cu O 砖红色 Cu (OH) CO 绿色
2 2 2 3
Cu S 黑色 Cu(OH) 蓝色
2 2
2.铜及其重要化合物的性质及应用
(1)铜在潮湿的空气中生成铜锈
[Cu (OH) CO]: _________________________________________________________
2 2 3
________________________________________________________________________。
(2)常用灼热的铜粉除去N 中的O,用灼热的CuO除去CO 中的CO。
2 2 2
(3)新制的Cu(OH) 常用来检验________。
2
(4)CuSO 遇水蒸气变为蓝色晶体(CuSO ·5H O),可用于检验______。
4 4 2
(5)过量的 Cu 和浓 HNO 反应,得到 NO 和 NO 的混合气体,再加入稀 HSO ,
3 2 2 4
Cu__________。
(6)Cu+2HSO (浓)=====CuSO +SO ↑+2HO,此反应中当Cu过量时,HSO 也不能完全
2 4 4 2 2 2 4
反应。此反应不适用于制备CuSO ,因为____________________________________。
4
1.CuO是黑色固体,与水反应生成Cu(OH) ( )
2
2.将铜片置于干燥的空气中,不易被腐蚀( )
3.CuSO ·5H O失去结晶水属于物理变化( )
4 2
4.常温下Cu和浓HSO 反应生成CuSO ( )
2 4 4
5.过量的铜与浓硝酸反应一定没有一氧化氮生成( )一、铜及其化合物的性质和应用
1.某研究小组通过实验探究Cu及其重要化合物的性质,下列操作正确且能达到目的的是(
)
A.将铜丝插入浓硫酸中加热,反应完后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl 的生成
2
C.将CuCl 溶液在蒸发皿中加热蒸干,得到无水CuCl 固体
2 2
D.将表面有铜绿的铜器放入稀盐酸中浸泡,除去铜绿
二、铜及其化合物的制备
2.碱式碳酸铜又名孔雀石,主要成分为 Cu (OH) CO ,呈绿色,是一种具有广泛用途的化
2 2 3
工产品。某化学小组探究制备碱式碳酸铜的反应条件并制备少量碱式碳酸铜。
试剂:0.25 mol·L-1 Na CO 溶液、0.5 mol·L-1 NaOH溶液、0.5 mol·L-1 Cu(NO ) 溶液各
2 3 3 2
100 mL。
实验1:探究Cu(NO ) 与NaOH和NaCO 溶液配比
3 2 2 3
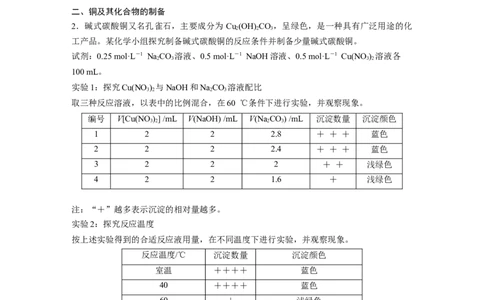
取三种反应溶液,以表中的比例混合,在60 ℃条件下进行实验,并观察现象。
编号 V[Cu(NO )] /mL V(NaOH) /mL V(Na CO) /mL 沉淀数量 沉淀颜色
3 2 2 3
1 2 2 2.8 + + + 蓝色
2 2 2 2.4 + + + 蓝色
3 2 2 2 + + 浅绿色
4 2 2 1.6 + 浅绿色
注:“+”越多表示沉淀的相对量越多。
实验2:探究反应温度
按上述实验得到的合适反应液用量,在不同温度下进行实验,并观察现象。
反应温度/℃ 沉淀数量 沉淀颜色
室温 ++++ 蓝色
40 ++++ 蓝色
60 + 浅绿色
75 ++ 绿色
80 +++ 绿色(少量黑色)
实验3:制备碱式碳酸铜
按最佳物料比取50 mL 0.5 mol·L-1 Cu(NO ) 溶液、50 mL 0.5 mol·L-1 NaOH溶液和相应体
3 2
积的0.25 mol·L-1NaCO 溶液,在最佳反应温度下进行实验,待反应完全后,静置、过滤、
2 3
洗涤、干燥后,得到2.5 g产品。
请回答下列问题:(1)本实验配制溶液时用到的玻璃仪器除烧杯、玻璃棒以外还有______________________。
(2)制备碱式碳酸铜时,Cu(NO ) 、NaOH和NaCO 溶液的最佳物质的量之比为__________,
3 2 2 3
最佳反应温度为____________,本实验的加热方式为________________。
(3)请写出本实验制备碱式碳酸铜的化学方程式: _______________________________。
(4)实验 2 中在 80 ℃反应生成的沉淀中有少量黑色的物质,产生该物质的原因可能是
________________________________________________________________________
________________________________________________________________________。
(5)简述实验3中洗涤沉淀的操作:_________________________________________
________________________________________________________________________。
(6)计算本实验的产率为________%(保留三位有效数字)。
考点二 金属冶炼及金属材料
1.常见的金属材料
(1)金属材料分类
(2)几种常见的合金
①
②
③
2.金属冶炼的一般方法及应用
(1)金属在自然界中的存在
(2)金属冶炼的实质金属的冶炼过程就是把金属从________态还原为________态的过程,即_______________(写
反应通式,用M表示金属)。
(3)金属冶炼的方法
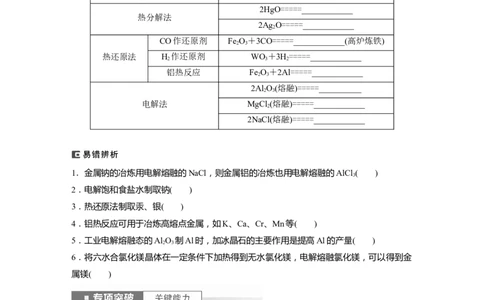
方法名称 主要反应原理(举例)
2HgO=====____________
热分解法
2Ag O=====____________
2
CO作还原剂 Fe O+3CO=====____________(高炉炼铁)
2 3
热还原法 H 作还原剂 WO+3H=====____________
2 3 2
铝热反应 Fe O+2Al=====____________
2 3
2Al O(熔融)=====__________
2 3
电解法 MgCl (熔融)=====____________
2
2NaCl(熔融)=====____________
1.金属钠的冶炼用电解熔融的NaCl,则金属铝的冶炼也用电解熔融的AlCl ( )
3
2.电解饱和食盐水制取钠( )
3.热还原法制取汞、银( )
4.铝热反应可用于冶炼高熔点金属,如K、Ca、Cr、Mn等( )
5.工业电解熔融态的Al O 制Al时,加冰晶石的主要作用是提高Al的产量( )
2 3
6.将六水合氯化镁晶体在一定条件下加热得到无水氯化镁,电解熔融氯化镁,可以得到金
属镁( )
金属冶炼方法的选择
1.根据已掌握的知识分析K、Na、Ca、Mg、Sn、Pb、Hg、Ag等金属单质的冶炼方法。
________________________________________________________________________
2.冶炼金属一般有下列四种方法:①焦炭法;②水煤气法;③活泼金属置换法;④电解法。
四种方法在工业上均有应用,古代有:(Ⅰ)火烧孔雀石炼铜;(Ⅱ)湿法炼铜。现代有:(Ⅲ)铝
热法炼铬;(Ⅳ)从光卤石中炼镁。对它们的冶炼对应方法的分析不正确的是( )
A.(Ⅰ)—① B.(Ⅱ)—②C.(Ⅲ)—③ D.(Ⅳ)—④
3.金属的冶炼一般用热分解法、热还原法和电解法,选用冶炼方法的依据主要是( )
A.金属在自然界里存在的形式
B.金属元素在地壳中的含量
C.金属阳离子得电子的能力
D.金属熔点的高低
1.正误判断,正确的打“√”,错误的打“×”。
(1)青铜和黄铜是不同结构的单质铜(2022·全国乙卷,7C)( )
(2)青铜比纯铜熔点低、硬度大,所以古代用青铜铸剑(2022·江苏,7C) ( )
2.(2022·广东,1)中华文明源远流长,在世界文明中独树一帜,汉字居功至伟。随着时代发
展,汉字被不断赋予新的文化内涵,其载体也发生相应变化。下列汉字载体主要由合金材料
制成的是( )
汉字载体
选项 A.兽骨 B.青铜器 C.纸张 D.液晶显示屏
3.(2020·全国卷Ⅲ,7)宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,
其中绿色来自孔雀石颜料[主要成分为Cu(OH) ·CuCO],青色来自蓝铜矿颜料[主要成分为
2 3
Cu(OH) ·2CuCO]。下列说法错误的是( )
2 3
A.保存《千里江山图》需控制温度和湿度
B.孔雀石、蓝铜矿颜料不易被空气氧化
C.孔雀石、蓝铜矿颜料耐酸耐碱
D.Cu(OH) ·CuCO 中铜的质量分数高于Cu(OH) ·2CuCO
2 3 2 3
4.(2022·海南,15)胆矾(CuSO ·5H O)是一种重要化工原料,某研究小组以生锈的铜屑为原
4 2
料[主要成分是Cu,含有少量的油污、CuO、CuCO、Cu(OH) ]制备胆矾。流程如下。
3 2
回答问题:
(1)步骤①的目的是_____________________________________________________________。
(2)步骤②中,若仅用浓HSO 溶解固体B,将生成__________(填化学式)污染环境。
2 4(3)步骤②中,在HO 存在下Cu溶于稀HSO ,反应的化学方程式为________________。
2 2 2 4
(4)经步骤④得到的胆矾,不能用水洗涤的主要原因是________________________________。
(5)实验证明,滤液D能将I-氧化为I。
2
ⅰ.甲同学认为不可能是步骤②中过量HO 将I-氧化为I,理由是______________。
2 2 2
ⅱ.乙同学通过实验证实,只能是 Cu2+将 I-氧化为 I ,写出乙同学的实验方案及结果
2
________________________________________________________________________
________________________________________________________________________
(不要求写具体操作过程)。