文档内容
第 24 讲 硫及其化合物的相互转化
[复习目标] 1.能从物质类别、硫的化合价变化理解硫及其化合物的转化关系。2.掌握硫及
其重要化合物的性质及制备方案。
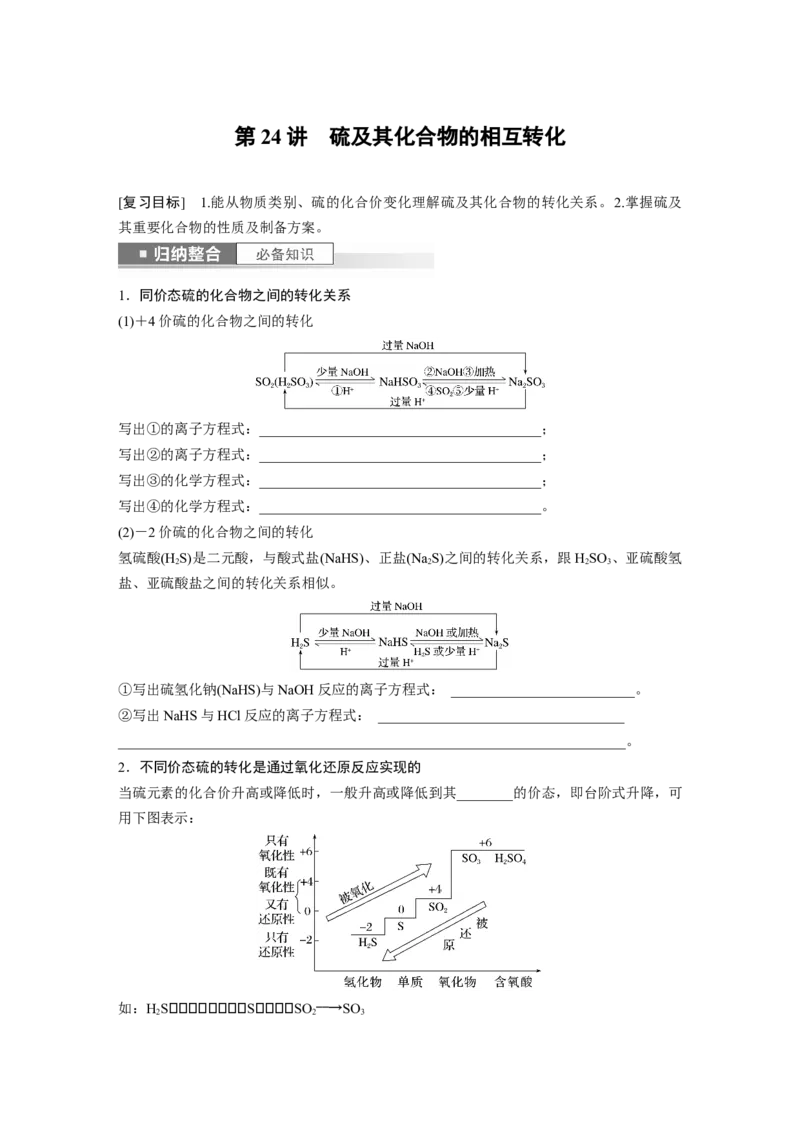
1.同价态硫的化合物之间的转化关系
(1)+4价硫的化合物之间的转化
写出①的离子方程式:________________________________________;
写出②的离子方程式:________________________________________;
写出③的化学方程式:________________________________________;
写出④的化学方程式:________________________________________。
(2)-2价硫的化合物之间的转化
氢硫酸(H S)是二元酸,与酸式盐(NaHS)、正盐(Na S)之间的转化关系,跟HSO 、亚硫酸氢
2 2 2 3
盐、亚硫酸盐之间的转化关系相似。
①写出硫氢化钠(NaHS)与NaOH反应的离子方程式: __________________________。
②写出NaHS与HCl反应的离子方程式: ___________________________________
________________________________________________________________________。
2.不同价态硫的转化是通过氧化还原反应实现的
当硫元素的化合价升高或降低时,一般升高或降低到其________的价态,即台阶式升降,可
用下图表示:
如:HSSSO ――→SO
2 2 3写出③④⑤反应的化学方程式:
③________________________________________________________________________;
④________________________________________________________________________;
⑤________________________________________________________________________。
注意 (1)同种元素相邻价态的粒子间不发生氧化还原反应,如 S和HS、S和SO 、SO 和
2 2 2
浓硫酸之间不发生氧化还原反应。
(2)当硫元素的高价态粒子与低价态粒子反应时,一般生成中间价态,如2NaS+NaSO +
2 2 3
3HSO ===3NaSO +3S↓+3HO。
2 4 2 4 2
一、硫的循环转化
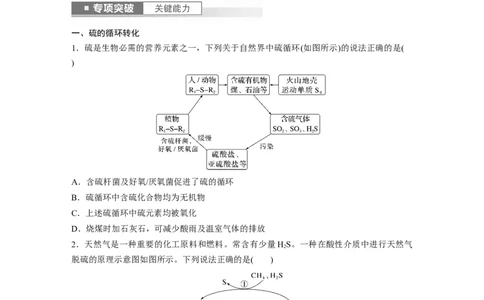
1.硫是生物必需的营养元素之一,下列关于自然界中硫循环(如图所示)的说法正确的是(
)
A.含硫杆菌及好氧/厌氧菌促进了硫的循环
B.硫循环中含硫化合物均为无机物
C.上述硫循环中硫元素均被氧化
D.烧煤时加石灰石,可减少酸雨及温室气体的排放
2.天然气是一种重要的化工原料和燃料。常含有少量HS。一种在酸性介质中进行天然气
2
脱硫的原理示意图如图所示。下列说法正确的是( )
A.整个脱硫过程中Fe (SO ) 溶液并未参与反应
2 4 3
B.整个脱硫过程中参加反应的n(H S)∶n(O )=2∶1
2 2
C.脱硫过程需不断补充FeSO
4
D.CH 是天然气脱硫过程的催化剂
4
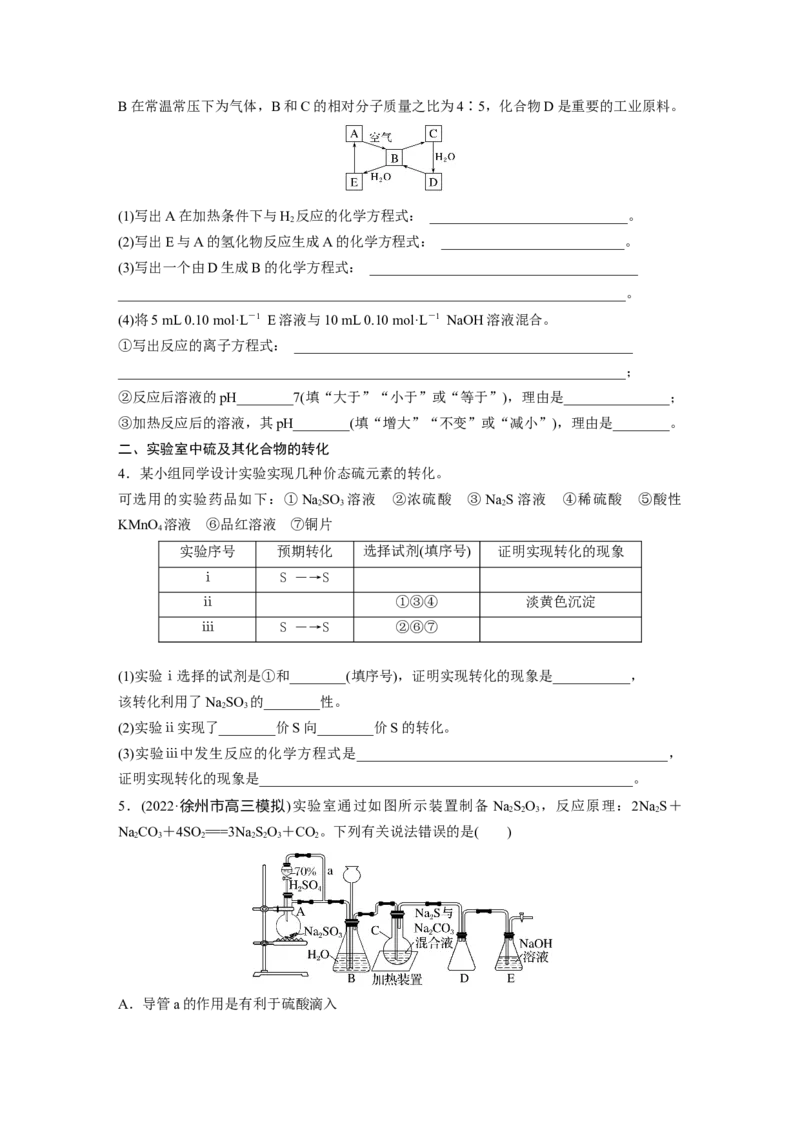
3.如图所示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去)。化合物B在常温常压下为气体,B和C的相对分子质量之比为4∶5,化合物D是重要的工业原料。
(1)写出A在加热条件下与H 反应的化学方程式: ____________________________。
2
(2)写出E与A的氢化物反应生成A的化学方程式: __________________________。
(3)写出一个由D生成B的化学方程式: ______________________________________
________________________________________________________________________。
(4)将5 mL 0.10 mol·L-1 E溶液与10 mL 0.10 mol·L-1 NaOH溶液混合。
①写出反应的离子方程式: ________________________________________________
________________________________________________________________________;
②反应后溶液的pH________7(填“大于”“小于”或“等于”),理由是_______________;
③加热反应后的溶液,其pH________(填“增大”“不变”或“减小”),理由是________。
二、实验室中硫及其化合物的转化
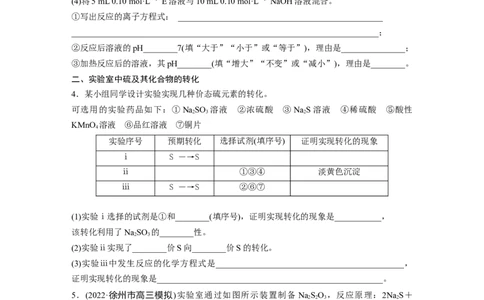
4.某小组同学设计实验实现几种价态硫元素的转化。
可选用的实验药品如下:①NaSO 溶液 ②浓硫酸 ③NaS溶液 ④稀硫酸 ⑤酸性
2 3 2
KMnO 溶液 ⑥品红溶液 ⑦铜片
4
实验序号 预期转化 选择试剂(填序号) 证明实现转化的现象
ⅰ S ―→S
ⅱ ①③④ 淡黄色沉淀
ⅲ S ―→S ②⑥⑦
(1)实验ⅰ选择的试剂是①和________(填序号),证明实现转化的现象是___________,
该转化利用了NaSO 的________性。
2 3
(2)实验ⅱ实现了________价S向________价S的转化。
(3)实验ⅲ中发生反应的化学方程式是____________________________________________,
证明实现转化的现象是_____________________________________________________。
5.(2022·徐州市高三模拟)实验室通过如图所示装置制备 NaSO ,反应原理:2NaS+
2 2 3 2
NaCO+4SO ===3NaSO+CO。下列有关说法错误的是( )
2 3 2 2 2 3 2
A.导管a的作用是有利于硫酸滴入B.装置A中的反应体现硫酸的酸性
C.装置B、D作用完全相同
D.装置C中先有淡黄色浑浊产生,后又变澄清,说明过程中有硫单质生成
三、化工生产中陌生含硫化合物的制备
6.[2018·全国卷Ⅰ,27(1)(2)]焦亚硫酸钠(Na SO)在医药、橡胶、印染、食品等方面应用广
2 2 5
泛。回答下列问题:
(1)生产NaSO ,通常是由NaHSO 过饱和溶液经结晶脱水制得。写出该过程的化学方程式:
2 2 5 3
________________________________________________________________________
________________________________________________________________________。
(2)利用烟道气中的SO 生产NaSO 的工艺为:
2 2 2 5
①pH=4.1时,Ⅰ中为_______________________________________________(写化学式)溶液。
②工艺中加入NaCO 固体,并再次充入SO 的目的是______________________________。
2 3 2
7.连二亚硫酸钠(Na SO)俗称保险粉,可以用作染色工艺的还原剂,纸浆、肥皂等的漂白
2 2 4
剂。NaSO 易溶于水,难溶于乙醇,在碱性介质中较稳定,在空气中易被氧化。回答下列
2 2 4
问题:
(1)Na SO 在潮湿空气中被氧化,生成的两种常见酸式盐是______________(填化学式)。
2 2 4
(2)锌粉法制备NaSO 的工艺流程如图所示:
2 2 4
①工业上常将锌块进行预处理得到锌粉—水悬浊液,其目的是___________________
________________________________________________________________________。
②步骤Ⅰ中发生反应的化学方程式为______________________________________
________________________________________________________________________。
③在步骤Ⅲ中得到的NaSO 固体要用乙醇洗涤,其优点是____________________,
2 2 4
“后续处理”最终要加入少量的NaCO 固体,其原因是_______________________。
2 3
(3)目前,我国普遍采用甲酸钠法生产连二亚硫酸钠,其原理是先将 HCOONa和烧碱加入乙
醇水溶液中,然后通入 SO 发生反应,有 CO 气体放出,总反应的离子方程式是
2 2
_______________________________________________________________________________。1.(2021·辽宁,8)含S元素的某钠盐a能发生如图转化。下列说法错误的是( )
A.a可能为正盐,也可能为酸式盐
B.c为不溶于盐酸的白色沉淀
C.d为含极性键的非极性分子
D.反应②中还可能生成淡黄色沉淀
2.[2022·全国甲卷,26(2)(3)(5)(6)]硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电
4
镀、医学上有诸多应用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为
3
SiO 以及Ca、Mg、Fe、Cu等的化合物。其制备流程如下:
2
本题中所涉及离子的氢氧化物溶度积常数如下表:
离子 Fe3+ Zn2+ Cu2+ Fe2+ Mg2+
K 4.0×10-38 6.7×10-17 2.2×10-20 8.0×10-16 1.8×10-11
sp
回答下列问题:
(2) 为 了 提 高 锌 的 浸 取 效 果 , 可 采 取 的 措 施 有 ________________________ 、
________________________________________________________________________。
(3)加入物质X调溶液pH=5,最适宜使用的X是__________(填标号)。
A.NH ·H O B.Ca(OH)
3 2 2
C.NaOH
滤渣①的主要成分是____________、__________、__________。
(5)滤液②中加入锌粉的目的是_____________________________________________
________________________________________________________________________。
(6)滤渣④与浓 HSO 反应可以释放 HF 并循环利用,同时得到的副产物是________、
2 4
__________。