文档内容
热点强化 14 微粒空间结构 大 π 键的判断
(一)微粒空间结构的判断
1.熟记常见分子(离子)的空间结构
微粒组成
中心原子的 中心原子的
(A为中心 实例 微粒空间结构
孤电子对数 杂化方式
原子)
BeCl 、CO、HCN
2 2
AB SO 、SnBr 、NO
2 2 2
HO、OF 、NH
2 2
BF 、SO 、CO
3 3
AB
3
NH 、PCl 、SO
3 3
AB CH、CHCl 、NH、SO
4 4 3
2.(知识拓展)等电子原理及应用
(1)基本观点
原子总数相同、价电子总数相同的分子(或离子)互为等电子体。等电子体具有相似的结构特
征(空间结构和化学键类型)及相近的性质。
(2)确定等电子体的方法(举例)
变换过程中注意电荷改变,并伴有元素种类的改变。
――――――――――――→―――――――――――→
―――――――――――――――→
(3)熟悉常见的等电子体及空间结构
等电子(价电子)类型 常见等电子体 空间结构
2原子10电子 N、CN-、C、NO+
2
2原子14电子 F、O、Cl
2 2
CO、NO、CNO-、N、NO、SCN-、
2 2
3原子16电子
HgCl 、BeCl (g)
2 2
3原子18电子 O、SO 、NO
3 2
4原子8电子 NH 、PH 、CH、HO+
3 3 3
4原子24电子 SO (g)、CO、NO、BO、BF
3 3
4原子26电子 SO、ClO、BrO、IO、XeO
35原子8电子 CH、SiH、NH、PH、BH
4 4
5原子32电子 CCl 、SiF、SiO、SO、ClO
4 4
12原子30电子 C H、NB H(俗称无机苯)
6 6 3 3 6
(二)大π键(离域π键)
1.形成条件
(1)中心原子采取sp或sp2杂化。
(2)参与形成大π键的多个原子应在同一个平面或同一直线上。
2.大π键共用电子数分析方法
(1)大π键中共用电子的数目等于垂直于分子或离子平面的p轨道中的电子数目总和。
(2)判断出中心原子的杂化方式,并画出价层电子轨道表示式。未参与成键的杂化轨道,优
先填充两个电子,形成孤电子对,杂化轨道中的电子不参与形成大π键。
(3)根据配位原子的价层电子轨道表示式,判断配位原子中未参与成键且垂直该分子或离子
平面的p轨道中电子数目(单电子优先形成π键)。
示例 推测CO中的大π键为________。
分析 根据价层电子对互斥模型判断CO为平面三角形结构,中心C原子为sp2杂化,价层
电子轨道表示式为 ,每个O原子有两个单电子,三个O分别用一个单
电子与中心C原子形成三个C—O σ键,另一个单电子参与形成大π键,形成两个负电荷的
电子也参与形成大π键。则大π键的电子总数为1+3+2=6,表示为Π。
1.下列关于NH、NH 、NH三种粒子的说法不正确的是( )
3
A.三种粒子所含有的电子数相等
B.三种粒子中氮原子的杂化方式相同
C.三种粒子的空间结构相同
D.键角大小关系:NH>NH>NH
3
2.(1)[2020·全国卷Ⅰ,35(3)]磷酸根离子的空间结构为________,其中P的价层电子对数为
________,杂化轨道类型为________。
(2)[2018·全国卷Ⅰ,35(3)节选]LiAlH 中的阴离子空间结构是________,中心原子的杂化形
4
式为________________________________________________________________________。
3.[2017·全国卷Ⅱ,35(3)②]经X射线衍射测得化合物(N )(H O) (NH )Cl的晶体结构,其
5 6 3 3 4 4
局部结构如图所示。该化合物中阴离子N中的σ键总数为________个。分子中的大π键可用符号Π表示,其中m
代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示
为Π),则N中的大π键应表示为________。
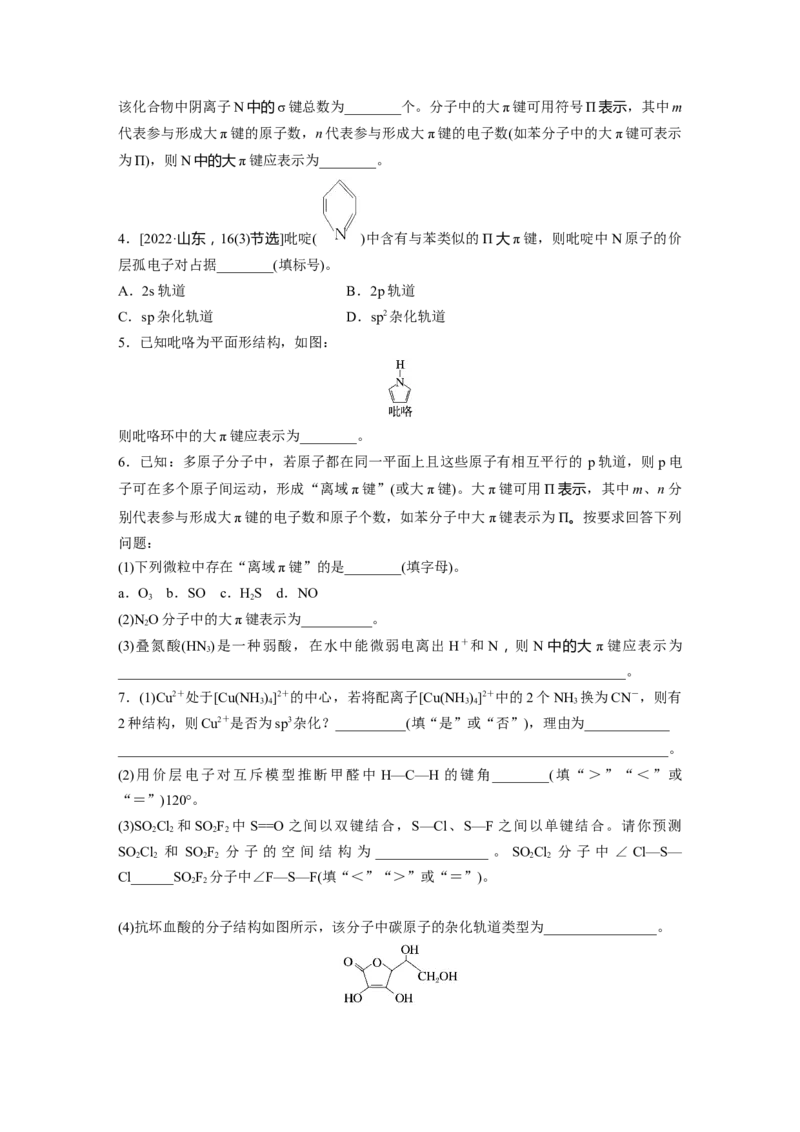
4.[2022·山东,16(3)节选]吡啶( )中含有与苯类似的Π大π键,则吡啶中N原子的价
层孤电子对占据________(填标号)。
A.2s轨道 B.2p轨道
C.sp杂化轨道 D.sp2杂化轨道
5.已知吡咯为平面形结构,如图:
则吡咯环中的大π键应表示为________。
6.已知:多原子分子中,若原子都在同一平面上且这些原子有相互平行的 p轨道,则p电
子可在多个原子间运动,形成“离域π键”(或大π键)。大π键可用Π表示,其中m、n分
别代表参与形成大π键的电子数和原子个数,如苯分子中大π键表示为Π。按要求回答下列
问题:
(1)下列微粒中存在“离域π键”的是________(填字母)。
a.O b.SO c.HS d.NO
3 2
(2)N O分子中的大π键表示为__________。
2
(3)叠氮酸(HN )是一种弱酸,在水中能微弱电离出 H+和N,则N中的大 π 键应表示为
3
________________________________________________________________________。
7.(1)Cu2+处于[Cu(NH )]2+的中心,若将配离子[Cu(NH )]2+中的2个NH 换为CN-,则有
3 4 3 4 3
2种结构,则Cu2+是否为sp3杂化?__________(填“是”或“否”),理由为____________
______________________________________________________________________________。
(2)用价层电子对互斥模型推断甲醛中 H—C—H 的键角________(填“>”“<”或
“=”)120°。
(3)SO Cl 和 SO F 中 S==O 之间以双键结合,S—Cl、S—F 之间以单键结合。请你预测
2 2 2 2
SO Cl 和 SO F 分 子 的 空 间 结 构 为 ________________ 。 SO Cl 分 子 中 ∠ Cl—S—
2 2 2 2 2 2
Cl______SOF 分子中∠F—S—F(填“<”“>”或“=”)。
2 2
(4)抗坏血酸的分子结构如图所示,该分子中碳原子的杂化轨道类型为________________。