文档内容
第3讲 铁及其重要化合物
【2020·备考】
最新考纲:1.掌握铁及其重要化合物的主要性质。2.掌握铁及其重要化合物的应用。
3.了解常见金属及其重要化合物的制备方法。
核心素养:1.宏观辨识与微观探析:认识铁及其化合物的性质,能以Fe2+、Fe3+的
相互转化为例,理解变价金属元素的氧化还原反应实质。2.科学探究与创新意识:
能发现和提出有探究价值的氢氧化亚铁的制备探究方案,进行实验探究。
考点一 铁的单质、氧化物及氢氧化物
(频数:★★☆ 难度:★★☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查铁的单质、氧化物及氢氧化物的性质,特别是氧化亚铁、氢氧化亚铁
的还原性和氧化亚铁、氢氧化亚铁的氧化性,另外还应关注氢氧化亚铁制备的实
验探究。
1.铁元素的存在形式
2.铁的性质(1)物理性质
导电、导热
颜色、状态 特性 地壳含量
性、延展性
银白色固体 良好 被磁铁吸引 占第四位
(2)化学性质
铁单质性质活泼,有较强的还原性,主要化合价为+2价和+3价。
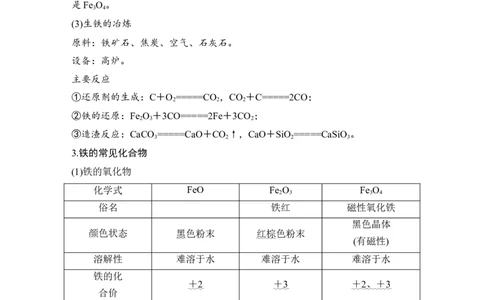
①与非金属单质反应:
Fe与S反应: Fe + S ===== FeS 。
②与水的反应:常温下铁与水不反应,在高温条件下与水蒸气反应: 3Fe +
4H O(g) ===== Fe O + 4H 。
2 3 4 2
③与酸的反应:
a.与非氧化性酸反应的离子方程式: Fe + 2H + == =Fe 2 + + H ↑。
2
b.与氧化性酸反应:遇冷的浓硫酸或浓硝酸钝化,与稀硝酸或在加热条件下与浓硫
酸、浓硝酸反应,但无H 产生。
2
④与某些盐溶液的反应:
a.与CuSO 溶液反应的离子方程式: Fe + Cu 2 + == =Fe 2 + + Cu 。
4b.与FeCl 溶液反应的离子方程式: Fe + 2Fe 3 + == =3Fe 2 + 。
3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①铁分别与氯气和盐酸反应所得的产物中铁元素的价态不同,Fe与Cl 反应无论
2
用量多少都生成FeCl ,而Fe与盐酸反应生成FeCl 。
3 2
②铁在潮湿的空气中生成的铁锈的主要成分是 Fe O ,而铁在纯氧中燃烧的产物
2 3
是Fe O 。
3 4
(3)生铁的冶炼
原料:铁矿石、焦炭、空气、石灰石。
设备:高炉。
主要反应
①还原剂的生成:C+O =====CO ,CO +C=====2CO;
2 2 2
②铁的还原:Fe O +3CO=====2Fe+3CO ;
2 3 2
③造渣反应:CaCO =====CaO+CO ↑,CaO+SiO =====CaSiO 。
3 2 2 3
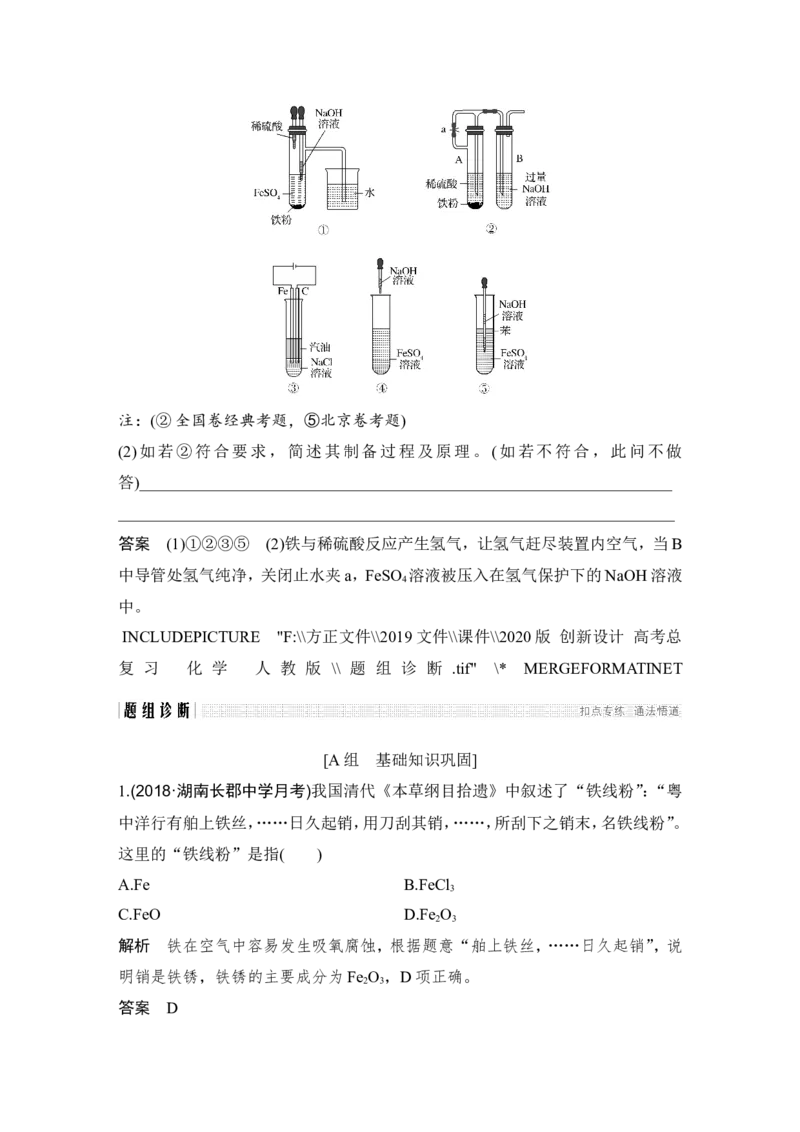
3.铁的常见化合物
(1)铁的氧化物
化学式 FeO Fe O Fe O
2 3 3 4
俗名 铁红 磁性氧化铁
黑色晶体
颜色状态 黑色粉末 红棕色粉末
(有磁性)
溶解性 难溶于水 难溶于水 难溶于水
铁的化
+ 2 + 3 + 2 、+ 3
合价
与H+反
FeO + 2H + == =Fe 2 + Fe O + 6H + Fe O +8H+===Fe2+
应的离子 2 3 3 4
+ H O == =2Fe 3 + + 3H O +2Fe3++4H O
2 2 2
方程式
(2)铁的氢氧化物
化学式 Fe(OH) Fe(OH)
2 3
色态 白色固体 红褐色固体
与盐酸反应 Fe(OH) + 2H + == =F e 2 + + Fe(OH) +3H+===Fe3++
2 32H O 3H O
2 2
2Fe(OH) ===== Fe O + 3H O
3 2 3 2
受热分解
可溶性亚铁盐与碱反应: 可溶性铁盐与碱反应: Fe 3 + +
制法
Fe 2 + + 2OH - = =Fe(OH) ↓ 3OH - == =Fe(OH) ↓
2 3
空气中,Fe(OH) 能够非常迅速地被氧气氧化成Fe(OH) ,
2 3
二者的关系 现象是白色沉淀迅速变成灰绿色,最后变成红褐色,化学
方程式为4Fe(OH) + O + 2H O == =4Fe(OH)
2 2 2 3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
①FeO、Fe O 、Fe(OH) 与足量HNO 反应时,发生氧化还原反应,Fe2+被HNO 氧
3 4 2 3 3
化生成Fe3+。
②Fe O 、Fe O 、Fe(OH) 与足量HI反应时,发生氧化还原反应,Fe3+被I-还原生成
2 3 3 4 3
Fe2+。
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)用铁制容器可以运输浓硝酸和浓硫酸(√)
(2)Fe与稀HNO 、稀H SO 反应均有气泡产生,说明Fe与两种酸均发生置换反应
3 2 4
(×)
(3)Fe在足量Cl 中燃烧生成FeCl ,在少量Cl 中燃烧生成FeCl (×)
2 3 2 2
(4)根据Cl 、S与铁的反应可以判断氯元素和硫元素的非金属性强弱(√)
2
2.(根据教材基础知识改编)将下列物质的颜色和用途或性质用短线连接起来。
①Fe O a.红褐色 A.具有较强的还原性
2 3
②Fe(OH) b.红棕色 B.易被氧化成灰绿色最终变成红褐色
2
③Fe(OH) c.白色 C.红色油漆、涂料
3
④Fe2+ d.棕黄色 D.受热分解成红棕色粉末
⑤Fe3+ e.浅绿色 E.具有较强的氧化性
答案 ①—b—C;②—c—B;③—a—D;④—e—A;⑤—d—E
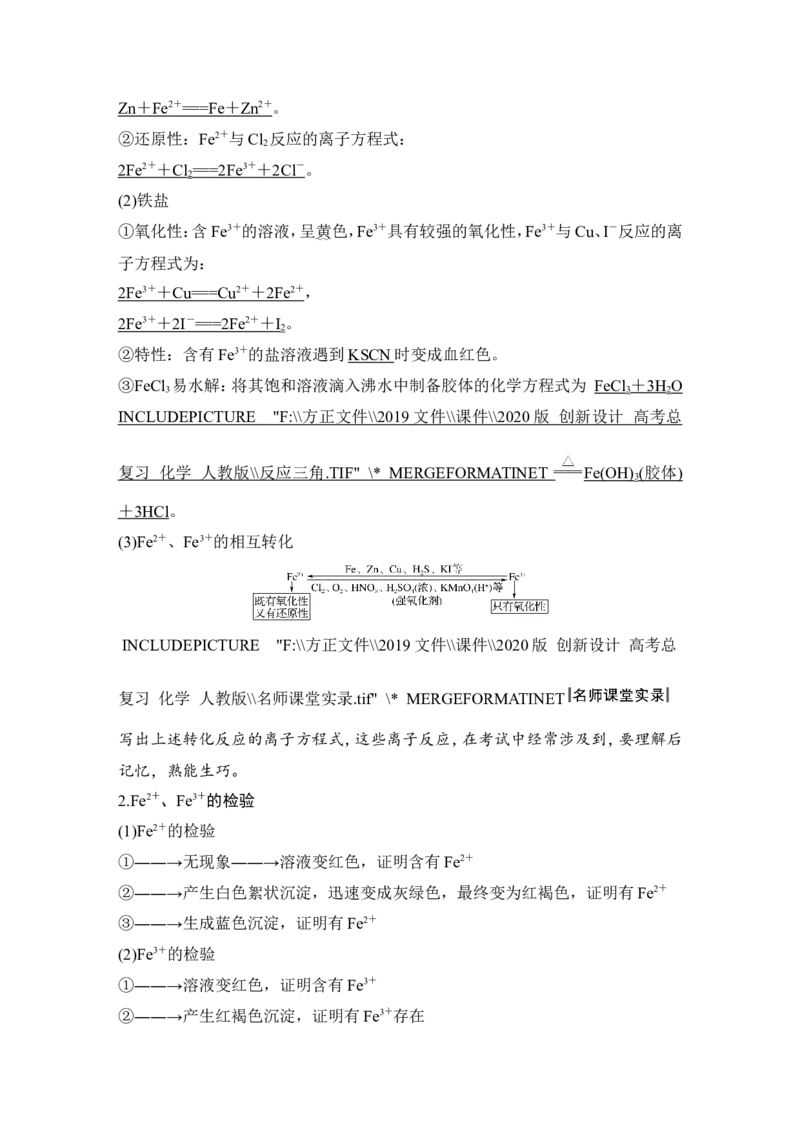
3.(实验探究题)(1)下列各图示中能较长时间看到 Fe(OH) 白色沉淀的是
2
________(填序号)。注:(②全国卷经典考题,⑤北京卷考题)
(2)如若②符合要求,简述其制备过程及原理。(如若不符合,此问不做
答)__________________________________________________________________
_____________________________________________________________________
答案 (1)①②③⑤ (2)铁与稀硫酸反应产生氢气,让氢气赶尽装置内空气,当B
中导管处氢气纯净,关闭止水夹a,FeSO 溶液被压入在氢气保护下的NaOH溶液
4
中。
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2018·湖南长郡中学月考)我国清代《本草纲目拾遗》中叙述了“铁线粉”:“粤
中洋行有舶上铁丝,……日久起销,用刀刮其销,……,所刮下之销末,名铁线粉”。
这里的“铁线粉”是指( )
A.Fe B.FeCl
3
C.FeO D.Fe O
2 3
解析 铁在空气中容易发生吸氧腐蚀,根据题意“舶上铁丝,……日久起销”,说
明销是铁锈,铁锈的主要成分为Fe O ,D项正确。
2 3
答案 D2.某同学欲探究铁及其化合物的性质,下列实验方案可行的是( )
A.将铁粉加入热的浓硫酸中:探究铁的活泼性
B.将热的NaOH溶液滴入FeCl 溶液中:制备Fe(OH) 胶体
3 3
C.在蒸发皿中加热蒸干FeSO 溶液:制备FeSO ·6H O晶体
4 4 2
D.将铜粉加入FeCl 溶液中:验证Fe3+的氧化性强于Cu2+
3
解析 由于浓硫酸具有强氧化性,铁与其反应生成Fe (SO ) 和SO ,无法说明铁
2 4 3 2
的活泼性,故A方案不可行;将NaOH加入FeCl 溶液中,得到Fe(OH) 沉淀,无法
3 3
得到Fe(OH) 胶体,B项方案不可行;在蒸发皿中加热蒸干FeSO 溶液,一方面氧
3 4
气可将FeSO 氧化,另一方面会得到不含结晶水的化合物,故C项方案不可行;将
4
铜粉加入FeCl 溶液中,发生反应:Cu+2Fe3+===Cu2++2Fe2+,该反应说明Fe3+的
3
氧化性强于Cu2+,故D项方案可行。
答案 D
3.一定质量的某铁的氧化物Fe O ,与足量的4 mol·L-1硝酸溶液充分反应,消耗硝
x y
酸溶液700 mL,生成2.24 L NO(标准状况)。则该铁的氧化物的化学式为( )
A.FeO B.Fe O
2 3
C.Fe O D.Fe O
3 4 4 5
解析 铁的氧化物Fe O 与足量的4 mol·L-1硝酸溶液充分反应,生成Fe(NO ) ,
x y 3 3
硝酸被还原生成NO,n(NO)==0.1 mol,根据氮原子守恒可得,3n[Fe(NO ) ]+
3 3
n(NO)=n(HNO ),3n[Fe(NO ) ]+0.1 mol=0.7 L×4 mol·L-1,n[Fe(NO ) ]=0.9
3 3 3 3 3
mol,令氧化物Fe O 中Fe元素的平均化合价为a,根据得失电子守恒可得,0.9
x y
mol×(3-a)=0.1 mol×(5-2),解得a=,由化合物中正负化合价代数和为0可得
x=2y,x∶y=3∶4,故该氧化物的化学式为Fe O 。
3 4
答案 C
【方法技巧】
确定铁的氧化物组成的基本方法
设铁的氧化物中铁元素与氧元素的质量比为m∶n,
则氧化物中n(Fe)∶n(O)=∶=a∶b,
若a∶b=1∶1,则铁的氧化物为FeO;
若a∶b=2∶3,则铁的氧化物为Fe O ;
2 3
若a∶b=3∶4,则铁的氧化物是Fe O 或FeO与Fe O 按物质的量之比为1∶1的
3 4 2 3混合物或FeO、Fe O 、Fe O 的混合物(其中FeO、Fe O 物质的量之比为1∶1,
2 3 3 4 2 3
Fe O 为任意值)。
3 4
[B组 考试能力过关]
4.(2016·浙江高考·27Ⅱ)磁性材料A是由两种元素组成的化合物,某研究小组按
如图流程探究其组成:
请回答:
(1)A的组成元素为________(用元素符号表示),化学式为____________________。
(2)溶液C可溶解铜片,列举该反应的一个实际应用____________________。
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的
密度为1.518 g·L-1),该气体分子的电子式为________。写出该反应的离子方程式
_____________________________________________________________________
_____________________________________________________________________
。
(4)写出F→G反应的化学方程式__________________________________________
___________________________________________________________________。
设计实验方案探究溶液G中的主要微粒(不考虑H O、H+、K+、I-)
2
___________________________________________________________________。
解析 (1)根据题中的探究过程,红棕色固体B为氧化铁,与盐酸反应后生成黄色
溶液C为氯化铁,氯化铁遇硫氰化钾显红色,溶液D为硫氰化铁。无色气体溶于水
后显酸性,与碘反应后生成无色溶液,酸性变强,说明原酸为弱酸,且具有还原性,
为亚硫酸,则无色气体为二氧化硫。则原化合物中含有铁和硫元素。由 2Fe~
Fe O ,得n(Fe)=×2=0.03 mol,m(Fe)=1.680 g;所以A中硫元素的质量为m(S)
2 3
=2.960 g-1.680 g=1.280 g,故n(S)==0.04 mol;n(Fe)∶n(S)=0.03 mol∶0.04
mol=3∶4,可知A的化学式为Fe S 。(2)因溶液C为氯化铁溶液,工业上常用于制
3 4
印刷电路板;(3)根据题意Fe S 与稀硫酸反应,生成的淡黄色不溶物为S,气体的
3 4
摩尔质量为1.518 g·L-1×22.4 L·mol-1=
34 g·mol-1,故应为H S,硫元素化合价升高,故产物还有Fe2+,该气体的电子式为
2,反应的离子方程式为 Fe S +6H+===3Fe2++3H S↑+S。
3 4 2
(4)H SO 与 I 反应生成 H SO 和 HI,反应的化学方程式为 H SO +I +
2 3 2 2 4 2 3 2
H O===H SO +2HI;检验G中主要微粒,目的在于检验SO和H SO 的存在。方法
2 2 4 2 3
是:取溶液G少许,加入过量BaCl 溶液,若产生白色沉淀,则有SO;过滤后取滤
2
液,滴加H O 溶液,若再产生白色沉淀,则有H SO 。
2 2 2 3
答案 (1)S、Fe Fe S (2)制印刷电路板
3 4
(3) Fe S +6H+===3Fe2++3H S↑+S
3 4 2
(4)H SO +I +H O===H SO +2HI 取溶液G少许,加入过量BaCl 溶液,若产生
2 3 2 2 2 4 2
白色沉淀,则有SO;过滤后取滤液,滴加H O 溶液,若再产生白色沉淀,则有
2 2
H SO
2 3
考点二 铁盐和亚铁盐
(频数:★☆☆ 难度:☆☆☆)
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 名 师 课 堂 .tif" \* MERGEFORMATINET
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 书名号 .TIF " \* MERGEFORMATINET 名师课堂导语 本
考点主要考查铁盐和亚铁盐的性质、Fe2+、Fe3+的鉴别,以及铁盐和亚铁盐实验探
究,特别是含铁化合物的工艺流程题更是近几年的考查热点,应多加关注。
1.亚铁盐和铁盐
(1)亚铁盐
含有Fe2+的溶液,呈浅绿色,既有氧化性,又有还原性。
①氧化性:Fe2+与Zn反应的离子方程式:Zn + Fe 2 + == =Fe + Zn 2 + 。
②还原性:Fe2+与Cl 反应的离子方程式:
2
2Fe 2 + + Cl == =2Fe 3 + + 2Cl - 。
2
(2)铁盐
①氧化性:含Fe3+的溶液,呈黄色,Fe3+具有较强的氧化性,Fe3+与Cu、I-反应的离
子方程式为:
2Fe 3 + + Cu == =Cu 2 + + 2Fe 2 + ,
2Fe 3 + + 2I - == =2Fe 2 + + I 。
2
②特性:含有Fe3+的盐溶液遇到KSCN 时变成血红色。
③FeCl 易水解:将其饱和溶液滴入沸水中制备胶体的化学方程式为 FeCl + 3H O
3 3 2
INCLUDEPICTURE "F:\\ 方正文件 \\2019 文件 \\ 课件 \\2020 版 创新设计 高考总
复习 化学 人教版 \ \ 反应三角 .TIF " \* MERGEFORMATINET Fe(OH) ( 胶体 )
3
+ 3HC l。
(3)Fe2+、Fe3+的相互转化
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
写出上述转化反应的离子方程式,这些离子反应,在考试中经常涉及到,要理解后
记忆,熟能生巧。
2.Fe2+、Fe3+的检验
(1)Fe2+的检验
①――→无现象――→溶液变红色,证明含有Fe2+
②――→产生白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,证明有Fe2+
③――→生成蓝色沉淀,证明有Fe2+
(2)Fe3+的检验
①――→溶液变红色,证明含有Fe3+
②――→产生红褐色沉淀,证明有Fe3+存在(3)混合溶液中Fe3+、Fe2+的检验
Ⅰ.Fe3+的检验
①――→溶液变红色,说明含有Fe3+
②――→试纸变蓝色,说明含有Fe3+
Ⅱ.Fe2+的检验
①――→酸性KMnO 溶液紫红色褪去,说明含有Fe2+
4
②――→溴水褪色,说明含有Fe2+
③――→生成蓝色沉淀,说明含有Fe2+
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\名师课堂实录.tif" \* MERGEFORMATINET
(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加
入到足量的新制氯水中(新制氯水可能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性KMnO 溶液检验Fe2+(Cl-能还原酸性
4
KMnO ,有干扰)。
4
[速查速测]
1.(易混点排查)正确的打“√”,错误的打“×”
(1)FeCl 溶液与KSCN溶液反应的离子方程式为Fe3++3SCN-===Fe(SCN) ↓(×)
3 3
(2)可用铁粉除去FeCl 溶液中的FeCl (√)
2 3
(3)将Fe(NO ) 样品溶于稀硫酸后,滴加 KSCN溶液,观察溶液是否变红,检验
3 2
Fe(NO ) 晶体是否已氧化变质(×)
3 2
(4)室温下,向FeCl 溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色,
3
说明Fe3+的氧化性比I 的强(√)
2
(5)用NaOH溶液和盐酸能除去FeCl 溶液中混有的CuCl (×)
2 2
2.(RJ必修1·P 7改编)要证明某溶液中不含Fe3+而可能含Fe2+,进行如下实验操
63
作时,最佳顺序是( )
①加足量氯水 ②加足量KMnO 溶液 ③加少量KSCN溶液
4
A.①② B.③②
C.③① D.①②③
答案 C3.(思维探究)(1)如何除去Mg2+中混有的Fe3+?
_____________________________________________________________________
答案 向混合溶液中加入MgO、MgCO 、Mg(OH) 中之一,与Fe3+水解产生的H+
3 2
反应,促进Fe3+的水解,将Fe3+转化为Fe(OH) 沉淀除去。
3
(2)如何除去Cu2+中混有的Fe2+?
_____________________________________________________________________
答案 先加入氧化剂(如H O )将溶液中的Fe2+氧化成Fe3+,再向混合溶液中加入
2 2
CuO、CuCO 、Cu(OH) 、Cu (OH) CO 中之一,与Fe3+水解产生的H+反应,促进Fe3
3 2 2 2 3
+的水解,将Fe3+转化为Fe(OH) 沉淀而除去。
3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复 习 化 学 人 教 版 \\ 题 组 诊 断 .tif" \* MERGEFORMATINET
[A组 基础知识巩固]
1.(2019·河南信阳模拟)几种中学常见的物质转化如图所示。
下表中R、X、Y、Z对应物质正确的是( )
选项 R X Y Z
A 紫色石蕊 Fe O Fe O 和Cu Cu
2 3 2 3
B 甲基橙 Fe(NO ) Fe(OH) Cu (OH) CO
3 2 2 2 2 3
C 酚酞 Fe(OH) FeO和Fe CuO
3
D Fe O NaAlO Na SiO Cu(OH)
2 3 2 2 3 2
解析 铜不和稀硫酸反应,A项错误;甲基橙遇稀硫酸变红色,硝酸亚铁遇稀硫酸
变成铁盐,氢氧化亚铁与稀硫酸反应生成硫酸亚铁,碱式碳酸铜与稀硫酸反应生
成硫酸铜,B项正确;稀硫酸不能使酚酞变色,C项错误;稀硫酸与氧化铁反应生
成硫酸铁,溶液呈黄色,稀硫酸与偏铝酸钠反应得不到黄色溶液,稀硫酸与硅酸钠
反应得不到浅绿色溶液,D项错误。
答案 B2.(2018·福建福州检测)下列检验试剂选用正确的是( )
A.用氯水、KSCN溶液检验FeCl 中是否有FeCl
3 2
B.用酸性KMnO 溶液检验FeCl 中是否有FeCl
4 3 2
C.用NaOH溶液检验MgCl 中是否有FeCl
2 2
D.用硝酸检验某黄色固体是纯铜还是黄铜
解析 A项中的Fe3+产生的干扰无法消除;B项中酸性KMnO 还能氧化Cl-;C
4
项中虽然Mg2+也能形成白色沉淀,但若有Fe2+,则生成的白色沉淀颜色会发生变
化;D项中纯铜和黄铜均能溶解在硝酸中。
答案 C
3.(2019·湖南长沙长郡中学月考)高铁酸钾(K FeO )作为多功能水处理剂具有广泛
2 4
的用途,下面是利用次氯酸盐在碱性条件下氧化硝酸铁制备K FeO 的生产工艺流
2 4
程图:
下列判断正确的是( )
A.反应①中氯气只起氧化剂的作用
B.溶液Ⅰ的溶质是KClO
C.反应③中氧化剂与还原剂的物质的量之比为1∶1
D.溶液Ⅱ的溶质成分中含有K FeO
2 4
解析 足量Cl 通入到KOH溶液中,温度低时发生反应Cl +2OH-===Cl-+ClO
2 2
-+H O,向溶液Ⅰ中加入KOH固体,使氯气完全反应,且将溶液转化为碱性溶液,
2
只有碱性条件下ClO-才能和Fe3+发生氧化还原反应生成 FeO,除去KCl得到碱
性的KClO浓溶液,向碱性的KClO浓溶液中加入90%的Fe(NO ) 溶液,发生反应
3 3
2Fe3++3ClO-+10OH-===2FeO+3Cl-+5H O,得到溶液Ⅱ,纯化得到湿产品,将
2
湿产品洗涤、干燥得到晶体K FeO 。反应Cl +2OH-===Cl-+
2 4 2
ClO-+H O中,氯气既作氧化剂也作还原剂,A项错误;由上述分析可知,溶液Ⅰ
2
的溶质是KClO、KCl和KOH,B项错误;反应2Fe3++3ClO-+10OH-===2FeO+
3Cl-+5H O中,氧化剂与还原剂的物质的量之比为3∶2,C项错误;由上述分析
2可知溶液Ⅱ的溶质成分中含有K FeO ,D项正确。
2 4
答案 D
【知识增补】
1.重要的铁盐
(1)绿矾(FeSO ·7H O):一种重要的还原剂,可用作补血剂及植物的补铁剂。
4 2
(2)高铁酸钾(K FeO ):深紫色晶体,具有强氧化性,可用作水处理剂和高能电池。
2 4
(3)铁铵矾[NH Fe(SO ) ·12H O]:无色晶体,易溶于水,常用作化学分析试剂、药物
4 4 2 2
和织物媒染剂。
(4)赤血盐[K Fe(CN) ]:红色晶体,易溶于水,常用于检验Fe2+,生成蓝色沉淀。
3 6
2.盐溶液的配制与保存
3.物质的制备
[B组 考试能力过关]
4.下列叙述正确的是( )
A.(2015·全国卷Ⅰ,10A)将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液,
有气体生成,溶液呈红色,稀硝酸将Fe氧化为Fe3+
B.(2017·天津理综,1B)用可溶性的铝盐和铁盐处理水中的悬浮物
C.(2015·广东理综,22D)向FeSO 溶液中先滴入KSCN溶液,再滴加H O 溶液,
4 2 2
加入H O 后溶液变成红色, Fe2+既有氧化性又有还原性
2 2
D.(2018·江苏,9D)给定条件下,能实现转化:Fe O (s)――→Fe(s)――→FeCl (aq)
2 3 3
答案 B
5.(2018·天津南开区二模)某班同学用如下实验探究Fe2+、Fe3+的性质。
请回答下列问题:
(1)分别取一定量氯化铁、氯化亚铁固体,均配制成0.1 mol·L-1的溶液。在FeCl 溶
2
液中需加入少量铁屑,其目的是_____________________________________。
(2)甲组同学取2 mL FeCl 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红,
2
说 明 Cl 可 将 Fe2 + 氧 化 。 FeCl 溶 液 与 氯 水 反 应 的 离 子 方 程 式 为 :
2 2_____________________________________________________________________。
(3)乙组同学认为甲组的实验不够严谨,该组同学在 2 mL FeCl 溶液中先加入0.5
2
mL煤油,再于液面下依次加入几滴氯水和1滴KSCN溶液,溶液变红,煤油的作
用是_______________________________________________________________
____________________________________________________________________。
(4)丙组同学取10 mL 0.1 mol·L-1 KI溶液,加入6 mL 0.1 mol·L-1FeCl 溶液混合。
3
分别取2 mL此溶液于3支试管中进行如下实验。
①第一支试管中加入1 mL CCl 充分振荡、静置,CCl 层显紫色;
4 4
②第二支试管中加入1滴K [Fe(CN) ]溶液,生成蓝色沉淀;
3 6
③第三支试管中加入1滴KSCN溶液,溶液变红。
实验②检验的离子是(填离子符号)________;实验①和③说明:在I-过量的情况下,
溶液中仍含有(填离子符号)________,由此可以证明该氧化还原反应为
____________________________________________________________________。
(5)丁组同学向盛有H O 溶液的试管中加入几滴酸化的FeCl 溶液,溶液变成棕黄
2 2 2
色,发生反应的离子方程式为_______________________________________;
一段时间后,溶液中有气泡出现,并放热,随后有红褐色沉淀生成。产生气泡的原
因是______________________________________________________________;
生 成 沉 淀 的 原 因 是 ( 用 平 衡 移 动 原 理 解
释)__________________________________________________________________。
(6)戊组同学模拟工业上用NaClO 氧化酸性FeCl 废液制备FeCl 。
3 2 3
①若酸性FeCl 废液中:c(Fe2+)=2.0×10-2mol·L-1,c(Fe3+)=1.0×10-3mol·L-1,
2
c(Cl-)=5.3×10-2mol·L-1,则该溶液的pH约为________。
②完成NaClO 氧化FeCl 的离子方程式:
3 2
③FeCl 具有净水作用,其原理是_________________________________________。
3
解析 (1)亚铁离子具有还原性,能被空气中的氧气氧化,所以在配制的氯化亚铁溶液中加入少量铁屑的目的是防止Fe2+被氧化;(2)Cl 可将Fe2+氧化成Fe3+,自身
2
得电子生成氯离子,反应的离子方程式为:2Fe2++Cl ===2Fe3++2Cl-;(3)防止空
2
气中的氧气将Fe2+氧化,产生干扰,所以煤油的作用是隔绝空气;(4)根据Fe2+的
检验方法,向溶液中加入1滴K [Fe(CN) ]溶液,生成蓝色沉淀,一定含有Fe2+;则
3 6
实验②检验的离子是Fe2+;碘易溶于CCl ,在CCl 中呈紫色,Fe3+遇KSCN溶液
4 4
显血红色,实验①和③说明在I-过量的情况下,溶液中仍含有Fe3+,由此可以证明
该氧化还原反应为可逆反应;(5)H O 溶液中加入几滴酸化的FeCl 溶液,溶液变
2 2 2
成棕黄色,发生反应的离子方程式为:2Fe2++H O +2H+===2Fe3++2H O,铁离
2 2 2
子的溶液呈棕黄色;一段时间后,溶液中有气泡出现,并放热。随后有红褐色沉淀
生成,产生气泡的原因是H O 分解放出氧气,而反应放热,促进Fe3+的水解平衡
2 2
正向移动;(6)①根据电荷守恒,则溶液中氢离子的浓度是 c(Cl-)-2c(Fe2+)-
3c(Fe3+)=1.0×10-2mol/L,所以pH=2;②根据题意,氯酸钠氧化酸性的氯化亚铁,
则反应物中有氢离子参加,则生成物中有水生成,Cl元素的化合价从+5价降低
到-1价,得到6个电子,而Fe元素的化合价从+2价升高到+3价,失去1个电
子,根据得失电子守恒,则氯酸根离子的系数为1,Fe2+的系数为6,则铁离子的系
数也是6,氯离子的系数是1,根据电荷守恒,则氢离子的系数是6,水的系数是3;
即:ClO+6Fe2++6H+===Cl-+6Fe3++3H O;
2
③Fe3+水解生成的Fe(OH) 胶体粒子能吸附水中的悬浮杂质,所以可起到净水的
3
作用。
答案 (1)防止Fe2+被氧化
(2)2Fe2++Cl ===2Fe3++2Cl-
2
(3)隔绝空气(排除氧气对实验的影响)
(4)Fe2+ Fe3+ 可逆反应
(5)2Fe2++H O +2H+===2Fe3++2H O Fe3+催化H O 分解产生O H O 分解
2 2 2 2 2 2 2 2
反应放热,促进Fe3+的水解平衡正向移动
(6)①2 ②1 6 6H+ 1 6 3H O
2
③Fe3+水解产生的Fe(OH) 胶体粒子能吸附水中悬浮的杂质
3
INCLUDEPICTURE "F:\\方正文件\\2019文件\\课件\\2020版 创新设计 高考总
复习 化学 人教版\\分层课时作业.TIF" \* MERGEFORMATINET[A级 全员必做题]
1.(2018·威海高三测试)铁是人类应用较早,当前应用量最大的金属元素。下列有
关铁及其化合物的有关说法中正确的是( )
A.赤铁矿的主要成分是Fe O
3 4
B.铁与水蒸气在高温下的反应产物为Fe O 和H
2 3 2
C.除去FeCl 溶液中的FeCl 杂质可以向溶液中加入铁粉,然后过滤
2 3
D.Fe3+与KSCN产生血红色沉淀
解析 赤铁矿的主要成分是Fe O ;铁与水蒸气在高温下的反应产物为 Fe O 和
2 3 3 4
H ;+3价铁离子遇KSCN溶液变为血红色,但没有沉淀产生,一般可以用此方法
2
检验+3价铁离子的存在。
答案 C
2.现榨的苹果汁在空气中会由淡绿色变为棕黄色,其原因可能是( )
A.苹果汁中的Fe2+变成Fe3+ B.苹果汁中含有Cu2+
C.苹果汁中含有OH- D.苹果汁中含有Fe3+
解析 A项,苹果汁中的Fe2+变成Fe3+,使得现榨的苹果汁在空气中会由淡绿色
变为棕黄色,正确;B项,Cu2+显蓝色,错误;C项,OH-无色,错误;D项,Fe3+本身
是棕黄色,错误。
答案 A
3.(2019·石家庄模拟)把铁片分别放入下列物质的溶液中,充分反应后,溶液质量
比反应前减轻的是( )
A.CuSO B.Fe (SO )
4 2 4 3
C.HCl D.FeSO
4
解析 铁与 CuSO 反应后,生成 FeSO 溶液,溶液质量减轻,A 正确;铁与
4 4
Fe (SO ) 反应后,生成FeSO 溶液,溶液质量增加,B错误;铁与盐酸反应后,生成
2 4 3 4
FeCl 溶液,溶液质量增加,C错误;铁与FeSO 溶液不反应,溶液质量不变,D错误
2 4
答案 A
4.下列中学常见实验的现象或表述正确的是( )
A.过量的铁投入到一定量的稀硝酸中,充分反应后取上层清液于试管中,滴加
KSCN溶液,溶液显红色B.制备氢氧化亚铁时,向硫酸亚铁溶液中滴加氢氧化钠溶液,边加边搅拌,即可制
得白色的氢氧化亚铁
C.检验红砖中的氧化铁成分,向红砖粉末中加入盐酸,充分反应后取上层清液于
试管中,滴加KSCN溶液2~3滴,溶液显红色即可证明
D.向CuSO 溶液中滴入过量NaOH溶液充分反应后,将混合液体倒入蒸发皿中加
4
热煮沸一会,然后冷却、过滤,滤纸上的物质为“蓝色固体”
解析 过量的铁粉与一定量的稀硝酸反应最终生成的是Fe2+,A错误;制备氢氧
化亚铁应避免被氧气氧化,向硫酸亚铁溶液中加氢氧化钠溶液时应把长胶头滴管
的下端插入液面以下且不能搅拌,B错误;CuSO 溶液中滴入过量NaOH溶液充分
4
反应后生成Cu(OH) 沉淀,加热后过滤,滤纸上留有的是CuO(黑色),D错误。
2
答案 C
5.下列离子在指定溶液中能大量共存的是( )
A.1.0 mol·L-1的KNO 溶液:H+、Fe2+、Cl-、SO
3
B.1.0 mol·L-1的FeCl 溶液:NO、Na+、K+、ClO-
2
C.使酚酞变红的溶液中:Na+、Cl-、SO、Fe3+
D.酸性溶液中:NO、SO、Fe3+、Mg2+
解析 A项,KNO 在酸性条件下能氧化Fe2+;B项,ClO-能氧化Fe2+;C项,Fe3+
3
在碱性条件下生成沉淀,不能存在。
答案 D
6.通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下
列实验事实的解释正确的是( )
选项 操作、现象 解释
向KI淀粉溶液中加入FeCl 溶液,
A 3 Fe3+能与淀粉发生显色反应
溶液变蓝
把生铁放置于潮湿的空气中,铁表
B 铁在潮湿的空气中易生成Fe(OH)
面有一层红棕色的斑点 3
向稀硝酸中加入少量铁粉,有气泡 说明Fe置换出硝酸中的氢,生成了
C
产生 氢气
新制Fe(OH) 露置于空气中一段时 说明Fe(OH) 易被O 氧化成
D 2 2 2
间,白色物质变成了红褐色 Fe(OH)
3
解析 A项中Fe3+将I-氧化为I ,淀粉遇碘变蓝;B项中红棕色的斑点是Fe O ;C
2 2 3
项中铁与稀硝酸反应产生的气体为NO。答案 D
7.(2019·绵阳诊断)下列有关0.2 mol/L Fe(NO ) 溶液的叙述正确的是( )
3 2
A.该溶液中Na+、K+、[Fe(CN) ]3-、I-可以大量共存
6
B.滴加稀硫酸,充分振荡无现象
C.通入H S气体,发生反应的离子方程式为Fe2++S2-===FeS↓
2
D.50 mL该溶液与过量Zn充分反应,生成0.56 g Fe
解析 Fe2+会与[Fe(CN) ]3-反应生成蓝色沉淀,因此不能大量共存,故A项错误;
6
滴加稀硫酸,使溶液呈酸性,在酸性条件下,NO能将Fe2+氧化为Fe3+,溶液由浅
绿色变为黄色,故B项错误;通入H S气体,溶液显酸性,硝酸根在酸性条件下具
2
有氧化性,能将硫离子氧化成硫单质、Fe2+被氧化成Fe3+,故C项错误;50 mL 0.2
mol/L Fe(NO ) 溶液与过量Zn充分反应,离子方程式为Zn+Fe2+===Zn2++Fe,计
3 2
算可知生成Fe的质量为0.56 g,故D项正确。
答案 D
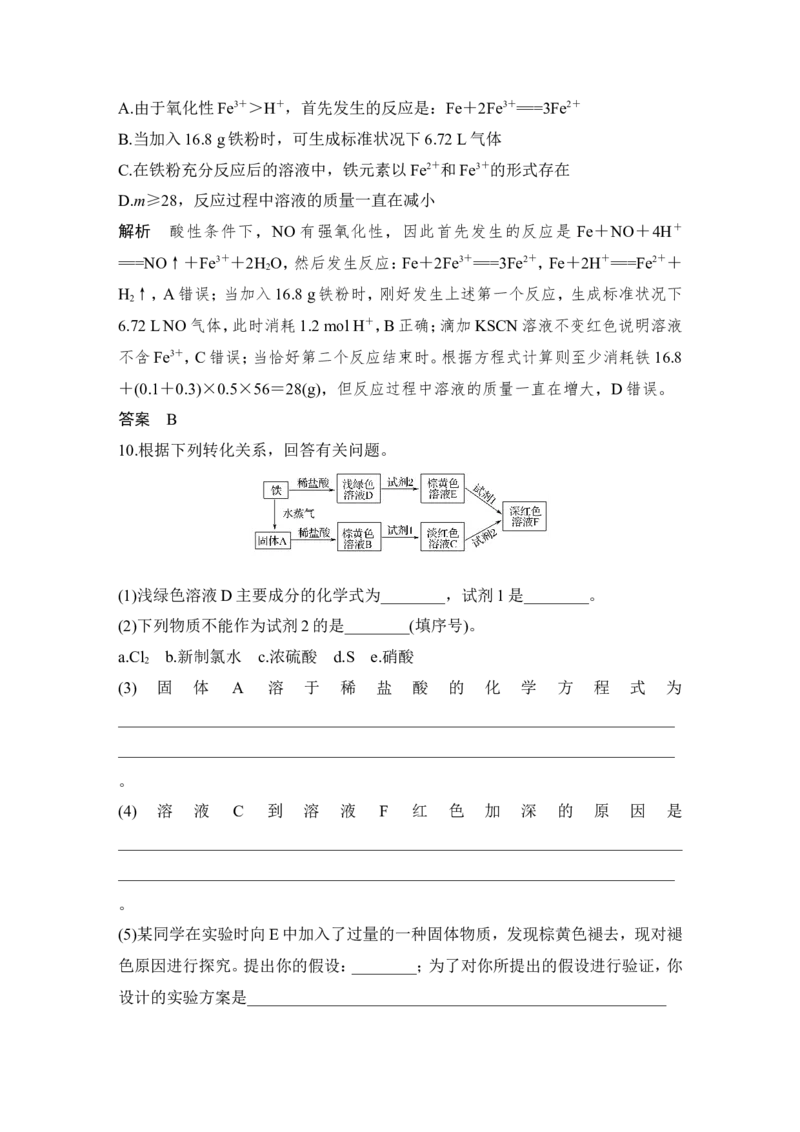
8.根据框图分析,下列说法正确的是( )
A.氧化性:E2+>M2+
B.在反应③中加稀硫酸可抑制E2+的水解
C.反应④的离子方程式为E3++3SCN- E(SCN) ↓
3
D.反应①中只能用浓硫酸,既表现了酸性,又表现了氧化性
解析 金属性:Fe>Cu,氧化性:E2+Fe3+>Cu2+,可知随铁粉的增加,反应的方
3
程式分别为
4HNO (稀)+Fe=== Fe(NO ) +NO↑+2H O
3 3 3 2
4 mol 1 mol 1 mol
2Fe(NO ) +Fe===3Fe(NO )
3 3 3 22 mol 1 mol 3 mol
Cu(NO ) +Fe===Fe(NO ) +Cu
3 2 3 2
1 mol 1 mol 1 mol
所以原溶液中 Fe(NO ) 、Cu(NO ) 、HNO 的物质的量之比为(2 mol-1 mol)∶1
3 3 3 2 3
mol∶4 mol=1∶1∶4。
答案 D
14.(全国卷)绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用
途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化
再 向 试 管 中 通 入 空 气 , 溶 液 逐 渐 变 红 。 由 此 可 知 :
_____________________________________________________________________、
____________________________________________________________________。
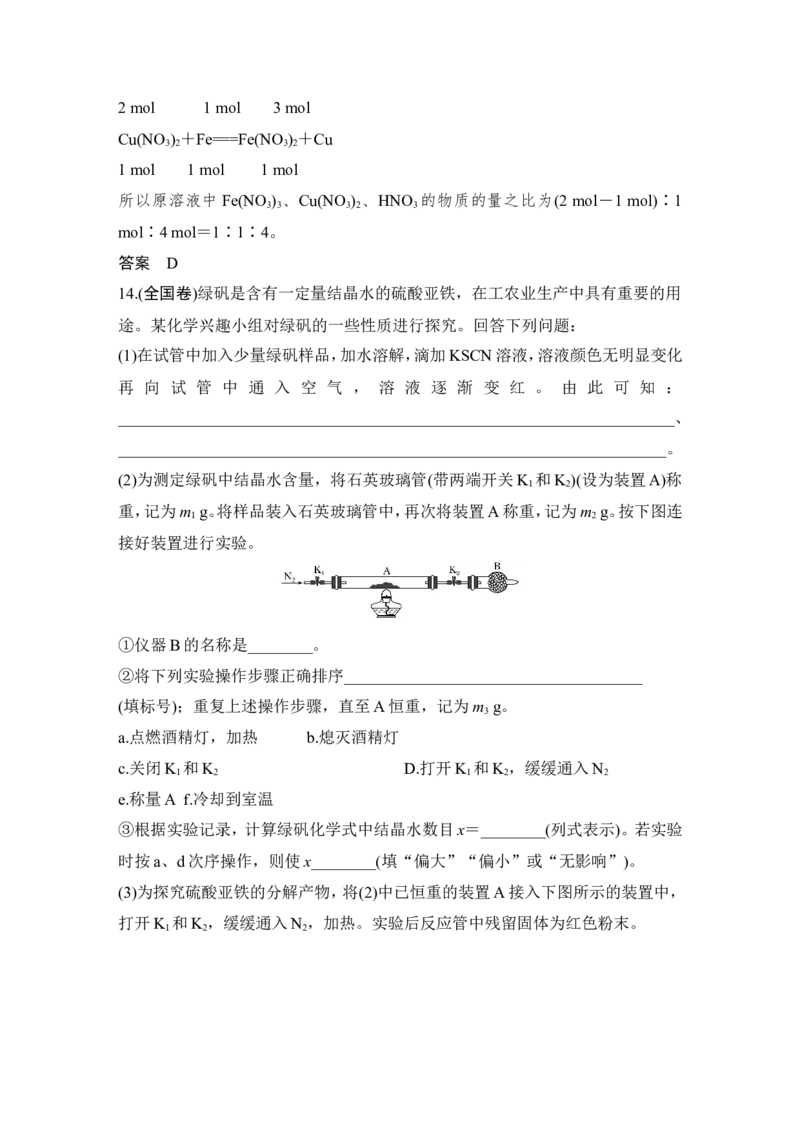
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K 和K )(设为装置A)称
1 2
重,记为m g。将样品装入石英玻璃管中,再次将装置A称重,记为m g。按下图连
1 2
接好装置进行实验。
①仪器B的名称是________。
②将下列实验操作步骤正确排序_____________________________________
(填标号);重复上述操作步骤,直至A恒重,记为m g。
3
a.点燃酒精灯,加热 b.熄灭酒精灯
c.关闭K 和K D.打开K 和K ,缓缓通入N
1 2 1 2 2
e.称量A f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=________(列式表示)。若实验
时按a、d次序操作,则使x________(填“偏大”“偏小”或“无影响”)。
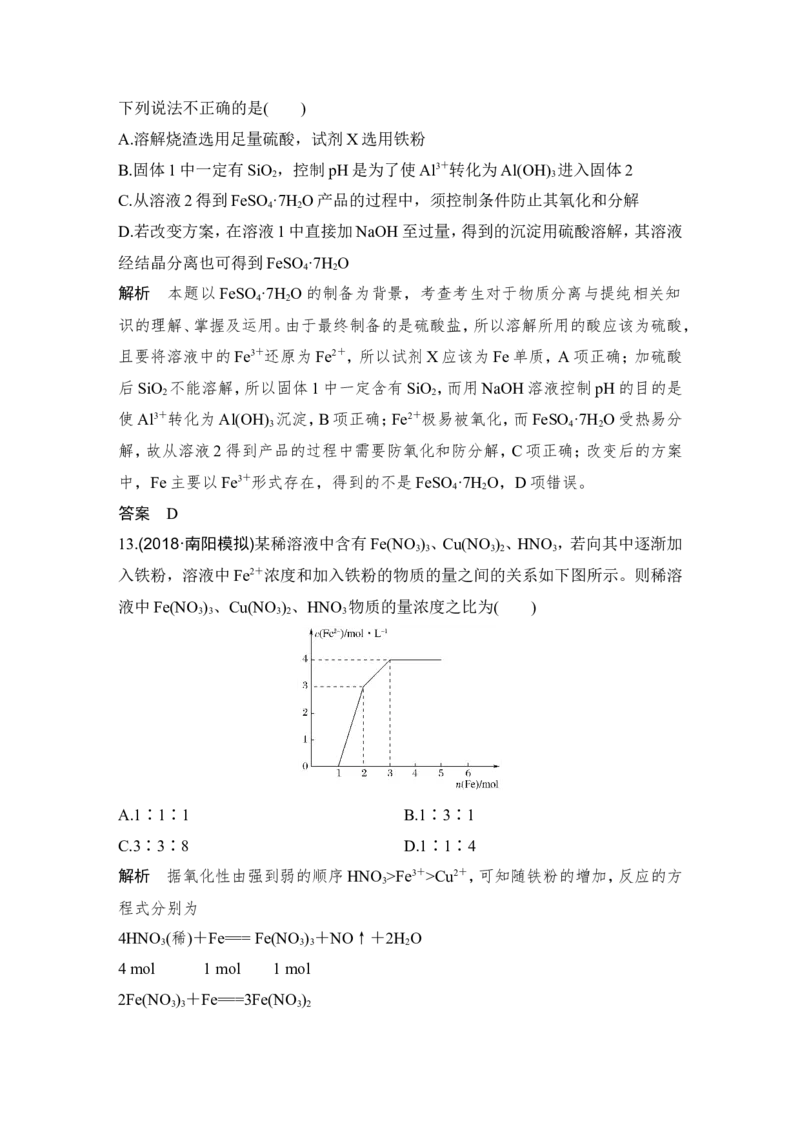
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,
打开K 和K ,缓缓通入N ,加热。实验后反应管中残留固体为红色粉末。
1 2 2①C、D中的溶液依次为________(填标号)。C、D中有气泡冒出,并可观察到的现
象分别为___________________________________________________________。
a.品红 b.NaOH c.BaCl d.Ba(NO )
2 3 2
e.浓H SO
2 4
② 写 出 硫 酸 亚 铁 高 温 分 解 反 应 的 化 学 方 程 式
_____________________________________________________________________
_____________________________________________________________________
。
解析 (1)绿矾溶解于水电离出Fe2+,滴加KSCN溶液后颜色无明显变化,说明样
品中没有Fe3+,通入空气之后,空气中的氧气把Fe2+氧化为Fe3+,Fe3+与KSCN反
应而使溶液显红色,说明Fe2+易被氧气氧化为Fe3+。
(2)①仪器B的名称是干燥管;②实验时先打开K 和K ,缓慢通入N ,排除装置中
1 2 2
的空气,防止空气中的氧气将绿矾中的Fe2+氧化为Fe3+,一段时间后点燃酒精灯,
使绿矾中的结晶水变为水蒸气并被N 排出,然后熄灭酒精灯,将石英玻璃管冷却
2
至室温后关闭K 和K ,防止空气进入石英玻璃管中,最后称量A;
1 2
③由题意可知FeSO 的物质的量为 mol,水的物质的量为 mol,则绿矾中结晶水
4
的数目x===;若先点燃酒精灯再通N ,则石英玻璃管中原有的空气会将绿矾
2
中的Fe2+氧化,最终剩余的固体质量会偏大,则计算得到的结晶水的数目会偏小;
(3)①实验后反应管中残留的红色粉末为Fe O ,根据得失电子守恒可知必然有
2 3
SO 产生,根据原子守恒可知还会生成SO ,检验的试剂应选择品红溶液、BaCl 溶
2 3 2
液,不能选择Ba(NO ) 溶液,因为SO 会与Ba(NO ) 溶液产生白色沉淀,干扰SO
3 2 2 3 2 3
的检验,由于SO 可与水反应生成硫酸,故应先检验SO ,再利用SO 能使品红褪
3 3 2
色 的 原 理 检 验 SO ; ② 由 题 意 可 以 得 到 硫 酸 亚 铁 分 解 的 方 程 式 为
2
2FeSO =====Fe O +SO ↑+SO ↑。
4 2 3 2 3
答案 (1)样品中没有Fe3+ Fe2+易被氧气氧化为Fe3+ (2)①干燥管 ②d、a、b、
f、c、e ③ 偏小 (3)①c、a 生成白色沉淀、品红褪色 ②2FeSO =====Fe O +
4 2 3SO ↑+SO ↑
2 3