文档内容
第三章能力提升检测卷
完卷时间:90分钟
可能用到的相对原子质量:H1 C12 O16 Al27 Cl35.5 Ca40 Fe56 Cu64
一、选择题(每小题只有一个正确选项,共16*3分)
1.(2021·上海复旦附中高三一模)下列金属冶炼的反应原理,错误的是
A.
B.
C.
D.
2.(2020·陕西西安市庆安高级中学高三二模)下列有关金属及其化合物的性质或用途叙述错误的是(
)
A.钛具有密度小,硬度大、熔点高且化学性质稳定的优点,广泛应用于航空领域
B.过氧化钠可用于潜艇的供氧剂
C.由于氢氧化铝的碱性不强,其可作为胃酸中和剂
D.明矾可用于水的消毒处理
3.(2021·上海高三二模)2021年3月1日,东方航空公司与中国商飞公司在上海正式签署了C919购机
合同。东航将成为全球首家运营C919大型客机的航空公司。大飞机 C919其主结构材料大量使用了铝锂合
金,铝锂合金的优点是
A.高强度、导热性 B.低密度、高强度 C.低密度、导电性 D.导热性、导电性
4.(2021·重庆高三零模)人工泳池水质须符合CJ/T244-2016标准,为此在泳池里需要加入某些化学品。
下列做法错误的是
A.用明矾作净水剂 B.用硫酸铜作杀藻剂
C.用氯化钠作pH 调节剂 D.用次氯酸钠作消毒剂
5.(2020·云南玉溪市·高三一模)2020年10月16日,国家药监局网站公布2026年起将全面禁止生产
含汞体温计。《本草纲目》记载:“水银乃至阴之毒物,因火煅丹砂而出,加以盐、(明)矾而为轻粉,加
以硫磺升而为银朱”。下列说法错误的是
A.短时间内吸入大量汞蒸气,会汞中毒
B.“火煅丹砂”是氧化还原反应
C.明矾的化学式是KAl(SO)·12HO,是混合物
4 2 2D.水银温度计打碎后,洒出的汞可以用硫磺处理
6.(2021·浙江宁波市·高三一模)下列说法或基本操作合理的是
A.在空气中,将氯化镁溶液蒸发结晶可以获得纯净的氯化镁固体
B.金属钠切割后的剩余部分不能放回原试剂瓶,应放置废液缸中
C.可用硝酸和硝酸银溶液鉴别氯化钠溶液与亚硝酸钠溶液
D.硝酸银溶液保存在棕色的广口瓶中,防止见光分解
7.(2020·郁南县蔡朝焜纪念中学高三月考)下列有关金属的工业制法中,正确的是
A.以海水为原料制得精盐,再电解精盐的水溶液制取钠
B.用海水、石灰乳等原料制得氧化镁,再用 H 还原氧化镁制得镁
2
C.用焦炭、空气、石灰石等原料,生产 CO 在高温下还原铁矿石制得铁
D.从铝土矿中获得氧化铝再制得氯化铝固体,电解熔融的氯化铝得到铝
8.(2021·宝鸡市渭滨中学高三月考)化学与生活密切相关,下列应用没有涉及氧化还原反应的是(
)
A.过氧化钠用作缺氧场所的供氧剂 B.氯化铁用于净水
C.铝热反应用于焊接铁轨 D.铝罐车用作运输浓硫酸
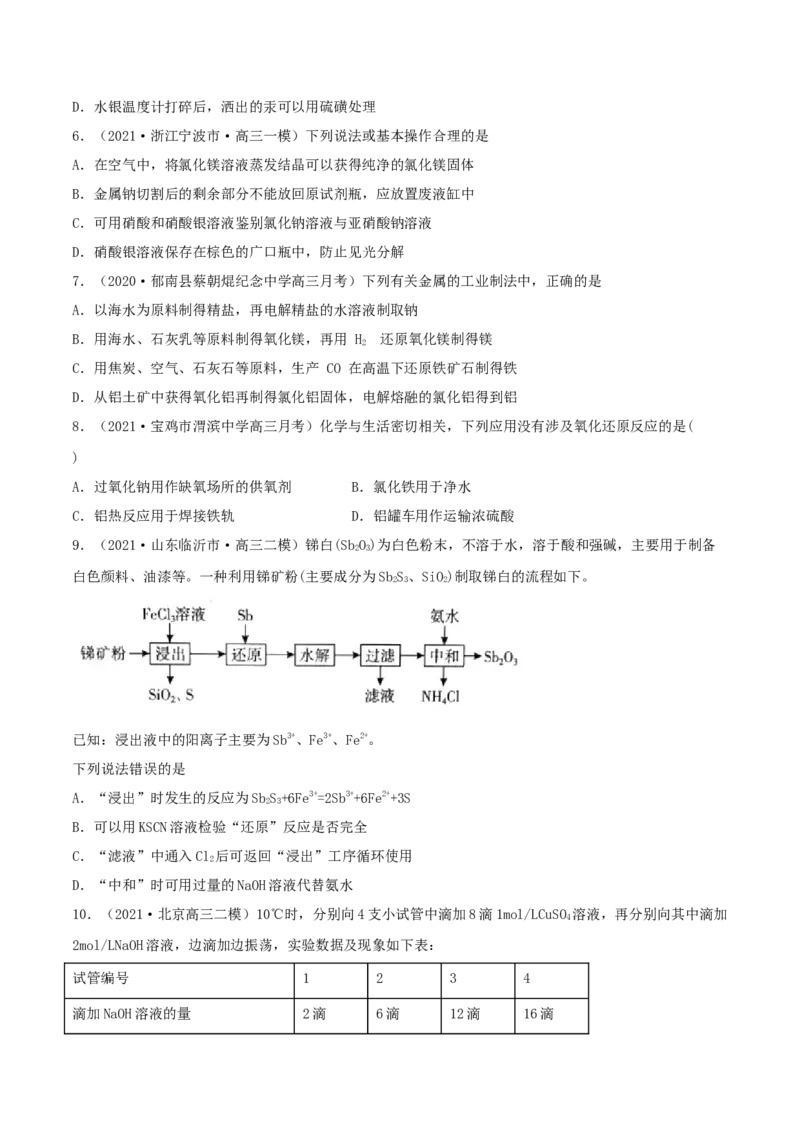
9.(2021·山东临沂市·高三二模)锑白(SbO)为白色粉末,不溶于水,溶于酸和强碱,主要用于制备
2 3
白色颜料、油漆等。一种利用锑矿粉(主要成分为SbS、SiO)制取锑白的流程如下。
2 3 2
已知:浸出液中的阳离子主要为Sb3+、Fe3+、Fe2+。
下列说法错误的是
A.“浸出”时发生的反应为SbS+6Fe3+=2Sb3++6Fe2++3S
2 3
B.可以用KSCN溶液检验“还原”反应是否完全
C.“滤液”中通入Cl 后可返回“浸出”工序循环使用
2
D.“中和”时可用过量的NaOH溶液代替氨水
10.(2021·北京高三二模)10℃时,分别向4支小试管中滴加8滴1mol/LCuSO 溶液,再分别向其中滴加
4
2mol/LNaOH溶液,边滴加边振荡,实验数据及现象如下表:
试管编号 1 2 3 4
滴加NaOH溶液的量 2滴 6滴 12滴 16滴立即观察沉淀的颜色 浅绿色 浅绿色 蓝色 蓝色
酒精灯加热浊液后沉淀的颜色 浅绿色 浅绿色 黑色 黑色
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl 溶液,产生大量白色沉淀。取
2
蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。
下列说法不正确的是
A.由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜
B.CuSO 溶液与NaOH溶液反应时,其相对量不同可以得到不同的产物
4
C.试管3、4中的固体在加热过程中发生了反应:Cu(OH) CuO+HO
2 2
D.取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
11.(2021·河北邯郸市·高三二模)沈括在《梦溪笔谈》中写道:“古以剂钢为刃,柔铁为茎干,不而
则多断折。剑之钢者,刃多毁缺”。其中“剂钢”即合金钢,“柔铁”即熟铁,下列说法正确的是
A.“剂钢”是混合物,“柔铁”是纯净物
B.合金都由两种或两种以上的金属熔合而成
C.改变合金中某种元素的含量可制得不同性能的合金
D.“剂钢”和“柔铁”的强度、硬度和熔点均比纯铁的高
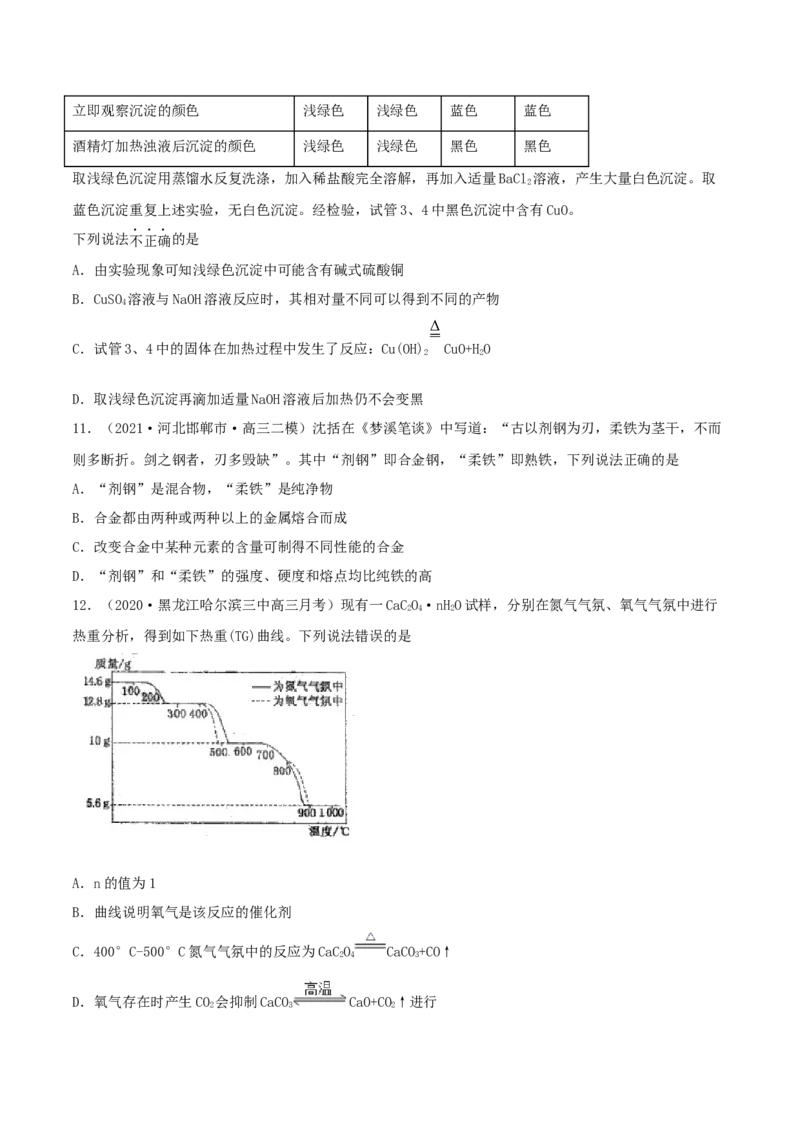
12.(2020·黑龙江哈尔滨三中高三月考)现有一CaCO·nHO试样,分别在氮气气氛、氧气气氛中进行
2 4 2
热重分析,得到如下热重(TG)曲线。下列说法错误的是
A.n的值为1
B.曲线说明氧气是该反应的催化剂
C.400°C-500°C氮气气氛中的反应为CaCO CaCO+CO↑
2 4 3
D.氧气存在时产生CO 会抑制CaCO CaO+CO↑进行
2 3 213.(2021·浙江杭州市·高三二模)有关铝及其化合物的说法错误的是
A.氧化铝熔点较高,是一种优良的耐火材料
B.可用铝壶烧开水,不可用其长期存放食醋、碱水
C.铁易生锈,而铝在空气中较稳定,所以铁比铝活泼
D.氢氧化铝能中和胃酸,可用于制胃药
14.(2021·厦门英才学校高三月考)下列物质在生活中的应用与氧化还原反应无关的是
A.CaO用作衣物防潮剂
B.还原Fe粉用作食品脱氧剂
C. 补血剂与维生素C配合使用效果更佳
D.用硅藻土中浸润的 吸收水果散发的乙烯
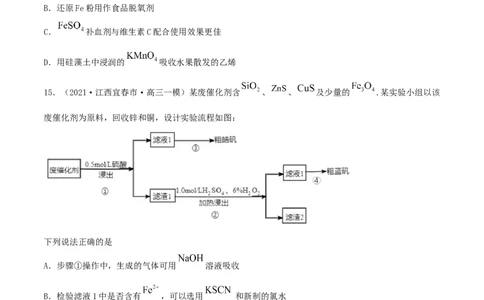
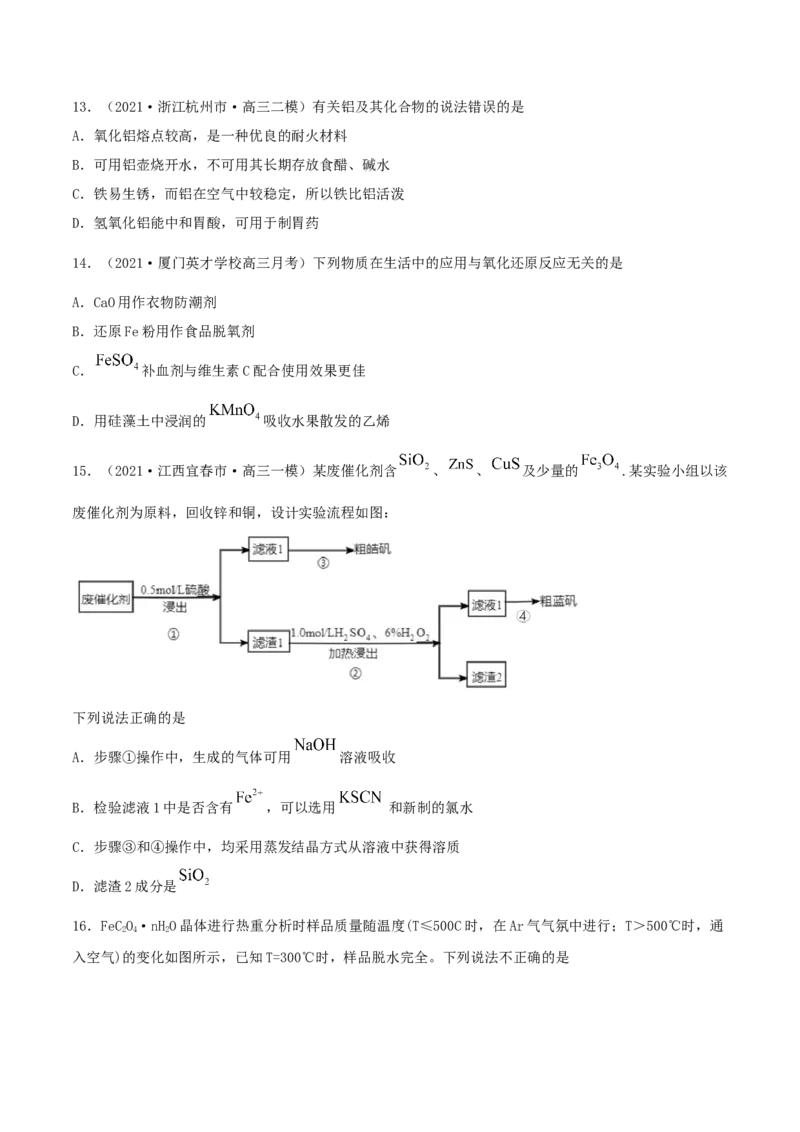
15.(2021·江西宜春市·高三一模)某废催化剂含 、 、 及少量的 .某实验小组以该
废催化剂为原料,回收锌和铜,设计实验流程如图:
下列说法正确的是
A.步骤①操作中,生成的气体可用 溶液吸收
B.检验滤液1中是否含有 ,可以选用 和新制的氯水
C.步骤③和④操作中,均采用蒸发结晶方式从溶液中获得溶质
D.滤渣2成分是
16.FeCO·nHO晶体进行热重分析时样品质量随温度(T≤500C时,在Ar气气氛中进行;T>500℃时,通
2 4 2
入空气)的变化如图所示,已知T=300℃时,样品脱水完全。下列说法不正确的是A.n=2
B.T=400℃时,每分解0.1 mol样品时,产生4.48L(标准状况)气体
C.T=600℃时,残留固体中Fe的质量分数为60.07%
D.T=1400℃时,残留固体为FeO
3 4
二、主观题(共5小题,共52分)
17.(10分)某再回收利用公司对一厨房铁铝合金废旧家具进行回收利用,其流程如下图所示:
请回答下列问题:
(1)流程中加碳酸钠溶液浸泡的目的是_______________;在空气中久置的目的是_________________。
(2)同条件下NaFeO 溶解度__________KFeO 溶解度(填“低于”,“高于”, “不确定”),推测KFeO
2 4 2 4 2 4
在净水方面的作用_______________。(至少答两条)
(3)已知KFeO 水解显碱性。在洗涤KFeO 固体时最好选用__________。
2 4 2 4
A.水 B.亚硫酸氢钠溶液 C.氢氧化钠溶液 D.先氢氧化钠溶液后乙醇
(4)熔融盐电镀中铝元素和氯元素主要以AlCl-和AlCl-形式存在,铝电镀的主要电极反应式为
4 2 7
___________________。(写出一个电极反应即可)
(5)已知氯化铝受热易升华,气态氯化铝的密度为11.92g/L(已转化为标准状况),则气态氯化铝的分子式为
______________________。
(6)氢氧化铝经常用于做药品,有两种溶解方式:可以溶解为Al3+或[Al(OH)]-。已知25℃时氢氧化铝在
4
pH=3和pH=10的两溶液中溶解度均为7.8×10-3g(溶液密度近似为1g/mL),则25℃下氢氧化铝的两种溶解
方式的溶度积之比为____________。
18.(7分)镁铝尖晶石(MgAlO)常做耐火材料。共沉淀制备尖晶石的方法是:用AlCl 和MgCl 的混合溶
2 4 3 2
液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。完成下列填空:(1)为使Mg2+、Al3+同时生成沉淀,应该把_____(填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
___________________(用离子符号表示)。
(3)AlCl 与氨水反应的反应物和生成物中,属于离子化合物的电子式是_________,属于难溶物的电离方
3
程式_____________________________。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________。
a. HO比NH 稳定 b. 共用电子对偏向:H-O>H-N
2 3
c. 沸点:HO>NH d. NO中氮是+2价,氧是-2价
2 3
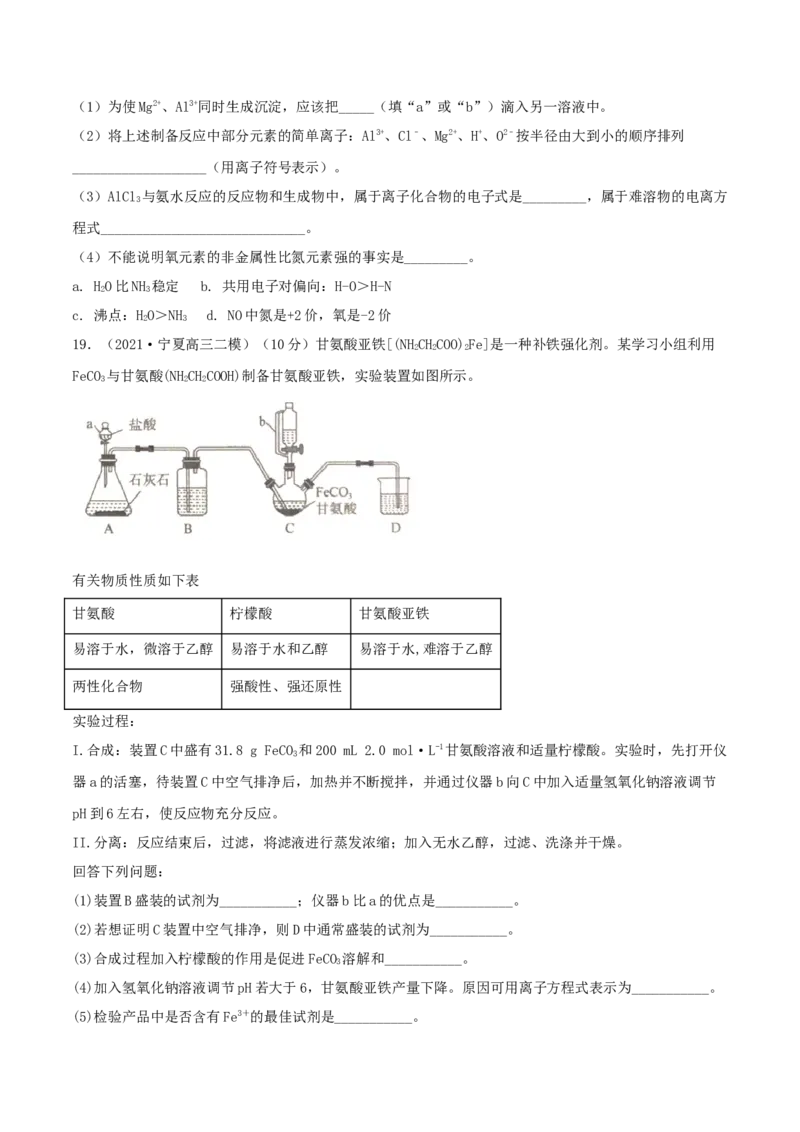
19.(2021·宁夏高三二模)(10分)甘氨酸亚铁[(NHCHCOO)Fe]是一种补铁强化剂。某学习小组利用
2 2 2
FeCO 与甘氨酸(NHCHCOOH)制备甘氨酸亚铁,实验装置如图所示。
3 2 2
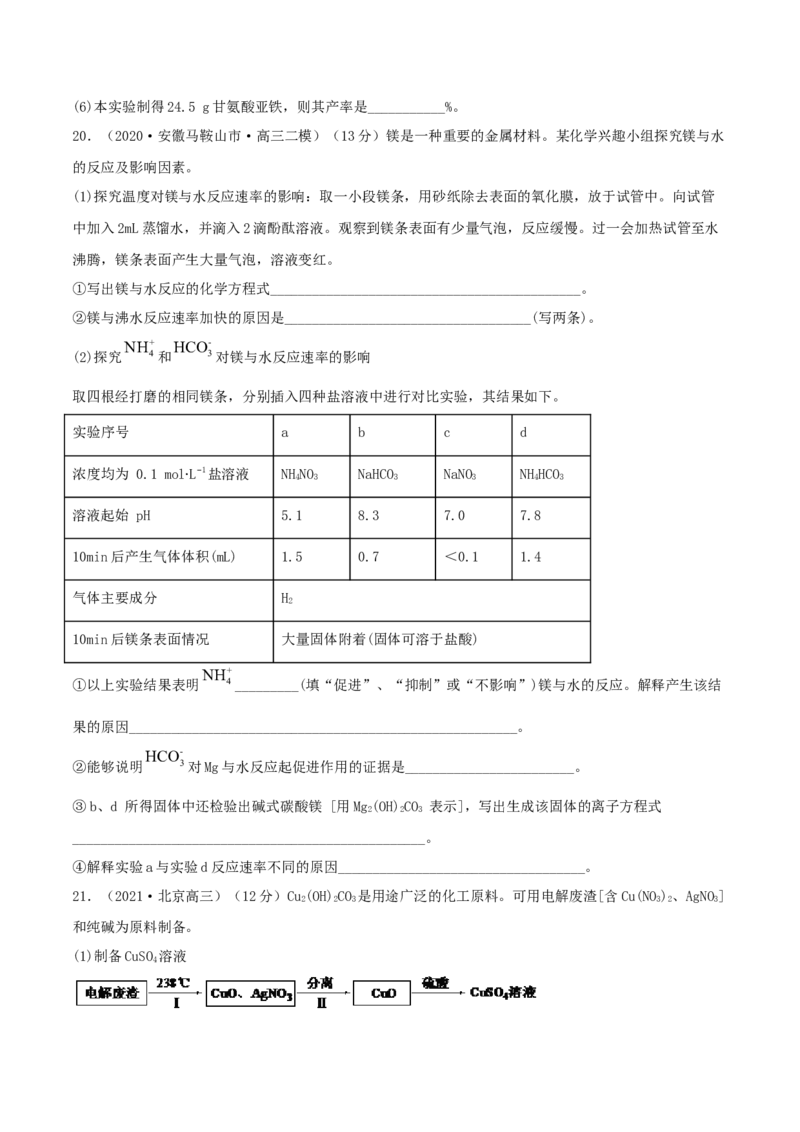
有关物质性质如下表
甘氨酸 柠檬酸 甘氨酸亚铁
易溶于水,微溶于乙醇 易溶于水和乙醇 易溶于水,难溶于乙醇
两性化合物 强酸性、强还原性
实验过程:
I.合成:装置C中盛有31.8 g FeCO 和200 mL 2.0 mol·L-1甘氨酸溶液和适量柠檬酸。实验时,先打开仪
3
器a的活塞,待装置C中空气排净后,加热并不断搅拌,并通过仪器b向C中加入适量氢氧化钠溶液调节
pH到6左右,使反应物充分反应。
II.分离:反应结束后,过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
回答下列问题:
(1)装置B盛装的试剂为___________;仪器b比a的优点是___________。
(2)若想证明C装置中空气排净,则D中通常盛装的试剂为___________。
(3)合成过程加入柠檬酸的作用是促进FeCO 溶解和___________。
3
(4)加入氢氧化钠溶液调节pH若大于6,甘氨酸亚铁产量下降。原因可用离子方程式表示为___________。
(5)检验产品中是否含有Fe3+的最佳试剂是___________。(6)本实验制得24.5 g甘氨酸亚铁,则其产率是___________%。
20.(2020·安徽马鞍山市·高三二模)(13分)镁是一种重要的金属材料。某化学兴趣小组探究镁与水
的反应及影响因素。
(1)探究温度对镁与水反应速率的影响:取一小段镁条,用砂纸除去表面的氧化膜,放于试管中。向试管
中加入2mL蒸馏水,并滴入2滴酚酞溶液。观察到镁条表面有少量气泡,反应缓慢。过一会加热试管至水
沸腾,镁条表面产生大量气泡,溶液变红。
①写出镁与水反应的化学方程式____________________________________________。
②镁与沸水反应速率加快的原因是___________________________________(写两条)。
NH+ HCO-
(2)探究 4和 3对镁与水反应速率的影响
取四根经打磨的相同镁条,分别插入四种盐溶液中进行对比实验,其结果如下。
实验序号 a b c d
浓度均为 0.1 mol∙L−1盐溶液 NHNO NaHCO NaNO NHHCO
4 3 3 3 4 3
溶液起始 pH 5.1 8.3 7.0 7.8
10min后产生气体体积(mL) 1.5 0.7 <0.1 1.4
气体主要成分 H
2
10min后镁条表面情况 大量固体附着(固体可溶于盐酸)
NH+
①以上实验结果表明 4_________(填“促进”、“抑制”或“不影响”)镁与水的反应。解释产生该结
果的原因_______________________________________________________。
HCO-
②能够说明 3对Mg与水反应起促进作用的证据是________________________。
③b、d 所得固体中还检验出碱式碳酸镁 [用Mg(OH)CO 表示],写出生成该固体的离子方程式
2 2 3
__________________________________________________。
④解释实验a与实验d反应速率不同的原因___________________________________。
21.(2021·北京高三)(12分)Cu(OH)CO 是用途广泛的化工原料。可用电解废渣[含Cu(NO)、AgNO]
2 2 3 3 2 3
和纯碱为原料制备。
(1)制备CuSO 溶液
4①过程Ⅰ中,分解产生的气体除NO 外,一定还含有_______。
2
②过程Ⅱ中,分离所采用的试剂是_______。
(2)制备Cu(OH)CO
2 2 3
ⅰ.取NaCO 溶液于锥形瓶中,水浴加热至适当温度。
2 3
ⅱ.将CuSO 溶液逐滴加入到NaCO 溶液中,产生沉淀,静置。
4 2 3
ⅲ.待沉淀完全沉降后,减压过滤、洗涤、干燥。
①步骤ⅰ中加热NaCO 溶液的目的是_______。
2 3
②步骤ⅱ中生成Cu(OH)CO 的化学方程式为_______。
2 2 3
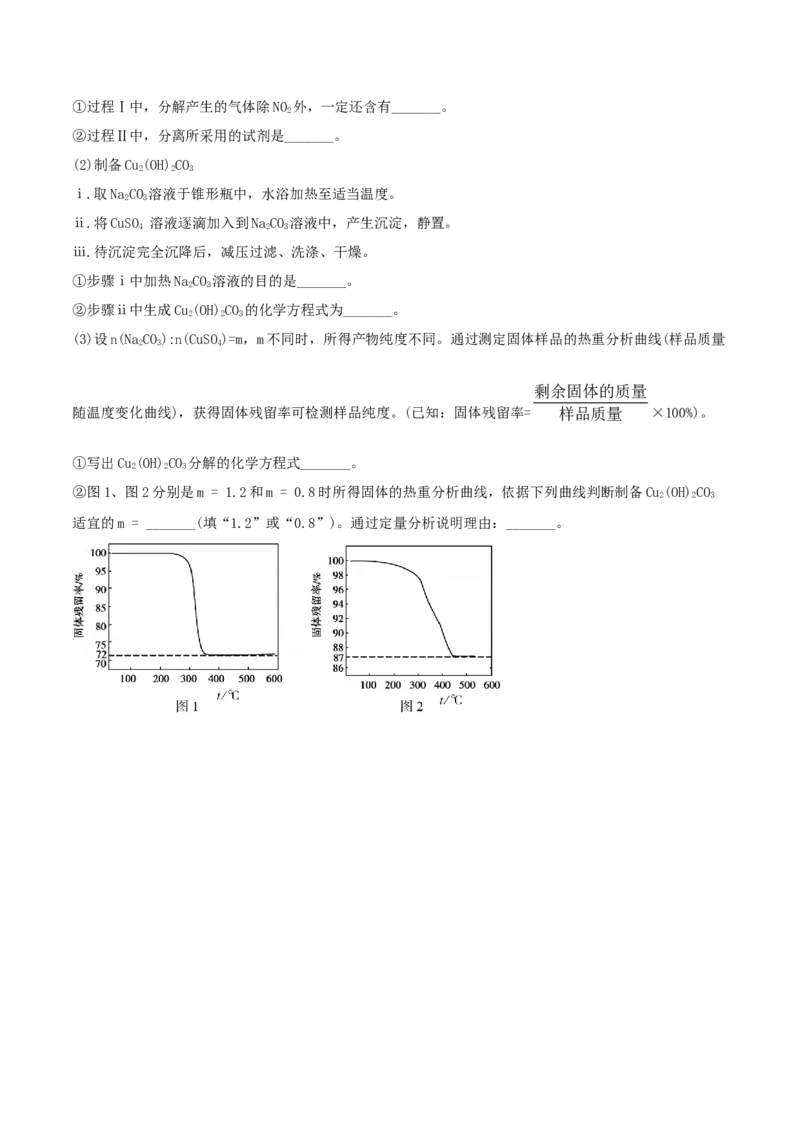
(3)设n(NaCO):n(CuSO)=m,m不同时,所得产物纯度不同。通过测定固体样品的热重分析曲线(样品质量
2 3 4
剩余固体的质量
随温度变化曲线),获得固体残留率可检测样品纯度。(已知:固体残留率= 样品质量 ×100%)。
①写出Cu(OH)CO 分解的化学方程式_______。
2 2 3
②图1、图2分别是m = 1.2和m = 0.8时所得固体的热重分析曲线,依据下列曲线判断制备Cu(OH)CO
2 2 3
适宜的m = _______(填“1.2”或“0.8”)。通过定量分析说明理由:_______。