文档内容
第二章 化学计量及其应用
测试卷
时间:75分钟 分值:100分
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O16 Na 23 Al 27 P 31 S 32 Cl 35.5 K 39 Ca
40 Fe 56 Cu 64 Br 80 Ag 108 Ba 137
一、选择题(每小题只有一个正确选项,共15×3分)
1.(2024·浙江省镇海中学期中)摩尔来源于拉丁文moles,原意为大量、堆积,是在1971年10月有41
个国家参加的第14届国际计量大会决定增加的国际单位制(SI)的第七个基本单位。下列对于“摩尔”的理
解正确的是( )
A.1mol任何物质所含有的分子数都相同
B.摩尔是物质的量的单位,简称摩,符号为mol
C.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
D.2H既可以表示2个氢原子又可以表示2mol氢原子
2.(2024·四川省成都市高三模拟)N 表示阿伏加德罗常数。下列说法正确的是( )
A
A.2g氘化锂( )中含有的中子数为2 N
A
B.25℃时,1L0.1 mol·L-1 NH Fe(SO ) 溶液中阳离子数小于0.2 N
4 4 2 A
C.28gC H 和C H 的混合气体完全燃烧生成CO 的分子数介于2 ~3
2 4 3 6 2
D.标准状况下,22.4L氖气含有的原子数约为N
A
3.(2024·黑龙江省哈尔滨市三模)设N 为阿伏加德罗常数的值。下列说法正确的是( )
A
A.等物质的量的C H 和C HO完全燃烧,消耗O 分子数目均为3N
2 4 2 6 2 A
B.NaO 与CO 反应生成标准状况下O44.8L,转移电子数目为4N
2 2 2 2 A
C.25℃,1LpH=12的Ba(OH) 溶液中含有OH-数目为0.02N
2 A
D.标准状况下,22.4 mLCHCl 中含有碳原子数目为10-3N
2 2 A
4.(2024·天津市部分区二模)设N 为阿伏加德罗常数的值,下列说法正确的是( )
A
A.7.1g Cl 与足量铁粉反应转移的电子数为0.2N
2 A
B.1molL-1 CaCl 溶液中含离子总数为3N
2 A
C.标准状况下,2.24L CO 分子中含有的σ键的数目为0.4N
2 A
D.44g CHCHO中sp3杂化的碳原子数目为2N
3 A
5.(2024•重庆市高三高考适应性考试)已知反应:P+2I +8H O=2PH I+2H PO +2HI,N 为阿伏加德罗
4 2 2 4 3 4 A
常数的值,若消耗36gHO,下列叙述的错误的是( )
2
A.转移电子数为2.5N
A
B.断裂的 键数为1.5 N
A
C.还原产物比氧化产物多0.5mol
D.将生成物配制成1L水溶液,溶液中c(H+)=2mol/L6.(2024•湖南省长沙市高三一轮复习总结性考试)科学家发现某些生物酶能将海洋中的NO 转化为
2
N,该过程的总反应为NaNO + NH Cl =NaCl+N ↑+2H O。设N 为阿伏加德罗常数的值,下列说法正确的
2 2 4 2 2 A
是( )
A.1L1.5mol·L-1NH Cl溶液中含NH +的数目为1.5 N
4 4 A
B.标准状况下,22.4LN 中含π键的数目为2N
2 A
C.生成18gHO转移电子数目为3 N
2 A
D.生物酶将NO 转化为N 的过程叫作氮的固定
2 2
7.(2024•广东省普通高中学科综合素养评价名校联考)N 代表阿伏加德罗常数的值,下列说法正确的
A
是( )
A.22.4L甲醛所含σ键数为4N
A
B.0.1mol·L-1的MgCl 溶液含Cl-的数目为0.1N
2 A
C.82g Na 18O 与足量水完全反应,电子转移数为2N
2 2 A
D.0.1mol的C HOH所含氢原子数为0.6N
2 5 A
8.(2024·辽宁省部分重点中学协作体高三模拟)三氟化氮(NF )在潮湿的环境中能发生反应:
3
3NF +5H O=2NO+HNO +9HF,N 代表阿伏加德罗常数的值。下列说法正确的是( )
3 2 3 A
A.生成22.4LNO,转移电子数为N
A
B.1molH O含有的中子数为10N
2 A
C.1mol/L的HNO 溶液含NO -离子数为N
3 3 A
D.反应中若有1molNF 被氧化,则理论上需要分子数为2N 的氧化剂
3 A
9.(2024•广东省两阳中学月考)设N 为阿伏加德罗常数,现向10mL0.2mol·L-1的KMnO 溶液中通入
A 4
一定量的SO ,使溶液的紫色恰好褪尽,若反应前后溶液的体积不变,则下列说法不正确的是( )
2
A.通入的SO 在标准状况下的体积为
2
B.反应后溶液中SO 2-的数目为0.005 N
4 A
C.该反应中转移的电子数为0.02 N
A
D.反应后的溶液中c(H+)=0.4mol·L-1
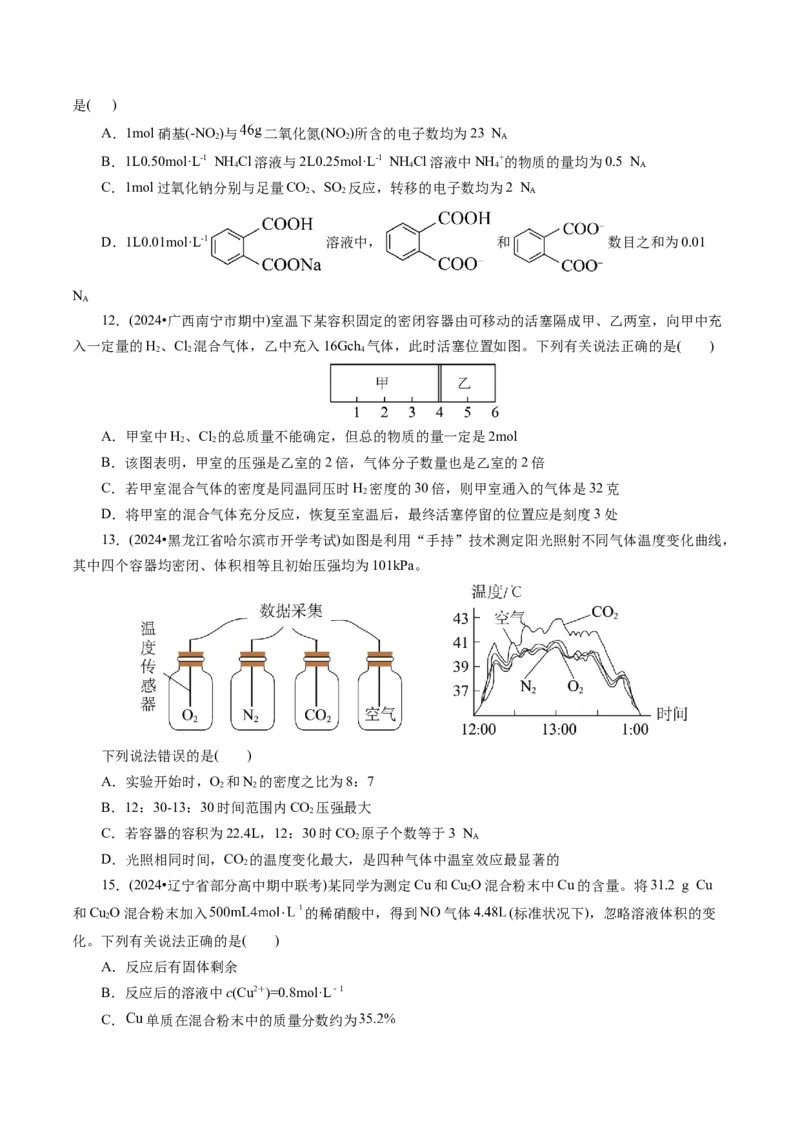
10.(2024•安徽省合肥市期中)沸石分子筛选择性催化还原NO的循环过程如图所示。下列说法正确的
是( )
A.步骤一中O 与HO的物质的量之比为1∶2
2 2
B.反应过程中催化剂Cu+未参与电子得失
C.每生成22.4LN 理论上消耗0.25mol O
2 2
D.所有步骤均有氧化还原反应发生
11.(2024•·广东省广州市天河外国语学校高三月考)设N 表示阿伏加德罗常数的值,下列说法正确的
A是( )
A.1mol硝基(-NO )与 二氧化氮(NO )所含的电子数均为23 N
2 2 A
B.1L0.50mol·L-1 NH Cl溶液与2L0.25mol·L-1 NH Cl溶液中NH +的物质的量均为0.5 N
4 4 4 A
C.1mol过氧化钠分别与足量CO、SO 反应,转移的电子数均为2 N
2 2 A
D.1L0.01mol·L-1 溶液中, 和 数目之和为0.01
N
A
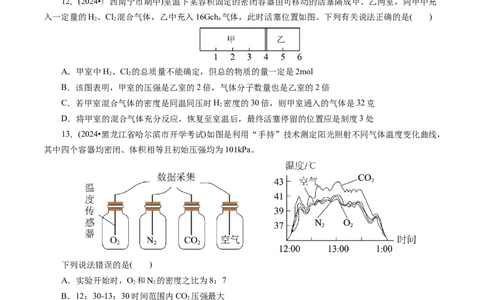
12.(2024•广西南宁市期中)室温下某容积固定的密闭容器由可移动的活塞隔成甲、乙两室,向甲中充
入一定量的H、Cl 混合气体,乙中充入16Gch 气体,此时活塞位置如图。下列有关说法正确的是( )
2 2 4
A.甲室中H、Cl 的总质量不能确定,但总的物质的量一定是2mol
2 2
B.该图表明,甲室的压强是乙室的2倍,气体分子数量也是乙室的2倍
C.若甲室混合气体的密度是同温同压时H 密度的30倍,则甲室通入的气体是32克
2
D.将甲室的混合气体充分反应,恢复至室温后,最终活塞停留的位置应是刻度3处
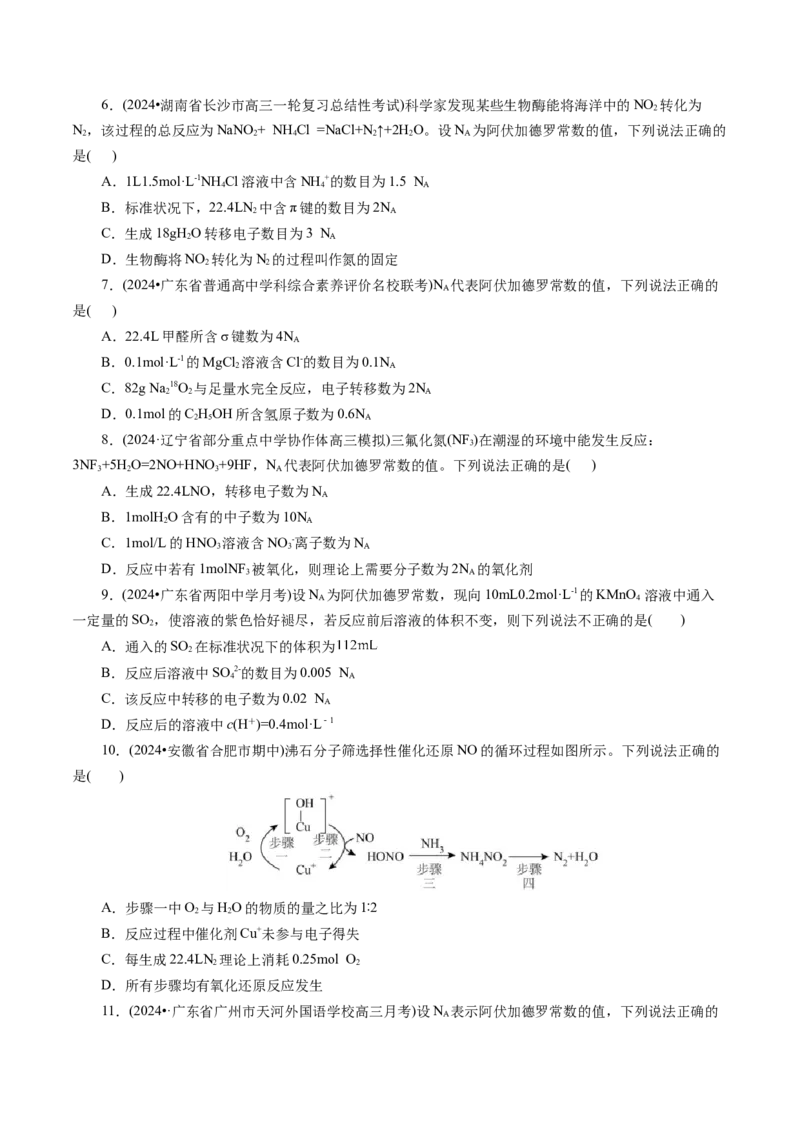
13.(2024•黑龙江省哈尔滨市开学考试)如图是利用“手持”技术测定阳光照射不同气体温度变化曲线,
其中四个容器均密闭、体积相等且初始压强均为101kPa。
下列说法错误的是( )
A.实验开始时,O 和N 的密度之比为8:7
2 2
B.12:30-13:30时间范围内CO 压强最大
2
C.若容器的容积为22.4L,12:30时CO 原子个数等于3 N
2 A
D.光照相同时间,CO 的温度变化最大,是四种气体中温室效应最显著的
2
15.(2024•辽宁省部分高中期中联考)某同学为测定Cu和Cu O混合粉末中Cu的含量。将31.2 g Cu
2
和Cu O混合粉末加入 的稀硝酸中,得到 气体 (标准状况下),忽略溶液体积的变
2
化。下列有关说法正确的是( )
A.反应后有固体剩余
B.反应后的溶液中c(Cu2+)=0.8mol·L-1
C. 单质在混合粉末中的质量分数约为D.在反应后的溶液中加入足量铁粉,可畳换出
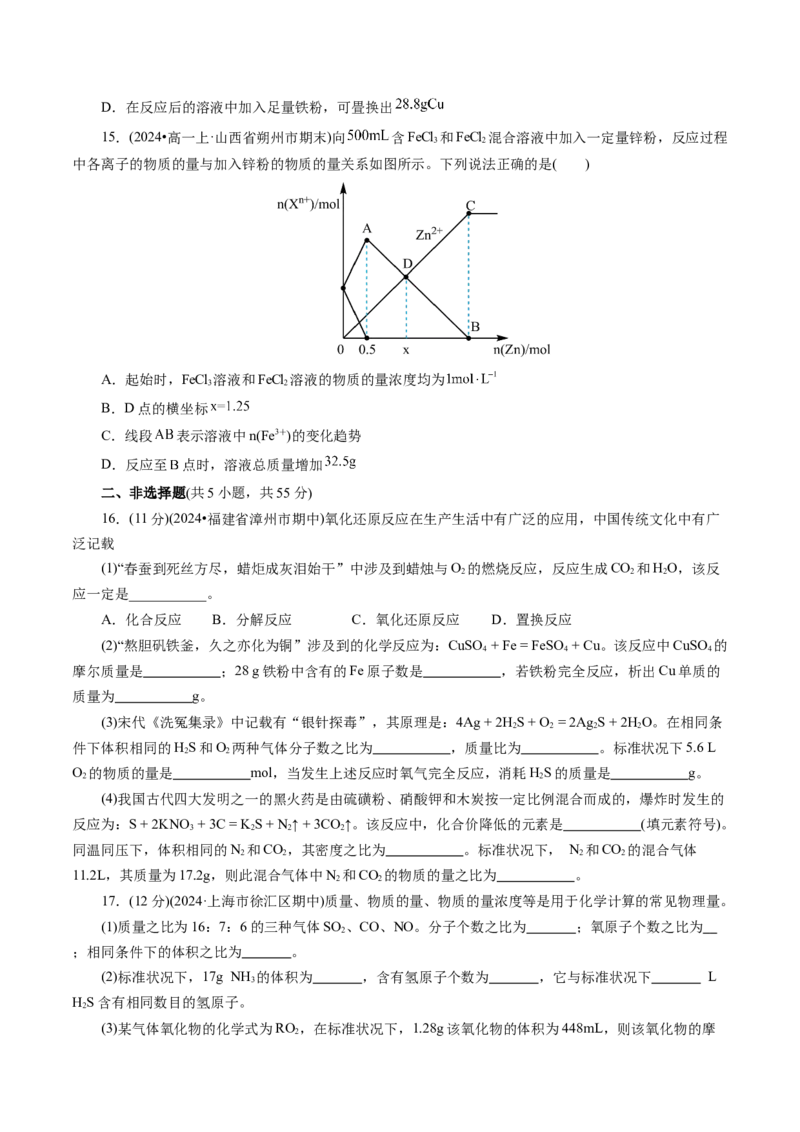
15.(2024•高一上·山西省朔州市期末)向 含FeCl 和FeCl 混合溶液中加入一定量锌粉,反应过程
3 2
中各离子的物质的量与加入锌粉的物质的量关系如图所示。下列说法正确的是( )
A.起始时,FeCl 溶液和FeCl 溶液的物质的量浓度均为
3 2
B.D点的横坐标
C.线段 表示溶液中n(Fe3+)的变化趋势
D.反应至 点时,溶液总质量增加
二、非选择题(共5小题,共55分)
16.(11分)(2024•福建省漳州市期中)氧化还原反应在生产生活中有广泛的应用,中国传统文化中有广
泛记载
(1)“春蚕到死丝方尽,蜡炬成灰泪始干”中涉及到蜡烛与O 的燃烧反应,反应生成CO 和HO,该反
2 2 2
应一定是___________。
A.化合反应 B.分解反应 C.氧化还原反应 D.置换反应
(2)“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:CuSO + Fe = FeSO + Cu。该反应中CuSO 的
4 4 4
摩尔质量是 ;28 g铁粉中含有的Fe原子数是 ,若铁粉完全反应,析出Cu单质的
质量为 g。
(3)宋代《洗冤集录》中记载有“银针探毒”,其原理是:4Ag + 2HS + O = 2Ag S + 2H O。在相同条
2 2 2 2
件下体积相同的HS和O 两种气体分子数之比为 ,质量比为 。标准状况下5.6 L
2 2
O 的物质的量是 mol,当发生上述反应时氧气完全反应,消耗HS的质量是 g。
2 2
(4)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的
反应为:S + 2KNO + 3C = K S + N ↑ + 3CO ↑。该反应中,化合价降低的元素是 (填元素符号)。
3 2 2 2
同温同压下,体积相同的N 和CO,其密度之比为 。标准状况下, N 和CO 的混合气体
2 2 2 2
11.2L,其质量为17.2g,则此混合气体中N 和CO 的物质的量之比为 。
2 2
17.(12分)(2024·上海市徐汇区期中)质量、物质的量、物质的量浓度等是用于化学计算的常见物理量。
(1)质量之比为16:7:6的三种气体SO 、CO、NO。分子个数之比为 ;氧原子个数之比为
2
;相同条件下的体积之比为 。
(2)标准状况下,17g NH 的体积为 ,含有氢原子个数为 ,它与标准状况下 L
3
HS含有相同数目的氢原子。
2
(3)某气体氧化物的化学式为RO,在标准状况下,1.28g该氧化物的体积为448mL,则该氧化物的摩
2尔质量为 ,R的相对原子质量为 。
(4)同温同压下,A 气体与B 气体等体积化合,生成AB 气体,已知反应前后气体的密度不变,则
2 2 x y
AB 的分子式为 。
x y
(5)在t℃时将a g NH 完全溶于水得到V mL溶液,该溶液的密度为 ;质量分数为w,
3
物质的量浓度为c mol·L-1。下列计算结果正确的是 。
A.溶质的质量分数
B.溶质的物质的量浓度
C.溶液密度 可表示为
D.上述溶液中再加入V mL水,所得溶液溶质的质量分数小于0.5w
(6)将a L Al (SO ) 和(NH )SO 的混合溶液分成两等份,一份加入b mol BaCl 溶液使溶液中的SO 2-刚
2 4 3 4 2 4 2 4
好完全沉定,另一份加入足量NaOH溶液并加热可得到c molNH ,则原溶液中Al3+的物质的量浓度为
3
。
(7)将0.24g Mg和0.27g Al的混合物投入到100mL 1mol/L的盐酸中,充分反应后固体完全溶解。向所
得溶液中加入2mol/L的NaOH溶液,恰好使金属离子全部沉淀完全,需要NaOH溶液的体积为
mL。
18.(14分)(2024•河南省信阳市期中)我国将力争2060年前实现碳中和,CO 的捕捉是减少碳排放的措
2
施之一。
I.一种利用 溶液捕捉回收CO 的过程如图所示。
2
(1)捕捉室中 溶液常喷成雾状,优点是 。
(2)整个过程中可以循环利用的物质是 。
II.实验室模拟捕捉回收CO,配制 溶液。
2
(3)配制溶液需要的玻璃仪器是烧杯、玻璃棒和。根据计算用托盘天平称量 固体 __
g。
(4)配制操作可分解成如下几步,以下正确的操作顺序是 →D→ →装瓶贴签。
A.向容量瓶中注入少量蒸馏水,检查是否漏水
B.用少量蒸馏水洗涤烧杯及玻璃棒 次,将洗涤液注入容量瓶后轻摇几下
C.将已冷却的溶液注入容量瓶中D.根据计算,称取取一定量的 固体
E、向盛有 固体的烧杯中加水,用玻璃棒搅拌溶解
F、盖上容量瓶塞了,摇匀
G、用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H、继续往容量瓶中小心地加蒸馏水,使液面接近刻度线 处
(5)配制过程中,会造成所配制NaOH溶液的物质的量浓度偏大的是
A.称量所用的砝码生锈
B.转移前,容量瓶内有蒸馏水
C.未冷至室温就转移定容
D.定容时仰视刻度线
E.定容时水加多用胶头滴管吸出
F.称量 时间过长
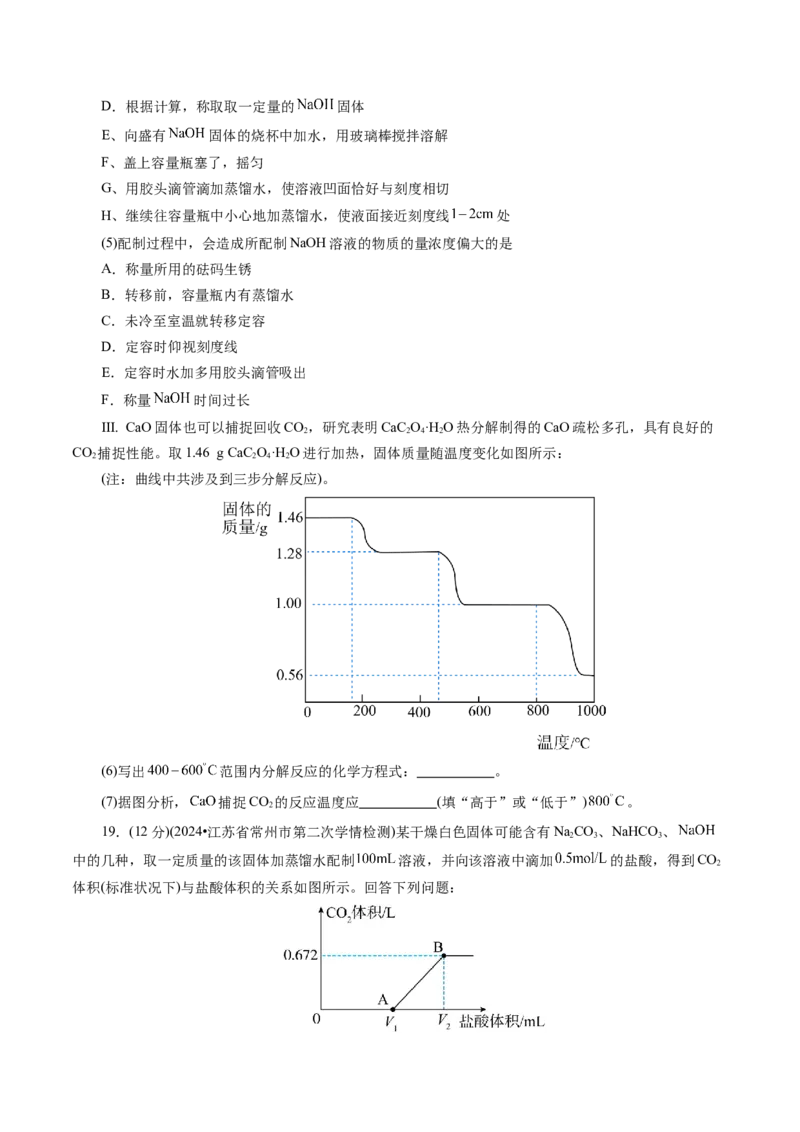
III. CaO固体也可以捕捉回收CO,研究表明CaC O·H O热分解制得的CaO疏松多孔,具有良好的
2 2 4 2
CO 捕捉性能。取1.46 g CaC O·H O进行加热,固体质量随温度变化如图所示:
2 2 4 2
(注:曲线中共涉及到三步分解反应)。
(6)写出 范围内分解反应的化学方程式: 。
(7)据图分析, 捕捉CO 的反应温度应 (填“高于”或“低于”) 。
2
19.(12分)(2024•江苏省常州市第二次学情检测)某干燥白色固体可能含有NaCO、NaHCO 、
2 3 3
中的几种,取一定质量的该固体加蒸馏水配制 溶液,并向该溶液中滴加 的盐酸,得到CO
2
体积(标准状况下)与盐酸体积的关系如图所示。回答下列问题:(1)产生的CO 的物质的量为 mol, 段反应的离子方程式为 。
2
(2)若白色固体由0.02mol Na CO 和xmol NaHCO 组成,则V= ,V= 。
2 3 3 1 2
(3)若白色固体由NaHCO 和 组成,2V= V,则NaHCO 与 溶于水后发生反应的离子方
3 1 2 3
程式为 , 。
(4)若白色固体只由 和NaCO 组成,且V=100,V=160,则 ,原
2 3 1 2
溶液中的c(Na+)= 。
(5)另取某NaCO 和NaHCO 组成的混合物样品,称取3份该样品溶于水后分别逐滴加入相同浓度盐酸
2 3 3
,充分反应,产生CO 的体积如下表(标准状况下,且不考虑CO 在水中的溶解):
2 2
实验序号 ① ② ③
100.0 100.0 100.0
3.80 7.60 11.40
896 1344 896
样品中 ,盐酸的 。
20.(6分)(2024•浙江省杭州八县市期末)某研究性学习小组,进行甲、乙、丙三组实验:各取
同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
实验序号 甲 乙 丙
合金质量(g) 1.008 1.260 1.512
生成气体体积(mL)(标况) 1075.2 1344 1344
请回答以下问题:
(1)计算丙中产生气体的物质的量为 mol;
(2)实验中所用合金粉末中镁、铝的物质的量之比为 ;
(3)实验乙结束后的混合体系中加入一定量的NOH溶液,充分反应,得到固体M。如果固体M的质量
不再减少,消耗NaOH的质量至少为 g。