文档内容
考点 24 化学反应的方向
分析近年各地高考试题,主要考查:认识自然界中发生的一些自发过程,加强从物质的微观层面理
解反应过程中能量和混乱度变化的能力;了解焓变与熵变的含义,理解焓变、熵变与反应方向的关系;能
综合运用焓变与熵变判断反应进行的方向。
预计2023年的高考仍然把化学反应进行方向判断融入反应原理综合题中。
一、自发过程与自发反应
二、化学反应进行方向的判据
自发过程与自发反应
1.自发过程:在一定条件下,不需借助外力就能自发进行的过程。其特点是高能状态 → 低能状态
(对外做功或释放热量);有序 → 无序(无序体系更加稳定)。如:高山流水,自由落体,冰雪融化。
2.自发反应:在给定的条件下,可以自发进行到显著程度的化学反应。如:钢铁生锈。
3.特征:具有方向性,即过程的某个方向在一定条件下自发进行,而该过程逆方向在该条件下肯定
不能自发进行。
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)所有自发进行的化学反应都是放热反应( )
(2)自发反应在任何条件下都能发生( )
(3)同一物质的固,液、气三种状态的熵值相同( )
(4)非自发过程在一定条件下可能变成自发过程( )
(5)需要加热才能够进行的过程肯定不是自发过程( )
答案:(1)× (2) × (3)× (4) √ (5)×
【典例】例1 下列过程是非自发的是( )
A.水由高处向低处流 B.氯气和溴化钾溶液的反应
C.铁在潮湿空气中生锈 D.室温下水结成冰
【答案】D
【解析】A项,水由高处向低处流,是自发进行的过程,故A不选;B项,氯气的氧化性比溴强,氯
气能够与KBr溶液发生置换反应,属于自发进行的过程,故B不选;C项,铁生锈为自发进行的氧化还原
反应,反应放热,常温下可自发进行,故C不选;D项,室温下冰会自发的融化,室温下水结成冰不是自
发进行的过程,故D选;故选D。
例2 下列不属于自发进行的变化是( )
A.红墨水加到清水使整杯水变红 B.冰在室温下融化成水
C.电解饱和食盐水 D.铁器在潮湿的空气中生锈
【答案】C
【解析】A项,扩散现象,是熵增加的自发过程,A不符合题意;B项,冰的熔点为0℃,水常温是液
体,冰在室温下融化成水,是熵增加的自发过程,B不符合题意;C项,电解饱和食盐水,是在外电场的
作用下强制发生的氧化还原反应,不是自发过程,C符合题意;D项,铁在潮湿的空气中生锈是发生了自
发的氧化还原反应,属于电化学腐蚀,是自发进行的化学过程,D不符合题意;故选C。
【对点提升】
对点1 下列说法中正确的是( )
A.吸热反应反应一定不能发生反应
B.某吸热反应能自发进行,因此该反应是熵增反应
C.需要加热才能发生的反应,一定是吸热反应
D.催化剂可以改变反应进行的方向
【答案】B
【解析】A项,吸热反应在一定条件下能发生反应,例如加热时碳和二氧化碳可以反应生成CO,A错
误;B项,某吸热反应能自发进行,即ΔH>0,根据ΔG=ΔH-TΔS<0可知该反应一定是熵增反应,B正
确;C项,需要加热才能发生的反应,不一定是吸热反应,例如碳燃烧等,C错误;D项,催化剂可以改
变反应速率,不能改变反应进行的方向,D错误;故选B。
对点2 知道了某过程有自发性之后,则( )
A.可判断出过程的方向 B.可确定过程是否一定会发生
C.可预测过程发生完成的快慢 D.可判断过程的热效应
【答案】A
【解析】判断某反应是否自发,只是判断反应的方向,与是否会发生、反应的快慢、反应的热效应无关。
【巧学妙记】
(1)自发过程或反应具有方向性,即过程或反应的某个方向在一定条件下自发进行,而该过程或反应
的逆方向在该条件下肯定不能自发进行。
(2)能够自发进行的过程或反应在常温下不一定能够发生,自发性只能用于判断过程或反应的方向,
不能确定过程或反应是否一定会发生和发生的速率。
化学反应进行方向的判据
1.焓判据
(1)放热过程中体系能量降低,ΔH <0 ,具有自发的倾向。
(2)实验发现,大多数放热反应是可以自发进行的。
例如:Zn(s) +CuSO (aq) =ZnSO (aq) +Cu(s) ΔH =-216.8kJ/mol
4 4
(3)有些吸热反应也可以自发进行,如Ba(OH) ·8H O晶体与NH Cl晶体的反应是吸热的,但是这个反
2 2 4
应却是可以自发进行的,故不能只根据放热或者吸热来判断化学反应的方向,焓变只是影响反应方向的一
种因素。
2.熵判据
(1)熵的定义
描述体系混乱程度的物理量,一般用S表示。熵值越大,体系的混乱度越大 。
(2)熵的大小
同种物质的熵值与其存在状态有关, S(g)>S(l)> S(s)。
(3)熵判据
体系的混乱度(即熵值)增加, ΔS>0,反应有自发的倾向。
有些熵减的过程也能自发进行,如乙烯聚合为聚乙烯的反应,故熵变只是影响反应方向的一种因素。
3.复合判据(自由能ΔG)
在等温、等压条件下的封闭体系中(不考虑体积变化做功以外的其他功),自由能的变化(符号为ΔG,
单位为kJ/mol) 综合反映了体系的焓变和熵变对自发过程的影响:ΔG = ΔH-TΔS。这时,化学反应总是向
着自由能减小的方向进行,直到体系达到平衡。即:
当ΔG <0时,反应能自发进行;
当ΔG =0时,反应处于平衡状态;
当ΔG >0时,反应不能自发进行。
情况 焓变 熵变 自由能变化 反应能否自发进行① ΔH<0 ΔS>0 ΔG<0 能
② ΔH>0 ΔS<0 ΔG>0 不能
③ ΔH<0 ΔS<0 无法判断 无法判断
④ ΔH>0 ΔS>0 无法判断 无法判断
【小试牛刀】
请判断下列说法的正误(正确的打“√”,错误的打“×”)
(1)ΔH<0,ΔS>0的反应在温度低时不能自发进行( )
(2)一定温度下,反应MgCl (l) Mg(l)+Cl(g)的ΔH>0、ΔS>0( )
2 2
(3)反应NH (g)+HCl(g)===NHCl(s)在室温下可自发进行,则该反应的ΔH<0( )
3 4
(4)2NO(g)+2CO(g)===N (g)+2CO(g)在常温下能自发进行,则该反应的ΔH>0( )
2 2
(5)SO (g)===S(g)+O(g) ΔH>0,ΔS>0,该反应不能自发进行( )
2 2
(6)SO (g)+2HS(g)===3S(s)+2HO(l) ΔH<0,低温下能自发进行( )
2 2 2
(7)常温下,反应C(s)+CO(g)===2CO(g)不能自发进行,则该反应的ΔH>0( )
2
(8)在其他外界条件不变的情况下,使用催化剂可以改变化学反应进行的方向( )
(9)放热过程有自发进行的倾向性,但并不一定能自发进行,吸热过程没有自发进行的倾向性,但在
一定条件下也可自发进行( )
(10)NH HCO (g)===NH(g)+HO(g)+CO(g) ΔH=185.57 kJ·mol-1能自发进行,原因是体系有自发
4 3 3 2 2
地向混乱度增加的方向转变的倾向( )
答案:(1)× (2)√ (3)√ (4)× (5)× (6)√ (7)√ (8)× (9)√ (10)√
【典例】
例1 (2021•浙江6月选考)相同温度和压强下,关于物质熵的大小比较,合理的是( )
A.1molCH(g)<1molH(g) B.1molHO(g)<2molHO(g)
4 2 2 2
C.1molHO(s)>1molHO(l) D.1molC(s,金刚石)>1molC(s,石黑)
2 2
【答案】B
【解析】A项,CH(g)和H(g)物质的量相同,且均为气态,CH(g)含有的原子总数多,CH(g)的摩尔
4 2 4 4
质量大,所以熵值1molCH (g)>1molH (g),A错误;B项,相同状态的相同物质,物质的量越大,熵值越
4 2
大,所以熵值1molH O(g)<2molH O(g),B正确;C项,等量的同物质,熵值关系为:S(g)>S(l)>S(s),
2 2
所以熵值1molH O(s)<1molH O(l),C错误;D项,从金刚石和石墨的结构组成上来看,金刚石的微观结
2 2
构更有序,熵值更低,所以熵值1molC(s,金刚石)<1molC(s,石黑),D错误;故选B。
例2 下列反应在任何温度下均能自发进行的是( )
A.2N(g)+O(g)===2N O(g) ΔH=163 kJ·mol-1
2 2 2
B.Ag(s)+Cl(g)===AgCl(s) ΔH=-127 kJ·mol-1
2
C.HgO(s)===Hg(l)+O(g) ΔH=91 kJ·mol-1
2D.HO(l)===O(g)+HO(l) ΔH=-98 kJ·mol-1
2 2 2 2
【答案】D
【解析】对于A项,ΔH>0,ΔS<0,在任何温度下,ΔH-TΔS>0,即任何温度下反应都不能自发进行;
对于B项,ΔH<0,ΔS<0,在较低温度下,ΔH-TΔS<0,即低温下反应能自发进行;对于C项,ΔH>0,
ΔS>0,若使反应自发进行,即ΔH-TΔS<0,必须升高温度,即反应只有在较高温度时能自发进行;对于
D项,ΔH<0,ΔS>0,在任何温度下,ΔH-TΔS<0,即在任何温度下反应均能自发进行。
【对点提升】
对点1 已知吸热反应2CO(g)===2C(s)+O(g),设ΔH 和ΔS不随温度而变,下列说法中正确的是(
2
)
A.低温下能自发进行 B.高温下能自发进行
C.任何温度下都能自发进行 D.任何温度下都不能自发进行
【答案】D
【解析】已知反应2CO(g)===2C(s)+O(g)的ΔH>0,ΔS<0,所以ΔH-TΔS>0,反应任何温度下都
2
是不能自发进行,D项正确。
对点2 下列对化学反应预测不正确的是( )
选项 化学方程式 已知条件 预测
A W(s)+G(g)= 2Q(g) 任何温度都自发进行 ΔH<0
B 4M(s)+N(g)+2W(l)= 4Q(s) 常温下自发进行 ΔH>0
B 3C(s)+CaO(s)= CaC (s)+CO(g) 常温下不能自发进行 ΔH>0
2
D 2NO(g)+O(g)===2NO (g) 常温下能够自发进行 ΔH<0
2 2
【答案】B
【解析】A项,W(s)+G(g)═2Q(g)反应为气体的化学计量数增大的反应,△S>0,△H<0,反应能够
自发进行,故A正确;B项,4M(s)+N(g)+2W(l)═4Q(s)为气体的化学计量数减小的反应,△S<0,当△H
>0时,△H-T S>0,一定不能自发进行,故B错误;C项,3C(s)+CaO(s)= CaC (s)+CO(g) 的∆S>0,
2
在常温下不能自△发进行,则表明反应吸热,即说明该反应的ΔH>0,C正确;D项,常温下,2NO(g)+
O(g)===2NO (g) 的∆S<0,能够自发进行,则表明反应放热,即该反应的ΔH<0,D正确。故选B。
2 2
【巧学妙记】
焓变、熵变和温度对化学反应方向的影响
ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下均自发进行+ - 永远是正值 在任何温度下均非自发进行
+ + 低温为正,高温为负 低温时非自发,高温时自发
- - 低温为负,高温为正 低温时自发,高温时非自发
1.某化学反应在较低温度下自发,较高温度下非自发.有关该反应的下列说法正确的是( )
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0 C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
【答案】D
【解析】A项,△H>0,△S>0,要使△H-T S<0,T值应较大,即应该在高温下才能自发进行,
故A错误;B项,△H>0,△S<0,△H-T S>0,△任何温度下都不能自发进行,故B错误;C项,△H<
0,△S>0,△H-T S<0一定成立,任何温△度下都能自发进行,故C错误;D项,△H<0,△S<0,要
使△H-T S<0,T△值应较小,即应该在低温下才能自发进行,故D正确;故选D。
2.下△列反应△S>0的是( )
A.HCl(g)+NH (g)=NH Cl(s) B.2CO(g)=2C(s)+O (g)
3 4 2
C.N(g)+3H(g)=2NH (g) D.CaCO (s)=CaO(s)+CO (g)
2 2 3 3 2
【答案】D
【解析】A项,该反应为气体系数之和减小的反应,ΔS<0,A不符合题意;B项,该反应为气体系数
之和减小的反应,ΔS<0,B不符合题意;C项,该反应为气体系数之和减小的反应,ΔS<0,C不符合题
意;D项,该反应为气体系数之和增大的反应,ΔS>0,D符合题意;故选D。
3.以下判断正确的是( )
A.C(s)+CO(g)=2CO(g) H>0,该反应常温下不能自发
2
B.2Mg(s)+O 2 (g)=2MgO(s) △ H<0,该反应高温才能自发
△C.自发反应的熵一定增大,非自发反应的熵一定减小
D.放热反应都可以自发进行,而吸热反应不能自发进行
【答案】A
【解析】A项,在高温下△G= H-T S<0反应能进行,△H>0,该反应常温下不能自发,故A正确;
B项,△G= H-T S<0反应能进行△,由于△△H<0,则该反应在常温就能自发进行,故B错误;C项,自
发进行的反应△熵值△不一定增大,化学反应的方向由焓变和熵变共同决定,非自发反应的熵不一定减小,故
C错误;D项,不能根据焓变判断反应的自发性,放热反应不一定都是自发进行的,吸热反应也可能是自
发进行,如碳酸氢铵的分解,故D错误;故选A。
4.下列说法正确的是( )
A.反应N(g)+3H(g) 2NH (g)的ΔH<0,ΔS>0
2 2 3
B.反应2CO+2NO===N +2CO 在常温下能自发进行,则反应的ΔH>0,ΔS<0
2 2
C.反应TiO(s)+2Cl(g)===TiCl (g)+O(g) ΔH>0能自发进行,其原因是ΔS>0
2 2 4 2
D.反应4Fe(s)+3O(g)===2Fe O(s)常温下可自发进行,该反应为吸热反应
2 2 3
【答案】C
【解析】该反应的正反应为气体分子数减少的反应,ΔS<0,A项错误;从反应方程式中气体物质化学
计量系数来看,物质的量在减小,即熵减小,但反应能自发,则该反应是放热反应,ΔH<0,B项错误;一
个吸热反应如果能自发进行,则该反应一定是熵增大反应,C项正确;该反应的气体分子数减小,即熵减
小,但反应能自发,说明反应一定为放热反应,D项错误。
5.对于反应A(s)+3B(g) C(g)+D(g) ΔH<0,下列说法正确是( )
A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.该反应△S>0,△H<0,在任何条件下能自发进行
C.恒温恒容条件下,混合气体密度不变达到化学平衡状态
D.达到平衡状态后,若增加A的量,平衡向正反应方向移动
【答案】C
【解析】A项,加入催化剂,改变了反应的途径,但不能改变反应物、生成物的能量,因此反应的
△H不会随之改变,A错误;B项,该反应的正反应是气体体积减小的放热反应,△S<0,△H<0,只有
在△H-T S<0时反应才能够自发进行,B错误;C项,反应在恒容密闭容器中进行,气体的质量反应前后
会发生变△化。在恒温恒容条件下,若混合气体密度不变,说明气体的质量不再发生变化,反应就达到化学
平衡状态,C正确;D项,A为固体,反应达到平衡状态后,若增加A的量,化学平衡不发生移动,D错
误;故选C。
6.对于化学反应能否自发进行,下列说法中错误的是( )A.非自发过程在一定条件下可能变成自发过程
B.若△H>0,△S<0,任何温度下都不能自发进行
C.若△H<0,△S>0,任何温度下都能自发进行
D.需要加热才能够进行的过程肯定不是自发过程
【答案】D
【解析】A项,非自发过程在一定条件下可能变成自发过程,如铜和稀硫酸在电解条件下可发生,故
A正确;B项,若△H>0,△S<0,则△H-T S>0任何温度下都不能自发进行,故B正确;C项,若△H
<0,△S>0,则△H-T S<0任何温度下都能△自发进行,故C正确;D项,需要加热才能够进行的过程可能
是自发过程,如碳酸钙△高温分解,故D错误;故选D。
7.下列关于化学反应方向及其判据的说法中正确的是( )
A.1molSO 在不同状态时的熵值:S[SO (s)]>S[SO (1)]>S[SO (g)]
3 3 3 3
B.常温下,反应C(s)+CO(g)=2CO(g)不能自发进行,则该反应的ΔH>0
2
C.放热反应都可以自发进行,而吸热反应不能自发进行
D.2KClO(s)=2KCl(s)+3CO (g) ΔH>0能否自发进行与温度无关
3 2
【答案】B
【解析】A项,物质聚集状态不同熵值不同,气体S> 液体S> 固体S,1molSO 在不同状态时的熵值:
3
S[SO (s)]0,常温不能自发,说明高温时△G= H-T• S<0,说明则该反应的ΔH>0,故B正确;C项,反应的
自发性由焓变和熵变共同决定,当△G=△H-T•△S<0时反应能自发进行,ΔG>0时反应不能自发进行,焓
变小于零的反应,ΔH<0,若ΔS<0<0,△高温△下可以ΔG>0,反应不能自发进行,熵变大于零的反应,
ΔS>0,若ΔH>0 ,高温下可以ΔG<0 时反应可自发进行,故C错误;D项,ΔH>0、ΔS>0 ,由△G= H-
T• S<0 的反应可自发进行,可知能否自发进行与温度有关,故D错误;故选B。 △
△ 8.下列关于判断过程的方向的说法正确的是( )
A.所有自发进行的化学反应都是放热反应
B.自发反应在任何条件下都能发生
C.由焓判据和熵判据组合而成的复合判据,将更适合于所有的过程
D.同一物质的固,液、气三种状态的熵值相同
【答案】C
【解析】A项,反应能否自发进行取决于焓变和熵变的复合判据,对于吸热反应,在一定温度下也能
进行,故A错误;B项,反应是否自发进行,由熵变、焓变、温度共同决定,故B错误;C项,△G= H-
T• S<0时,反应能自发进行,适合于所有的过程,所以由能量判据和熵判据组合而成的复合判据,将△更
△适合于所有的过程,故C正确;D项,熵值表示混乱度的大小,混乱度越大,熵值越大,同一物质的固态、
液态、气态混乱度依次增大,故D错误;故选C。
9.已知ΔG=ΔH-TΔS (设ΔH、ΔS不随温度而变化),当ΔG<0时反应能自发进行。关于反应
CaSO(s)=CaO(g)+SO (g) ΔH>0,ΔS>0。下列说法正确的是( )
4 3
A.低温下能自发进行 B.任意湿度下都不能自发进行
C.高温下能自发进行 D.任意温度下都能自发进行
【答案】C
【解析】反应CaSO(s)=CaO(g)+SO (g),若ΔG=ΔH-TΔS<0,则反应可自发进行,ΔH>0,ΔS>0,
4 3
因此T为较大正数时,反应能自发进行,故选C。
10.下列关于焓判据和熵判据的说法中,不正确的是( )
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.4Fe(OH) (s)+2HO(l)+O(g)=4Fe(OH) (s) ΔH=-444.3kJ·mol-1ΔS=-280.1J·mol-1·K-1在常温常压下能自
2 2 2 3
发进行
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200K)下则能自发
进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
【答案】D
【解析】A项,反应自发进行的判断依据是ΔH-TΔS<0,放热的自发过程中ΔH<0,ΔS可能小于0
也可能大于0,所以放热的自发过程可能是熵减小的过程,吸热的自发过程中ΔH>0、ΔH-TΔS<0,则ΔS
必须>0,所以吸热的自发过程一定为熵增加的过程,A正确;B项,常温下T=298K,则-444.3kJ•mol-1-
298K×(-280.1J•mol-1•K-1)=-366.8302kJ/mol<0,即ΔH-TΔS<0,所以该反应在常温常压能自发进行,B正确;
C项,碳酸钙分解的方程式为CaCO (s) CaO(s)+CO (g),其中ΔH>0,ΔS>0,高温时才能满足反应自发
3 2
进行的条件ΔH-TΔS<0,所以碳酸钙的⇌分解在室温下不能自发进行,但在较高温度(1200K)下能自发进行,
C正确;D项,当ΔG=ΔH-TΔS<0时反应自发,仅ΔH<0或ΔS>0无法确保ΔG<0,即不一定自发,D
错误;故选D。
11.化学反应进行的方向是一个比较复杂的问题。下列有关说法正确的是( )
A.反应 的
B. 在不同状态时的熵值:
C.反应 能否自发进行与温度有关D. 或 的反应一定能自发进行
【答案】C
【解析】A项,反应 的气体分子数减少,该反应的△S<0,A错误;B
项,同一物质在固态时的熵值小于气态时的熵值,B错误;C项,反应 的气体分
子数增加,△S>0,又因为△H>0,△H-T S<0时,反应能自反进行,因此选项所给反应能否自发进行
与温度有关,C正确;D项,△H>0且△S>△0的反应一定能自发进行,D错误;故选C。
12.下列说法不正确的是( )
A.CaCO (s)=CaO(s)+CO (g)室温下不能自发进行,说明该反应的
3 2
B.放热及熵增加的反应,一定能自发进行
C.已知反应 ,高温下为自发过程,低温下为非自发过程
D.知道了某过程有自发性之后,则可确定过程是否一定会发生
【答案】D
【解析】A项,根据反应方程式,该反应为熵增,根据△G= H-T• S进行分析,该反应不能自发进行,
△G>0,因此可以说明该反应为△H>0,故A说法正确;B项,△放热反△应,推出△H<0,熵增,推出△S
>0,根据复合判据,任何温度下,该反应都能自发进行,故B说法正确;C项,该反应是熵增,推出△S
>0,该反应△H>0,根据复合判据,高温下能够自发进行,低温下非自发进行,故C说法正确;D项,
过程的自发性只能用于判断过程的方向,不能确定过程是否一定会发生和过程发生的概率,故D说法错误;
故选D。
13.现有两个热化学反应方程式:
(l)+H (g) (l) ΔH>0 ①
2
(l)+2H (g) (l) ΔH<0 ②
2
下列说法正确的是( )
A.反应①②中都存在:ΔS>0
B.反应①一定不能自发进行C.在通常情况下,①②都能自发进行
D.反应②高温时,可自发进行
【答案】B
【解析】A项,由题中热化学反应方程式可知,反应①②均为熵减反应,即ΔS<0,A项错误;B项,
由题可知,反应①ΔH>0,ΔS<0,则ΔH-TΔS>0,所有温度下反应都不能自发进行,B项正确;项,由
B项可知,反应①在所有温度下都不能自发进行;反应②的ΔH<0,ΔS<0,则在低温条件下,ΔH-TΔS<
0,即反应②低温时,可自发进行,C项错误;D项,由题可知,反应②ΔH<0,ΔS<0,则在低温条件下,
ΔH-TΔS<0,即反应②低温时,可自发进行,D项错误;故选B。
14.某化学反应A(s)=D(g)+E(g) ΔH-TΔS=(-4500+11T)kJ·mol-1(其中ΔH为焓变,ΔS为熵变,T为热
力学温度,单位为K),要防止反应发生,温度必须( )
A.高于409 K B.低于136 K
C.高于136 K而低于409 K D.低于409 K
【答案】A
【解析】要防止反应发生,ΔH-TΔS>0,则-4500+11T>0,解得T>409,故选A。
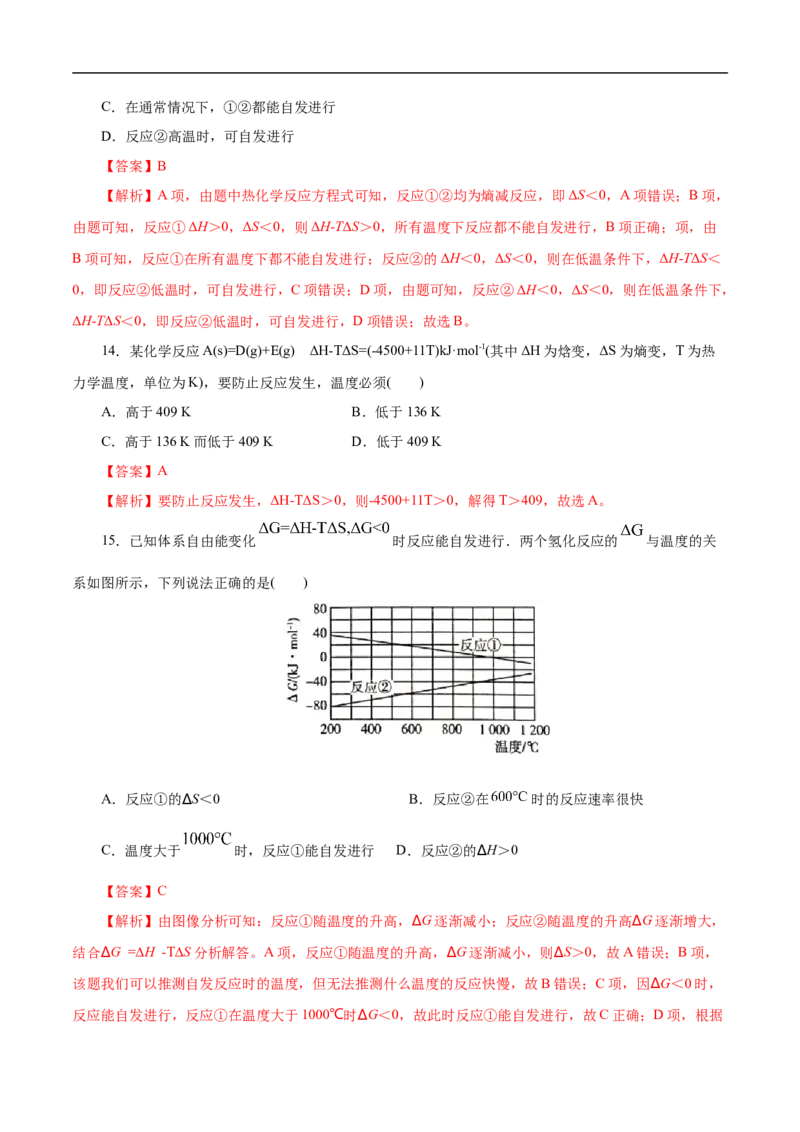
15.已知体系自由能变化 时反应能自发进行.两个氢化反应的 与温度的关
系如图所示,下列说法正确的是( )
A.反应①的∆S<0 B.反应②在 时的反应速率很快
C.温度大于 时,反应①能自发进行 D.反应②的∆H>0
【答案】C
【解析】由图像分析可知:反应①随温度的升高,∆G逐渐减小;反应②随温度的升高∆G逐渐增大,
结合∆G =∆H -T∆S分析解答。A项,反应①随温度的升高,∆G逐渐减小,则∆S>0,故A错误;B项,
该题我们可以推测自发反应时的温度,但无法推测什么温度的反应快慢,故B错误;C项,因∆G<0时,
反应能自发进行,反应①在温度大于1000℃时∆G<0,故此时反应①能自发进行,故C正确;D项,根据数学知识可知,∆H为该图像的截距,而反应而的截距小于0,故∆H<0,故D错误;故选C。
16.有A、B、C、D四个反应:
反应 A B C D
ΔH/(kJ·mol-1) 10.5 1.80 -126 -11.7
ΔS/(J·mol-1·K-1) 30.0 -113.0 84.0 -105.0
(1)在任何温度下都能自发进行的反应是______;
(2)任何温度下都不能自发进行的反应是______;
(3)另两个反应中,在温度高于______℃时可自发进行的反应是______;在温度低于______℃时可自发
进行的反应是______。
【答案】(1)C (2)B (3)77 A -161.6 D
【解析】①自发反应需满足△G=ΔH-TΔS<0,若ΔH<0且ΔS>0,则△G一定小于0,反应在任何温
度下都能自发进行,故此处填C;②若ΔH>0且ΔS<0,则△G一定大于0,反应在任何温度下都不能自
发进行,故此处填B;③将反应A对应数据代入ΔH-TΔS<0计算,得反应自发进行的温度要求为:T>
350 K,即350-273=77 ℃,故此处A、77 ℃;将反应D对应数据代入ΔH-TΔS<0计算,得反应自发进行
的温度要求为:T<111.4 K,即111.4-273= -161.6 ℃,故此处D、-161.6 ℃。
17.回答下列问题:
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解CO,发生反应:2CO(g)=2CO(g)+O(g),
2 2 2
该反应的∆H________(填“>”或“<”,下同)0,∆S_______0,在低温下,该反应________(填“能”或“不
能”)自发进行。
(2)超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中
的NO和CO转变成CO 和N,化学方程式为2NO+2CO 2CO+N 。反应在常温下能够自发进行,则
2 2 2 2
反应的∆H______(填“>”或“<”)0。
(3)已知在 、298K时石灰石分解反应CaCO (s)=CaO(s)+CO (g)的∆H>0、∆S>0。
3 2
①常温下,该反应________(填“能”或“不能”)自发进行。
②据本题反应数据分析,温度________(填“能”或“不能”)成为反应进行方向的决定因素。
(4)已知CaSO(s)+ CO(g)=CaO(s)+SO (g)+CO (g) ΔH=+218kJ·mol-1,该反应能够自发进行的反应条件
4 2 2
是__________________________。
(5)某吸热反应能自发进行,则该反应的∆S_____(填“>”或“<”)0。
【答案】(1)> > 不能 (2)< (3)不能 能 (4)高温 (5) >
【解析】(1)由于CO在O 中燃烧生成CO 为放热反应,则二氧化碳分解生成CO和氧气的反应为吸热
2 2反应,∆H>0,根据化学方程式可知,反应后气体的化学计量数之和增加,∆S>0,故低温下ΔG=ΔH-
TΔS>0,反应不能自发进行;(2) ΔG=ΔH-TΔS<0时反应自发进行,通过化学方程式可知常温下△S<0,
常温下反应能够自发进行,则△H<0;(3)①根据ΔG=ΔH-TΔS<0时反应自发进行,已知∆H>0,∆S>0,
则常温下不能自发进行;②该反应的∆H>0、∆S>0,高温条件下能使ΔG=ΔH-TΔS<0,而常温条件下
ΔG=ΔH-TΔS>0,则该反应中温度能成为决定反应进行方向的因素;(4)该反应的∆S>0、∆H>0,则高温时
ΔG=ΔH-TΔS<0,反应能自发进行;(5)已知某吸热反应能自发进行,即ΔG=ΔH-TΔS<0,∆H>0,则∆S>
0。
1.(2022·浙江省宁波“十校”高三选考模拟)相同温度和压强下,关于物质熵的大小比较合理的是(
)
A.1 mol Cl (g)>2 mol Cl (g) B.2 mol H O(l)>2 mol H O(g)
2 2 2 2
C.1 mol CH (g)<1 mol C H(g) D.1 mol C(s,金刚石)的熵值>1 mol C(s,石墨)
4 2 6
【答案】C
【解析】A项,气体的物质的量越多,熵越大,则物质的熵值1 mol Cl (g)<2 mol Cl (g),A错误;B
2 2
项,等物质的量的物质,气态物质含有的熵值大于液体物质的熵值,则2 mol H O(l)<2 mol H O(g),B错
2 2
误;C项,当气体物质的量相等时,气体分子中含有的原子数越多,其熵值就越大,故熵值1 mol CH (g)
4
<1 mol C H(g),C正确;D项,由于金刚石中C的排列比石墨中的C的排列更有序,所以1 mol C(s,金
2 6
刚石)的熵值<1 mol C(s,石墨),D错误;故选C。
2.(2022·浙江省金华十校高三选考模拟)奥地利物理学家Boltzmann首次把熵和混乱度定量地联系起来,
即 (k为Boltzmann常数, 为混乱度,也即微观状态数,可粗略地看作空间排列的可能性数目)。
在相同的温度和压强下,下列关于熵的大小排序正确的是( )
A.1 mol C(CH )<1 mol (CH )CHCH CH B.2mol C H(g)<1 mol CH (g)
3 4 3 2 2 3 2 6 4
C.1mol CuSO ·5H O (s)<1mol CuSO O(s) D.1mol HO(g)<1mol HO(s)
4 2 4 2 2
【答案】A
【解析】A项,对于同分异构体来说,物质分子中含有的支链越多,分子间作用力就越小,物质的熔
沸点就越低;1 mol C(CH ) 转化为1 mol (CH )CHCH CH 时要吸收热量,物质含有的能量越多,体系混乱
3 4 3 2 2 3
程度就越大,其熵值就越大,说明熵值大小关系为:1 mol C(CH )<1 mol (CH )CHCH CH,A正确;B
3 4 3 2 2 3
项,当物质状态相同时,体系中含有气体分子数越多,熵值就越大,则熵的大小关系为:2mol C H(g)>1
2 6mol CH(g),B错误;C项,当物质状态相同、物质的量相同时,物质内含有的原子数目越多,熵值就越大,
4
熵的大小关系为:1mol CuSO ·5H O (s)>1mol CuSO O(s),C错误;D项,同一物质在不同状态时,熵的
4 2 4
大小关系为:气态>液态>固态,故熵的大小关系为:1mol HO(g)>1mol HO(s),D错误;故选A。
2 2
3.(2022·浙江省普通高中强基联盟高三统测)下列说法正确的是( )
A.常温常压下,NaCO、CaCO 的溶解焓变相近,NaCO(s) 2Na+(aq)+CO 2-(aq) ΔS;
2 3 3 2 3 3 1
CaCO (s) Ca2+(aq)+CO 2-(aq) ΔS,则ΔS>ΔS
3 3 2 1 2
B.NaCl(s)=NaCl (1) ΔS<0
C.常温常压下,3O(g) 2O (g) ΔS>0
2 3
D.常温常压下,2CO(g) C(s)+O (g) ΔS>0
2
【答案】A
【解析】A项,溶解焓相近,主要由熵变决定反应方向,NaCO(s)更易溶解,所以ΔS>ΔS,A正确;
2 3 1 2
B项,固体变为液体,混乱程度增大,ΔS>,B错误;C项,气体分子数减少,混乱程度减小,ΔS<0,C
错误;D项,反应前后,气体分子数减少,混乱程度减小,ΔS<0,D错误;故选A。
4.(2022·浙江省温州市高三高考适应性测试二模)相同的温度和压强下,有关下列两个反应的说法不
正确的是( )
反应 ΔH/kJ/mol
MgCO(s) MgO(s)+CO(g) 117.6 1 a
3 2
CaCO (s) CaO(s)+CO(g) 177.9 1 b
3 2
注:①其中 表示反应方程式中气体化学计量数差;
②ΔH-TΔS<0的反应方向自发
A.因为 相同,所以a与b大小相近
B.热分解温度:MgCO(s)>CaCO (s)
3 3
C.a-b=S[MgO(s)]+S[CaCO (s)]-S[MgCO(s)]- S[CaO(s)]
3 3
D.两个反应在不同温度下的ΔH和 都大于零
【答案】B
【解析】A项,熵变的大小与气体体积的改变大小有关,由方程式可知,两反应中气体化学计量数差
相同,则反应的熵变a与b大小相近,故A正确;B项,由MgCO 和CaCO 都为离子晶体,MgCO 和
3 3 3
CaCO 离子所带电荷相等,由于Mg2+半径小于Ca2+半径, MgO晶格能大于CaO晶格能, Mg2+比Ca2+更
3
易与碳酸根离子中的氧离子结合,使碳酸根离子分解为CO,则MgCO 的热分解温度小于CaCO ,故B错
2 3 3
误;C项,由方程式可知,两反应中气体化学计量数差相同,则反应的熵变a与b的差值为a-b=S[MgO(s)]+S[CaCO (s)]-S[MgCO(s)]- S[CaO(s)],故C正确;D项,由表格数据可知,两个反应都是气体体积增大的
3 3
吸热反应,则两个反应在不同温度下的ΔH和 都大于零,故D正确;故选B。
1.【2022·浙江省1月选考】AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+
(aq)+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。对于不同组成的AB型强电解质,下列说法正确的是( )
A.ΔH和ΔS均大于零
B.ΔH和ΔS均小于零
C.ΔH可能大于零或小于零,ΔS大于零
D.ΔH和ΔS均可能大于零或小于零
【答案】D
【解析】强电解质溶于水有的放热,如硫酸铜等;有的吸热,如碳酸氢钠等,所以在水中溶解对应的
ΔH可能大于零或小于零。熵表示系统混乱程度。体系越混乱,则熵越大。AB型强电解质固体溶于水,存
在熵的变化。固体转化为离子,混乱度是增加的,但离子在水中存在水合过程,这样会引发水的混乱度的
变化,让水分子会更加规则,即水的混乱度下降,所以整个溶解过程的熵变ΔS,取决于固体转化为离子的
熵增与水合过程的熵减两个作用的相对大小关系。若是前者占主导,则整个溶解过程熵增,即ΔS>0,反
之,熵减,即ΔS<0。综上所述,D项符合题意。故选D。
2.【2021•浙江6月选考】相同温度和压强下,关于物质熵的大小比较,合理的是( )
A.1molCH(g)<1molH(g) B.1molHO(g)<2molHO(g)
4 2 2 2
C.1molHO(s)>1molHO(l) D.1molC(s,金刚石)>1molC(s,石黑)
2 2
【答案】B
【解析】A项,CH(g)和H(g)物质的量相同,且均为气态,CH(g)含有的原子总数多,CH(g)的摩尔
4 2 4 4
质量大,所以熵值1molCH (g)>1molH (g),A错误;B项,相同状态的相同物质,物质的量越大,熵值越
4 2
大,所以熵值1molH O(g)<2molH O(g),B正确;C项,等量的同物质,熵值关系为:S(g)>S(l)>S(s),
2 2
所以熵值1molH O(s)<1molH O(l),C错误;D项,从金刚石和石墨的结构组成上来看,金刚石的微观结
2 2
构更有序,熵值更低,所以熵值1molC(s,金刚石)<1molC(s,石黑),D错误;故选B。
3.【2020•浙江1月选考】在干燥的HCl气流中加热MgCl ·6H O,能得到无水MgCl 。下列说法不正
2 2 2
确的是( )
A.MgCl ·nH O(s)=MgCl ·(n-1)H O(s)+HO(g) ΔH>0
2 2 2 2 2
B.MgCl ·2H O(s)=Mg(OH) (s)+2HCl(g),HCl气流可抑制反应进行
2 2 2C.MgCl ·H O(s)=Mg(OH)Cl(s)+HCl(g),升高温度,反应更易发生
2 2
D.MgCl ·4H O(s)=MgCl ·2H O(s)+2HO(g),HCl气流可抑制反应进行
2 2 2 2 2
【答案】D
【解析】A项,MgCl ·nH O的失水反应是吸热反应,焓变ΔH>0,故A正确;B项,在HCl气流中,
2 2
能使MgCl ·2H O的水解平衡向逆反应方向移动,抑制反应进行,故B正确;C项,MgCl ·H O的水解反应
2 2 2 2
是吸热反应,升高温度,水解平衡向正反应方向移动,促进反应进行,故C正确;D项,MgCl ·4H O的失
2 2
水反应没有氯化氢生成,HCl气流对反应没有影响,故D错误;故选D。
4.【2022•湖南选择性考试】钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为
TiO,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
2
已知“降温收尘”后,粗TiCl 中含有的几种物质的沸点:
4
物质 TiCl VOCl SiCl AlCl
4 3 4 3
沸点/℃ 136 127 57 180
回答下列问题:
(1)已知ΔG= ΔH-TΔS, 的值只决定于反应体系的始态和终态,忽略 、 随温度的变化。若
ΔG<0,则该反应可以自发进行。根据下图判断:600℃时,下列反应不能自发进行的是_______。
A.C(s)+O(g)=CO (g)
2 2
B.2C(s)+O(g)=2CO(g)
2
C.TiO (s)+2Cl(g)= TiCl (g)+O(g)
2 2 4 2
D.TiO (s)+C(s)+2Cl(g)= TiCl (g)+CO(g)
2 2 4 2(2) TiO 与C、Cl,在600℃的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
2 2
物质 TiCl CO CO Cl
4 2 2
分压
①该温度下,TiO 与C、Cl 反应的总化学方程式为_______;
2 2
②随着温度升高,尾气中 的含量升高,原因是_______。
(3)“除钒”过程中的化学方程式为_______;“除硅、铝”过程中,分离TiCl 中含 、 杂质的方法
4
是_______。
(4)“除钒”和“除硅、铝”的顺序_______(填“能”或“不能”)交换,理由是_______。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼 的方法相似的是_______。
A.高炉炼铁 B.电解熔融氯化钠制钠
C.铝热反应制锰 D.氧化汞分解制汞
【答案】(1)C
(2) 5TiO+6C+10Cl 5TiCl +2CO+4CO 随着温度升高,CO 与C发生反应C+CO 2CO
2 2 4 2 2 2
(3) 3VOCl +Al=3VOCl +AlCl 蒸馏
3 2 3
(4) 不能 若先“除硅、铝”再“除钒”,“除钒”时需要加入Al,又引入Al杂质;
(5)AC
【解析】钛渣中加入C、Cl 进行沸腾氯化,转化为相应的氯化物,降温收尘后得到粗TiCl ,加入单
2 4
质Al除钒,再除硅、铝得到纯TiCl ,加入Mg还原得到Ti。(1)记①C(s)+O(g)=CO (g),②2C(s)+
4 2 2
O(g)=2CO(g),③TiO (s)+2Cl(g)= TiCl (g)+O(g),④TiO (s)+C(s)+2Cl(g)= TiCl (g)+CO(g);A项,
2 2 2 4 2 2 2 4 2
由图可知,600℃时C(s)+O(g)=CO (g)的ΔG<0,反应自发进行,故A不符合题意;B项,由图可知,
2 2
600℃时2C(s)+O(g)=2CO(g)的ΔG<0,反应自发进行,故B不符合题意;C项,由图可知,600℃时TiO
2 2
(s)+2Cl(g)= TiCl (g)+O(g)的ΔG>0,反应不能自发进行,故C符合题意;D项,根据盖斯定律,TiO
2 4 2 2
(s)+C(s)+2Cl(g)= TiCl (g)+CO(g)可由①+③得到,则600℃时其ΔG<0,反应自发进行,故D不符合题
2 4 2
意;故选C;(2)①根据表中数据可知,该温度下C主要生成CO和CO,根据相同条件下气体的压强之比
2
是物质的量之比可知TiCl 、CO和CO 的物质的量之比约是5:2:4,所以TiO 与C、Cl 反应的总化学方
4 2 2 2
程式为5TiO+6C+10Cl 5TiCl +2CO+4CO ;②随着温度升高,CO 与C发生反应C+CO
2 2 4 2 2 2
2CO,导致CO含量升高;(3)“降温收尘”后钒元素主要以VOCl 形式存在,加入Al得到VOCl 渣,根据
3 2
得失电子守恒和元素守恒配平方程式为3VOCl +Al=3VOCl +AlCl ;AlCl 、SiCl 与TiCl 沸点差异较大,
3 2 3 3 4 4“除硅、铝"过程中可采用蒸馏的方法分离AlCl 、SiCl ;(4)若先“除硅、铝”再“除钒”,“除钒”时需
3 4
要加入Al,又引入Al杂质,因此“除钒”和“除硅、铝”的顺序不能交换;(5)本工艺中加入Mg冶炼Ti
的方法为热还原法;A项,高炉炼铁的原理是用还原剂将铁矿石中铁的氧化物还原成金属铁,属于热还原
法,故A符合题意;B项,电解熔融氯化钠制取金属钠的原理是电解法,故B不符合题意;C项,铝热反
应制锰是利用Al作还原剂,将锰从其化合物中还原出来,为热还原法,故C符合题意;D项,Hg为不活
泼金属,可以直接用加热分解氧化汞的方法制备汞,故D不符合题意;故选AC。