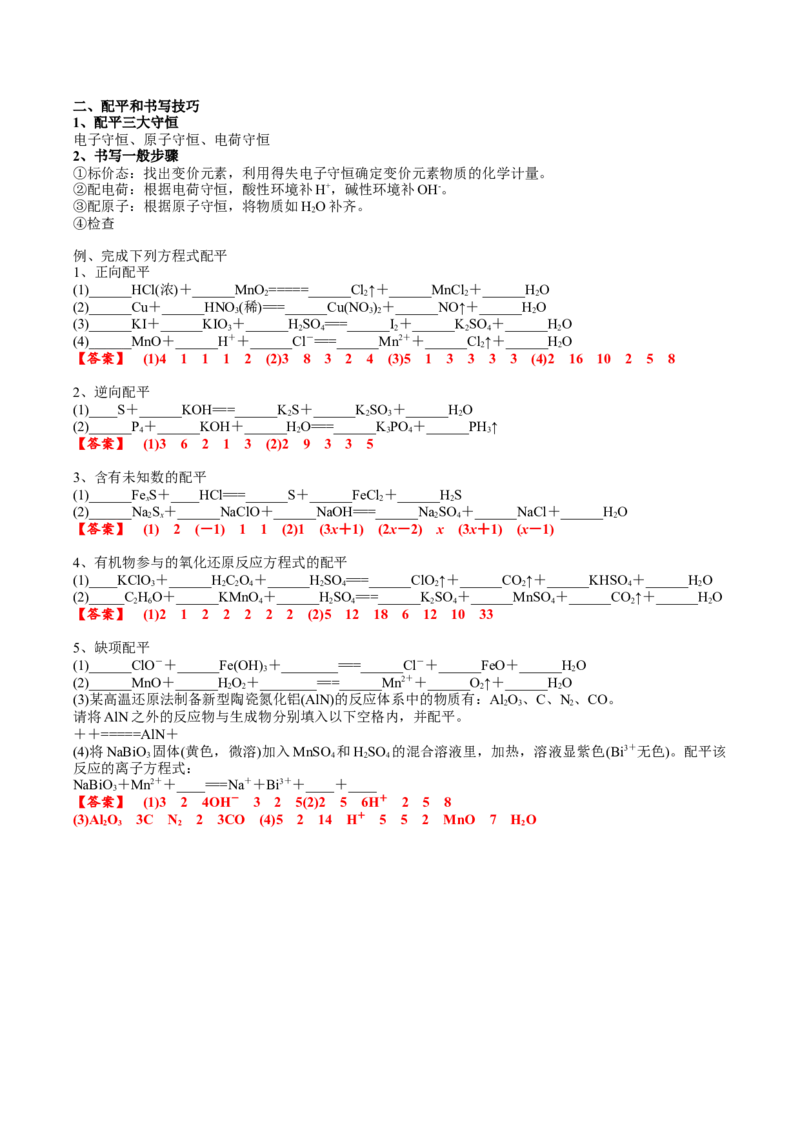文档内容
【基础知识】氧化还原反应
考点三 氧化还原反应方程式的配平与书写
【知识储备】
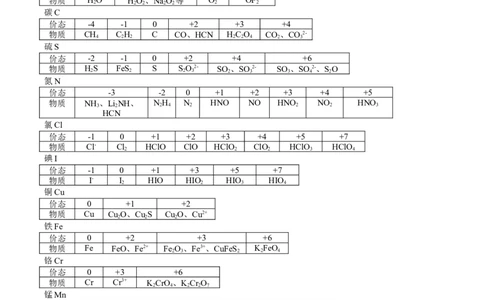
一、元素的常见价态
氢H
价态 -1 0 +1
物质 金属氢化物、NaBH H HO
4 2 2
氧O
价态 -2 -1 0 +2
物质 HO HO、NaO 等 O OF
2 2 2 2 2 2 2
碳C
价态 -4 -1 0 +2 +3 +4
物质 CH C H C CO、HCN HC O CO、CO2-
4 2 2 2 2 4 2 3
硫S
价态 -2 -1 0 +2 +4 +6
物质 HS FeS S SO2- SO 、SO 2- SO 、SO 2-、SO
2 2 2 3 2 3 3 4 2
氮N
价态 -3 -2 0 +1 +2 +3 +4 +5
物质 NH、LiNH、 NH N HNO NO HNO NO HNO
3 2 2 4 2 2 2 3
HCN
氯Cl
价态 -1 0 +1 +2 +3 +4 +5 +7
物质 Cl- Cl HClO ClO HClO ClO HClO HClO
2 2 2 3 4
碘I
价态 -1 0 +1 +3 +5 +7
物质 I- I HIO HIO HIO HIO
2 2 3 4
铜Cu
价态 0 +1 +2
物质 Cu Cu O、Cu S Cu O、Cu2+
2 2 2
铁Fe
价态 0 +2 +3 +6
物质 Fe FeO、Fe2+ Fe O、Fe3+、CuFeS KFeO
2 3 2 2 4
铬Cr
价态 0 +3 +6
物质 Cr Cr3+ KCrO、KCr O
2 4 2 2 7
锰Mn
价态 0 +2 +3 +4 +6 +7
物质 Mn Mn2+、 MnO(OH) MnO KMnO KMnO
2 2 4 4
MnO
过渡元素一般为变价元素,在习题中要注意有没有化合价变化。二、配平和书写技巧
1、配平三大守恒
电子守恒、原子守恒、电荷守恒
2、书写一般步骤
①标价态:找出变价元素,利用得失电子守恒确定变价元素物质的化学计量。
②配电荷:根据电荷守恒,酸性环境补H+,碱性环境补OH-。
③配原子:根据原子守恒,将物质如HO补齐。
2
④检查
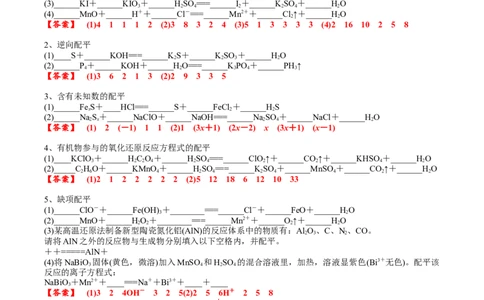
例、完成下列方程式配平
1、正向配平
(1)______HCl(浓)+______MnO =====______Cl↑+______MnCl +______HO
2 2 2 2
(2)______Cu+______HNO(稀)===______Cu(NO)+______NO↑+______HO
3 3 2 2
(3)______KI+______KIO +______HSO ===______I +______KSO +______HO
3 2 4 2 2 4 2
(4)______MnO+______H++______Cl-===______Mn2++______Cl↑+______HO
2 2
【答案】 (1)4 1 1 1 2 (2)3 8 3 2 4 (3)5 1 3 3 3 3 (4)2 16 10 2 5 8
2、逆向配平
(1)____S+______KOH===______K S+______KSO +______HO
2 2 3 2
(2)______P +______KOH+______HO===______K PO +______PH ↑
4 2 3 4 3
【答案】 (1)3 6 2 1 3 (2)2 9 3 3 5
3、含有未知数的配平
(1)______FeS+____HCl===______S+______FeCl +______HS
x 2 2
(2)______Na S+______NaClO+______NaOH===______Na SO +______NaCl+______HO
2 x 2 4 2
【答案】 (1) 2 (-1) 1 1 (2)1 (3x+1) (2x-2) x (3x+1) (x-1)
4、有机物参与的氧化还原反应方程式的配平
(1)____KClO +______HC O+______HSO ===______ClO ↑+______CO↑+______KHSO+______HO
3 2 2 4 2 4 2 2 4 2
(2)_____C HO+______KMnO +______HSO ===______K SO +______MnSO +______CO↑+______HO
2 6 4 2 4 2 4 4 2 2
【答案】 (1)2 1 2 2 2 2 2 (2)5 12 18 6 12 10 33
5、缺项配平
(1)______ClO-+______Fe(OH) +________===______Cl-+______FeO+______HO
3 2
(2)______MnO+______HO+________===______Mn2++______O↑+______HO
2 2 2 2
(3)某高温还原法制备新型陶瓷氮化铝(AlN)的反应体系中的物质有:Al O、C、N、CO。
2 3 2
请将AlN之外的反应物与生成物分别填入以下空格内,并配平。
++=====AlN+
(4)将NaBiO 固体(黄色,微溶)加入MnSO 和HSO 的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该
3 4 2 4
反应的离子方程式:
NaBiO+Mn2++____===Na++Bi3++____+____
3
【答案】 (1)3 2 4OH- 3 2 5(2)2 5 6H+ 2 5 8
(3)AlO 3C N 2 3CO (4)5 2 14 H+ 5 5 2 MnO 7 HO
2 3 2 2【题型练习】
一、依据陈述信息书写方程式
1、[2021·全国甲卷,26(2)]以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO ,生成
3 2 3 3
碘化物;再向混合溶液中加入 NaIO 溶液,反应得到 I 。上述制备 I 的总反应的离子方程式为
3 2 2
_________________________________________________________________。
【答案】 2IO+5HSO===I +5SO+3H++HO
2 2
2、工业上可由天然二氧化锰粉和硫化锰矿用硫酸溶浸得硫单质和硫酸锰,写出该反应的化学方程式:
________________________________________________________________________。
【答案】 MnO +MnS+2HSO ===2MnSO +S+2HO
2 2 4 4 2
3、KMnO 能与热的经硫酸酸化的 NaC O 溶液反应,生成 Mn2+和 CO ,该反应的离子方程式是
4 2 2 4 2
_____________________________________________________________________________。
【答案】 2MnO+5CO+16H+=====2Mn2++10CO ↑+8HO。
2 2 2
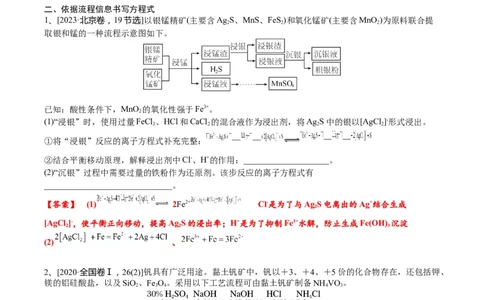
二、依据流程信息书写方程式
1、[2023·北京卷,19节选]以银锰精矿(主要含Ag S、MnS、FeS)和氧化锰矿(主要含MnO )为原料联合提
2 2 2
取银和锰的一种流程示意图如下。
已知:酸性条件下,MnO 的氧化性强于Fe3+。
2
(1)“浸银”时,使用过量FeCl 、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以[AgCl ]-形式浸出。
3 2 2 2
①将“浸银”反应的离子方程式补充完整:
②结合平衡移动原理,解释浸出剂中Cl-、H+的作用:____________________。
(2)“沉银”过程中需要过量的铁粉作为还原剂。该步反应的离子方程式有
______________________________。
【答案】 (1) 2Fe2+ Cl-是为了与Ag S电离出的Ag+结合生成
2
[AgCl ]-,使平衡正向移动,提高Ag S的浸出率;H+是为了抑制Fe3+水解,防止生成Fe(OH) 沉淀
2 2 3
(2) 、
2、[2020·全国卷Ⅰ,26(2)]钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、
镁的铝硅酸盐,以及SiO、Fe O。采用以下工艺流程可由黏土钒矿制备NH VO 。
2 3 4 4 3
“酸浸氧化”中,VO+和VO2+被氧化成VO,同时还有________离子被氧化。写出VO+转化为VO反应的
离子方程式:____________________________________。
【答案】 Fe2+ VO++MnO +2H+===VO+Mn2++HO
2 2
【解析】 FeO 与稀硫酸反应:FeO +8H+===2Fe3++Fe2++4HO,“酸浸氧化”过程中,Fe2+具有还
3 4 3 4 2
原性,也能被MnO 氧化生成Fe3+。VO+被氧化为VO,MnO 则被还原为Mn2+,溶液呈酸性,结合守恒
2 2
规律,写出离子方程式:VO++MnO +2H+===VO+Mn2++HO。
2 2三、依据反应机理图书写方程式
1、在酸性条件下,黄铁矿(FeS ,其中S为-1价)催化氧化的反应转化如图所示。
2
总反应:2FeS+7O+2HO===2Fe2++4SO+4H+
2 2 2
分别写出反应Ⅰ、Ⅱ的离子方程式:
①反应Ⅰ:______________________________________________________________。
②反应Ⅱ:______________________________________________________________。
【答案】 (1)①4Fe(NO)2++O+4H+===4Fe3++4NO+2HO
2 2
②14Fe3++FeS +8HO===15Fe2++2SO+16H+
2 2
2、某催化转化过程如图所示:
过程1:Ni O+ClO-===2NiO+Cl-,
2 3 2
过程2的离子方程式:__________________________________________。
【答案】 2NiO +ClO-===NiO+Cl-+2O
2 2 3
3、NaClO氧化可除去氨氮,反应机理如图所示(其中HO和NaCl略去):
2
NaClO氧化NH 的总反应的化学方程式为__________________________________________。
3
【答案】 2NH +3NaClO===N +3HO+3NaCl
3 2 2
【跟踪练习】
1、根据信息完成下列方程式。
(1)KMnO 氧化废水中Mn2+生成MnO 的离子方程式为________________________________。
4 2
(2)NaAlH 与水发生氧化还原反应的化学方程式为____________________________________。
4
(3)在酸性条件下, NaClO 可发生反应生成 NaCl 并释放出 ClO ,该反应的离子方程式为
2 2
_______________________________________________________________________________。
(4)PbO 可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为______________________。
2
(5)在45~50 ℃时向CuCl悬浊液中持续通入空气,得到碱式氯化铜[Cu (OH) Cl·3H O],该反应的化学方
2 2 2 2
程式为_____________________________________________________________。
(6)(2018·全国卷Ⅰ节选)Na S O 可用作食品的抗氧化剂。在测定某葡萄酒中Na S O 残留量时,取50.00
2 2 5 2 2 5
mL葡萄酒样品,用0.01000 mol·L-1的碘标准液滴定至终点,消耗10.00 mL。滴定反应的离子方程式为
_________________________________。
(7)(2018·江苏卷节选)用酸性(NH ) CO水溶液吸收NO ,吸收过程中存在 HNO 与(NH ) CO生成N 和
2 2 x 2 2 2 2
CO 的反应。写出该反应的化学方程式:___________________________________。
2
(8)(2017·江苏卷节选)①45~50 ℃时,向CuCl悬浊液中持续通入空气得到Cu (OH) Cl ·3H O,该反应的
2 2 2 2
化学方程式为______________________________________。
②NaClO溶液与Ag反应的产物为AgCl、NaOH和O ,该反应的化学方程式为
2
_______________________。(9)(2016·上海卷节选)NaOCN与NaClO反应,生成Na CO 、CO 、NaCl和N ,已知HCN、HOCN中N
2 3 2 2
元素的化合价相同。写出发生反应的离子方程式:____________________________________。
【答案】 (1)2MnO+3Mn2++2HO===5MnO ↓+4H+ (2)NaAlH +4HO===Na[Al(OH) ]+4H↑
2 2 4 2 4 2
(3)4H++5ClO===Cl-+4ClO ↑+2HO (4)PbO+ClO-===PbO +Cl-
2 2 2
(5)4CuCl+O+8HO=======2Cu (OH) Cl ·3HO
2 2 2 2 2 2
(6)SO+2I+3HO===2SO+4I-+6H+ (7)2HNO +(NH)CO===2N ↑+CO ↑+3HO
2 2 2 2 2 2 2 2 2
(8)①4CuCl+O+8HO=====2Cu (OH) Cl ·3HO ②4Ag+4NaClO+2HO===4AgCl+4NaOH+O↑
2 2 2 2 2 2 2 2
(9)2OCN-+3ClO-===CO+CO ↑+3Cl-+N↑
2 2
2、[2020·全国卷Ⅱ,26节选]化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化
工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)Cl O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl 反应来制备,该反应为歧化反应(氧化
2 2
剂和还原剂为同一种物质的反应)。上述制备ClO的化学方程式为___________________________________。
2
(2)ClO 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO 、NaHSO 、
2 2 4
NaHCO 的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO 溶液。上述过程中,生成ClO
3 2 2
的反应属于歧化反应,每生成1 mol ClO 消耗NaClO 的量为____________mol;产生“气泡”的化学方程
2 2
式为___________________________________。
【答案】 (1)2Cl+HgO===HgCl +Cl O (2)1.25 NaHCO +NaHSO ===CO↑+Na SO +HO
2 2 2 3 4 2 2 4 2
【解析】 (1)由新制的HgO和Cl 反应制备Cl O,由于该反应为歧化反应,所以只有氯元素的化合价发
2 2
生变化,由0价变为+1价和-1价,所以反应的化学方程式为2Cl +HgO===HgCl +Cl O。
2 2 2
(2)由题意知,在 NaClO 生成 ClO 的过程中,发生歧化反应,NaClO 既是氧化剂,又是还原剂,
2 2 2
4NaClO――→4ClO,NaClO――→NaCl,每生成4 mol ClO ,需消耗5 mol NaClO ,所以每生成1 mol
2 2 2 2 2
ClO ,需消耗 mol(即1.25 mol)NaClO 。产生的气泡的成分为 CO ,反应的化学方程式为 NaHCO +
2 2 2 3
NaHSO ===CO↑+Na SO +HO。
4 2 2 4 2
3、[2022·全国甲卷,26节选]硫酸锌(ZnSO)是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应
4
用。硫酸锌可由菱锌矿制备。菱锌矿的主要成分为ZnCO ,杂质为SiO 以及Ca、Mg、Fe、Cu等的化合物。
3 2
其制备流程如下:
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______________________________________。
(2)向80~90 ℃的滤液①中分批加入适量KMnO 溶液充分反应后过滤,滤渣②中有MnO ,该步反应的离
4 2
子方程式为__________________________________________。
【答案】 (1)ZnCO =====ZnO+CO ↑ (2)3Fe2++MnO+7HO===3Fe(OH) ↓+MnO ↓+5H+
3 2 2 3 2
【解析】 (1)焙烧时,生成ZnO的反应为ZnCO =====ZnO+CO ↑。
3 2
(2)向80~90 ℃的滤液①中加入KMnO 溶液,可氧化Fe2+,得到含Fe(OH) 和MnO 的滤渣②,反应的离
4 3 2
子方程式为3Fe2++MnO+7HO===3Fe(OH) ↓+MnO ↓+5H+。
2 3 2
4、[2023·辽宁卷,16节选]某工厂采用如下工艺处理镍钴矿硫酸浸取液含(Ni2+、Co2+、Fe2+、Fe3+、Mg2+
和Mn2+)。实现镍、钴、镁元素的回收。回答下列问题:
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸HSO ,1 mol H SO 中过氧
2 5 2 5
键的数目为_______。
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被HSO 氧化为MnO ,该反应的离子方程式为
2 5 2
_____________________( HSO 的电离第一步完全,第二步微弱);滤渣的成分为MnO 、_______(填化学
2 5 2
式)。
(5)“沉钴镍”中得到的MnO (Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为
2
__________________。
【答案】 (1)N (3) Fe(OH) (5)
A 3
5、NaClO 是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如图所示:
2
(1)写出“反应”步骤中生成ClO 的化学方程式:__________________________________。
2
(2)“尾气吸收”是吸收电解过程中排出的少量 ClO 。写出此吸收反应的化学方程式:
2
___________________________________________________。
【答案】 (1)2NaClO +SO +HSO ===2ClO +2NaHSO
3 2 2 4 2 4
(2)2ClO +HO+2NaOH===2NaClO +O+2HO
2 2 2 2 2 2
6、锰广泛存在于自然界中,工业可用软锰矿(主要成分是MnO )制备锰。
2
资料:①MnCO 难溶于水,可溶于稀酸。
3
②在Mn2+催化下,SO 在水溶液中被氧化成HSO 。
2 2 4
(1)写出铝热法还原MnO 制备锰的化学方程式:_______________________________。
2
(2)工业上制备锰时,会产生大量废水和锰渣。锰渣煅烧会产生含高浓度SO 的烟气,可用以下方法处理。
2
①用软锰矿进行脱硫可生成硫酸锰,从而达到资源的循环使用。写出一定条件下利用 MnO 进行脱硫的化
2
学方程式:______________________________________________________。
②研究表明,用Fe2+/Fe3+可强化脱硫效果,其过程如图所示:
过程Ⅰ:……
过程Ⅱ:2Fe3++SO +2HO===2Fe2++SO+4H+
2 2
过程Ⅰ的离子方程式是_________________________________________________________。
【答案】 (1)4Al+3MnO =====3Mn+2Al O
2 2 3
(2)①MnO +SO ======MnSO ②2Fe2++MnO +4H+===Mn2++2Fe3++2HO
2 2 4 2 2
【解析】 (1)铝热法还原MnO 制备锰即高温条件下铝单质和MnO 反应得到氧化铝和Mn单质,化学方
2 2
程式为4Al+3MnO =====3Mn+2Al O。
2 2 3
(2)①根据题意可知MnO 会将SO 氧化得到MnSO ,化学方程式应为MnO +SO ======MnSO 。②据图
2 2 4 2 2 4
可知过程Ⅰ中MnO 被Fe2+还原生成Mn2+,Fe2+被氧化为Fe3+,根据电子守恒和元素守恒可得离子方程
2式为2Fe2++MnO +4H+===Mn2++2Fe3++2HO。
2 2