文档内容
解密 07 化学反应速率与化学平衡
考点热度 ★★★★★
【考纲导向】
1.了解化学反应速率的概念和表示方法。能正确计算反应物的转化率(α)。
2.了解活化能的概念和催化剂的重要作用。
3.了解化学反应的可逆性及化学平衡的建立。
4.掌握化学平衡的特征。了解化学平衡常数(K)的含义,并能进行相关计算。
5.理解外界条件对反应速率和化学平衡的影响,能用相关理论解释其一般规律。
6.了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。
【命题分析】
化学反应速率与化学平衡是高考的必考内容,其中外界因素对平衡状态的影响、化学平衡常数、与化学平
衡和化学反应速率相关的计算是考查的重点。试题对计算能力、语言组织表达能力、数形结合分析能力要
求较高。难度以中等或中等偏难为主。预计2023年高考对本专题的考查仍会以综合题为主,侧重考查考生
分析问题能力,信息整合应用能力等,试题难度有逐渐加大的趋势。
核心考点一 化学反应速率及其影响因素
一、化学反应速率及其影响因素1.化学反应速率的计算
(1)根据图表中数据和定义计算:v(X)=,即v(X)==,计算时一定要注意容器或溶液的体积,不能忽视容
器或溶液的体积V,盲目地把Δn当作Δc代入公式进行计算。
(2)根据化学方程式计算:对于反应“mA+nB pC+qD”,有 v(A)∶v(B)∶v(C)∶v(D)=
m∶n∶p∶q。
2.外界因素对化学反应速率的影响及规律
(1)当其他条件相同时,增大反应物浓度时,v正 增大,v逆 瞬间不变,随后也增大。
(2)压强对反应速率的影响(有气体参加的化学反应)
①恒温时,压缩体积→压强增大→反应物浓度增大→反应速率加快。
②恒温时,对于恒容密闭容器
a.充入气体反应物→总压强增大→气体反应物浓度增大→反应速率加快。
b.充入“惰性”气体→总压强增大→气体反应物浓度未改变→反应速率不变。
③恒温恒压时
充入“惰性”气体→体积增大→气体反应物浓度减小→反应速率减小。
(3)升高温度,v正 和v逆 都增大,但吸热反应方向的反应速率增大的程度大;降低温度,v正 和v逆 都减小,
但吸热反应方向的反应速率减小的程度大。
(4)使用催化剂,能同等程度地改变正、逆反应速率。
3.化学反应速率常数及应用
(1)速率常数含义
速率常数(k)是指在给定温度下,反应物浓度皆为1 mol·L-1时的反应速率。在相同的浓度条件下,可用速
率常数大小来比较化学反应的反应速率。
化学反应速率与反应物浓度(或浓度的次方)成正比,而速率常数是其比例常数,在恒温条件下,速率常数
不随反应物浓度的变化而改变。因此,可以应用速率方程求出该温度下任意浓度时的反应速率。
(2)速率方程
一定温度下,化学反应速率与反应物浓度以其计量数为指数的幂的乘积成正比。
对于反应:aA(g)+bB(g) gG(g)+hH(g)
则v正 =k
正
ca(A)·cb(B)(其中k
正
为正反应的速率常数),v逆 =k
逆
·cg(G)·ch(H)(其中k
逆
为逆反应的速率常数)。
如反应2NO
2
(g) 2NO(g)+O
2
(g),v正 =k
正
·c2(NO
2
),v逆 =k
逆
·c2(NO)·c(O
2
)。
(3)速率常数与化学平衡常数之间的关系
一定温度下,可逆反应:aA(g)+bB(g) gG(g)+hH(g),达到平衡状态时,v正 =k
正
·ca(A)·cb(B),v逆 =
k ·cg(G)·ch(H),
逆
因平衡时v正 =v逆 ,则k
正
·ca(A)·cb(B)=k
逆
·cg(G)·ch(H),==K
4.理论解释——有效碰撞理论
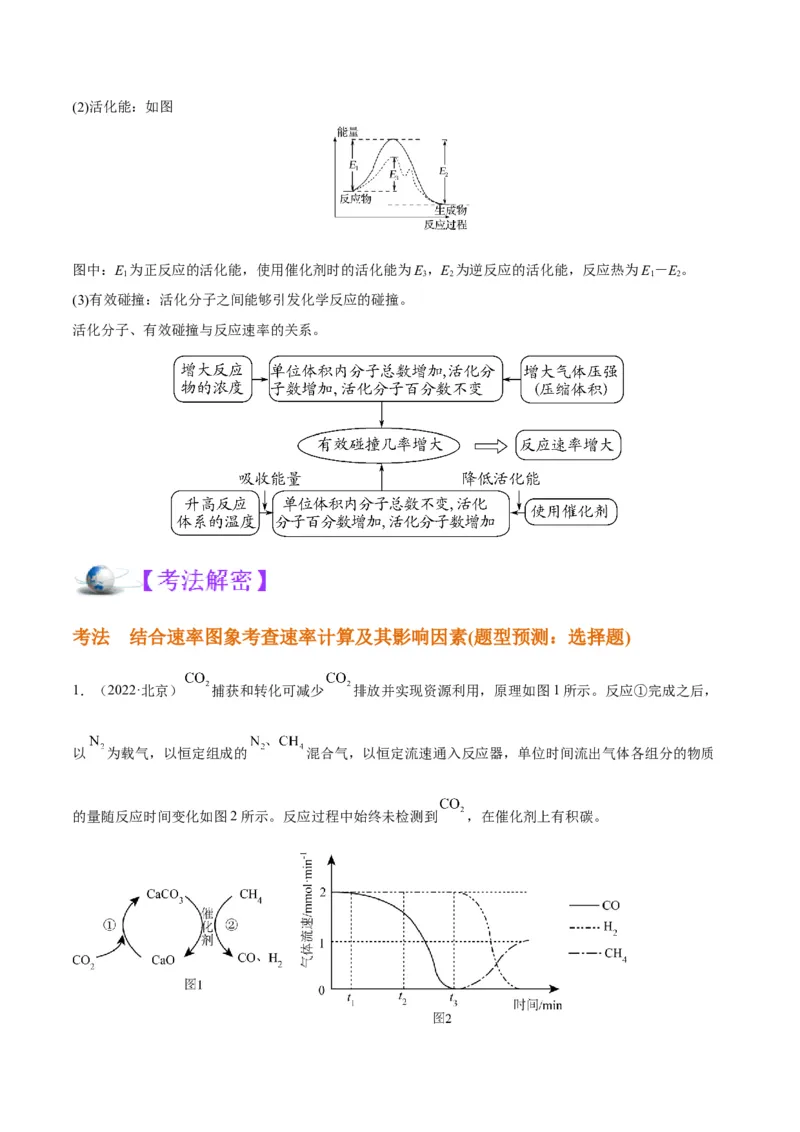
(1)活化分子:能够发生有效碰撞的分子。(2)活化能:如图
图中:E 为正反应的活化能,使用催化剂时的活化能为E,E 为逆反应的活化能,反应热为E-E。
1 3 2 1 2
(3)有效碰撞:活化分子之间能够引发化学反应的碰撞。
活化分子、有效碰撞与反应速率的关系。
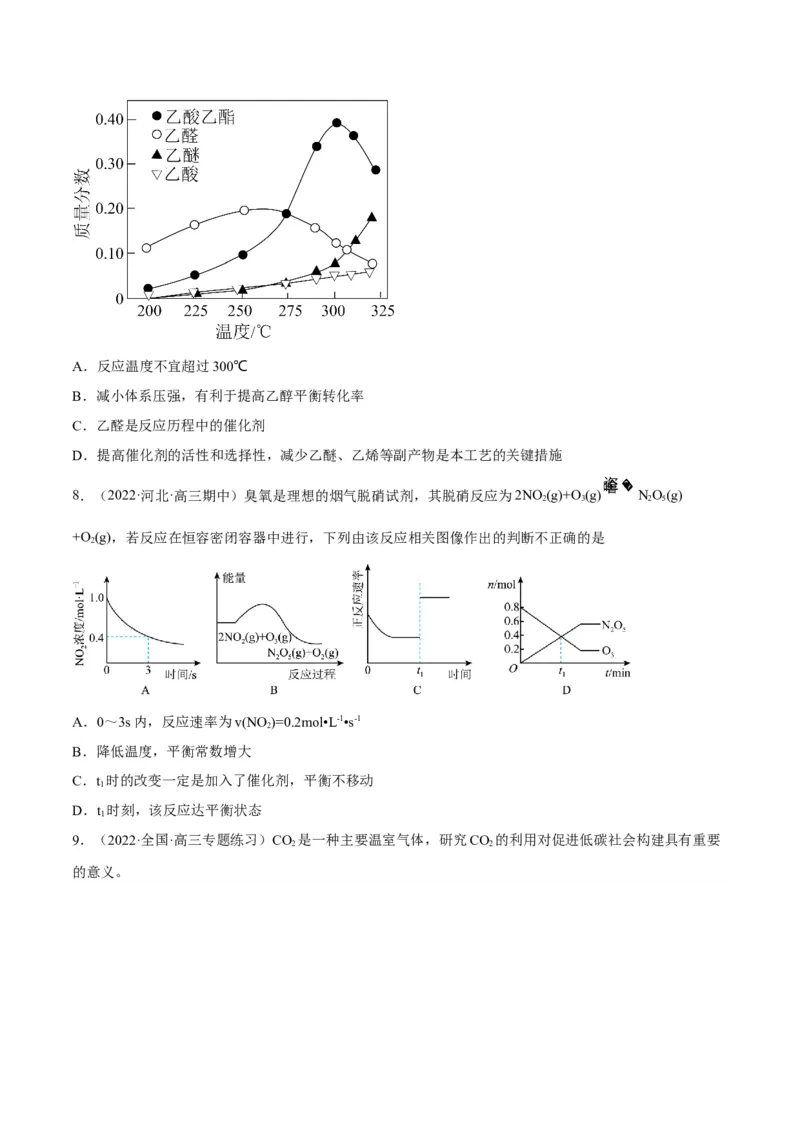
考法 结合速率图象考查速率计算及其影响因素(题型预测:选择题)
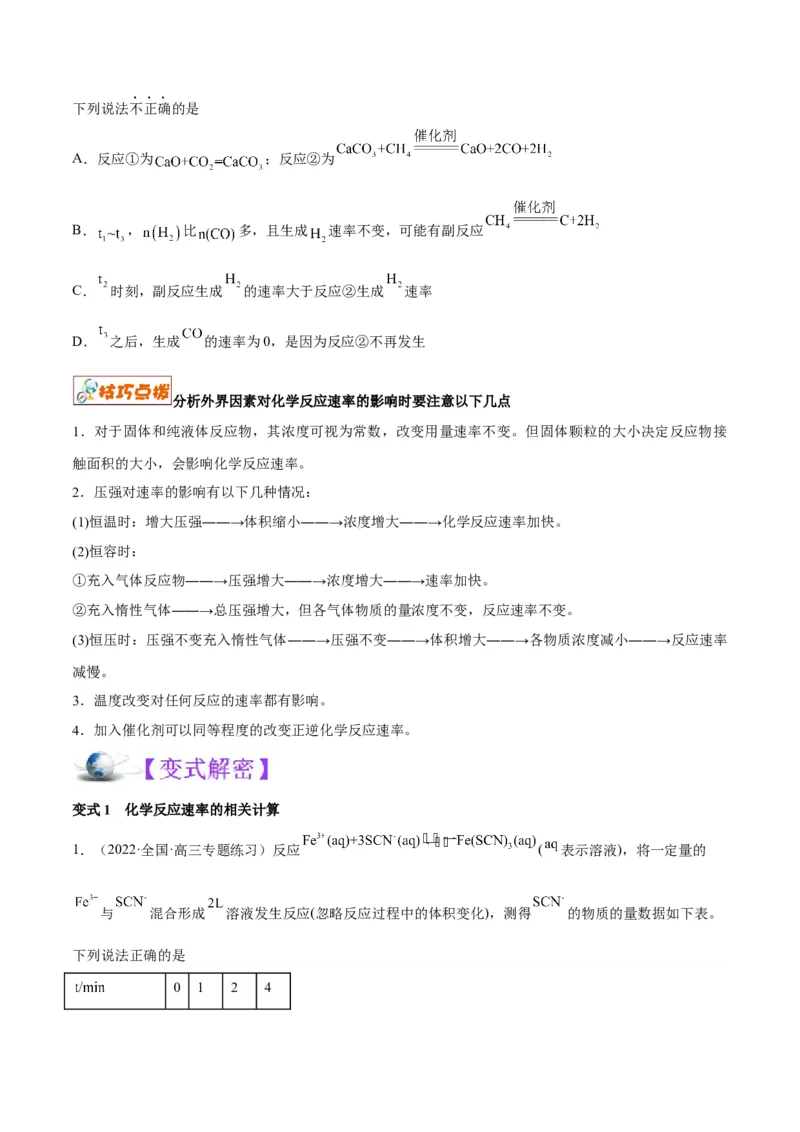
1.(2022·北京) 捕获和转化可减少 排放并实现资源利用,原理如图1所示。反应①完成之后,
以 为载气,以恒定组成的 混合气,以恒定流速通入反应器,单位时间流出气体各组分的物质
的量随反应时间变化如图2所示。反应过程中始终未检测到 ,在催化剂上有积碳。下列说法不正确的是
A.反应①为 ;反应②为
B. , 比 多,且生成 速率不变,可能有副反应
C. 时刻,副反应生成 的速率大于反应②生成 速率
D. 之后,生成 的速率为0,是因为反应②不再发生
分析外界因素对化学反应速率的影响时要注意以下几点
1.对于固体和纯液体反应物,其浓度可视为常数,改变用量速率不变。但固体颗粒的大小决定反应物接
触面积的大小,会影响化学反应速率。
2.压强对速率的影响有以下几种情况:
(1)恒温时:增大压强――→体积缩小――→浓度增大――→化学反应速率加快。
(2)恒容时:
①充入气体反应物――→压强增大――→浓度增大――→速率加快。
②充入惰性气体――→总压强增大,但各气体物质的量浓度不变,反应速率不变。
(3)恒压时:压强不变充入惰性气体――→压强不变――→体积增大――→各物质浓度减小――→反应速率
减慢。
3.温度改变对任何反应的速率都有影响。
4.加入催化剂可以同等程度的改变正逆化学反应速率。
变式1 化学反应速率的相关计算
1.(2022·全国·高三专题练习)反应 ( 表示溶液),将一定量的
与 混合形成 溶液发生反应(忽略反应过程中的体积变化),测得 的物质的量数据如下表。
下列说法正确的是
0 1 2 43 1.5 0.6 0.6
A. 时,
B. 时,溶液中剩余 物质的量为
C. 内,
D. 时,
变式2 化学反应速率的大小比较
2.(2022·黑龙江·鹤岗一中高三阶段练习)已知反应 在四种不同情况下的反应
速率分别如下:
①v(A)=0.1 mol·L-1·min-1
②v(B)=0.15 mol·L-1·min-1
③
④v(D=0.1 mol·L-1·min-1
则该反应进行速率快慢顺序正确的是
A.①>②>③>④ B.②>①=④>③
C.③>①>②>④ D.④>③>①>②
变式3 外界条件对化学反应速率的影响
3.(2022·吉林·延边二中高三阶段练习)2SO (g)+O(g) 2SO (g) ΔH=-198 kJ·mol-1,在VO 存在时,该
2 2 3 2 5
反应的机理为:VO+SO =2VO+SO (快),4VO +O=2⇌V O(慢)。下列说法中正确的是
2 5 2 2 3 2 2 2 5
A.反应速率主要取决于VO 的质量 B.VO 是该反应的催化剂
2 5 2
C.逆反应的活化能大于198 kJ·mol-1 D.增大SO 的浓度可显著提高反应速率
2
变式4 控制变量法探究影响化学反应速率的因素
4.(2022·黑龙江·佳木斯一中高三期中)某小组探究
反应速率的影响因素,有关实验数据如
表所示:酸性 溶液 溶液
实验编 温 催化剂用 溶液褪色平均时
号 度/℃ 量/g 体积/ 浓度/ 体积/ 浓度/ 间/min
mL mL
I 25 0.5 4 0.1 6 0.2 12.7
II 80 0.5 4 0.1 6 0.2 a
Ⅲ 25 0.5 4 0.01 6 0.2 4.0
IV 25 0 4 0.01 6 0.2 b
下列说法不正确的是A.可通过相同时间内收集 的体积大小来判断反应速率快慢
B. ,
C.实验III中用酸性 溶液的浓度变化表示的反应速率
D.向实验中加入适量 固体会加快反应速率
变式5 化学反应速率的图象
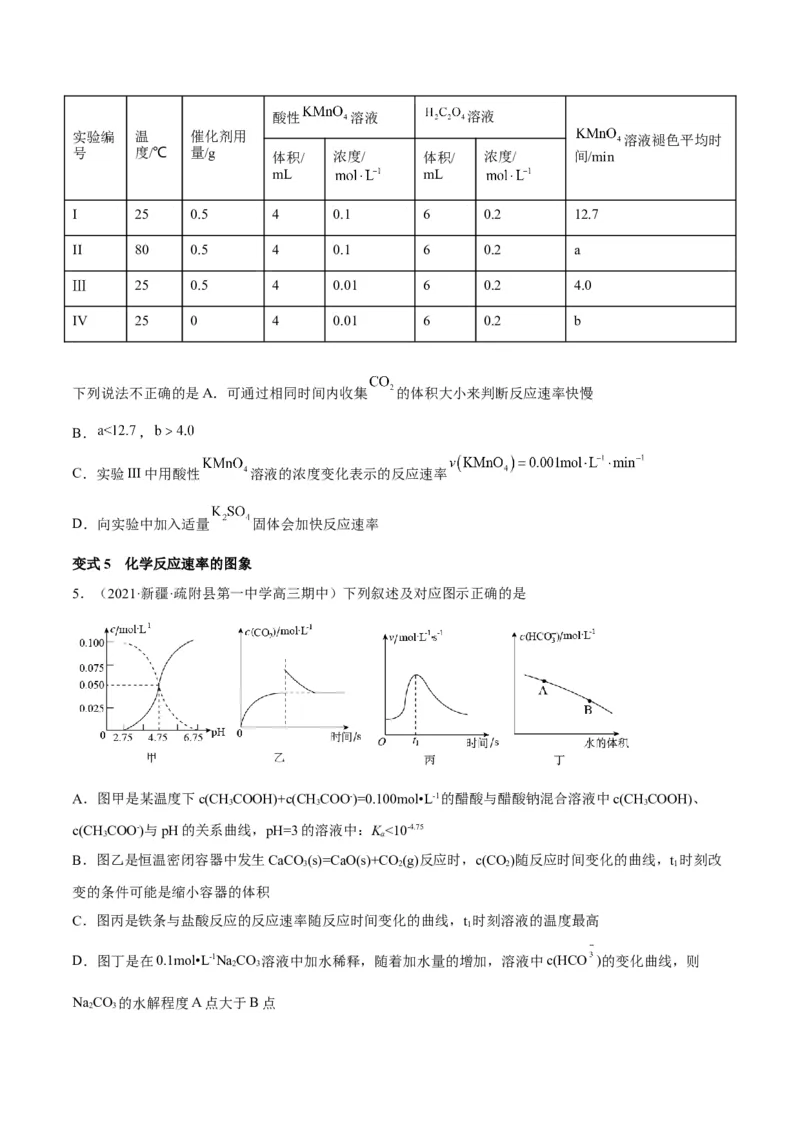
5.(2021·新疆·疏附县第一中学高三期中)下列叙述及对应图示正确的是
A.图甲是某温度下c(CHCOOH)+c(CH COO-)=0.100mol•L-1的醋酸与醋酸钠混合溶液中c(CHCOOH)、
3 3 3
c(CHCOO-)与pH的关系曲线,pH=3的溶液中:K <10-4.75
3 a
B.图乙是恒温密闭容器中发生CaCO (s)=CaO(s)+CO (g)反应时,c(CO)随反应时间变化的曲线,t 时刻改
3 2 2 1
变的条件可能是缩小容器的体积
C.图丙是铁条与盐酸反应的反应速率随反应时间变化的曲线,t 时刻溶液的温度最高
1
D.图丁是在0.1mol•L-1NaCO 溶液中加水稀释,随着加水量的增加,溶液中c(HCO )的变化曲线,则
2 3
NaCO 的水解程度A点大于B点
2 3变式6 化学反应速率的综合分析
6.(2021·河北·沧州市一中高三阶段练习)反应CO(g)+NO (g)=CO (g)+NO(g)的速率方程可表示为
2 2
v=k·cm(CO)·cn(NO ),其中k为与温度有关的常数,实验测得反应在650K时的数据如下:
2
实验编号 c(CO)/(mol·L-1) c(NO )/(mol·L-1) v/(mol·L-1·s-1)
2
① 0.025 0.040 2.2×10-4
② 0.050 0.040 4.4×10-4
③ 0.025 0.120 6.6×10-4
④ x y 8.8×10-4
⑤ 0.100 0.160 z
下列说法错误的是A.m=n=1 B.650K时k=0.22L·mol-1·s-1
C.若x=0.50,则y=0.080 D.z=3.52×10-3mol·L-1·s-1
1.(2018·全国·高三专题练习)反应4NH (g)+5O(g) 4NO(g)+6H O(g)在10 L密闭容器中进行,半分钟
3 2 2
后,水蒸气的物质的量增加了0.45 mol,则此反应的速率可表示为
A.υ(NH )=0.01 mol∙L−1∙s−1 B.υ(O )=0.001 mol∙L−1∙s−1
3 2
C.υ(NO)=0.001 mol∙L−1∙s−1 D.υ(H O)=0.045 mol∙L−1∙s−1
2
2.(2022·上海市彭浦中学高三期中)T℃时在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程
中X、Y、Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T 和T 时,Y的体积分数与
1 2
时间的关系如图2所示。则下列结论正确的是
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol/(L·min)
B.容器中发生的反应可表示为3X(g)+Y(g) 2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强3.(2022·江西·金溪一中高三阶段练习)我国科学家通过 和 合成淀粉,能够有效降低“碳排放”,
其中的一步反应为 ,一定温度下,向固定
容积为2L的密闭容器中充入 和 ,20min后反应达到平衡,容器内压强变为原来的75%。
下列有关说法正确的是
A.平衡时,
B. 内用 示的平均反应速率为
C.达到平衡后,再充入 和 , 、 的转化率均减小
D.达到平衡后,再充入 和 ,平衡正向移动
4.(2022·黑龙江·牡丹江市第三高级中学高三阶段练习)在 中,表示该反应
最快的是
A. B.
C. D.
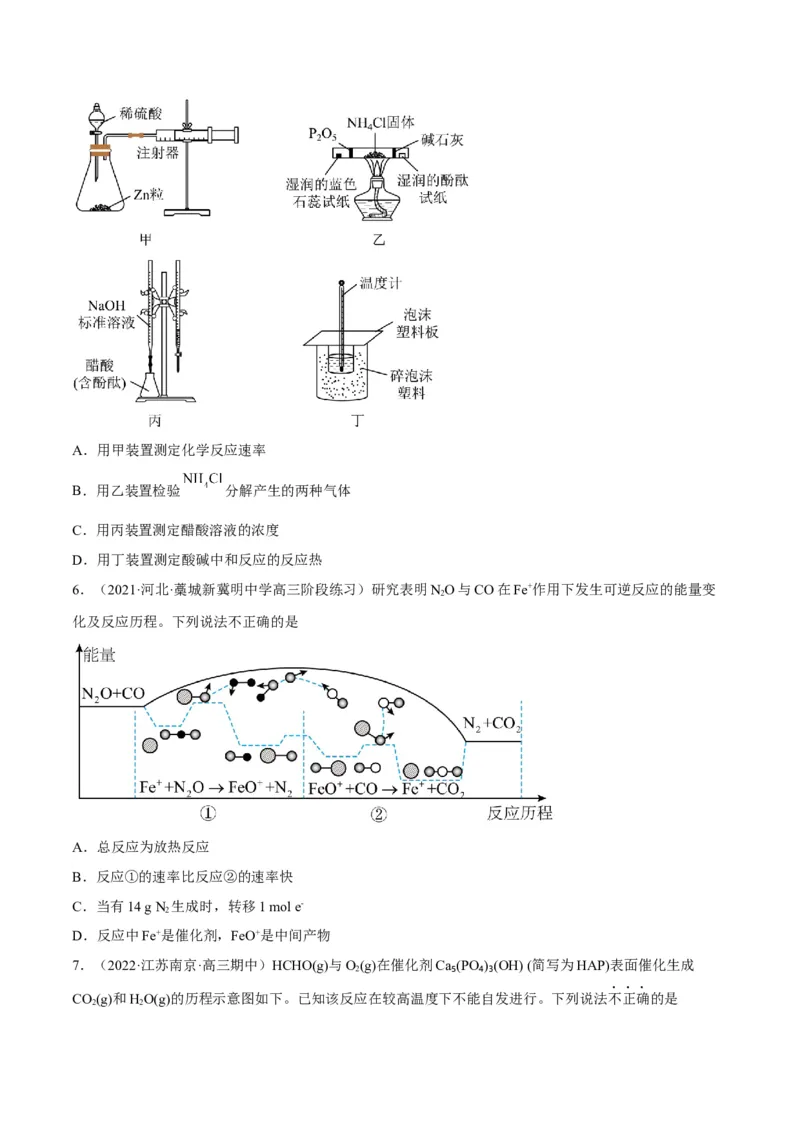
5.(2022·山东·高密三中高三阶段练习)一定温度下,利用下列装置进行实验,达不到实验目的的是A.用甲装置测定化学反应速率
B.用乙装置检验 分解产生的两种气体
C.用丙装置测定醋酸溶液的浓度
D.用丁装置测定酸碱中和反应的反应热
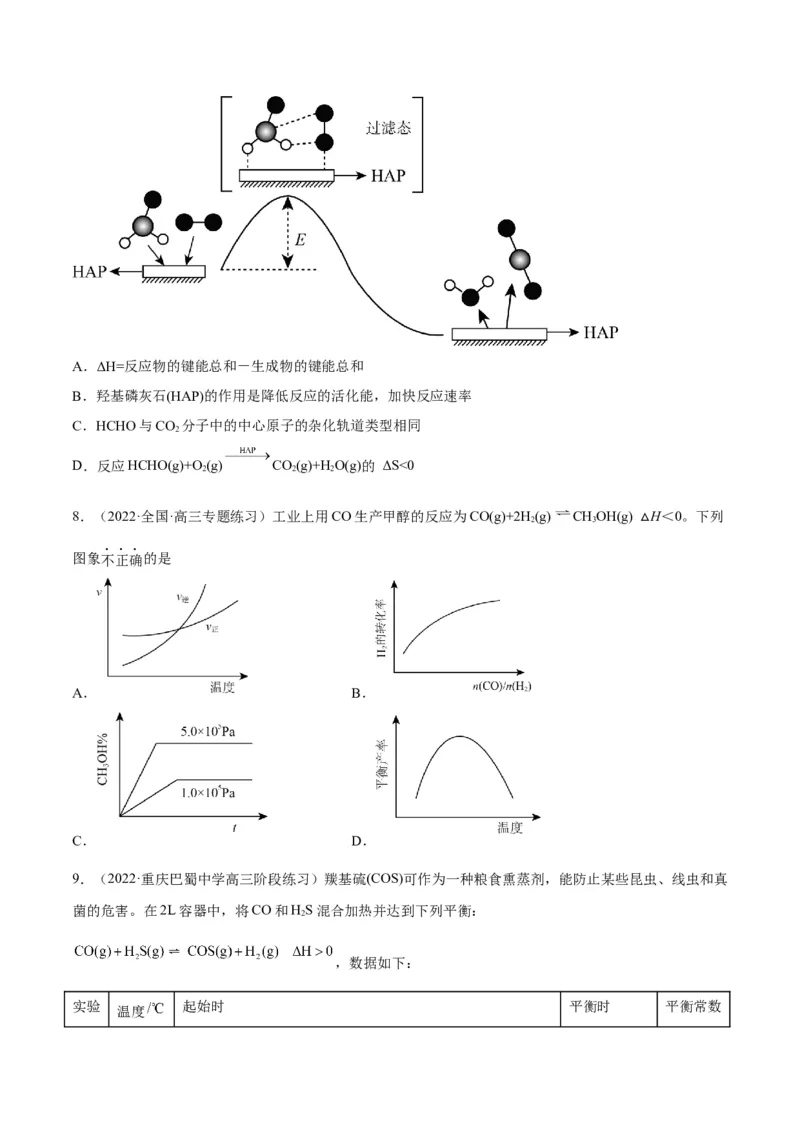
6.(2021·河北·藁城新冀明中学高三阶段练习)研究表明NO与CO在Fe+作用下发生可逆反应的能量变
2
化及反应历程。下列说法不正确的是
A.总反应为放热反应
B.反应①的速率比反应②的速率快
C.当有14 g N 生成时,转移1 mol e-
2
D.反应中Fe+是催化剂,FeO+是中间产物
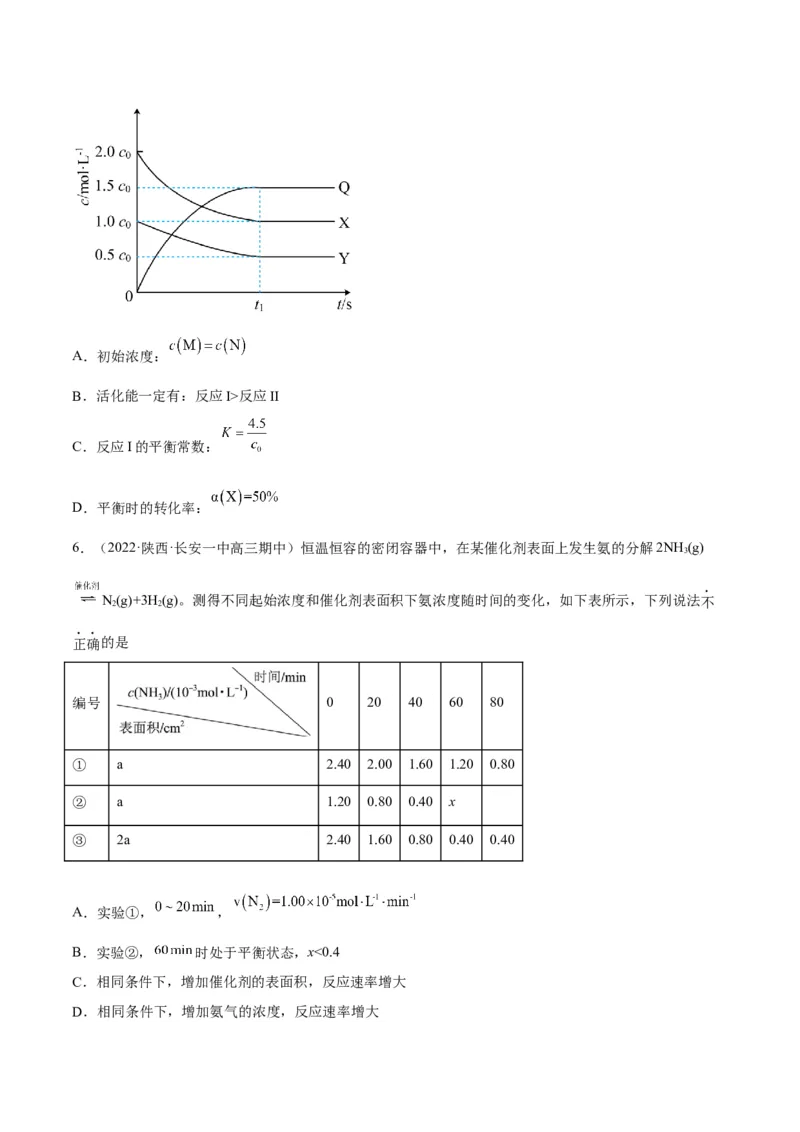
7.(2022·江苏南京·高三期中)HCHO(g)与O(g)在催化剂Ca₅(PO₄)₃(OH) (简写为HAP)表面催化生成
2
CO(g)和HO(g)的历程示意图如下。已知该反应在较高温度下不能自发进行。下列说法不正确的是
2 2A.ΔH=反应物的键能总和-生成物的键能总和
B.羟基磷灰石(HAP)的作用是降低反应的活化能,加快反应速率
C.HCHO与CO 分子中的中心原子的杂化轨道类型相同
2
D.反应HCHO(g)+O(g) CO(g)+HO(g)的 ΔS<0
2 2 2
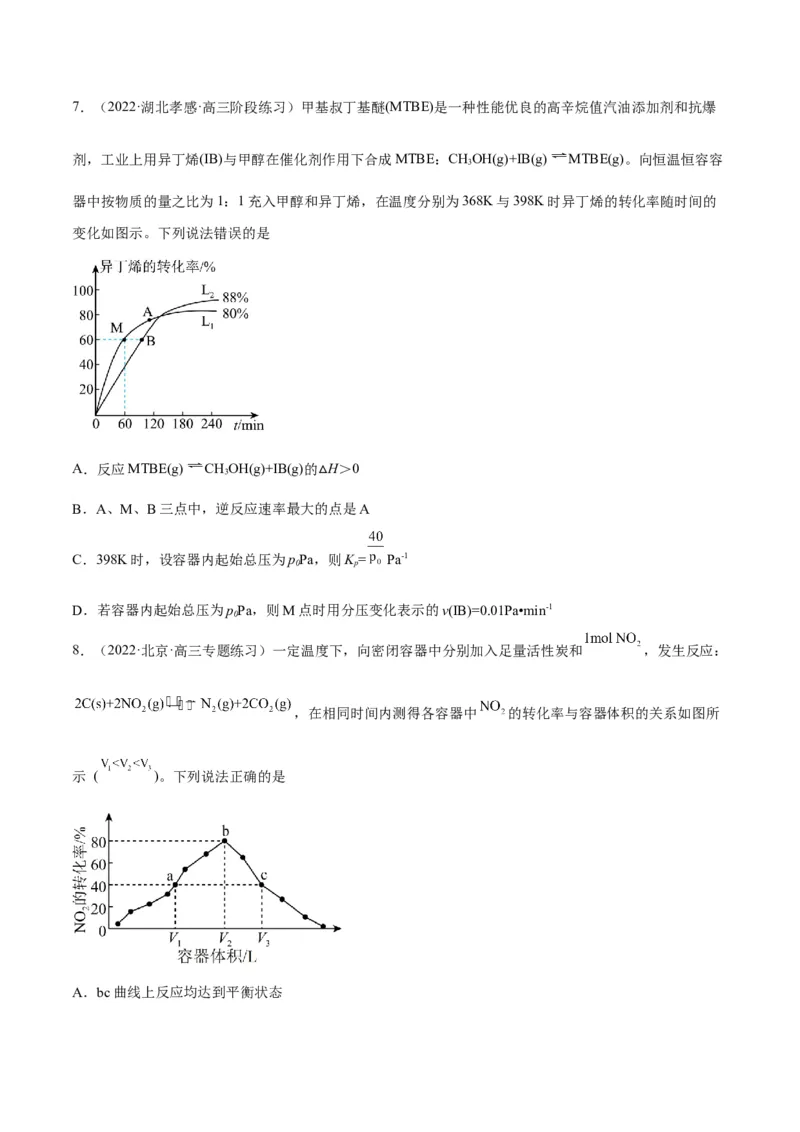
8.(2022·全国·高三专题练习)工业上用CO生产甲醇的反应为CO(g)+2H(g) CHOH(g) H<0。下列
2 3
△
图象不正确的是
A. B.
C. D.
9.(2022·重庆巴蜀中学高三阶段练习)羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真
菌的危害。在2L容器中,将CO和HS混合加热并达到下列平衡:
2
,数据如下:
实验 起始时 平衡时 平衡常数
温度1 0.200 0.200 0 0
2 0.200 0.200 0 0
3 0.400 0.400 0 0
下列判断错误的是A. B. 且
C.初始反应速率:实验3>实验2>实验1 D.通入 后,正反应速率逐渐增大
10.(2022·广东·蕉岭县蕉岭中学高三阶段练习)下列说法正确的是
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高化学反应速率越快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④ 的反应速率一定比 的反应速率大
⑤有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加单位体积内活化分子数,从而使
单位时间有效碰撞次数增多从而使反应速率增大
⑥若平衡正向移动,则平衡常数一定增大
⑦若化学平衡向逆反应方向移动,则正反应速率不一定减小
A.①②⑥ B.②⑤⑦ C.①②③⑤⑥ D.②④⑤
11.(2021·全国·高三专题练习)某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0,反
应物A的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
实验序
0 10 20 30 40 50 60
号
1 800℃ 1.0 0.80 0.67 0.57 0.50 0.50 0.50
2 800℃ c2 0.60 0.50 0.50 0.50 0.50 0.50
3 800℃ c3 0.92 0.75 0.63 0.60 0.60 0.60
4 820℃ 1.0 0.40 0.25 0.20 0.20 0.20 0.20根据上述数据,完成下列填空:
(1)在实验1中,反应在10至20分钟时间内的平均速率为___________mol·L-1·min-1。
(2)在实验2中,A的初始浓度c=___________mol·L-1。
2
(3)设实验3的反应速率为v,实验1的反应速率为v,则v___________v,且c___________1.0mol·L-1.(填
3 1 3 1 3
“>”“=”或“<”)
(4)比较实验4和实验1,可推测该反应是___________反应(填“吸热”或“放热”)。理由是___________。
核心考点二 化学平衡及平衡移动
一、化学平衡状态及移动方向判断
1.化学平衡状态的判断
(1)等——“逆向相等”(三种表述)。
①同一物质(两种表述):v正 =v逆 、断键数=成键数。
②不同物质:=
(2)定——“变量不变”:如果一个量是随反应进行而改变的(即变量),当其“不变”时反应就达到平衡状
态,即“变量”不变―→平衡状态。
(3)浓度标志
反应混合物中各组分的浓度不变是平衡状态的宏观表现,可逆反应中各组分的物质的量、浓度、百分含量、
气体的体积分数一定时,可逆反应达到平衡状态。
(4)混合气体的平均相对分子质量()标志
①当反应物与生成物均为气体时:对于反应前后气体分子数不等的反应,为定值可作为反应达到平衡状态
的标志;对于反应前后气体分子数相等的反应,为定值不能作为反应达到平衡状态的标志。
②若有非气体参与,无论反应前后气体的分子数是否相等,为定值一定可作为反应达到平衡状态的标志。
(5)混合气体的密度(ρ)标志
①当反应物与生成物均为气体时:在恒容条件下,无论反应前后气体分子数是否相等,ρ为定值,不能作
为反应达到平衡状态的标志;在恒压条件下,对于反应前后气体分子数相等的反应,ρ为定值,不能作为
反应达到平衡状态的标志,对于反应前后气体分子数不等的反应,ρ为定值,可作为反应达到平衡状态的
标志。
②当有非气体物质参与反应时:对于恒容体系,ρ为定值,可作为反应达到平衡状态的标志。
(6)混合气体的压强标志
因为恒容、恒温条件下,气体的物质的量n(g)越大则压强p就越大,则无论各成分是否均为气体,只需要
考虑Δn(g)。对于Δn(g)=0的反应,当p为定值时,不能作为反应达到平衡状态的标志;对于Δn(g)≠0的反
应,当p为定值时,可作为反应达到平衡状态的标志。(7)有色体系的颜色保持不变。
(8)依Q 与K关系判断:若Q=K,反应处于平衡状态。
c c
2.平衡移动方向的判断
(1)依勒夏特列原理判断。
(2)根据图像中正、逆反应速率相对大小判断:若v正 >v逆 ,则平衡向正反应方向移动;反之向逆反应方向
移动。
(3)依变化过程中速率变化的性质判断:若平衡移动过程中,正反应速率逐渐增大(减小),则平衡向逆(正)
反应方向移动。
(4)依浓度商(Q)规则判断:若某温度下QK,反应向逆反应方向进行。
c c c
二、化学反应进行的方向
(1)判据
(2)一般规律:
①ΔH<0,ΔS>0的反应任何温度下都能自发进行;
②ΔH>0,ΔS<0的反应任何温度下都不能自发进行;
③ΔH和ΔS的作用相反,且相差不大时,温度对反应的方向起决定性作用。当ΔH<0,ΔS<0时低温下反应
能自发进行;当ΔH>0,ΔS>0时,高温下反应能自发进行。
说明:对于一个特定的气相反应,熵变的大小取决于反应前后的气体物质的化学计量数大小。
考法 比较反应熵变、焓变确实反应方向及化学平衡状态判断(题型预测:选择
题)
1.(2022·江苏·徐州市第七中学高三阶段练习)在恒温恒压条件下,对于反应
下列有关说法正确的是A.该反应的 ,
B.当气体密度不变时能说明该反应达到化学平衡状态
C.其他条件不变,向平衡后的容器中再加入少量 达新平衡,与原平衡相比 的值减小
D.使用高效催化剂能增大反应的平衡常数
1.可逆反应不等同于可逆过程,可逆过程包括物理变化和化学变化,而可逆反应属于化学变化。
2.化学反应的平衡状态可以从正反应方向建立,也可以从逆反应方向建立。
3.化学反应达到平衡状态的正、逆反应速率相等,是指同一物质的消耗速率和生成速率相等,若用不同
物质表示时,反应速率不一定相等。
4.化学反应达平衡状态时,各组分的浓度、百分含量保持不变,但不一定相等。
5.判断化学平衡状态的方法——“正逆相等,变量不变”
—
|
—
6.浓度对化学平衡的影响:谁增耗谁,谁减补谁。但不能将外加条件削减为0,此规律只适用于气态或溶
液中的平衡混合物。对固体、纯液体来说,其浓度是常数,改变它们的量平衡不移动。
7.构建“过渡态”判断两个平衡状态的联系
(1)构建等温等容平衡思维模式:新平衡状态可认为是两个原平衡状态简单的叠加并压缩而成,相当于增大
压强。
(2)构建等温等压平衡思维模式(以气体物质的量增加的反应为例,见图示):新平衡状态可以认为是两个原
平衡状态简单的叠加,压强不变,平衡不移动。
8.焓变、熵变和温度对化学反应方向的影响ΔH ΔS ΔH-TΔS 反应情况
- + 永远是负值 在任何温度下过程均自发进行
+ - 永远是正值 在任何温度下过程均非自发进行
+ + 低温为正高温为负 低温时非自发,高温时自发
- - 低温为负高温为正 低温时自发,高温时非自发
变式1 化学反应的自发进行
1.(2022·浙江·高三专题练习)在低温条件下,下列过程能自发进行的是
A.Na→Na ++e- B.HO(g)→H O(l)
2 2
C.NH Cl→NH↑+HCl↑ D.Cu+H SO →CuSO +H ↑
4 3 2 4 4 2
变式2 化学反应进行的方向
2.(2022·广东·东莞市万江中学高三阶段练习)下列有关化学反应方向及其判据的说法中错误的是
A.1mol 在不同状态时的嫡值:
B.反应 能否自发进行与温度有关
C. 分解和HClO分解均是自发过程,故这两个反应的 和 的变化相同
D.常温下,反应 能自发进行,则该反应的
变式3 化学平衡状态的判断
3.(2022·黑龙江·哈尔滨三中高三期中)将一定量纯净的氨基甲酸铵固体置于密闭真空容器中(假设容器
体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡
。能判断该反应已经达到化学平衡的是
①
②密闭容器中氨气的物质的量浓度不变
③密闭容器中混合气体的密度不变
④混合气体的平均相对分子质量不变
⑤密闭容器混合气体的总物质的量不变
⑥形成6mol N-H键同时消耗44gA.②③⑤⑥ B.①②⑤⑥ C.①③⑤⑥ D.全部
1.(2022·全国·高三专题练习)向容积为2L的密闭容器中充入2molX气体和1mo1Y气体,在一定条件下
发生如下反应:2X(g)+Y(g) 3R(g);经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误
的是
A.用物质Y表示该反应在2s内的平均反应速率为0.1mol/(L·s)
B.平衡时物质X与Y的转化率相等
C.0~2s时间段内,v >v
正 逆
D.4molX(g)和2molY(g)在密闭容器中反应可得得到6molR(g)
2.(2022·安徽·高三阶段练习)一定温度下,向一个体积可变的密闭容器中充入 气体,发生反应:
。下列能说明该反应达到平衡状态的是
A.容器的体积不再发生变化 B.气体的平均相对分子质量不再变化
C.气体的颜色不再发生变化 D. 的分解速率为 的生成速率的2倍
3.(2022·江西·南昌二中高三阶段练习)我国科学家王亮在CO 合成燃料CH 的催化剂选择方面取得了重
2 4
大突破,其反应原理如下:CO(g)+4H(g) CH(g)+2HO(g) △H=-165.0kJ·mol-1 ,在恒容密闭容器中通入
2 2 4 2
1 mol CO 与4 mol H ,下列情形能表示该反应达到平衡状态的是
2 2
A.容器内混合气体的平均摩尔质量不再改变B.容器内气体的密度不再改变
C. 的值保持不变 D.v (CO)=4 v(H )
正 2 逆 2
4.(2022·上海市育才中学高三期中) 和 存在平衡: 。下列说
法正确的是
A.1mol平衡混合气体中含1molN原子
B.恒容时,温度升高,则平衡逆向移动,正反应速率减小
C.若要测定 的相对分子质量,应采用“高温低压”条件
D.恒温时,缩小容器体积,气体颜色变深,这是平衡正向移动导致的
5.(2022·上海市宜川中学高三期中)氯气溶于水达到平衡后,若只改变某一条件,下列叙述正确的是
A.通入少量SO ,溶液漂白性增强
2B.加入少量NaHCO 固体,c(ClO-)减小
3
C.加入少量水,水的电离平衡向逆方向移动
D.加入NaOH固体至恰好完全反应,一定有c(Na+)=c(Cl-)+c(ClO-)+c(HClO)
6.(2022·北京·101中学高三阶段练习)下列实验方案能达实验目的的是
A.图1探究温度对平衡的影响
B.图2探究浓度对化学平衡的影响
C.图3探究浓度对化学反应速率的影响
D.图4探究碳酸、醋酸苯酚的酸性强弱
7.(2023·重庆·高三阶段练习)某实验小组将足量 置于温度为T℃、体积为V的密闭容器中,
发生反应 ,测出总压p随时间的变化如下图中A曲线所示。下列
有关说法正确的是
A.在T℃时,该反应压强平衡常数为
B.若在 时刻减小体积为 ,则容器内压强变化为曲线B
C.若减少适量 ,平衡向逆反应方向移动D.若充入少量 ,发生反应 ,T℃达平衡时,与原平衡相
比, 的分压减小, 的分压增大
8.(2022·广东·蕉岭县蕉岭中学高三阶段练习)下列事实能用勒夏特列原理来解释的是
A. 、 、HI平衡混合气体加压后颜色加深
B. 左右的温度比室温更有利于合成氨反应
C.实验室采用排饱和食盐水的方法收集氯气
D. 被氧化为 ,往往需要使用催化剂
9.(2022·黑龙江·哈尔滨三中高三期中)向一容积固定的容器中充入2mol (g)发生反应:
。达到平衡后,保持温度不变,继续向该容器中充入1mol (g)则
达到新平衡时 (g)的体积分数率将
A.变大 B.变小 C.不变 D.无法判断
10.(2021·上海市吴淞中学高三阶段练习)某温度下,反应2A(g) B(g)-Q(Q>0)在密闭容器中达到平衡,
⇌
平衡后 ,若改变某一条件,足够时间后反应再次达到平衡状态,此时 ,下列叙述正确的是
A.若其他条件不变,升高温度,则ab
C.若保持温度、容积不变,充入少量B气体,则a0
2
C.N(g)+3H(g)=2NH (g ) △H<0
2 2 3
D.CaCO (s)=CaO(s)+CO (g) △H>0
3 2
核心考点三 化学平衡常数及转化率的计算
一、化学平衡常数与转化率的计算
1.化学平衡常数表达式的书写
(1)不要把反应体系中纯固体、纯液体以及稀水溶液中水的浓度写进平衡常数表达式。如:
CaCO (s) CaO(s)+CO(g) K=c(CO)
3 2 2
Cr O(aq)+HO(l) 2CrO(aq)+2H+(aq) K=
2 2
但在非水溶液中,若有水参加或生成,则此时水的浓度不可视为常数,应写进平衡常数表达式中。如:
C HOH+CHCOOH CHCOOC H+HO K=
2 5 3 3 2 5 2
C(s)+HO(g) CO(g)+H(g) K=
2 2
(2)同一化学反应,化学反应方程式写法不同,其平衡常数表达式及数值亦不同。如:
NO(g) 2NO (g) K=
2 4 2
NO(g) NO (g) K′==
2 4 2
(3)有气体参与的反应,用平衡分压(总压乘以各自的物质的量分数)表示平衡常数。
如:2A(g)+B(s) C(g)。若达到平衡时,n(A)=n、n(C)=n 密闭体系的压强为p,则K ==。
1 2 p
2.化学平衡常数(K)的应用
(1)K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,即该反应进行得越完全,
反应物转化率越大;反之,就越不完全,转化率就越小。
(2)若用任意状态的浓度幂之积的比值(称为浓度商,用Q表示)与K比较,可判断可逆反应是否达到平衡状态和反应进行的方向。即对于反应mA(g)+nB(g) pC(g)+qD(g),Q=。
QK 反应向逆反应方向进行
(3)利用K可判断反应的热效应。
若升高温度,K值增大,则正反应为吸热反应;
若升高温度,K值减小,则正反应为放热反应。
3.化学平衡常数与转化率的计算
(1)牢记一个万能模式(“三段式”法)
如mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量浓度分别为a mol·L-1、b mol·L-1,达到平
衡后消耗A的物质的量浓度为mx mol·L-1。
mA(g)+nB(g) pC(g)+qD(g)
起始/(mol·L-1) a b 0 0
变化/(mol·L-1) mx nx px qx
平衡/(mol·L-1) a-mx b-nx px qx
K=
(2)掌握三个百分数
①转化率=×100%=×100%
②生成物的产率:实际产量(指生成物)占理论产量的百分数。一般来讲,转化率越大,原料利用率越高,
产率越大。
产率=×100%
③平衡混合物某组分的百分含量=×100%
考法 化学平衡常数概念的理解及其运用(题型预测:选择题)
1.(2022·江苏省如东高级中学高三开学考试)对于反应4NH (g)+5O(g) 4NO(g)+6H O(g),下列说法
3 2 2
正确的是
A.上述反应的平衡常数表达式K=
B.增大起始反应物中 ,可以提高NH 的转化率
3C.4molNH 与足量氧气充分反应后,转移电子的数目等于20×6.02×1023
3
D.研发更高效的催化剂,可以缩短达到平衡所需的时间及提高NH 的平衡转化率
3
1.不同反应化学平衡常数的关系
(1)同一化学反应,化学反应方程式写法不同,其平衡常数表达式及数值亦不同。如:
K=
NO(g) 2NO (g)
2 4 2
K′==
NO(g) NO (g)
2 4 2
K″==
2NO (g) NO(g)
2 2 4
因此书写平衡常数表达式及数值时,要与化学反应方程式相对应,否则意义就不明确。
(2)不同的化学反应,可利用已知反应,找到不同反应化学平衡常数(K)之间的关系。
Ⅰ.若两反应之和等于第三个反应,即反应①(平衡常数K )+反应②(K )=反应③(K )
1 2 3
则K =K ·K
3 1 2
如:①C(s)+HO(g) CO(g)+H(g) K
2 2 1
②CO(g)+HO(g) CO(g)+H(g) K
2 2 2 2
①+②得反应C(s)+2HO(g) CO(g)+2H(g) K
2 2 2 3
则K =K ·K
3 1 2
Ⅱ.若两反应之差等于第三个反应,即反应④(平衡常数K )-反应⑤(K )=反应⑥(K )
4 5 6
则K =
6
(3)对于气体反应,写平衡常数关系式时,除可以用平衡时的物质的量浓度表示外,也可以用平衡时各气体
的分压来表示,例如:
N(g)+3H(g) 2NH (g)
2 2 3
K =
p
[注意] p(NH )、p(N )、p(H )分别为NH 、N 、H 的平衡分压,某气体平衡分压=平衡时总压×该气体的
3 2 2 3 2 2
物质的量分数。
2.化学平衡计算的一般方法——“三段式法”
对于反应:mA(g)+nB(g) pC(g)+qD(g),令A、B起始物质的量(mol)分别为a、b,达到平衡后,A
的消耗量为mx,容器容积为V L。
mA(g) + n(B)(g) pC(g)+qD(g)
起始(mol) a b 0 0
变化(mol) mx nx px qx
平衡(mol) a-mx b-nx px qx建立等式求解:
(1)K=
(2)c(A) = mol·L-1
平
(3)α(A) =×100%
平
α(A)∶α(B)=∶=
(4)φ(A)=×100%
(5)=
(6)(混)= g·L-1
变式1 化学平衡常数的表达式
1.(2022·江苏·海门中学高三阶段练习)用活性炭与NO 反应:为2C(s)+2NO (g) 2CO(g)+N(g)
2 2 2 2
来消除氮氧化物产生的空气污染。下列说法正确的是 ⇌
A.该反应只在高温条件下能自发进行
B.该反应平衡常数的表达式为
C.该反应中消耗1molNO ,转移电子的数目为
2
D.该反应到达平衡后,升高温度,正反应速率减慢,逆反应速率加快
变式2 利用化学平衡常数判断反应进行的方向
2.(2021·河南·确山县第二高级中学高三期中)已知:2Fe3+(aq)+2I-(aq) 2Fe2+(aq)+I (aq),向试管中滴
2
加1mL0.1mol/LKI溶液与5mL0.1mol/LFeCl 溶液,反应达到平衡时,下列说法错误的是
3
A.该反应平衡常数K=
B.加入FeSO 固体,平衡逆向移动
4
C.加入苯,振荡,平衡正向移动
D.经苯两次萃取分离后,在水溶液中加入KSCN,溶液呈红色,则该化学反应存在限度
变式3 化学平衡常数的运用
3.(2022·四川省内江市第六中学高三开学考试) 也是一种很好的消毒剂,具有高效、洁净、方便、经
济等优点。 可溶于水,在水中易分解,产生的 为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应① ,平衡常数为 ;
反应② ,平衡常数为 ;
总反应: ,平衡常数为K。
下列叙述正确的是
A.升高温度,K增大 B.
C.适当升温可提高消毒效率 D.压强增大, 减小
变式4 有关化学平衡“三段式”计算
4.(2022·全国·高三专题练习)目前,大规模和低成本制取氢能实质上都是通过烃重整实现的,该过程主
要是甲烷水蒸气重整,甲烷水蒸气重整得到的CO 和H,也可用来制备甲醇,反应方程式CO(g)+3H(g)
2 2 2 2
CHOH(g)+H O(g) ∆H<0,某温度下,将1molCO 和1molH 充入体积不变的2L密闭容器中,初始总
3 2 2 2
压为8MPa,发生上述反应,测得不同时刻反应后与反应前的压强关系如表:
时间/h 1 2 3 4 5
0.92 0.85 0.79 0.75 0.75
用CO 表示前2h的平均反应速率v(CO)=_____mol/(L•h)。
2 2
1.(2019·江西·南昌十中高三阶段练习)在恒容密闭容器中,由CO合成甲醇:CO(g)+2H(g)
2
CHOH(g),在其他条件不变的情况下,研究温度对反应的影响,实验结果如图所示,下列说法正确的是
3
A.CO合成甲醇的反应为吸热反应B.平衡常数K=
C.该反应在T 时的平衡常数比T 时的小
1 2
D.处于A点的反应体系从T 变到T,达到平衡时 增大
1 2
2.(2022·江苏南京·高三期中)一定温度下,在2个容积均为1 L的密闭容器中,充入一定量的反应物,
发生反应:2NO(g)+2CO(g) N(g)+2CO (g) ΔH<0,相关反应数据如下表所示:
2 2
起始时物质的量/mol 10 s时物质的量/mol
容器编号 温度
NO CO N
2
Ⅰ T℃ 0.2 0.2 0.05
1
Ⅱ T℃(T >T) 0.2 0.2 0.05
2 2 1
下列说法正确的是A.10 s时,容器Ⅰ中的反应处于平衡状态
B.10 s时,容器Ⅰ中的化学反应速率v(CO)=0.005mol·L-1·s-1
2
C.化学平衡常数:K >K
Ⅱ Ⅰ
D.若起始时,向容器Ⅱ中充入0.08 mol NO、0.1 mol CO、0.04 mol N 和0.1 mol CO ,反应将向逆反应方
2 2
向进行
3.(2022·重庆市万州第二高级中学高三阶段练习) 排放到空气中会引起酸雨等环境问题,严重危害
人类健康。 的水溶液中存在下列平衡:
已知: 、 、 为各步反应的平衡常数,且 [ 表示 的平衡压强]。下列说
法正确的是
A.由图平衡可知 溶液和 溶液都可以水解,溶液一定呈碱性B.氨水也可吸收 ,防止大气污染,同时通入 能进一步提高 去除率
C.当 的平衡压强为p时,测得 ,则溶液
D.用 的 溶液吸收0.2mol的 ,则溶液中存在关系式:
4.(2022·北京师大附中高三阶段练习)相同温度下,分别在起始体积均为1L的两个密闭容器中发生反应:
。实验测得反应的有关数据如下表。
起始物质的量/mol
容
反应条件 达到平衡所用时间/min 达平衡过程中的能量变化
器
① 恒容 1 3 0 10 放热
② 恒压 1 3 0 t 放热
下列叙述正确的是A.
B.反应的平衡常数K:①<②
C.①中:从开始至10min内的平均反应速率
D.②中: 的平衡转化率小于10%
5.(2022·广东·高三阶段练习)某温度下,在一恒容密闭容器中进行如下两个反应并达到平衡:
反应I:
反应II:
如图是部分组分浓度随时间变化曲线,平衡时M、N浓度相等。该温度下,下列说法不正确的是A.初始浓度:
B.活化能一定有:反应I>反应II
C.反应I的平衡常数:
D.平衡时的转化率:
6.(2022·陕西·长安一中高三期中)恒温恒容的密闭容器中,在某催化剂表面上发生氨的分解2NH (g)
3
N(g)+3H(g)。测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不
2 2
正确的是
编号 0 20 40 60 80
① a 2.40 2.00 1.60 1.20 0.80
② a 1.20 0.80 0.40 x
③ 2a 2.40 1.60 0.80 0.40 0.40
A.实验①, ,
B.实验②, 时处于平衡状态,x<0.4
C.相同条件下,增加催化剂的表面积,反应速率增大
D.相同条件下,增加氨气的浓度,反应速率增大7.(2022·湖北孝感·高三阶段练习)甲基叔丁基醚(MTBE)是一种性能优良的高辛烷值汽油添加剂和抗爆
剂,工业上用异丁烯(IB)与甲醇在催化剂作用下合成MTBE:CHOH(g)+IB(g) MTBE(g)。向恒温恒容容
3
器中按物质的量之比为1:1充入甲醇和异丁烯,在温度分别为368K与398K时异丁烯的转化率随时间的
变化如图示。下列说法错误的是
A.反应MTBE(g) CHOH(g)+IB(g)的 H>0
3
△
B.A、M、B三点中,逆反应速率最大的点是A
C.398K时,设容器内起始总压为pPa,则K = Pa-1
0 p
D.若容器内起始总压为pPa,则M点时用分压变化表示的v(IB)=0.01Pa•min-1
0
8.(2022·北京·高三专题练习)一定温度下,向密闭容器中分别加入足量活性炭和 ,发生反应:
,在相同时间内测得各容器中 的转化率与容器体积的关系如图所
示 ( )。下列说法正确的是
A.bc曲线上反应均达到平衡状态B.容器内的压强:
C.a、c两点时气体的颜色相同
D.该温度下,a、b、c三点时反应的平衡常数:
9.(2022·上海市杨浦高级中学高三阶段练习)氮、碳氧化物的无害化处理是研究的热点。一定条件下
发生如下反应:
Ⅰ.
Ⅱ.
完成下列填空:
(1)反应Ⅰ平衡常数的表达式K=_______。
(2)某温度下,反应Ⅰ的 ,该温度下,测得容器中 、 、 的浓度分别为 、
、 ,此时,反应Ⅰ是否处于平衡状态?若不是,预测反应的方向。_______
(3)甲为10L的恒温容器。盛有 和1mol CO,发生反应Ⅰ和反应Ⅱ,5min时,测得CO转化率为
60%, ,则 _______mol;0~5min, 的平均反应速率 _______
。
(4)乙为10L的绝热容器。向其中充入 和1mol CO,发生反应Ⅰ和反应Ⅱ,乙中反应达到平衡的时
间_______甲;此时乙中 比甲中_______(以上两空选填“>”“<”或“=”),理由是:_______。
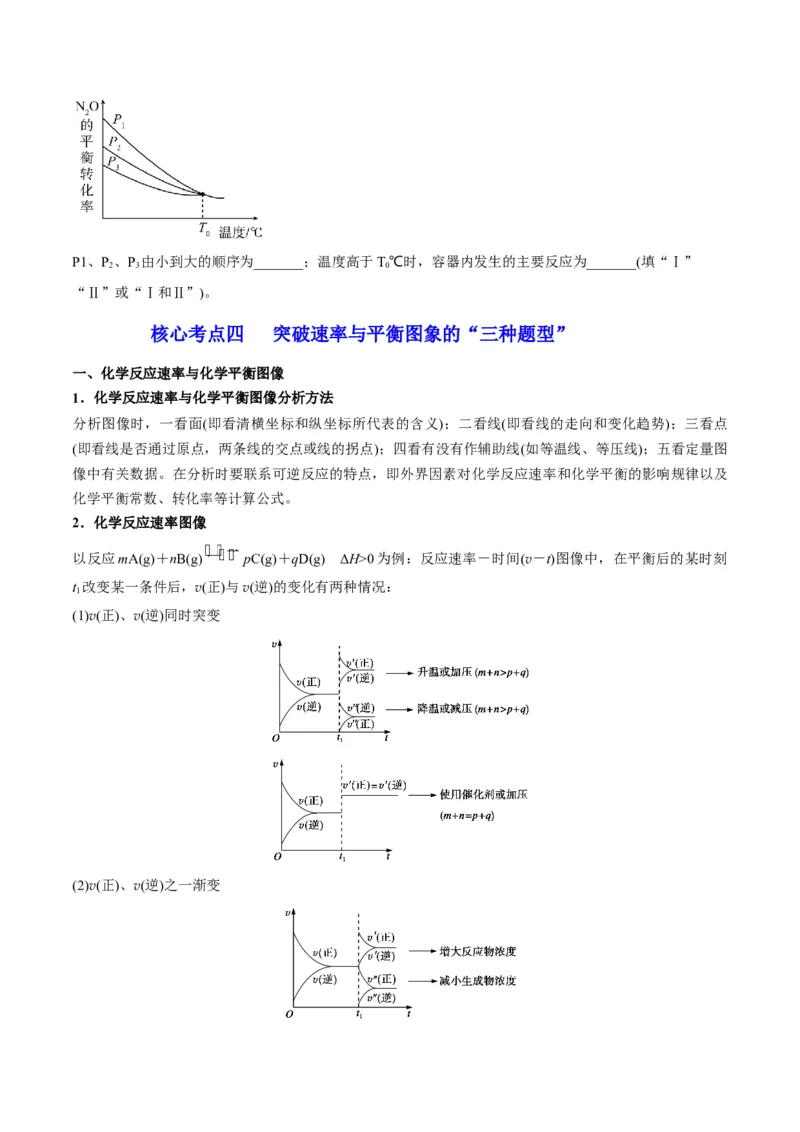
(5)不同压强的密闭容器中,分别充入 和1mol CO,发生反应Ⅰ和反应Ⅱ,测得 的平衡转化
率与温度的关系如图所示。P1、P、P 由小到大的顺序为_______;温度高于T℃时,容器内发生的主要反应为_______(填“Ⅰ”
2 3 0
“Ⅱ”或“Ⅰ和Ⅱ”)。
核心考点四 突破速率与平衡图象的“三种题型”
一、化学反应速率与化学平衡图像
1.化学反应速率与化学平衡图像分析方法
分析图像时,一看面(即看清横坐标和纵坐标所代表的含义);二看线(即看线的走向和变化趋势);三看点
(即看线是否通过原点,两条线的交点或线的拐点);四看有没有作辅助线(如等温线、等压线);五看定量图
像中有关数据。在分析时要联系可逆反应的特点,即外界因素对化学反应速率和化学平衡的影响规律以及
化学平衡常数、转化率等计算公式。
2.化学反应速率图像
以反应mA(g)+nB(g) pC(g)+qD(g) ΔH>0为例:反应速率-时间(v-t)图像中,在平衡后的某时刻
t 改变某一条件后,v(正)与v(逆)的变化有两种情况:
1
(1)v(正)、v(逆)同时突变
(2)v(正)、v(逆)之一渐变3.化学平衡图像的三种类型
对于反应mA(g)+nB(g) pC(g)+qD(g),m+n>p+q,且ΔH>0。
(1)速率—时间图
t 时增大反应物的浓度,正反应速率瞬间增大,然后逐渐减小,而逆反应速率逐渐增大;t 时升高温度,对
1 2
任何反应,正反应和逆反应速率均增大,吸热反应的正反应速率增大较快;t 时减小压强,正反应速率和
3
逆反应速率均减小;t 时使用催化剂,正反应速率和逆反应速率均瞬间增大。
4
(2)转化率(或含量)—时间图
甲表示压强对反应物转化率的影响,对于气体反应物化学计量数之和大于气体生成物化学计量数之和的反
应,压强越大,反应物的转化率越大;乙表示温度对反应物转化率的影响,对于吸热反应,温度越高,反
应物的转化率越大;丙表示催化剂对反应物转化率的影响,催化剂只能改变化学反应速率,不能改变平衡
时反应物的转化率。
(3)恒压(温)线
分析时可沿横轴作一条平行于纵轴的虚线,即为等压线或等温线,然后分析另一条件变化对该反应的影响。
考法 分析外界条件对化学平衡的影响(题型预测:选择题)
1.(2022·山西吕梁·高三阶段练习)下列图示与对应的叙述相符的是A.图一表示反应 在一定温度下达到平衡时B的转化率与压强变化的关系,x点的
反应速率比y点的快
B.图二表示反应 的速率一时间图象,在 时刻改变的条件可,能是加入催化
剂或增大压强
C.图三表示反应 中A的百分含量与温度(T)的变化情况,则该反应的
D.图四所示图中的阴影部分面积的含义是( )
1.化学平衡图像题的解题流程
2.等效平衡判断“四步曲”
:观察可逆反应特点(物质状态、气体分子数),判断反应是反应前后气体体积不变的可逆反应还是反应前
后气体体积改变的可逆反应;:挖掘反应条件,是恒温恒容还是恒温恒压,注意密闭容器不等于恒容容器;
:采用一边倒法,将起始物质按可逆反应化学计量数之比转化成同一边的物质;
:联系等效平衡判断依据,结合题目条件判断是否达到等效平衡。
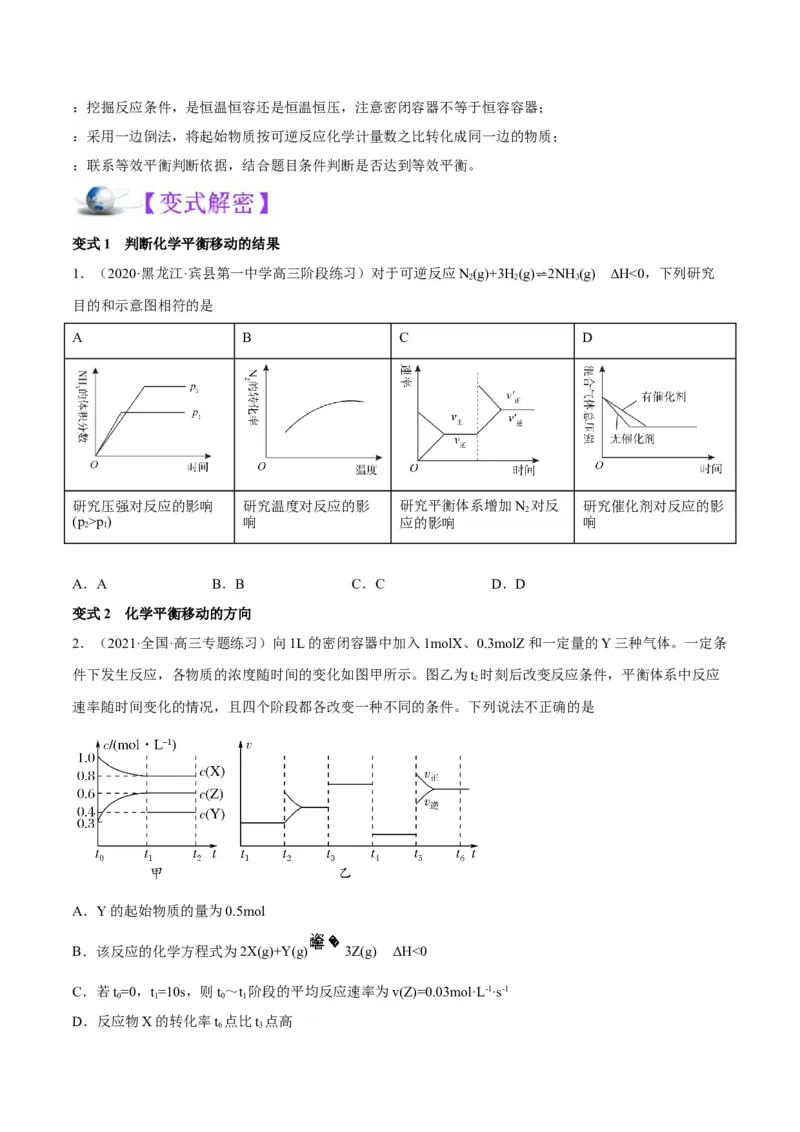
变式1 判断化学平衡移动的结果
1.(2020·黑龙江·宾县第一中学高三阶段练习)对于可逆反应N
2
(g)+3H
2
(g)⇌2NH
3
(g) ΔH<0,下列研究
目的和示意图相符的是
A B C D
研究压强对反应的影响 研究温度对反应的影 研究平衡体系增加N 对反 研究催化剂对反应的影
2
(p>p) 响 应的影响 响
2 1
A.A B.B C.C D.D
变式2 化学平衡移动的方向
2.(2021·全国·高三专题练习)向1L的密闭容器中加入1molX、0.3molZ和一定量的Y三种气体。一定条
件下发生反应,各物质的浓度随时间的变化如图甲所示。图乙为t 时刻后改变反应条件,平衡体系中反应
2
速率随时间变化的情况,且四个阶段都各改变一种不同的条件。下列说法不正确的是
A.Y的起始物质的量为0.5mol
B.该反应的化学方程式为2X(g)+Y(g) 3Z(g) ΔH<0
C.若t=0,t=10s,则t~t 阶段的平均反应速率为v(Z)=0.03mol·L-1·s-1
0 1 0 1
D.反应物X的转化率t 点比t 点高
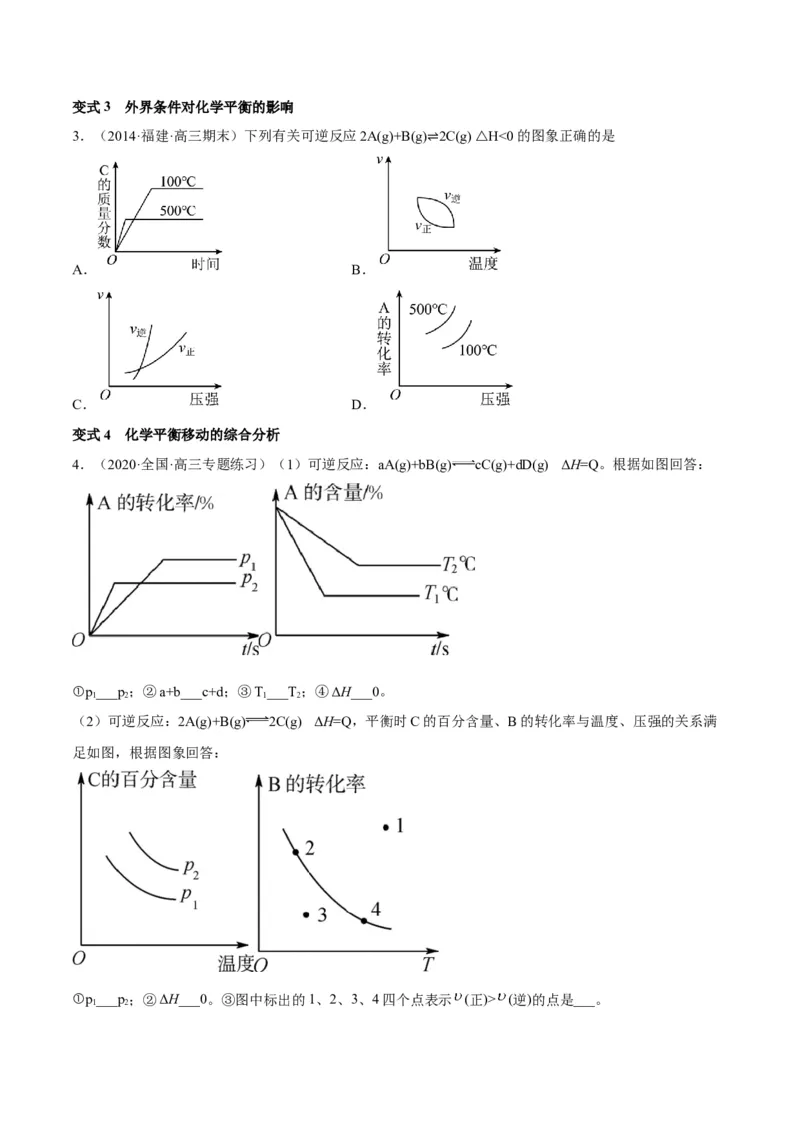
6 3变式3 外界条件对化学平衡的影响
3.(2014·福建·高三期末)下列有关可逆反应2A(g)+B(g) 2C(g) △H<0的图象正确的是
⇌
A. B.
C. D.
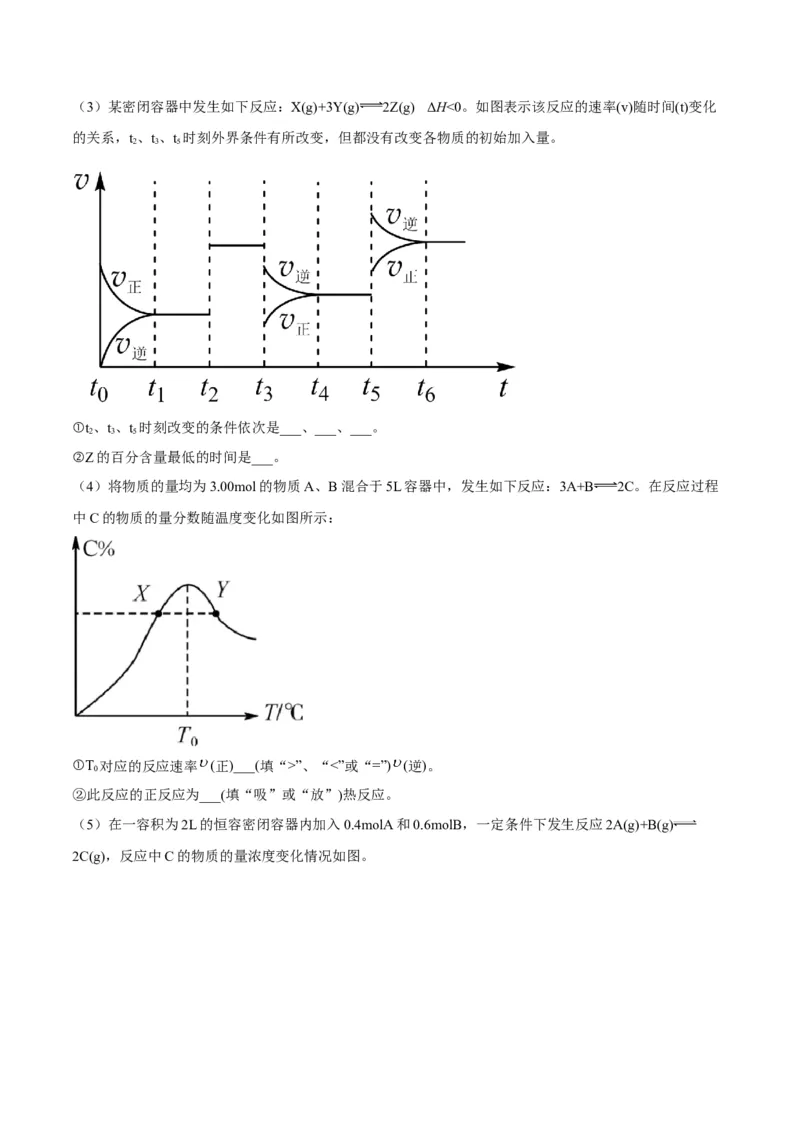
变式4 化学平衡移动的综合分析
4.(2020·全国·高三专题练习)(1)可逆反应:aA(g)+bB(g) cC(g)+dD(g) ΔH=Q。根据如图回答:
①p___p;②a+b___c+d;③T___T;④ΔH___0。
1 2 1 2
(2)可逆反应:2A(g)+B(g) 2C(g) ΔH=Q,平衡时C的百分含量、B的转化率与温度、压强的关系满
足如图,根据图象回答:
①p___p;②ΔH___0。③图中标出的1、2、3、4四个点表示 (正)> (逆)的点是___。
1 2(3)某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化
的关系,t、t、t 时刻外界条件有所改变,但都没有改变各物质的初始加入量。
2 3 5
①t、t、t 时刻改变的条件依次是___、___、___。
2 3 5
②Z的百分含量最低的时间是___。
(4)将物质的量均为3.00mol的物质A、B混合于5L容器中,发生如下反应:3A+B 2C。在反应过程
中C的物质的量分数随温度变化如图所示:
①T 对应的反应速率 (正)___(填“>”、“<”或“=”) (逆)。
0
②此反应的正反应为___(填“吸”或“放”)热反应。
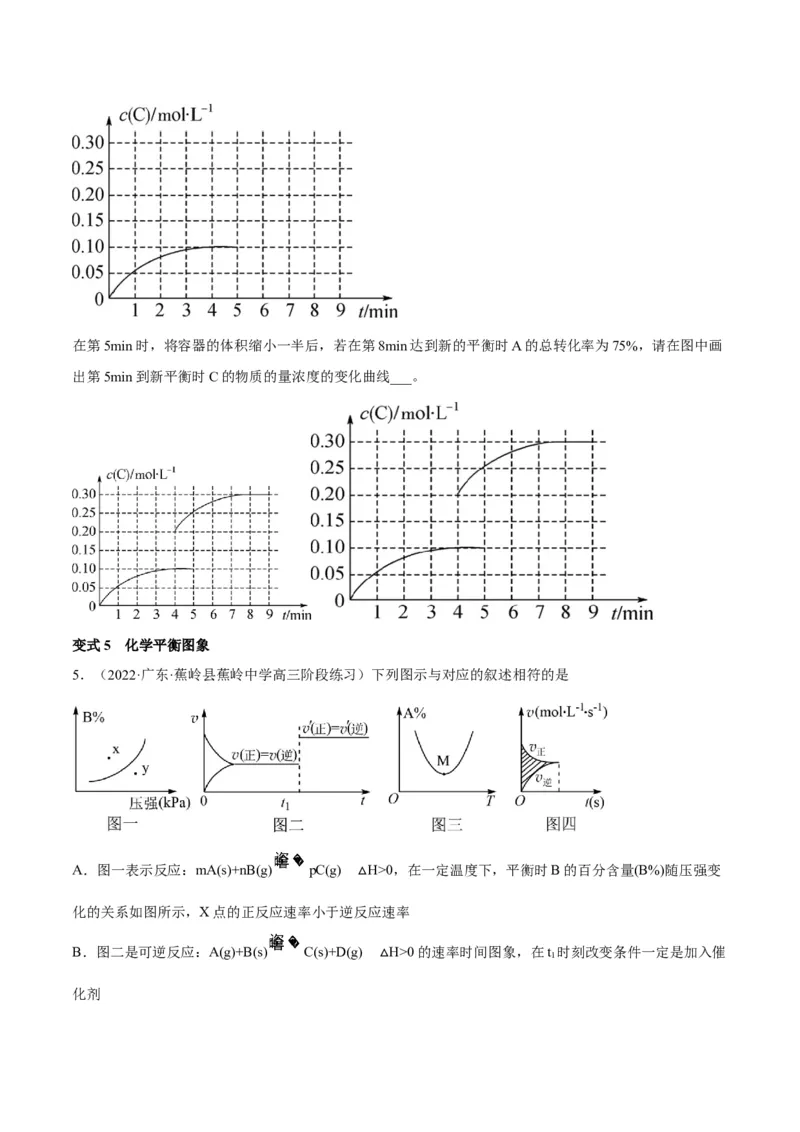
(5)在一容积为2L的恒容密闭容器内加入0.4molA和0.6molB,一定条件下发生反应2A(g)+B(g)
2C(g),反应中C的物质的量浓度变化情况如图。在第5min时,将容器的体积缩小一半后,若在第8min达到新的平衡时A的总转化率为75%,请在图中画
出第5min到新平衡时C的物质的量浓度的变化曲线___。
变式5 化学平衡图象
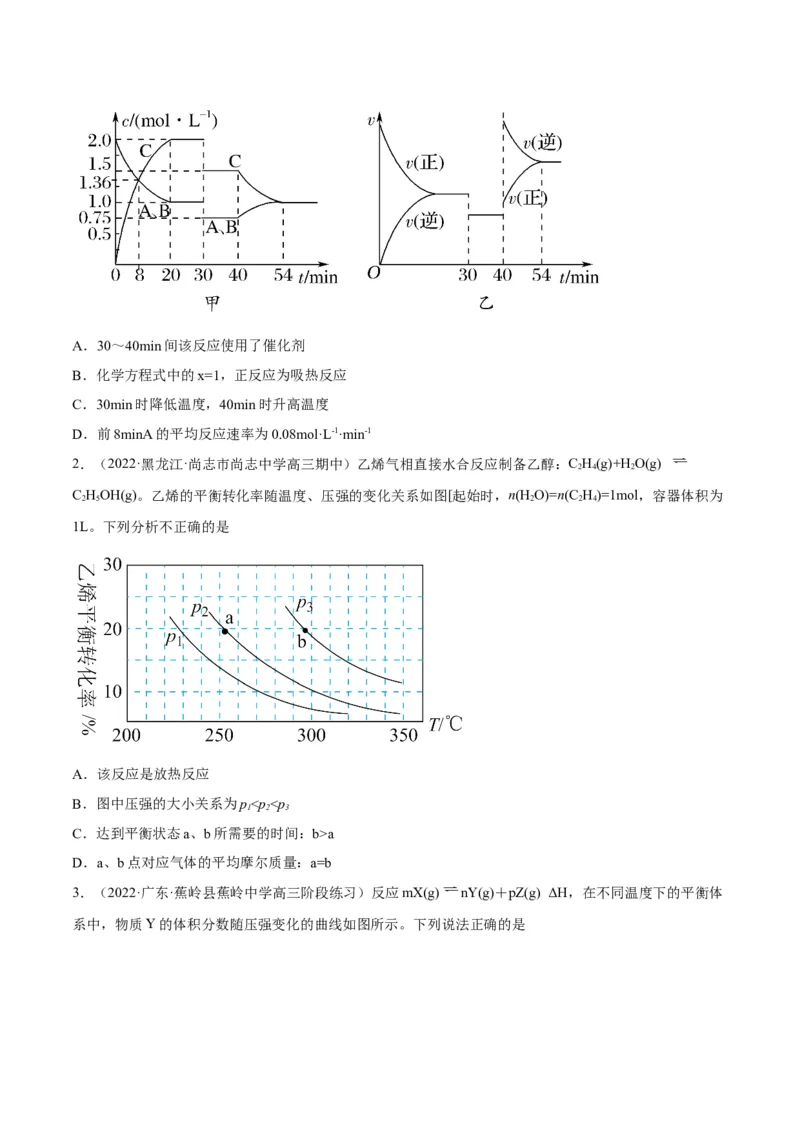
5.(2022·广东·蕉岭县蕉岭中学高三阶段练习)下列图示与对应的叙述相符的是
A.图一表示反应:mA(s)+nB(g) pC(g) H>0,在一定温度下,平衡时B的百分含量(B%)随压强变
△
化的关系如图所示,X点的正反应速率小于逆反应速率
B.图二是可逆反应:A(g)+B(s) C(s)+D(g) H>0的速率时间图象,在t 时刻改变条件一定是加入催
1
△
化剂C.图三表示对于化学反应mA(g)+nB(g) pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反
应的 H<0
D.图△四所示图中的阴影部分面积的含义是(v
正
-v
逆
)
变式6 “等效平衡”理论的应用
6.(2022·湖南·永顺县第一中学高三期中)向体积均为0.5L的三个恒容密闭容器中分别按题表加入X和
Y,一定条件下发生反应:3X(g)+Y(g) 2Z(g) H<0,448K时该反应的化学平衡常数K=1,反应体
△
系中各物质的物质的量相关数据如表:
起始时物质的量/mol 10min时物质的量/mol
容器 温度/K
n(X) n(Y) n(Z)
1 448 1.5 0.5 0.25
2 T 1.5 0.5 0.28
3 448 1.5 1 a
下列说法不正确的是A.容器1中,10min内X的平均反应速率:v(X)=0.075mol·L-1·min-1
B.容器1中,10min时反应已达到化学平衡状态
C.容器2中,T>448、平衡常数K<K
2 1
D.容器3中,反应达到化学平衡状态时,X的转化率大于25%
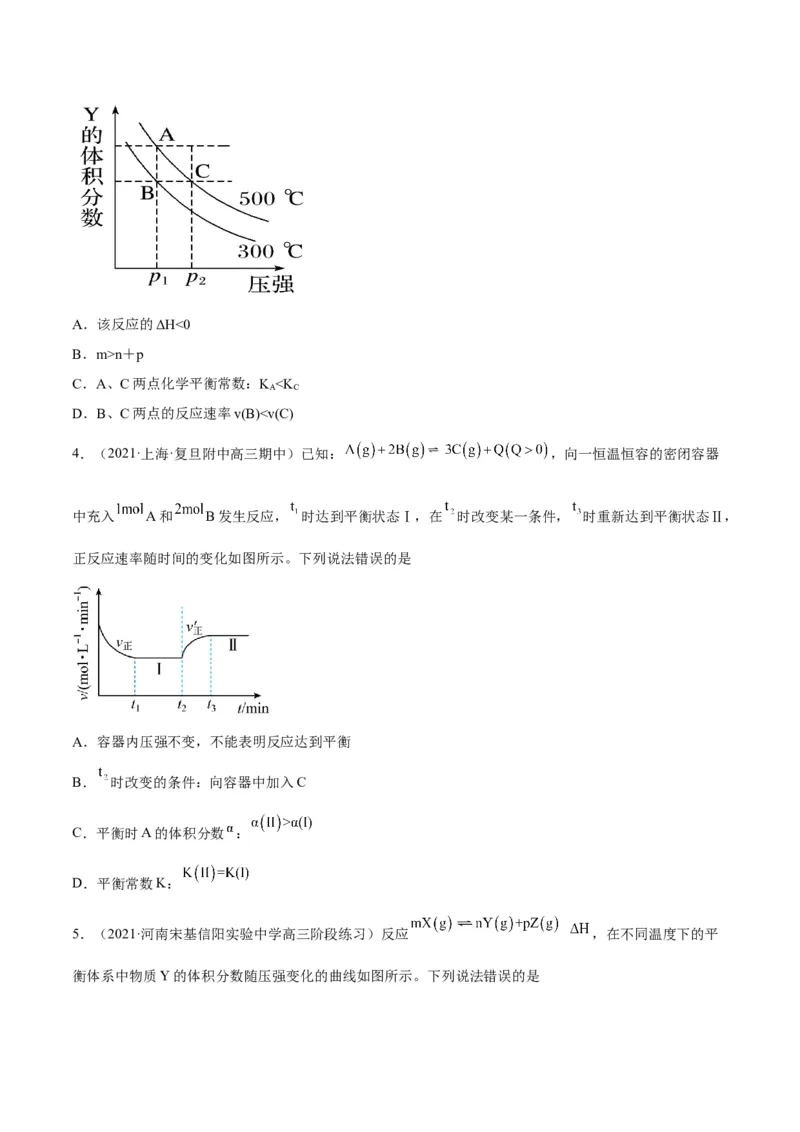
1.(2022·全国·高三专题练习)某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+
xB(g) 2C(g),达到平衡后,在不同的时间段内反应物的浓度随时间的变化如图甲所示,正逆反应速率随
时间的变化如图乙所示,下列说法中正确的是A.30~40min间该反应使用了催化剂
B.化学方程式中的x=1,正反应为吸热反应
C.30min时降低温度,40min时升高温度
D.前8minA的平均反应速率为0.08mol·L-1·min-1
2.(2022·黑龙江·尚志市尚志中学高三期中)乙烯气相直接水合反应制备乙醇:C H(g)+HO(g)
2 4 2
C HOH(g)。乙烯的平衡转化率随温度、压强的变化关系如图[起始时,n(H O)=n(C H)=1mol,容器体积为
2 5 2 2 4
1L。下列分析不正确的是
A.该反应是放热反应
B.图中压强的大小关系为pa
D.a、b点对应气体的平均摩尔质量:a=b
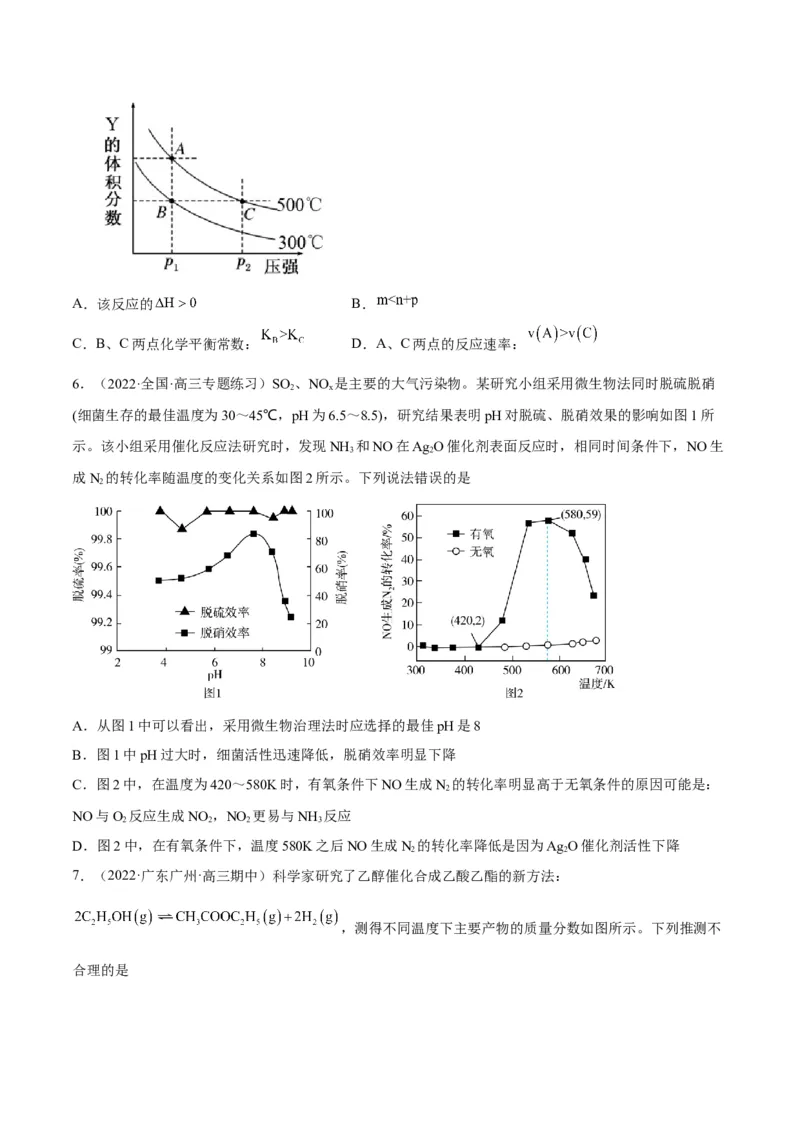
3.(2022·广东·蕉岭县蕉岭中学高三阶段练习)反应mX(g) nY(g)+pZ(g) ΔH,在不同温度下的平衡体
系中,物质Y的体积分数随压强变化的曲线如图所示。下列说法正确的是A.该反应的ΔH<0
B.m>n+p
C.A、C两点化学平衡常数:K