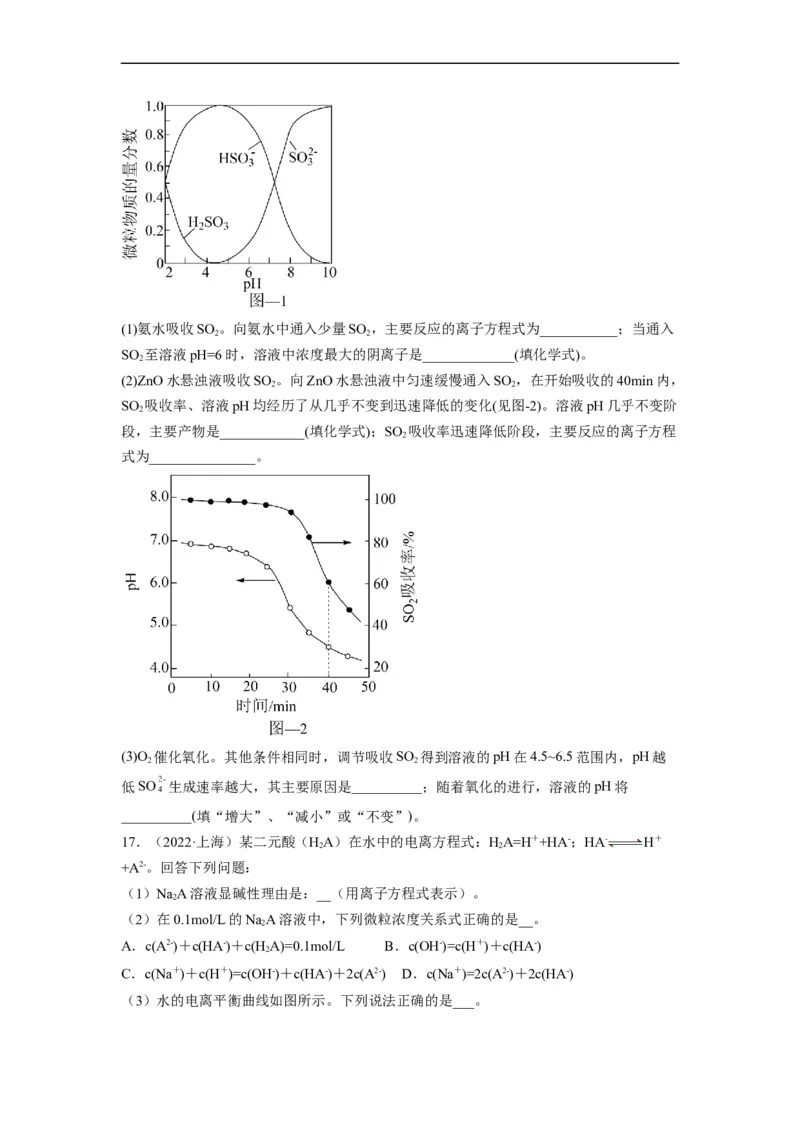
文档内容
解密 08 水溶液中的离子平衡
一、单选题
1.(2023·北京顺义·一模)最近《科学》杂志评出“十大科技突破”,其中“火星
上‘找’到水的影子”名列第一、下列关于水的说法中不正确的是
A.水是含极性键的极性分子
B.水的电离方程式为:
C.纯水中加入少量酸,水的电离受到抑制
D.升高温度,水的电离程度增大
2.(2022·浙江·模拟预测)下列说法不正确的是
A.将纯水加热, 增大, 不变,仍为中性
B.常温下,向 的 溶液中加入少量 固体,溶液的 增
大,说明 溶液存在电离平衡
C.常温下,酸式盐 的 ,则 一定是弱酸
D.常温下,等 的盐酸和醋酸溶液加水稀释10倍后,
3.(2023·湖南邵阳·统考一模)下列设计的实验方案能达到相应实验目的的是
选
实验目的 实验方案
项
A 证明 有漂白性 将 通入酸性高锰酸钾溶液中,溶液褪色
证明碳和浓硫酸共热产生的气 将产生的气体直接通入澄清石灰水中,有白色沉
B
体中含有 淀生成
用洁净的玻璃棒蘸取氨水点在湿润的pH试纸上,
C 测定 氨水的pH
与标准比色卡对照读取pH
证明“84”消毒液的氧化能力随 将“84”消毒液(含NaClO)滴入品红溶液中,褪色
D
溶液pH的减小而增强 缓慢,若同时加入醋酸,红色很快褪为无色
A.A B.B C.C D.D
4.(2022·浙江·模拟预测)下列说法不正确的是
A.25℃时,浓度均为 的 溶液和 溶液,后者的pH较大
B.25℃时,pH相同的HCl溶液和 溶液,后者的 较大C.常温下,将 的 溶液与 的NaOH溶液混合,混合溶液pH仍为9
D.相同温度下,中和相同pH、相同体积的盐酸和醋酸溶液,消耗NaOH物质的量不同
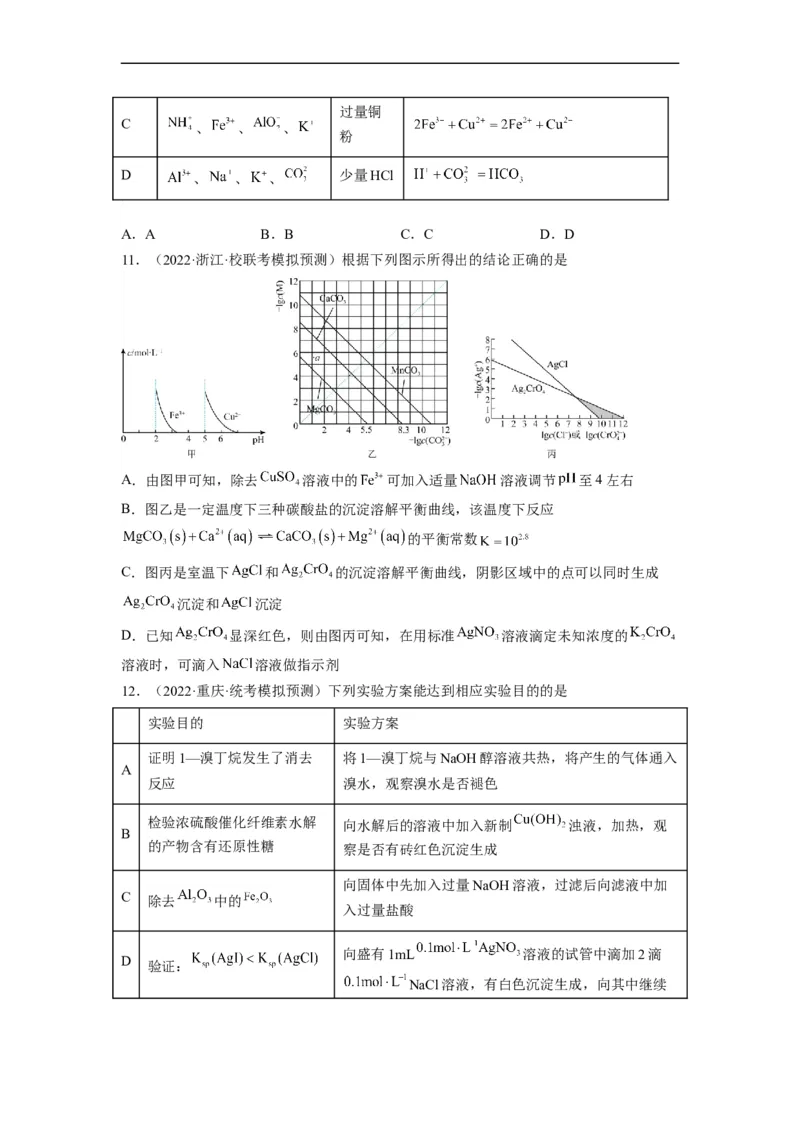
5.(2023·广东·华南师大附中校联考模拟预测)肼( )又称联氨,为二元弱碱,与硫酸
反应可生成 、 。下列说法正确的是
A.室温下0.01mol/L 水溶液
B.稀释0.01mol/L 水溶液, 升高
C. 的水溶液中存在:
D.水溶液中 的电离方程式为
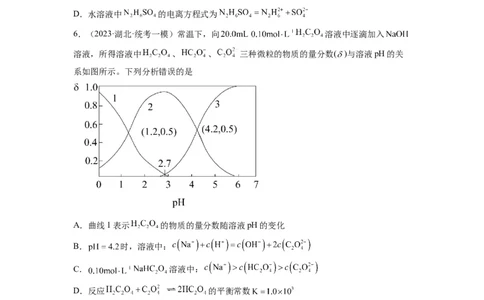
6.(2023·湖北·统考一模)常温下,向 溶液中逐滴加入
溶液,所得溶液中 、 、 三种微粒的物质的量分数( )与溶液pH的关
系如图所示。下列分析错误的是
A.曲线1表示 的物质的量分数随溶液pH的变化
B. 时,溶液中:
C. 溶液中:
D.反应 的平衡常数
7.(2023·广东惠州·统考三模)下列实验设计可以达到实验目的的是
选
实验目的 实验设计
项
验证氢氧化铝属于两性氢氧 将2~3mL2mol/L氯化铝溶液注入洁净的试管中,逐
A
化物 滴加入6mol/L氨水至过量验证Na 2 CO 3 溶液中存在CO 向含有酚酞的NaCO 溶液中加入少量BaCl 固体,
2 3 2
B
-的水解平衡 观察现象
向10mL1mol/L的HCl溶液中滴加少量等浓度的
C 比较Cl与C的非金属性
NaCO 溶液,观察现象
2 3
向两只盛有稀硫酸的烧杯中分别投入表面积相同的铜
D 比较金属的活泼性
丝和银丝
A.A B.B C.C D.D
8.(2022·浙江·校联考模拟预测)下列反应的离子方程式正确的是
A.氨水中通入过量 :
B. 溶液中滴入少量 溶液:
C.新制氯水中加入少量 :
D.明矾溶液中滴加 溶液至沉淀质量最大:
9.(2022·福建福州·福建省福州第八中学校考模拟预测)下列各组物质混合充分反应后,
再加热蒸干并灼烧至质量不变,最终残留固体一定是纯净物的有
A.向 溶液中通入过量
B.向 溶液中加入一定质量
C.将等浓度的 溶液与 溶液等体积混合
D.向NaI与KBr的混合溶液中通入过量
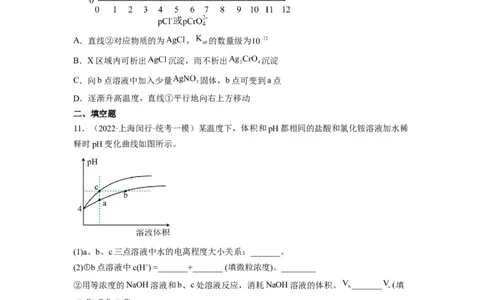
10.(2023·湖南永州·统考二模) 时 和 两种难溶化合物的溶解平衡曲线
如下图所示,两条相交直线把图象分成了X、Y、Z、M四个区域。已知:
,其余离子类推。下列说法正确的是A.直线②对应物质的为 , 的数量级为
B.X区域内可析出 沉淀,而不析出 沉淀
C.向b点溶液中加入少量 固体,b点可变到a点
D.逐渐升高温度,直线①平行地向右上方移动
二、填空题
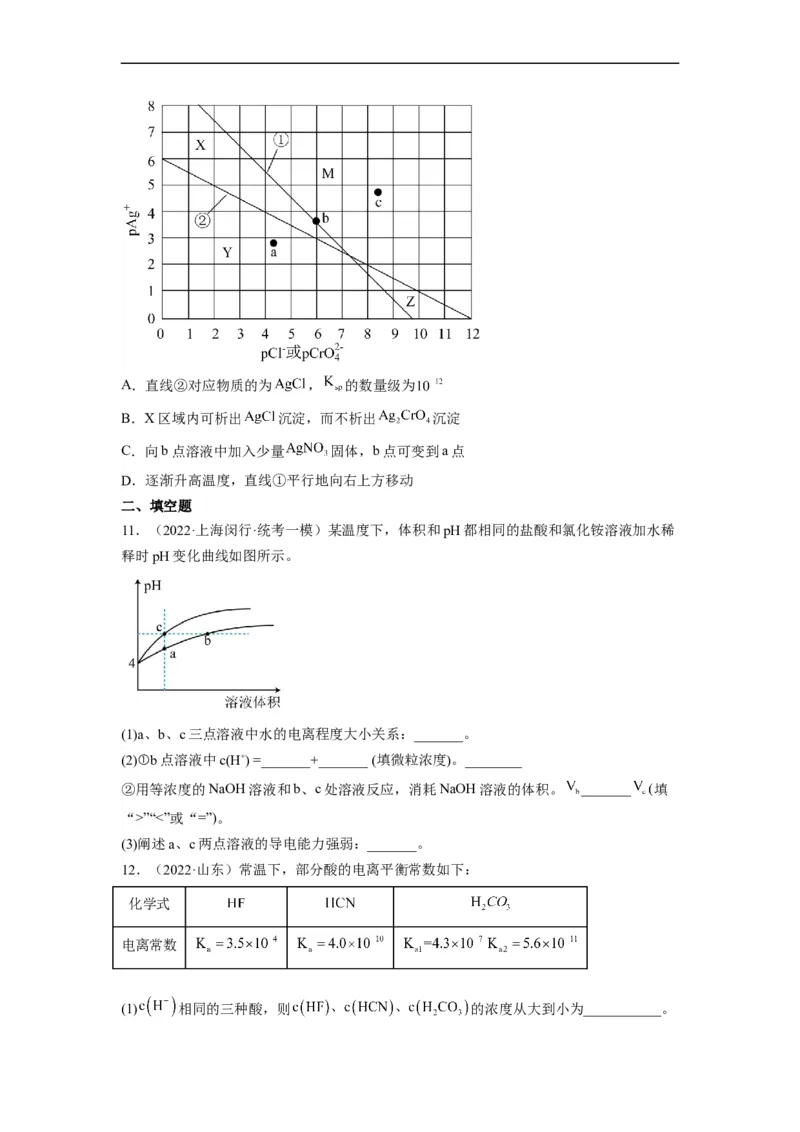
11.(2022·上海闵行·统考一模)某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀
释时pH变化曲线如图所示。
(1)a、b、c三点溶液中水的电离程度大小关系:_______。
(2)①b点溶液中c(H+) =_______+_______ (填微粒浓度)。________
②用等浓度的NaOH溶液和b、c处溶液反应,消耗NaOH溶液的体积。 _______ (填
“>”“<”或“=”)。
(3)阐述a、c两点溶液的导电能力强弱:_______。
12.(2022·山东)常温下,部分酸的电离平衡常数如下:
化学式
电离常数
(1) 相同的三种酸,则 的浓度从大到小为___________。(2) 的 溶液中, 为_____ ,使此溶液中 的电离程度增大且
也增大的方法是_______。
(3)中和等量的 ,消耗等 的氢氟酸和硫酸的体积分别为 ,则a______b(填
“大于”、“小于”或“等于”,下同)。中和等浓度、等体积的氢氟酸和硫酸需要
的物质的量为 ,则 ___________ 。
(4)向 中通入少量的 ,发生的离子方程式为___________。
(5)设计实验证明氢氟酸比盐酸的酸性弱___________。
13.(2022·上海松江·统考一模)氰化提金工艺在黄金生产领域仍占主导地位,但会产生
大量含氰 废水,含氰低于 废水才可排放,研究发现可以用亚硫酸盐——空
气法等处理含氰废水。
完成下列填空:
(1)室温下, 溶液呈碱性,溶液中离子浓度从大到小关系为__________,向 溶
液中加入 盐酸溶液 ,使溶液显中性,则溶液中 __________ 。物质的
量之比为 的 溶液呈碱性,原因是__________。
(2)含氰废水中加入足量的 ,发生反应的离子方程式为
。理论上处理含氰废水(含100gCN-),需要消耗
__________ (保留2位小数)。按照理论值投放,含氰废水处理效果并不理想,
请分析原因__________。多种含氯氧化剂均可以处理含氰废水,比如漂粉精、二氧化氯等。
(3)漂粉精的有效成分为__________(填写化学式)。
(4)请配平下列方程式:CN-+ClO-+H O→CO +N +Cl-+OH-_______________。若上述反应恰
2 2 2
好完全,写出检验反应后溶液中Cl-的方法__________。
14.(2022·江苏·模拟预测)纳米微晶碱式碳酸锌是一种新型的碱式碳酸锌,在医药行业
可用作皮肤保护剂。工业级硫酸锌(主要成分为ZnSO·7H O,含少量Fe2+、Cu2+、Cd2+、
4 2
Co2+、Ni2+)制备纳米微晶碱式碳酸锌[Zn CO(OH) ]。回答下列各步转化涉及的问题:
4 3 6
(1)氧化除杂:向ZnSO 溶液中加HO 除去溶液中Fe2+。Fe2+的电子排布式为___________。
4 2 2
(2)还原除杂:除Cu2+、Cd2+后,再加入Zn粉和少量Sb S,形成锑锌微电池,提高除
2 3
Co2+、Ni2+的反应速率。则该条件下Zn2+、Ni2+、Sb3+的氧化性强弱顺序:___________(用离
子符号表示)。
(3)沉锌:加入NH HCO 溶液、MgSO ·7H O(只用于控制晶粒大小),过滤、洗涤得纳米微
4 3 4 2
晶。
①生成纳米微晶碱式碳酸锌的离子方程式为___________。
②实验测得在一段时间内加入等量NH HCO 所得纳米微晶质量随反应温度的变化如图所示,
4 3
分析曲线下降可能的原因:___________。(4)用乙二胺四乙酸(俗称EDTA,HY2-表示乙二胺四乙酸根离子)滴定法测样品中锌的含量,
2
反应原理为Zn2++H Y2-=ZnY2-+2H+。取1.840g纳米微晶碱式碳酸锌样品,溶于pH为5~6的
2
乙酸-乙酸钠缓冲溶液中配成100mL溶液,滴入少量的铬黑T作指示剂,取25.00mL置于
锥形瓶中,向锥形瓶中加入过量的10.00mL2.000mol·L-1EDTA,振荡。用1.000mol·L-1锌标
准溶液滴定过量的EDTA至终点,消耗锌标准溶液16.00mL。则样品中Zn元素的含量为
___________(写出计算过程)。
一、单选题
1.(2022·上海·一模)下图三条曲线表示不同温度下水的离子积常数,下列说法不正确的
是
A.图中温度: B.图中 的关系:
C.C点物质可能是盐酸 D.图中五点 间的关系:
2.(2020·江苏·模拟预测)常温下,下列各组离子定能大量共存的是
A. 的溶液中:
B.滴加 溶液显红色的溶液中:
C. 的 溶液中:
D.水电离产生的 的溶液中:
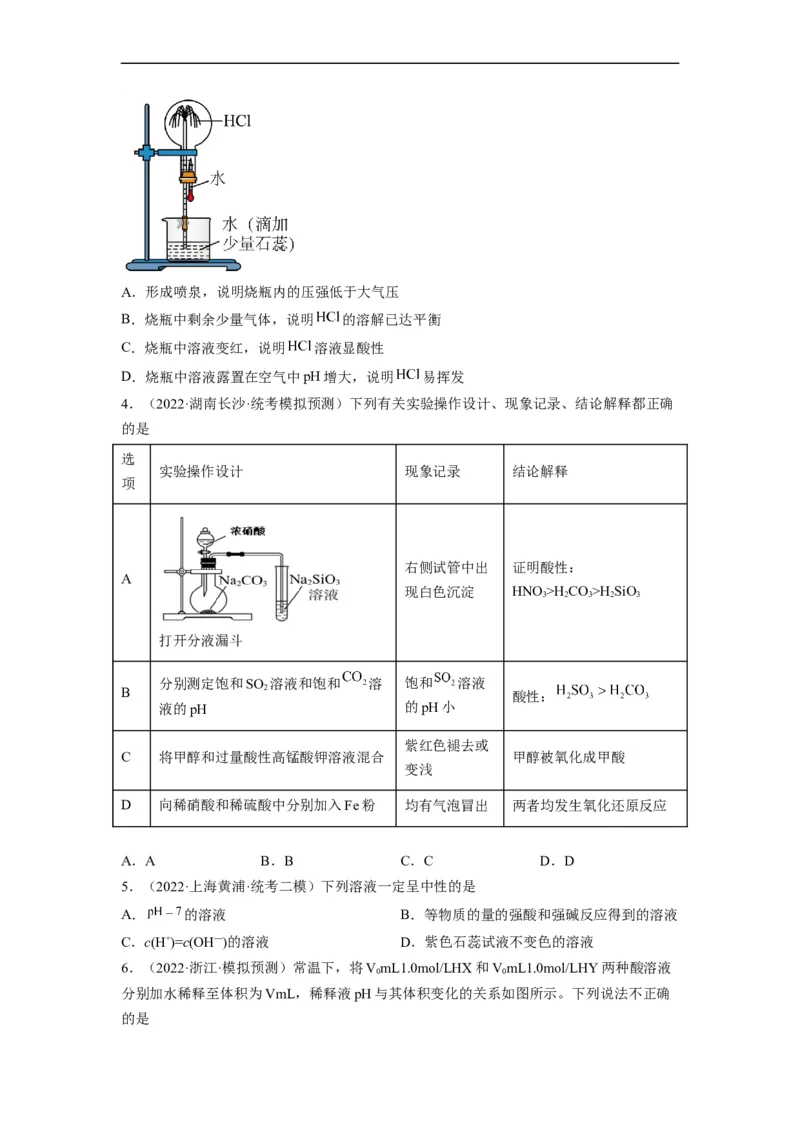
3.(2022·上海杨浦·统考一模)如图,收集 后做喷泉实验。下列分析错误的是A.形成喷泉,说明烧瓶内的压强低于大气压
B.烧瓶中剩余少量气体,说明 的溶解已达平衡
C.烧瓶中溶液变红,说明 溶液显酸性
D.烧瓶中溶液露置在空气中pH增大,说明 易挥发
4.(2022·湖南长沙·统考模拟预测)下列有关实验操作设计、现象记录、结论解释都正确
的是
选
实验操作设计 现象记录 结论解释
项
右侧试管中出 证明酸性:
A
现白色沉淀 HNO>H CO>H SiO
3 2 3 2 3
打开分液漏斗
分别测定饱和SO 溶液和饱和 溶 饱和 溶液
B 2 酸性:
液的pH 的pH小
紫红色褪去或
C 将甲醇和过量酸性高锰酸钾溶液混合 甲醇被氧化成甲酸
变浅
D 向稀硝酸和稀硫酸中分别加入Fe粉 均有气泡冒出 两者均发生氧化还原反应
A.A B.B C.C D.D
5.(2022·上海黄浦·统考二模)下列溶液一定呈中性的是
A. 的溶液 B.等物质的量的强酸和强碱反应得到的溶液
C.c(H+)=c(OH—)的溶液 D.紫色石蕊试液不变色的溶液
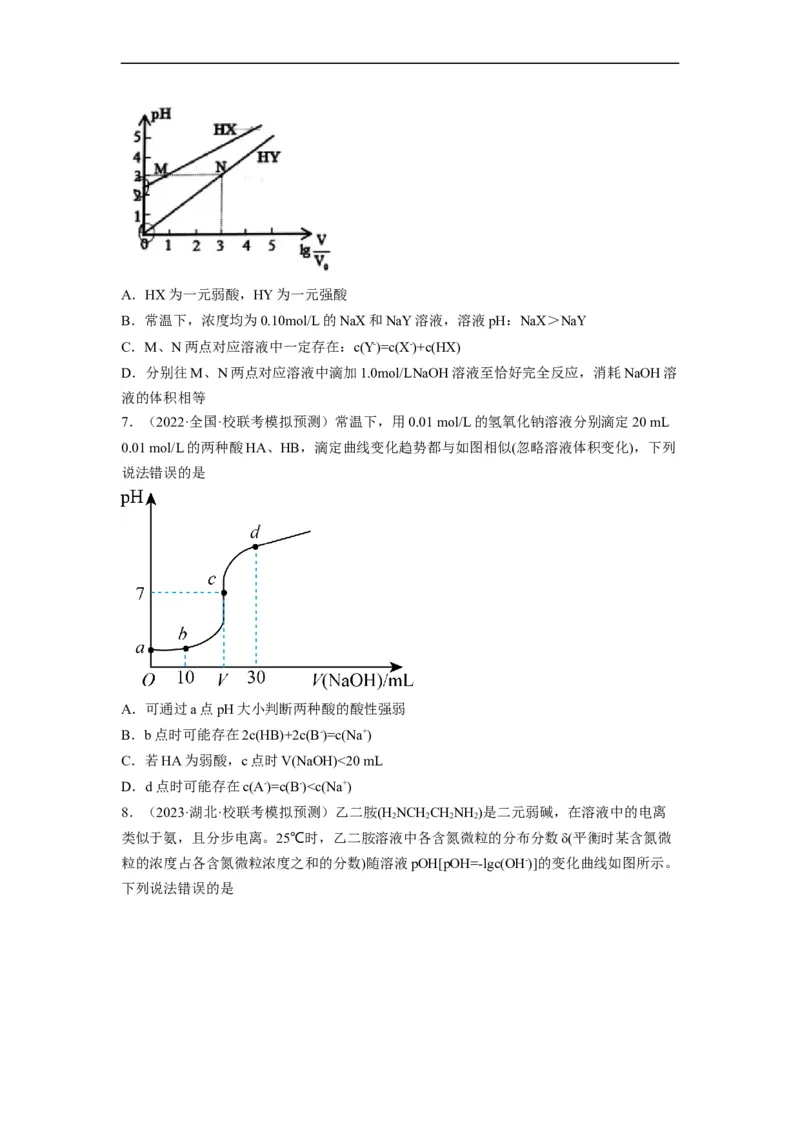
6.(2022·浙江·模拟预测)常温下,将VmL1.0mol/LHX和VmL1.0mol/LHY两种酸溶液
0 0
分别加水稀释至体积为VmL,稀释液pH与其体积变化的关系如图所示。下列说法不正确
的是A.HX为一元弱酸,HY为一元强酸
B.常温下,浓度均为0.10mol/L的NaX和NaY溶液,溶液pH:NaX>NaY
C.M、N两点对应溶液中一定存在:c(Y-)=c(X-)+c(HX)
D.分别往M、N两点对应溶液中滴加1.0mol/LNaOH溶液至恰好完全反应,消耗NaOH溶
液的体积相等
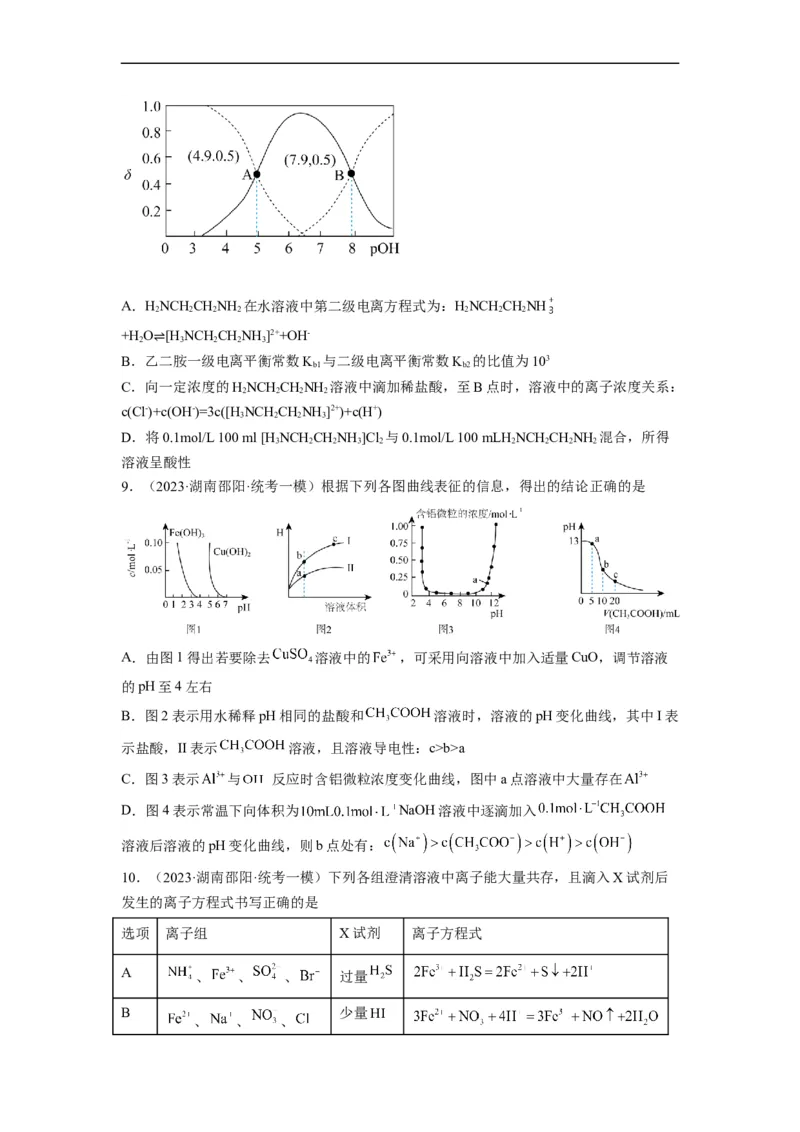
7.(2022·全国·校联考模拟预测)常温下,用0.01 mol/L的氢氧化钠溶液分别滴定20 mL
0.01 mol/L的两种酸HA、HB,滴定曲线变化趋势都与如图相似(忽略溶液体积变化),下列
说法错误的是
A.可通过a点pH大小判断两种酸的酸性强弱
B.b点时可能存在2c(HB)+2c(B-)=c(Na+)
C.若HA为弱酸,c点时V(NaOH)<20 mL
D.d点时可能存在c(A-)=c(B-)b>a
C.图3表示 与 反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在
D.图4表示常温下向体积为 NaOH溶液中逐滴加入
溶液后溶液的pH变化曲线,则b点处有:
10.(2023·湖南邵阳·统考一模)下列各组澄清溶液中离子能大量共存,且滴入X试剂后
发生的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
A 、 、 、 过量
B 少量HI
、 、 、过量铜
C
、 、 、
粉
D 、 、 、 少量HCl
A.A B.B C.C D.D
11.(2022·浙江·校联考模拟预测)根据下列图示所得出的结论正确的是
A.由图甲可知,除去 溶液中的 可加入适量 溶液调节 至4左右
B.图乙是一定温度下三种碳酸盐的沉淀溶解平衡曲线,该温度下反应
的平衡常数
C.图丙是室温下 和 的沉淀溶解平衡曲线,阴影区域中的点可以同时生成
沉淀和 沉淀
D.已知 显深红色,则由图丙可知,在用标准 溶液滴定未知浓度的
溶液时,可滴入 溶液做指示剂
12.(2022·重庆·统考模拟预测)下列实验方案能达到相应实验目的的是
实验目的 实验方案
证明1—溴丁烷发生了消去 将1—溴丁烷与NaOH醇溶液共热,将产生的气体通入
A
反应 溴水,观察溴水是否褪色
检验浓硫酸催化纤维素水解 向水解后的溶液中加入新制 浊液,加热,观
B
的产物含有还原性糖 察是否有砖红色沉淀生成
向固体中先加入过量NaOH溶液,过滤后向滤液中加
C 除去 中的
入过量盐酸
向盛有1mL 溶液的试管中滴加2滴
D
验证:
NaCl溶液,有白色沉淀生成,向其中继续滴加 KI溶液,有黄色沉淀产生
A.A B.B C.C D.D
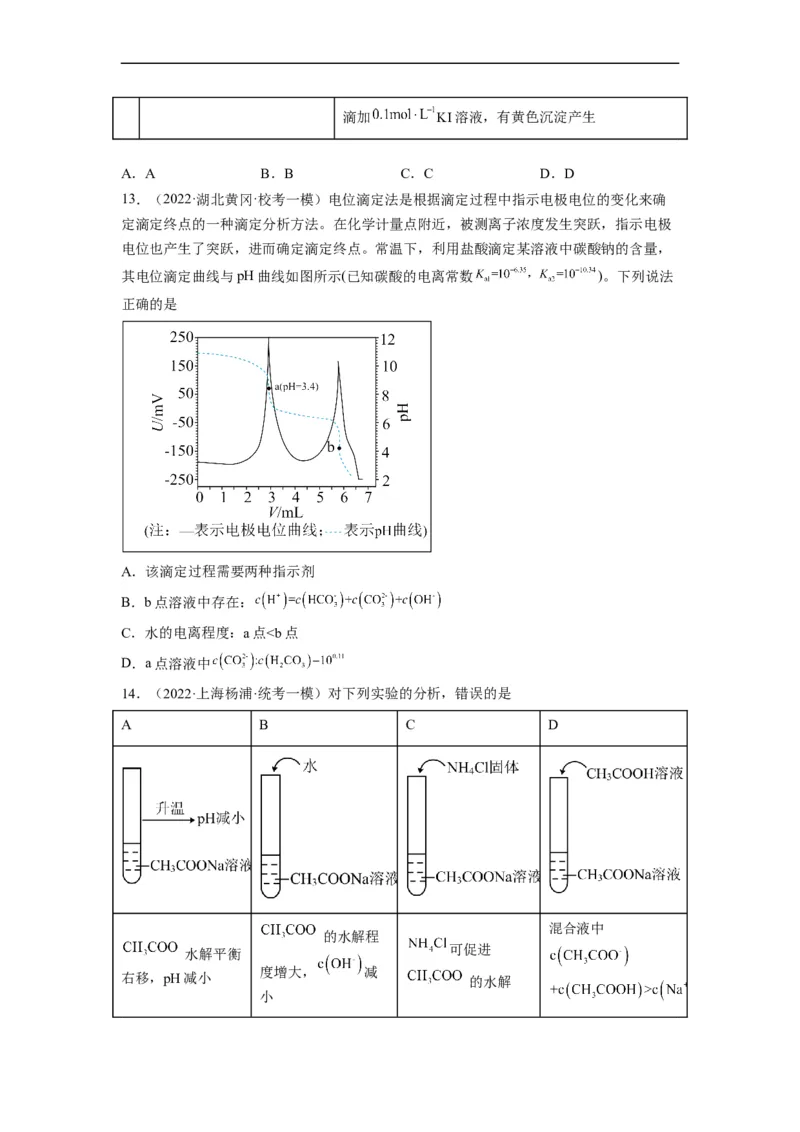
13.(2022·湖北黄冈·校考一模)电位滴定法是根据滴定过程中指示电极电位的变化来确
定滴定终点的一种滴定分析方法。在化学计量点附近,被测离子浓度发生突跃,指示电极
电位也产生了突跃,进而确定滴定终点。常温下,利用盐酸滴定某溶液中碳酸钠的含量,
其电位滴定曲线与pH曲线如图所示(已知碳酸的电离常数 )。下列说法
正确的是
A.该滴定过程需要两种指示剂
B.b点溶液中存在:
C.水的电离程度:a点