文档内容
题型 13 化学平衡常数的计算及应用
目录
.....................................................................................................................................1
【考向一】同一反应不同化学计量数的平衡常数的转化..............................................................................1
【考向二】等温等容条件下的K 的计算.........................................................................................................5
c
【考向三】等温等压条件下的K 的计算.........................................................................................................8
c
【考向四】等温等容条件下的K 的计算.......................................................................................................12
p
【考向五】等温等压条件下的K 的计算.......................................................................................................15
p
【考向六】工业生产中多平衡体系化学平衡常数的计算............................................................................17
【考向七】化学平衡常数的应用....................................................................................................................21
【考向八】化学平衡常数与速率常数、转化率之间计算............................................................................23
...................................................................................................................................27
【考向一】同一反应不同化学计量数的平衡常数的转化
【典例1】(2023上·贵州贵阳·高三统考)已知在T℃时高炉炼铁可发生如下反应:
① ,平衡常数为 ;
② ,平衡常数为 。
以下说法正确的是
A.反应②的平衡常数表达式为
B.T℃时,反应 的平衡常数
C.T℃时增大压强, 减小、 不变
D.T℃时,反应 的平衡常数【答案】D
【解析】A.反应②的平衡常数表达式为 ,A错误;
B.反应 的平衡常数应为 ,B错误;
C.平衡常数只与温度有关,与压强无关,增大压强 不变,C错误;
D.根据盖斯定理, 可由①×3+②得到,可知该反应的平衡常数
,D正确;
故选D。
1.化学平衡常数表达式
对于反应aA(g)+bB(g) cC(g)+dD(g);
K=(固体和纯液体的浓度视为常数,通常不计入平衡常数表达式中)。
2.表达意义
(1)K值越大,反应物的转化率越大,正反应进行的程度越大。
(2)K只受温度影响,与反应物或生成物的浓度变化无关。
(3)化学平衡常数是指某一具体反应的平衡常数。
3.化学平衡常数与化学方程式书写形式的关系
①对于同一可逆反应,正反应的平衡常数等于逆反应的平衡常数的倒数,即:K =。
正
②若化学方程式中的系数等倍扩大或缩小,尽管是同一反应,平衡常数也会发生改变。
③两反应加和,得到的新反应,其化学平衡常数是两反应平衡常数的乘积;两反应相减,得到的新反应,
其化学平衡常数是两反应平衡常数相除得到的商。
如:1.①N(g)+3H(g) 2NH(g) K
2 2 3 1
②N (g)+H(g) NH(g) K
2 2 3 2
③2NH (g) N (g)+3H(g) K
3 2 2 3
(1)K 和K ,K =K。
1 2 1
(2)K 和K ,K =。
1 3 1
4.在一定温度下,已知以下三个反应的平衡常数
反应①:CO(g)+CuO(s) CO(g)+Cu(s) K
2 1
反应②:H (g)+CuO(s) Cu(s)+HO(g) K
2 2 2
反应③:CO(g)+H O(g) CO(g)+H(g) K
2 2 2 3
[CO ]
(1)反应①的平衡常数表达式为K = 2 。
1 [CO]K
1
(2)反应③的K 与K 、K 的关系是K = 。
3 1 2 3 K
2
【变式1-1】(2023·黑龙江大庆·统考二模)25C时,0.1mol/LK Cr O 溶液中存在如下平衡:①
2 2 7
,② ,
随溶液pH的变化如图所示,下列说法错误的是
A.溶液中:
B.向KCr O 溶液中加入少量NaSO 固体,溶液的pH不变
2 2 7 2 4
C.溶液中
D.当溶液pH=9.0时,HCrO 的平衡浓度:
【答案】D
【解析】A.由物料守恒可知,重铬酸钾溶液中 ,则溶液中
,故A正确;
B.向重铬酸钾溶液中加入硫酸钠固体,反应①和②中的各微粒的浓度均不发生变化,平衡不移动,溶液
中氢离子浓度不变,溶液pH不变,故B正确;
C.由方程式可知,反应的平衡常数K= = = ,故C正确;
D.由图可知,溶液pH为9时,溶液中 >104,则由物料守恒可知,溶液中
,由反应②可知,K = = = ,解联立方程可
2
知,溶液中 ,故D错误;
故选D。
【变式1-2】在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2molNO 、0.2moINO和0.1molCl ,
2 2
发生如下两个反应:①2NO
2
(g)+NaCl(s)⇌NaNO
3
(s)+ClNO(g) △H
1
<0 平衡常数K
1
②2NO(g)+Cl
2
(g)⇌2ClNO(g) △H
2
<0 平衡常数K
2
10分钟时反应达到平衡,测得容器内体系的压强减少20%,10分钟内用ClNO(g)表示的平均反应速率
v(ClNO)=7.5×10-3mol/(L·min)。下列说法正确的是
A.平衡时NO 的转化率为50%
2
B.平衡后c(NO)=2.5×10-2mol·L-1
C.其它条件保持不变,反应在恒压条件下进行,则平衡常数K 增大
2
D.反应4NO
2
(g)+2NaCl(s)⇌2NaNO
3
(s)+2NO(g)+Cl
2
(g)的平衡常数为K -K
1
【答案】A
【解析】A.10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为
(0.2+0.2+0.1)mol×(1-20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10-3mol/(L·min),
则平衡时n(ClNO)=7.5×10-3mol/(L•min)×10min×2L=0.15mol,设①中反应的NO 为x mol,②中反应的Cl 为
2 2
ymol,则: ,
,则0.5x+2y=0.15,(0.2-x+0.2-2y+0.1-y)+0.5x+2y=0.4,联立方程,
解得x=0.1、y=0.05,故平衡时NO 的转化率为 ,A选项正确;
2
B.由A项分析,平衡后c(NO)= ,B选项错误;
C.平衡常数只受温度影响,温度不变,平衡常数不变,则其它条件保持不变,反应在恒压条件下进行,
平衡常数K 不变,C选项错误;
2
D.①2NO (g)+NaCl(s) NaNO (s)+ClNO(g) △H<0平衡常数K ;②2NO(g)+Cl (g) 2ClNO(g) △H
2 3 1 1 2 2
<0平衡常数K ;由盖斯定律可知,由①×2-②可得反应4NO (g)+2NaC1(s) 2NaNO (s)+2NO(g)
2 2 3
+Cl(g),则4NO (g)+2NaC1(s) 2NaNO (s)+2NO(g)+Cl (g)的平衡常数 ,D选项错误;
2 2 3 2
答案选A。【考向二】等温等容条件下的K 的计算
C
【典例2】(2023上·山东·高三校联考)在160℃、200℃条件下,分别向两个容积为2L的刚性容器中充入
2molCO(g)和2molN O(g),发生反应:CO(g)+NO(g) CO(g)+N(g) ΔH<0。实验测得两容器中CO或N
2 2 2 2 2
的物质的量随时间的变化关系如图所示。下列说法正确的是
A.CO的转化率:d﹥c
B.ac段N 的平均反应速率为0.10mol/(L·min)
2
C.该反应达到平衡状态时c(CO)+c(CO )=2mol/L
2
D.200℃时,该反应的平衡常数Kc=2.25
【答案】AD
【分析】已知随着反应的进行,N 的物质的量增大,CO的物质的量减小,故ac曲线表示N 的随时间的变
2 2
化,bd曲线表示CO随时间的变化,由图中可知ac先达到平衡,说明ac对应的温度更高,据此分析解题。
【解析】A.据分析可知,ac对应的温度更高,该反应△H<0,温度升高,平衡向逆移动,CO的转化率:
d﹥c,故A正确;
B.ac段N 的平均反应速率为 ,故B错误;
2
C.根据反应CO(g)+NO(g) CO(g)+N(g),原子守恒由c(CO)+c(CO )=1mol/L,故C错误;
2 2 2 2
D.由分析可知,ac曲线对应温度为200℃,达到平衡,平衡时N 的物质的量为1.2mol,故三段分析为
2
,平衡常数 ,故D正确;
故答案选AD。
1.等温等容条件下的浓度平衡常数如:a A(g)+b B(g) c C(g)+d D(g)
cc(C)×cd(D)
K=ca(A)×cb(B)
c
(1)表达式:
①平衡量必须为平衡时的浓度
②反应前后气体体积相等的反应:可以用平衡时的物质的量代替平衡时的浓度
2.常用计算公式
某物质反应的量
该物质的总量
(1)反应物的转化率: = ×100%
某组分的量
混合物的总量
(2)某组分的百分含量:含量= ×100%
①常见量:体积分数、物质的量分数
②关系式:体积分数=物质的量分数
3.计算模式——“三段式”
(1)确定反应物或生成物的起始加入量。
(2)确定反应过程的变化量。
(3)确定平衡量。
(4)依据题干中的条件,建立等量关系进行计算。
反应 aA(g) + bB(g) cC(g) + dD(g)
起始量/mol m n 0 0
转化量/mol ax bx cx dx
平衡量/mol m-ax n-bx cx dx
ax
①反应速率:v(A)=
V×t
(时间为tmin)
bx
n
②反应物转化率: (B)= ×100%
cx
③C的体积分数:φ(C)=_
m-ax+n-bx+cx+dx
×100%
p n
始 始 m+n
④反应前后气体的压强比:
p
平=
n 平=m-ax+n-bx+cx+dx
(恒温恒容)
【变式2-1】(2024上·湖南长沙·高三长沙一中校考) 是常见的环境污染性气体。一定温度下,向三
个容积不等的恒容密闭容器中分别投入 ,发生反应: 。反应相同时间
内,三个容器中 的转化率如图中A、B、C三点。下列叙述正确的是A.A点的 小于C点的
B.C点加入适当催化剂,不能提高 的转化率
C.若B点为平衡点,在该温度下,反应的平衡常数
D.在恒温恒容下,向A点平衡体系中再充入一定量的 ,与原平衡相比, 的平衡转化率减小
【答案】D
【解析】A.A点体积小,压强大,反应速率快,故A错误;
B.由题干图像可知,容器的容积依次增大,反应速率依次减小可知,C点未达到平衡状态,使用催化剂
可加快反应速率,提高 的转化率,故B错误;
C.B点对应的体系为 , 的平衡转化率为80%,
因此平衡常数 ,故C错误;
D.在恒温恒容下,向A点平衡体系中充入一定量的 ,等效于加压,平衡逆向移动, 的平衡转化
率减小,故D正确;
选D。
【变式2-2】(2024上·重庆·高三重庆南开中学校考)甲醇可通过 氢化法合成:
。恒定温度为 时,将 和 充入 密闭
容器中,测得 按I变化。下列说法不正确的是A. 时,I中反应进行到B点时释放的热量为
B. 时,该反应平衡常数为
C.若其他条件不变,增大起始 ,所得 可能按Ⅱ变化
D.若其他条件不变,缩小容器体积,所得 可能按Ⅱ无变化
【答案】C
【解析】A.由图像可知,I中反应进行到B点时, 为3mol/L,则 为3mol,起始H 为
2
12mol,则转化的H 为9mol,故释放的热量为 ,A正确;
2
B.由图像可知,I中反应进行到C点时,反应达平衡, 为2mol/L,列三段式为
,则 ,B正
确;
C.若其他条件不变,增大起始 ,则在相同时间时, 大于Ⅰ中的 ,故 不能按照Ⅱ
变化,C错误;
D.若其他条件不变,缩小容器体积,体系压强增大,则化学反应速率加快,平衡向正反应方向移动,达
平衡时 减小,故 可能按照Ⅱ变化,D正确;
答案选C。
【考向三】等温等压条件下的K 的计算
C
【典例3】(2023上·广东汕头·高三统考期中) 的排放来自汽车尾气,研究利用反应
,用活性炭可对其进行吸附。已知在密闭容器中
加入足量的C和一定量的NO气体,保持恒压测得NO的转化率随温度的变化如图所示。(已知:气体分压=气体总压×物质的量分数),下列有关说法错误的是
A.若能测得反应产生22g ,则反应放出的热量为17.0kJ
B.达到平衡后增大活性炭的用量,平衡不移动
C.在950K~1000K之间,化学反应速率:
D.1050K时,反应的化学平衡常数
【答案】C
【解析】A. ,可知,每生成44g二氧化碳放出
34kJ热量,若能测得反应产生22g ,则反应放出的热量为17.0kJ,故A正确;
B. 活性炭是固体,达到平衡后增大活性炭的用量,平衡不移动,故B正确;
C. 1050K前反应末达到平衡状态,随着温度升高,反应速率加快,反应正向进行,在950K~1000K之
间,化学反应速率: ,故C错误;
D. 在1050K、1.1×106Pa时,NO的转化率为80%,设n(NO)=xmol,消耗的n(NO)=0.8xmol,可逆反应
反应前后气体计量数之和不变,则反应前后气体总物质的量不变,为xmol,p(NO)=
×1.1×106Pa=0.22×106Pa,p(N )=p(CO )=2p(NO)=2×0.22×106Pa=0.44×106Pa,该反应的平衡常数K =
2 2 p
=4,1050K时,反应的化学平衡常数 ,故D正确;
故选C。
1.等温等压条件下的浓度平衡常数
如:a A(g)+b B(g) c C(g)+d D(g)cc(C)×cd(D)
K=ca(A)×cb(B)
c
(1)浓度平衡常数:
①平衡量必须为平衡时的浓度
②恒压条件下:
V n
始 始
V n
a.先计算平衡体积 平= 平
n
平
V
b.再计算平衡浓度:c 平 = 平
c.再算平衡常数
2.计算模式——“三段式”
(1)确定反应物或生成物的起始加入量。
(2)确定反应过程的变化量。
(3)确定平衡量。
(4)依据题干中的条件,建立等量关系进行计算。
反应 aA(g) + bB(g) cC(g) + dD(g)
起始量/mol m n 0 0
转化量/mol ax bx cx dx
平衡量/mol m-ax n-bx cx dx
ax
①反应速率:v(A)=
V×t
(时间为tmin)
bx
n
②反应物转化率: (B)= ×100%
cx
③C的体积分数:φ(C)=_
m-ax+n-bx+cx+dx
×100%
V n
始 始 m+n
④反应前后气体的体积比:
V
平=
n 平=m-ax+n-bx+cx+dx
(恒温恒压)
ρ 始 V 平 n 平 m-ax+n-bx+cx+dx
⑤反应前后气体的密度比: ρ 平= V 始= n 始= m+n (恒温恒压)
【变式3-1】(2023上·黑龙江大庆·高三肇州县第二中学校考)一定量的 与足量的碳,在体积可变的恒
压密闭容器中反应: 。平衡时,体系中气体体积分数与温度的关系如图所示。已
知: 。下列说法正确的是A.550℃时,若充入稀有气体, 、 均减小,平衡不移动
B.925℃时,用平衡分压代替平衡浓度表示的化学平衡常数
C.T℃时,反应达平衡后 的转化率为50%
D.T℃时,若充入等体积的 和 ,平衡不移动
【答案】D
【解析】A.550℃时,在体积可变的恒压密闭容器中充入稀有气体,等效于扩容减压,v 、v 均减小,
正 逆
平衡右移,A错误;
B.925℃时,CO的体积分数为96%,则CO 的体积分数都为4%,所以用平衡分压代替平衡浓度表示的化
2
学平衡常数:K= ,故B错误;
p
C.T℃时,CO 和CO体积分数为50%,
2
1-x=2x,x= ,反应达平衡后 ,故C错误;
D.T℃时,充入等体积的CO 和CO,CO 和CO体积分数仍为50%,不影响原来平衡状态,平衡不移动,
2 2
故D正确;
故选D。
【变式3-2】(2023上·四川遂宁·高三四川省遂宁市第二中学校校考)相同温度下,分别在起始体积均为
的两个密闭容器中发生反应: ,实验测得反应的有关数据
如下表。
起始物质的量/mol
容
反应条件 达到平衡所用时间/min 达到平衡过程中的能量变化
器
X Y XY
2 2 3
① 恒容 1 3 0 10 放热0.1akJ② 恒压 1 3 0 t 放热bkJ
下列叙述正确的是
A.反应②的平衡常数K约为0.0046
B.①中:从开始至10min内的平均反应速率v(X )=0.1mol-1·L·min-1
2
C.②中:X 的平衡转化率小于10%
2
D.b>0.1a
【答案】D
【解析】A.①②中反应温度相同,平衡常数K的数值相同,故根据放出的热量值,可知参加反应的
为0.1mol,则:
则反应①的平衡常数: 0.0023,A错误;
B.①中反应放热0.1akJ,说明10min内X 反应了0.1mol,物质的量浓度改变量为0.1mol·L-1,所以其平均
2
速率为v(X )=0.01mol·L-1·min-1,B错误;
2
C.据容器①中数据,可算出X 的平衡转化率为10%,容器②是恒温恒压,容器①是恒温恒容,容器②相
2
当于在容器①的基础上加压,平衡右移,所以X 的转化率大于10%,容器②放出的热量比容器①多,C错
2
误;
D.结合C分析可知,b>0.1a,D正确;
故选D。
【考向四】等温等容条件下的K 的计算
P
【典例4】(2023上·福建泉州·高三福建省泉州市培元中学校联考期中)在一定条件下 、 主要发生
以下反应:
① kJ⋅mol-1
② kJ⋅mol-1
若在一定温度下,投料比例相同(充入物质的量之比为1∶4的 和 ),通入恒容密闭容器中,发生上述
反应达到平衡,测得反应前容器内压强为 ,平衡时 压强为 ,甲烷压强为 。则甲烷的选择性为
(用 、 、 中相关字母表示,下同),反应②的压强平衡常数 的值为 。【答案】
【解析】反应前容器内压强为 ,平衡时 压强为 ,甲烷压强为 ,则反应①消耗的二氧化碳的压强
为 ,反应②消耗的二氧化碳的压强为 ,则甲烷的选择性: ;平衡时二氧化碳压强:
, 压强为 ,CO压强 ,氢气压强: ,代入平衡常数表达
式可得 。
1.等温等容条件下的压强平衡常数
如:a A(g)+b B(g) c C(g)+d D(g)
pc(C)×pd(D)
K =
pa(A)×pb(B)
p
表达式:
c V
i i
c V
①先计算平衡时物质的量分数:x= = 总= 总
i
②再计算平衡时总压: =
③再算出平衡时各组分的分压P=P ×x=P × =(P+P +P +…)×
i 平总 i 平总 1 2 3
pc(C)×pd(D)
④最后计算压强平衡常数:K =
pa(A)×pb(B)
p
2.恒温恒容下:可以直接根据“分压比=化学计量数比”进行计算
aA +bB
反应 cC(g) +dD(g)
(g) (g)
起始量Pa P P 0 0
A B
转化量Pa ax bx cx dx
平衡量Pa P-ax P -bx cx dx
A B
【变式4-1】(2023上·湖南长沙·雅礼中学校考)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应减少尾气污染。已知 。
一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所
示:
t/min 0 1 2 3 4 5
20 16
p/kPa 185 173 165 160
0 0
该反应条件下的平衡常数 。
【答案】1.6
【解析】(3) ,设向恒容容器中通入amolNO和amolCO,设转化
率为x,则可列三段式如下:
气体反应前容器内压强为200kPa,平衡后容器内压强为160kPa,恒容条件下,容器内的压强比等于气体总
物质的量比,反应起始总物质的量为2amol,平衡后总物质的量为2a-0.5ax,则可得到:
,解得x=80%,则平衡后总物质的量为1.6amol,可以求出平衡后各气体的分压
为:
该反应条件下的平衡常数 。
【变式4-2】(2023上·河南许昌)在体积为 的密闭容器中,进行如下化学反应:
,化学平衡常数 与温度 的关系如下表:
70
800 850 1000 1200
0
0.6 0.9 1.0 1.7 2.6
回答下列问题:在 条件下,将 和 按体积比 通入 的恒容密闭容器中发生上述反应, 后反应达平衡,
此时压强为 。该反应的分压平衡常数 。( 为以分压表示的平衡常数,分压 总压 物质的
量分数)
【答案】(5) 1
【解析】(5)根据表格数据可知,在850℃条件下,该反应的平衡常数为1.0,将CO 和 H 按体积比3:7
2 2
通入2 L的恒容密闭容器中发生上述反应,10min后反应达平衡,此时压强为P,设反应前加入CO 和 H
2 2
的物质的量浓度为:3xmol/L、7xmol/L,达到平衡时消耗CO 的物质的量浓度为amol/L,列三段式为:
2
,达到平衡时,气体总物质的量浓度为:
(3x-a)mol/L+(7x-a) mol/L +a mol/L +a mol/L =10x mol/L,达到平衡时,该反应的平衡常数:
;850℃条件下该反应的分压平衡常数: ;
【考向五】等温等压条件下的K 的计算
P
【典例5】(2023·吉林·统考模拟预测)“碳达峰·碳中和”是我国社会发展重大战略之一, CH 还原CO
4 2
是实现“双碳”经济的有效途径之一,相关的主要反应有:
Ⅰ:CH(g) + CO (g) 2CO(g) + 2H(g) ΔH = +247 kJ·mol−1
4 2 2
Ⅱ:CO(g) + H(g) CO(g) + HO(g) ΔH = +41 kJ·mol−1
2 2 2
请回答下列问题:
(3)恒温恒压条件下,1mol CH(g)和1mol CO (g)反应达平衡时,CH(g)的转化率为 ,HO (g)的物质的
4 2 4 2
量为bmol,则反应Ⅰ的平衡常数K = (写出含有α、b的计算式;对于反应mA(g) + nB(g) pC(g)
x
+ qD(g), ,x为物质的量分数)。
【答案】(3)
【解析】(3)恒温恒压条件下,1mol CH(g)和1mol CO (g)反应达平衡时,CH(g)的转化率为 ,HO (g)
4 2 4 2的物质的量为bmol,由三段式分析可知: ,
,平衡时CH、CO、CO、H 的物质的量分数分别为:
4 2 2
、 、 、 ,则反应Ⅰ的平衡常数K = = ,故答案为:
x
;
1.等温等压条件下的压强平衡常数
如:a A(g)+b B(g) c C(g)+d D(g)
pc(C)×pd(D)
表达式:K =
pa(A)×pb(B)
p
n c
i i
n c
①计算各组分的物质的量分数:x= 总= 总
i
n
i
n
②计算平衡时各组分的分压:P i =P 总 ×x i =P 总 × 总
pc(C)×pd(D)
③最后计算压强平衡常数:K =
pa(A)×pb(B)
p
2.也可以直接根据分压和分体积进行计算
恒温恒压:气体体积比=物质的量比=化学计量数比
aA +bB
反应 cC(g) +dD(g)
(g) (g)
起始量L V V 0 0
A B
转化量L ax bx cx dx
平衡量L V -ax V -bx cx dx
A B【变式5-1】(2023·辽宁沈阳·校联考一模)在 下,恒压反应器中,按初始投料 发
生反应: ,初始总压为 ,反应平衡后, 的平衡转化率为
,则该反应的平衡常数 (用平衡分压代替平衡浓度计算,分压=总压×物质的
量分数)。
【答案】0.5
【解析】设CO、H 的初始物质的量均为amol。列三段式
2 2
,平衡总物质的量为1.6amol,平衡时CO、H、
2 2
CHOH、HO的分压依次为1MPa、0.5MPa、0.25MPa、0.25MPa,则该反应的平衡常数K =
3 2 p
=0.5(MPa)-2。
【变式5-2】(2023上·广西)将SO 转化为SO 是工业上生产硫酸的关键步骤,发生的反应为2SO (g)
2 3 2
+O (g) 2SO (g) △H=-196 kJ/mol,在450℃、100kPa的恒温恒压条件下,SO 的平衡体积分数随起始时
2 3 3
投料 的变化如图所示,用平衡压强(平衡压强=该物质的体积分数×总压强)代替平衡浓度,则450℃
时,该反应的K= 。
p
【答案】0.05kPa-1
【解析】当反应物的投料比等于计量数之比时,生成物的体积分数最大,所以此条件下当 时,
平衡时SO 的体积分数为40%,则平衡时p(SO )=40kPa,SO 和O 投料比为2:1;按照2:1的比例反应,
3 3 2 2
所以平衡时二者的物质的量之比仍为2:1,则p(SO )=40kPa,p(O )=20kPa; 。
2 2【考向六】工业生产中多平衡体系化学平衡常数的计算
【典例6】(2024上·云南昆明)CO 资源化利用受到越来越多的关注,它能有效减少碳排放,有效应对全
2
球的气候变化,并且能充分利用碳资源。二氧化碳催化加氢制甲醇有利于减少温室气体排放,涉及的反应
如下:
Ⅰ.
Ⅱ. kJ⋅mol-1
Ⅲ. kJ⋅mol-1
回答下列问题:
(1)在恒温恒压(压强为p)的某密闭容器中,充入1 mol 和3 mol ,仅发生反应Ⅰ和Ⅱ,经
过一段时间后,反应Ⅰ和Ⅱ达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为50%{甲醇选
择性[ ]},则该温度下反应Ⅰ的平衡常数 (写出计算式
即可,分压=总压×物质的量分数)。
【答案】(1)
【解析】(1)在恒温恒压(压强为p)的某密闭容器中,充入1 mol 和3 mol ,仅发生反应Ⅰ
和Ⅱ,经过一段时间后,反应Ⅰ和Ⅱ达到平衡,此时测得 的平衡转化率为20%,甲醇的选择性为
50%,根据三段式分析可知,
,此时CO 的平衡分压为:P(CO )=
2 2
= ,同理有:P(H )= = ,P(CH OH)=
2 3
= ,P(H O)= = ,则该温度下反应Ⅰ的平衡常数
2= ,故答案为: 。
1.多重平衡是指相互关联的若干平衡同时存在于一个平衡系统中,且至少有一种物质同时参与几个相互关
联的平衡。多重平衡涉及的反应多,看似杂乱,但各个平衡之间存在内在联系,要么连续,要么竞争,这
样可将三个平衡简化为两个平衡,从而快速解答。也可以从元素守恒入手,只要抓住起始状态与平衡状态
即可,可以忽略复杂的反应过程,从而使复杂问题简单化。
2.同一容器内的多平衡体系,相同组分的平衡浓度相同
①化学平衡:a A(g) b B(g)+c C(g),c C(g) d D(g)+e E(g)
②特点:计算K 、K 时,用到的c(C)相同
1 2
3.计算方法
(1)元素守恒法:根据某元素守恒,计算出平衡时相应组分的浓度
(2)设未知数法
①有几个平衡假设几个未知数(变化量)
②用这些未知数表示出平衡时相应组分的浓度
③根据相关等量计算出未知数,带入平衡常数表达式求解
【变式6-1】(2024上·湖北·高三校联考期末)一定条件下, 和 可以发生如下两个平行反应:
Ⅰ.
Ⅱ.
保持温度恒定,向一定体积的密闭容器中按体积比1:3充入 和 ,起始压强为4MPa。发生上述平行
反应,达到平衡后压强为2.8MPa。已知达到平衡时 的选择性为75%(反应中转化的 中生成
的百分比)。则:
的转化率为 ;该条件下反应Ⅱ的压强平衡常数 为 。(用分压表示,分压=总压×
物质的量分数)
【答案】
【解析】 正反应气体系数和减小,容器内气体压强减小是因为发生
反应 ,
a=0.6 MPa、b=1.8MPa、x= 0.6MPa、y= 0.6MPa;达到平衡时 的选择性为75%,则反应使CO 的压强降低 0.2 Mpa、氢气的压强降低
2
0.2MPa、CO的压强增大0.2MPa、HO的压强增大0.2MPa,容器中CO 的压强为(1-0.6-0.2)=0.2 MPa、H
2 2 2
的压强为(3-1.8-0.2)=1MPa、甲醇的压强为0.6MPa、HO的压强为(0.6+0.2)=0.8MPa, 的转化率为
2
;该条件下反应Ⅱ的压强平衡常数 = ;
【变式6-2】工业上,可以采用 催化还原制备 、 。发生反应如下:
① (主反应);
② (主反应);
③ (副反应)。
一定温度下,向总压强恒定为100kPa的反应器中充入 和 ,发生(4)中反应①②③,
达到平衡时 转化率为50%,甲醇选择性为 ,生成 ,则反应①的平衡常数 为
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲
醇选择性: ]。
【答案】
【解析】由题意可知,平衡时二氧化碳的转化率为50%、乙醇的物质的量为0.05mol、甲醇的选择性为 ,
设平衡时甲醇的物质的量为amol、一氧化碳的物质的量为bm,由题意可建立如下三段式:由二氧化碳的转化率可得:0.9—a—b=0.5,由甲醇的选择性可得:a=(0.05+a+b)× ,解得a=0.3、b=0.1,
则平衡时二氧化碳、氢气、甲醇、乙醇、一氧化碳、水蒸气的物质的量分别为0.5mol、1.7mol、0.3mol、
0.05mol、0.1mol、0.55mol,则混合气体的总物质的量为3.2mol,反应①的平衡常数K =
p
,故答案为: 。
【考向七】化学平衡常数的应用
【典例7】(2023上·四川南充)在恒容密闭容器中充入2 mol CO 和0.5 mol H 发生如下反应: CO(g)+
2 2 2
H(g) CO(g)+HO(g) ΔH>0如图所示为该反应正反应的平衡常数K 和逆反应的平衡常数K 随温度变
2 2 正 逆
化的曲线。下列分析正确的是
A.曲线Ⅰ为K ,曲线Ⅱ为K
逆 正
B.T 时,A点 >
2 正 逆
C.T 时,CO 的平衡转化率为40%
1 2
D.其他条件不变,在原平衡基础上再充入2 mol CO 和1 mol H ,达新平衡时CO 转化率将减小
2 2 2
【答案】B
【分析】对于反应CO
2
(g)+H
2
(g)⇌CO(g)+H
2
O(g)ΔH>0,正反应为吸热反应,则升高温度,平衡正向移动,
正反应平衡常数增大,由图可知曲线Ⅰ为K ,曲线Ⅱ为K ,结合外界条件对平衡移动的影响解答该题。
正 逆
【解析】A.由以上分析可知曲线Ⅰ为K ,曲线Ⅱ为K ,A错误;
正 逆
B.T 时,A点K <K<K ,则反应正向移动, > ,B正确;
2 逆 正 正 逆
C.T 时,K =K ,因K ×K =1,则K =1,设转化xmolCO ,三段式分析为:
1 逆 正 逆 正 正 2
则 =1,x= ,CO 的平衡转化率为20%,C错误;
2D.其他条件不变,如在原平衡基础上再充入“2mol CO 和1mol H”,将该充入量改为“2mol CO 和
2 2 2
0.5mol H +0.5mol H”,若去掉后面的“0.5molH“,根据等效平衡规律新平衡时的转化率与原平衡相同,平
2 2 2
衡后再将后面“0.5molH”加入,平衡正向移动,CO 转化率将增大,D错误;
2 2
故答案为:B。
平衡常数的应用
①判断、比较可逆反应进行的程度
一般来说,一定温度下的一个具体的可逆反应:
正反应进行 平衡时生 平衡时反应 反应物
K值
的程度 成物浓度 物浓度 转化率
越大 越大 越大 越小 越高
越小 越小 越小 越大 越低
②判断正在进行的可逆反应的方向以及反应是否达到平衡
对于可逆反应:mA(g)+nB(g) pC(g)+qD(g),若浓度商Q=,则将浓度商和平衡常数作比较可得
c
可逆反应所处的状态。
③判断可逆反应的反应热
【变式7-1】(2023上·河南焦作)在可逆反应2SO
2
(g)+O 2⇌2SO
3
(g)的平衡状态下,保持恒温恒容向容器中
加入一定量的O,下列说法正确的是(K为平衡常数,Q 为浓度商)
2 c
A.Q 不变,K变大,O 转化率增大 B.Q 不变,K变大,SO 转化率增大
c 2 c 2
C.Q 变小,K不变,O 转化率减小 D.Q 增大,K不变,SO 转化率增大
c 2 c 2
【答案】C
【解析】当可逆反应2SO
2
(g)+O 2⇌2SO
3
(g)达到平衡状态后,保持温度不变,则平衡常数K不变;浓度商
,容器容积不变,向容器中充入一定量的O,分母变大,所以浓度商Q 减小,平衡正
2 c
向移动,由于充入了O,所以O 的转化率减小,故C正确;
2 2故选C。
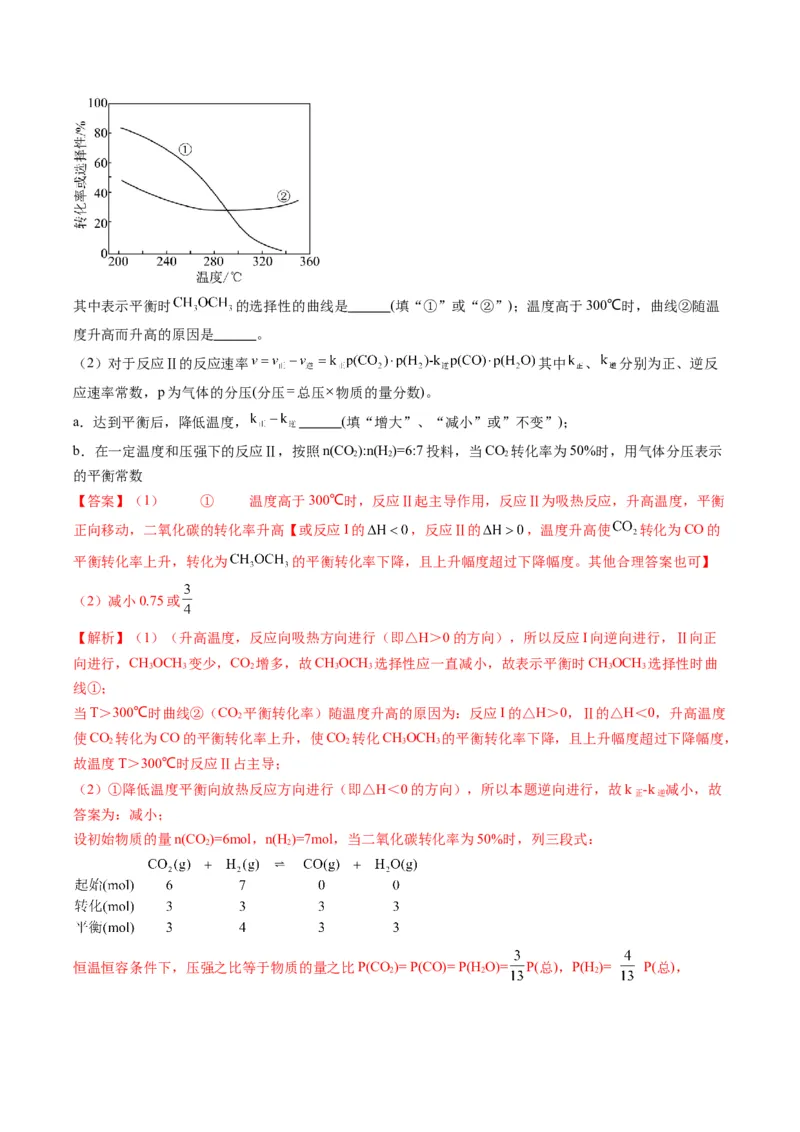
【变式7-2】(2023上·山西大同·高三统考期末)减少 排放并实现 的有效转化是科研的热点。以下
几种为常见的 利用方法,回答下列问题:
I.利用 干重整反应不仅可以对天然气资源综合利用,还可以缓解温室效应对环境的影响。该反
应一般认为通过如下步骤来实现:
反应iii:主反应
反应iv:副反应
反应iii、iv的平衡常数的 随 的变化曲线如图所示:
由图可知,代表反应iii的曲线是 (填“ ”或“ ”),原因是 ;升高温度,反应
iv的平衡常数 (填“增大”“减小”或“不变”)。
【答案】 Q 反应iii的 ,随温度升高,平衡常数 减小,故 随 的增大而增大
增大
【解析】因为反应ⅲ的 ,随温度升高,平衡常数 减小,故 随 的增大而增
大,对应图中的 曲线,另一条曲线 是反应ⅳ的变化曲线,故 ,随温度升高平衡常数 增大;
【考向八】化学平衡常数与速率常数、转化率之间计算
【典例8】(2023上·云南曲靖·高三曲靖一中校考)以节能减排为基础的低碳经济已成为实现人类可持续
发展的重要课题,“减排”的关键是减少CO 排放,而“减排” 的重要手段是合理利用CO。回答下列问
2 2
题:
(2)由CO 合成二甲醚的反应原理为:2CO(g)+6H(g)=CH OCH (g)+3HO(g) <0 。在恒容密闭容器
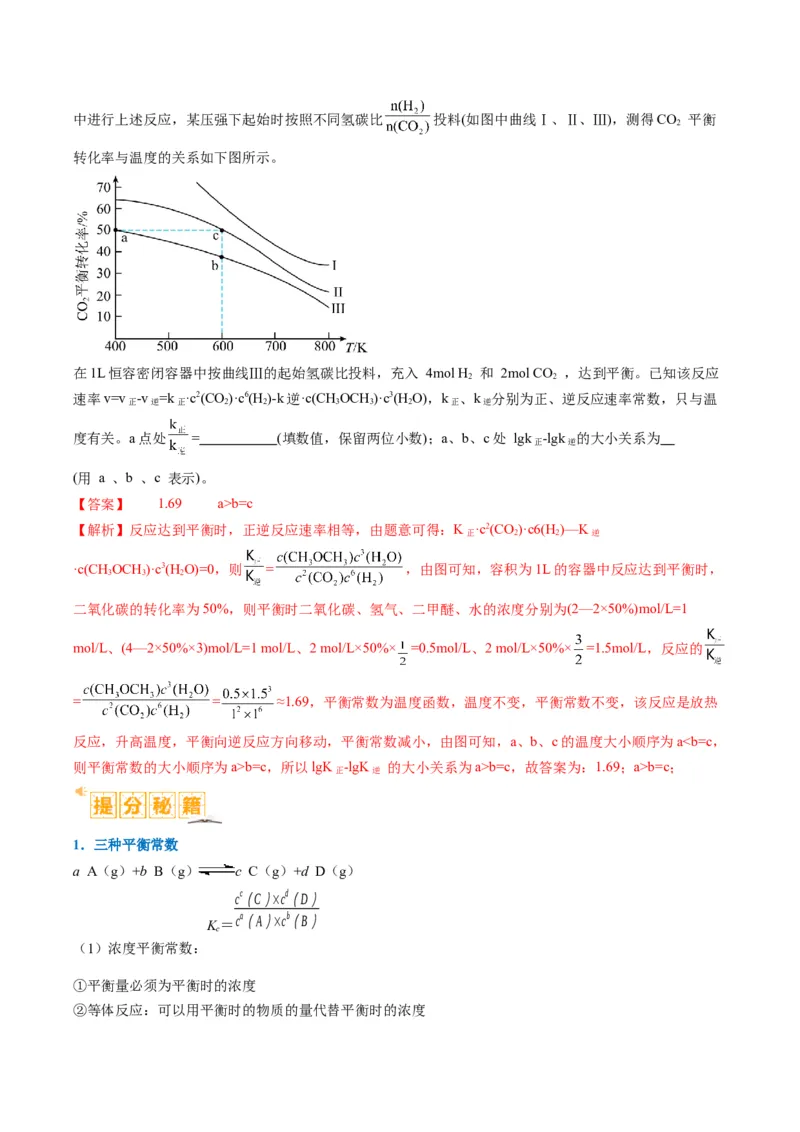
2 2 2 3 3 2中进行上述反应,某压强下起始时按照不同氢碳比 投料(如图中曲线Ⅰ、Ⅱ、Ⅲ),测得CO 平衡
2
转化率与温度的关系如下图所示。
在1L恒容密闭容器中按曲线Ⅲ的起始氢碳比投料,充入 4mol H 和 2mol CO ,达到平衡。已知该反应
2 2
速率v=v -v =k ·c2(CO)·c6(H )-k逆·c(CHOCH )·c3(H O),k 、k 分别为正、逆反应速率常数,只与温
正 逆 正 2 2 3 3 2 正 逆
度有关。a点处 = (填数值,保留两位小数);a、b、c处 lgk -lgk 的大小关系为
正 逆
(用 a 、b 、c 表示)。
【答案】 1.69 a>b=c
【解析】反应达到平衡时,正逆反应速率相等,由题意可得:K ·c2(CO)·c6(H)—K
正 2 2 逆
·c(CHOCH )·c3(H O)=0,则 = ,由图可知,容积为1L的容器中反应达到平衡时,
3 3 2
二氧化碳的转化率为50%,则平衡时二氧化碳、氢气、二甲醚、水的浓度分别为(2—2×50%)mol/L=1
mol/L、(4—2×50%×3)mol/L=1 mol/L、2 mol/L×50%× =0.5mol/L、2 mol/L×50%× =1.5mol/L,反应的
= = ≈1.69,平衡常数为温度函数,温度不变,平衡常数不变,该反应是放热
反应,升高温度,平衡向逆反应方向移动,平衡常数减小,由图可知,a、b、c的温度大小顺序为ab=c,所以lgK -lgK 的大小关系为a>b=c,故答案为:1.69;a>b=c;
正 逆
1.三种平衡常数
a A(g)+b B(g) c C(g)+d D(g)
cc(C)×cd(D)
K=ca(A)×cb(B)
c
(1)浓度平衡常数:
①平衡量必须为平衡时的浓度
②等体反应:可以用平衡时的物质的量代替平衡时的浓度③恒压条件下:先计算平衡体积,再算平衡常数
pc(C)×pd(D)
K =
pa(A)×pb(B)
p
(2)压强平衡常数:
①平衡量为平衡时的浓度、物质的量、体积等均可
n n
i i
n n
②分压P i =P 总 ×x i =P 总 × 总=(P 1 +P 2 +P 3 +…)× 总
③恒容条件下:先计算平衡总压,再算平衡常数或直接根据分压计算
xc(C)×xd(D)
(3)物质的量分数平衡常数:K=xa(A)×xb(B)
x
①平衡量为平衡时的浓度、物质的量、体积等均可
n
i
n
②物质的量分数:x= 总
i
2.常用计算公式
某物质反应的量
该物质的总量
(1)反应物的转化率: = ×100%
某组分的量
混合物的总量
(2)某组分的百分含量:含量= ×100%
①常见量:体积分数、物质的量分数
②关系式:体积分数=物质的量分数
3.速率常数和平衡常数的关系
基元反应:a A(g)+b B(g) c C(g)+d D(g)
速率方程
(1)抽象化速率方程:笼统的正逆反应速率
①v
正
=k
正
·ca(A)·cb(B)、v
逆
=k
逆
·cc(C)·cd(D)
②v
正
=k
正
·pa(A)·pb(B)、v
逆
=k
逆
·pc(C)·pd(D)
③v
正
=k
正
·xa(A)·xb(B)、v
逆
=k
逆
·xc(C)·xd(D)
(2)具体化速率方程:以具体物质表示的正逆反应速率
①v
A正
=k
正
·ca(A)·cb(B)、v
C逆
=k
逆
·cc(C)·cd(D)
②v
A正
=k
正
·pa(A)·pb(B)、v
C逆
=k
逆
·pc(C)·pd(D)
③v
A正
=k
正
·xa(A)·xb(B)、v
C逆
=k
逆
·xc(C)·xd(D)
4.速率常数和平衡常数
k k k
正 正 正
k k k
(1)抽象化:平衡条件v
正
=v
逆
,① 逆=K
c
;② 逆=K
p
;③ 逆=K
x
v k k k
a a a a
A正 正 正 正
(2)具体化:平衡条件 v C逆=c ,① k 逆=c K;② k 逆=c K ;③ k 逆=c K
c p x(3)升温对k 、k 的影响
正 逆
①放热反应:K值减小;k 值增大,k 值增大,k 变化更大
正 逆 逆
②吸热反应:K值增大;k 值增大,k 值增大,k 变化更大
正 逆 正
【变式8-1】(2023上·福建福州·高三福建省福州高级中学校考)在机动车发动机中,燃料燃烧产生的高温
会使空气中的氮气和氧气反应,生成氮氧化物,某些硝酸盐分解,也会产生氮氧化物,已知如下反应:
①
②
实验测得 , , 为速率常数且只受温度
影响。则化学平衡常数K与速率常数 的数学关系是 。若将容器的温度改变为 时,
其 ,则 (填“>”“<”或“=”)。
【答案】 <
【解析】由反应达到平衡时,正逆反应速率相等可得: = ,整理可得: =
=K,由三段式数据可知,反应的平衡常数K= =12.5,若将容器的温度改变为T 时,
2
其k =10k ,则T 下平衡常数K = =10<12.5,平衡向逆反应方向移动,该反应为放热反应,升高温度,
正 逆 2 2
平衡向逆反应方向移动,则T 小于T,故答案为: ;<;
1 2
【变式8-2】(2023上·云南)亚硝酰氯(ClNO)是有机合成中的重要试剂,可由NO与Cl 在通常条件下反
2
应得到,化学方程式为2NO(g)+Cl (g) 2ClNO(g)。
2
(1)已知亚硝酰氯的结构为Cl-N=O,几种化学键的键能数据如下表:
化学键 N≡O Cl-Cl Cl-N N=O
键能/(kJ/mol) 630 243 a 607
则2NO(g) +Cl (g) 2ClNO(g) 的ΔH= kJ/mol。(用含a的代数式表示)
2
(2)反应Cl(g) +2NO(g) 2ClNO(g)的速率方程式可表示为v =k ·c(Cl )c(NO), v =k ·c2(ClNO),其
2 正 正 2 逆 逆
中k 、k 代表正、逆反应的速率常数,其与温度、催化剂等有关,与浓度无关。已知:pk=-lgk。如图所
正 逆示有2条直线分别代表pk正、pk逆与 的关系,若该反应为放热反应,其中代表pk正与 关系的直线是
(填字母),理由是 。
【答案】(1)289-2a
(2) b 该可逆反应的正反应是放热反应,降温,平衡常数增大,正反应速率常数减小的程度小
于逆反应速率常数减小的程度
【解析】(1)2NO(g) +Cl (g) 2ClNO(g) 的ΔH=反应物的键能之和-生成物的键能之和=
2
(2×630+243)kJ·mol-1-(2a+2×607)kJ·mol-1=(289-2a)kJ·mol-1;
(2)该反应为放热反应,降低温度,平衡向正反应方向移动,反应的平衡常数增大,则正反应速率常数
减小的程度小于逆反应速率常数减小的程度,所以代表p与关系的直线是为b;
1.(2023·江苏卷)金属硫化物( )催化反应 ,既可以除去天然气
中的 ,又可以获得 。下列说法正确的是
A.该反应的B.该反应的平衡常数
C.题图所示的反应机理中,步骤Ⅰ可理解为 中带部分负电荷的S与催化剂中的M之间发生作用
D.该反应中每消耗 ,转移电子的数目约为
【答案】C
【解析】A.左侧反应物气体计量数之和为3,右侧生成物气体计量数之和为5, ,A错误;
B.由方程形式知, ,B错误;
C.由题图知,经过步骤Ⅰ后, 中带部分负电荷的S与催化剂中的M之间形成了作用力,C正确;
D.由方程式知,消耗 同时生成 ,转移 ,数目为 ,D错误;
故选C。
2.(2023·湖南卷)向一恒容密闭容器中加入 和一定量的 ,发生反应:
。 的平衡转化率按不同投料比 随温度的变化曲线
如图所示。下列说法错误的是
A.
B.反应速率:
C.点a、b、c对应的平衡常数:
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态
【答案】B
【解析】A.一定条件下,增大水的浓度,能提高CH 的转化率,即x值越小,CH 的转化率越大,则
4 4
,故A正确;
B.b点和c点温度相同,CH 的起始物质的量都为1mol,b点x值小于c点,则b点加水多,反应物浓度
4
大,则反应速率: ,故B错误;
C.由图像可知,x一定时,温度升高CH 的平衡转化率增大,说明正反应为吸热反应,温度升高平衡正向
4
移动,K增大;温度相同,K不变,则点a、b、c对应的平衡常数: ,故C正确;D.该反应为气体分子数增大的反应,反应进行时压强发生改变,所以温度一定时,当容器内压强不变时,
反应达到平衡状态,故D正确;
答案选B。
3.(2022·天津卷)向恒温恒容密闭容器中通入2mol 和1mol ,反应
达到平衡后,再通入一定量 ,达到新平衡时,下列有关判断错误的是
A. 的平衡浓度增大 B.反应平衡常数增大
C.正向反应速率增大 D. 的转化总量增大
【答案】B
【解析】A.平衡后,再通入一定量 ,平衡正向移动, 的平衡浓度增大,A正确;
B.平衡常数是与温度有关的常数,温度不变,平衡常数不变,B错误;
C.通入一定量 ,反应物浓度增大,正向反应速率增大,C正确;
D.通入一定量 ,促进二氧化硫的转化, 的转化总量增大,D正确;
故选B。
4.(2022·江苏卷)用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数
C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;
B.由方程式可知,反应平衡常数 ,故B正确;
C.由方程式可知,反应每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数
目为3mol×4× ×6.02×1023=3×6.02×1023,故C错误;
D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,柴油机车辆排放的氨气对空气污染程度
增大,故D错误;
故选B。
5.(2022·海南卷)某温度下,反应CH=CH (g)+HO(g) CHCHOH(g)在密闭容器中达到平衡,下列说
2 2 2 3 2
法正确的是A.增大压强, ,平衡常数增大
B.加入催化剂,平衡时 的浓度增大
C.恒容下,充入一定量的 ,平衡向正反应方向移动
D.恒容下,充入一定量的 , 的平衡转化率增大
【答案】C
【解析】A.该反应是一个气体分子数减少的反应,增大压强可以加快化学反应速率,正反应速率增大的
幅度大于逆反应的,故v > v ,平衡向正反应方向移动,但是因为温度不变,故平衡常数不变,A不正
正 逆
确;
B.催化剂不影响化学平衡状态,因此,加入催化剂不影响平衡时CHCHOH(g)的浓度,B不正确;
3 2
C.恒容下,充入一定量的HO(g),HO(g)的浓度增大,平衡向正反应方向移动,C正确;
2 2
D.恒容下,充入一定量的CH=CH (g),平衡向正反应方向移动,但是CH=CH (g)的平衡转化率减小,
2 2 2 2
D不正确;
综上所述,本题选C。
6.(2021·海南卷)制备水煤气的反应 ,下列说法正确的是
A.该反应
B.升高温度,反应速率增大
C.恒温下,增大总压,HO(g)的平衡转化率不变
2
D.恒温恒压下,加入催化剂,平衡常数增大
【答案】B
【解析】A.该反应的正反应是气体体积增大的反应,所以△S>0,A错误;
B.升高温度,物质的内能增加,分子运动速率加快,有效碰撞次数增加,因此化学反应速率增大,B正
确;
C.恒温下,增大总压,化学平衡向气体体积减小的逆反应方向移动,使HO(g)的平衡转化率减小,C错
2
误;
D.恒温恒压下,加入催化剂,化学平衡不移动,因此化学平衡常数不变,D错误;
故合理选项是B。
7.(2020·海南卷)NO与CO是燃油汽车尾气中的两种有害气体,常温常压下它们之间的反应:
CO(g)+ NO(g)=CO(g)+ N(g) ΔH= -374.3 kJ·mol-1 K=2.5×1060, 反应速率较小。有关该反应的说法正确
2 2
的是
A.K很大,NO与CO在排入大气之前就已反应完全
B.增大压强,平衡将向右移动,K> 2.5×1060
C.升高温度,既增大反应速率又增大K
D.选用适宜催化剂可达到尾气排放标准
【答案】D【解析】A.平衡常数很大,表示该反应所能进行的程度大,由于NO与CO反应速率较小,在排入大气之
前没有反应完全,故A错误;
B.平衡常数只与温度有关,增大压强,K不变,故B错误;
C.CO(g)+ NO(g)=CO(g)+ N(g)正反应放热,升高温度,速率加快,平衡逆向移动,K减小,故C错误;
2 2
D.选用适宜催化剂可加快反应速率,使尾气得到净化,达到尾气排放标准,故D正确;
选D。
8.(2022·湖南卷)向体积均为1L的两恒容容器中分别充入 和 发生反应:
,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所
示。下列说法正确的是
A. B.气体的总物质的量:
C.a点平衡常数: D.反应速率:
【答案】BC
【解析】A.甲容器在绝热条件下,随着反应的进行,压强先增大后减小,根据理想气体状态方程
PV=nRT可知,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即 <0,故A
错误;
B.根据A项分析可知,上述密闭溶液中的反应为放热反应,图中a点和c点的压强相等,因甲容器为绝
热过程,乙容器为恒温过程,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明甲容器中
气体的总物质的量此时相比乙容器在减小即气体总物质的量:n<n,故B正确;
a c
C.a点为平衡点,此时容器的总压为p,根据理想气体状态方程PV=nRT可知,在恒容条件下进行,气体
的物质的量之比等于 整体之比,根据A项分析可知,绝热条件下,反应到平衡状态放热,所以T>T ,
a 始
压强:Pa= P ,则n< n ,可设Y转化的物质的量浓度为xmol∙L−1,则列出三段式如下:
始 a 始
,则有 < ,计算得到x>0.75,那么化学平衡常数K= > ,故C正确;
D.根据图象可知,甲容器达到平衡的时间短,温度高,所以达到平衡的速率相对乙容器的快,即V >V
a正 b
,故D错误。
正
综上所述,答案为BC。
1.(2023·北京丰台·统考一模)下列三个化学反应焓变、平衡常数与温度的关系分别如下表所示。下列说
法正确的是
温度
平衡常
化学反应
数
973K 1173K
① 1.47 2.15
② 2.38 1.67
③ a b
A.1173K时,反应①起始 ,平衡时 约为0.4
B.反应②是吸热反应,
C.反应③达平衡后,升高温度或缩小反应容器的容积平衡逆向移动
D.相同温度下, ;
【答案】D
【解析】A.1173K时,反应①起始 ,
, ,x≈0.4,平衡时
约为0.2 ,A错误;
B.升温,化学平衡常数减小,说明平衡向逆反应方向移动,所以②的正反应为放热反应, ,B错
误;
C.根据盖斯定律可知②-①可得③,故 ,a=1.62,b=0.78,升温,化学平衡常数减小,说明平衡
向逆反应方向移动,所以 ,反应③达平衡后,升高温度平衡逆向移动,但是由于反应两端气体的化
学计量数之和相等缩小反应容器的容积化学平衡不移动,C错误;D.相同温度下,根据盖斯定律可知②-①可得③,故 ; ,D正确;
故选D。
2.O 也是一种很好的消毒剂,具有高效、洁净、方便、经济等优点。O 可溶于水,在水中易分解,产生
3 3
的[O]为游离氧原子,有很强的杀菌消毒能力。常温常压下发生反应如下:
反应①O O+[O] ΔH>0,平衡常数为K
3 2 1 1
反应②[O]+O 2O ΔH<0,平衡常数为K
3 2 2 2
总反应:2O 3O ΔH<0,平衡常数为K
3 2
下列叙述正确的是
A.压强增大,K 减小 B.总反应中当2v (O )=3v (O )时,反应达到平衡
2 正 2 逆 3
C.[O]为催化剂 D.K=K+K
1 2
【答案】B
【解析】A.平衡常数只受温度变化的影响,压强增大,温度不变,则平衡常数K 不变,A错误;
2
B.总反应为2O 3O,当2v (O )=3v (O )时,正、逆反应速率之比等于化学计量数之比,则反应达到
3 2 正 2 逆 3
平衡,B正确;
C.从题干可以看出,[O]为反应①的产物,对总反应来说,仅属于反应的中间产物,所以[O]不是该反应
的催化剂,C错误;
D.总反应=反应①+反应②,则K=K ∙K ,D错误;
1 2
故选B。
3.T℃时,在一固定容积的密闭容器中发生反应: ,按照不同配比充入A、
B,达到平衡时容器中A、B浓度变化如图中曲线(实线)所示,下列判断正确的是
A.T℃时,该反应的平衡常数值为4 B.c点没有达到平衡,此时反应向逆向进行
C.若c点为平衡点,则此时容器内的温度高于T℃D.T℃时,直线cd上的点均为平衡状态
【答案】C【解析】A.根据平衡常数的表达式并结合图中曲线可知, ,故A错误;
B.c点没有达到平衡,如果达到平衡,应向d点移动,A、B的浓度降低,说明平衡向正反应方向移动,
故B错误;
C.如果c点达到平衡,此时的平衡常数小于T℃时的平衡常数,说明平衡向逆反应方向移动,即升高温度,
故C正确;
D.平衡常数只受温度的影响,与浓度、压强无关,因此曲线b是平衡线,故D错误;
故选C。
4.(2024上·云南昆明·高二统考期末)CO 资源化利用受到越来越多的关注,它能有效减少碳排放,有效
2
应对全球的气候变化,并且能充分利用碳资源。二氧化碳催化加氢制甲醇有利于减少温室气体排放,涉及
的反应如下:
Ⅰ.
Ⅱ. kJ⋅mol-1
Ⅲ. kJ⋅mol-1
回答下列问题:
(1) kJ⋅mol-1。
(2)平衡常数 (用 、 表示)。
【答案】(1)-49.5
(2)
【解析】(1)由题干信息可知,反应Ⅱ. kJ⋅mol-1,反
应Ⅲ. kJ⋅mol-1,反应Ⅱ+反应Ⅲ即可得到反应Ⅰ.
根据盖斯定律可知, =
=40.9kJ/mol+(-90.4kJ/mol)=-49.5kJ/mol,故答案为:-49.5;
(2)由小问(1)分析可知,反应Ⅱ+反应Ⅲ即可得到反应Ⅰ,故平衡常数 × ,故答案为: ×
;
5.(2023上·浙江嘉兴)在可逆反应2SO +O 2SO 的平衡状态下,保持恒温、恒容向容器中加入一定
2 2 3
量的O,下列说法正确的是(K为平衡常数,Q 为浓度商)
2 c
A.K不变,Q