文档内容
高考解密04 氧化还原反应
A 组 基础练
1.(2022·天津·耀华中学模拟预测)水热法制备Fe O 纳米颗粒的总反应为:3Fe2++2S O +O +XOH-
3 4 2 2
=Fe O+S O +2H O,下列说法正确的是
3 4 4 2
A.铁元素被氧化,硫元素被还原 B.Fe2+、SO 都是还原剂
2
C.X=2 D.每生成1molFe O,则转移电子数2mol
3 4
2.(2022·河南·模拟预测)下列物质按给定的投料方式,两者均能恰好完全反应的是
A.把 、 按物质的量之比为1:3充入容器中,在一定条件下充分反应
B.向 溶液中滴入 溶液使 恰好沉淀完全
C.常温下,将2molFe投入到含7mol硝酸的稀硝酸中充分反应
D.常温下,将1mol铝投入到含5mol硫酸的浓硫酸中充分反应
3.(2022·陕西·西安工业大学附中模拟预测)利用NaClO氧化尿素制备NH•H O(水合肼)的实验流程如图
2 4 2
所示:
已知:①氯气与烧碱溶液的反应是放热反应;②NH•H O有强还原性,能与NaClO剧烈反应生成N。下
2 4 2 2
列说法正确的是
A.步骤I中无需控制反应的温度
B.步骤I制备NaClO溶液时,测得产物中NaClO与NaClO 的物质的量之比为5∶1,则参与反应的氧化
3
剂与还原剂的物质的量之比为3∶5
C.步骤II中可将尿素水溶液逐滴滴入NaClO碱性溶液中
D.生成水合肼反应的离子方程式为:ClO-+CO(NH )+2OH-=Cl-+N H•H O+CO
2 2 2 4 24.(2023·广东·深圳市光明区高级中学模拟预测)工业上可用如下方法处理含HS的尾气,同时制得
2
NaSO,工艺流程如下:含HS的尾气、空气→反应炉(高温)→Na CO 溶液吸收→一系列操作→NaSO
2 2 3 2 2 3 2 2 3
晶体
已知:2HS+3O 2SO +2H O、 。
2 2 2 2
下列说法中错误的是
A.含HS的尾气可以用NaOH溶液处理后直接排放
2
B.反应中至少发生3个氧化还原反应
C.反应过程中证明了HSO 的酸性强于HS
2 3 2
D.每制取1 mol Na SO,理论上消耗氧气的体积为44.8 L(标准状况)
2 2 3
5.(2022·四川雅安·模拟预测)铁橄榄石 [Fe (SiO)]是嫦娥五号月壤的主要含铁矿物之一,我国科学家发
2 4
现陨石撞击过程的高温高压可引发铁橄榄石发生熔融产生 , 发生反应形成 与 ,下列相关选
项错误的是
A.铁橄榄石是一种硅酸盐,可改写为
B.该反应的方程式为:
C.铁橄榄石熔融产生自由移动的 属于化学变化
D.该研究证明了月壤中存在歧化成因的单质铁
6.(2022·河北·霸州市第一中学模拟预测)铼(Re)是一种极其稀少的贵金属。一种以辉钼矿(主要含有
MoS 以及少量ReS 、CuReS 、FeS、SiO 等)为原料制备铼的工艺流程如下:
2 2 4 2
已知“氧化焙烧”后成分有:SiO、Re O、MoO 、CuO、Fe O,其中Re O、MoO 与氨水反应分别生成
2 2 7 3 3 4 2 7 3
NH ReO、(NH )MoO 。
4 4 4 2 4
下列说法错误的是
A.“氧化焙烧”时,ReS 反应后的氧化产物为Re O 和SO
2 2 7 2
B.若改用NaOH溶液代替氨水“浸出”,滤渣成分不变C.由MoS 生成1mol MoO ,转移14mol电子
2 3
D.“电沉积”后,金属铼在阴极生成
7.(2022·河北·霸州市第一中学模拟预测)连二亚硫酸钠(Na SO)也称保险粉,该物质不溶于乙醇,溶于
2 2 4
氢氧化钠溶液,遇少量水或暴露在潮湿的空气中会发生剧烈反应并燃烧,且有刺激性气味气体产生;将甲
酸和NaOH溶液混合,再通入SO 气体,会得到保险粉。下列说法错误的是
2
A. NaSO 遇水所发生的是放热反应,燃烧时会有SO 产生
2 2 4 2
B. NaSO 属于盐,既有氧化性又有还原性
2 2 4
C. NaSO 能和新制氯水反应,但不能和浓硝酸反应
2 2 4
D.制备保险粉的反应为
8.(2022·海南·一模)(双选)工业上将氯气通入到石灰乳中制备漂白粉,制备流程如下。下列有关说法
正确的是
A.漂白粉是混合物
B.“反应”中 是氧化剂,石灰乳是还原剂
C.将 通入到烧碱溶液中也可以制得具有漂白性的物质
D.工业制备漂白粉的离子方程式为
9.(2022·浙江省宁波市鄞州中学模拟预测)K[Fe(C O)]·3H O晶体光照分解后产生KC O 和FeC O,
3 2 4 3 2 2 2 4 2 4
且分解产物中的CO 和HO以气体形式离子晶体。某次测定分解后的样品中C 的质量分数为53.86%。
2 2 2
请回答:
已知:M{K [Fe(C O)]·3H O}=491 g·mol-1。
3 2 4 3 2
(1)写出K[Fe(C O)]·3H O晶体分解反应的化学方程式:___________。
3 2 4 3 2
(2)晶体的分解百分率为___________。(写出简要计算过程)
10.(2022·安徽·淮北市教育科学研究所一模)铬是人体必须的微量元素,在人体代谢中发挥着特殊作用。
回答下列问题:
(1)金属铬可以通过焦炭高温还原铬铁矿(FeCrO)制取,同时生成一种有毒的气体,该反应的化学方程式为
2 4______。
(2)①取冶炼所得的金属铬溶解在盐酸中制取CrCl 溶液,其中混有FeCl 杂质,请完成除杂方案:向溶液中
3 2
加入足量NaOH溶液,过滤,向滤液中______,过滤,将固体溶解在稀盐酸中(已知Cr(OH) 是两性氢氧化
3
物)。
②由CrCl 溶液得到CrCl •6H O,除去其结晶水的操作是______。
3 3 2
(3)Cr3+在碱性条件下易被氧化成CrO ,写出向CrCl 溶液中加入氨水和过氧化氢发生反应的离子方程式
3
______。
(4)CrO 在酸性条件下可转化为Cr O ,Cr O 可以用来检验HO,原理是Cr O +4H O+2H+
2 2 2 2 2 2 2
2CrO(蓝色)+5H O。
5 2
①CrO 中铬元素为+6价,其中过氧键的数目为______。
5
②酸化重铬酸钾选用的酸为______(填标号)。
a.稀盐酸 b.稀硫酸 c.氢碘酸 d.磷酸
B 组 提升练
1.(2022·浙江·模拟预测)误服白磷( ),应立即用2%硫酸铜溶液洗胃,其反应是
,下列说法正确的是
A.白磷( )只发生了氧化反应
B. 是还原产物
C.氧化产物和还原产物的物质的量之比为
D. 能氧化
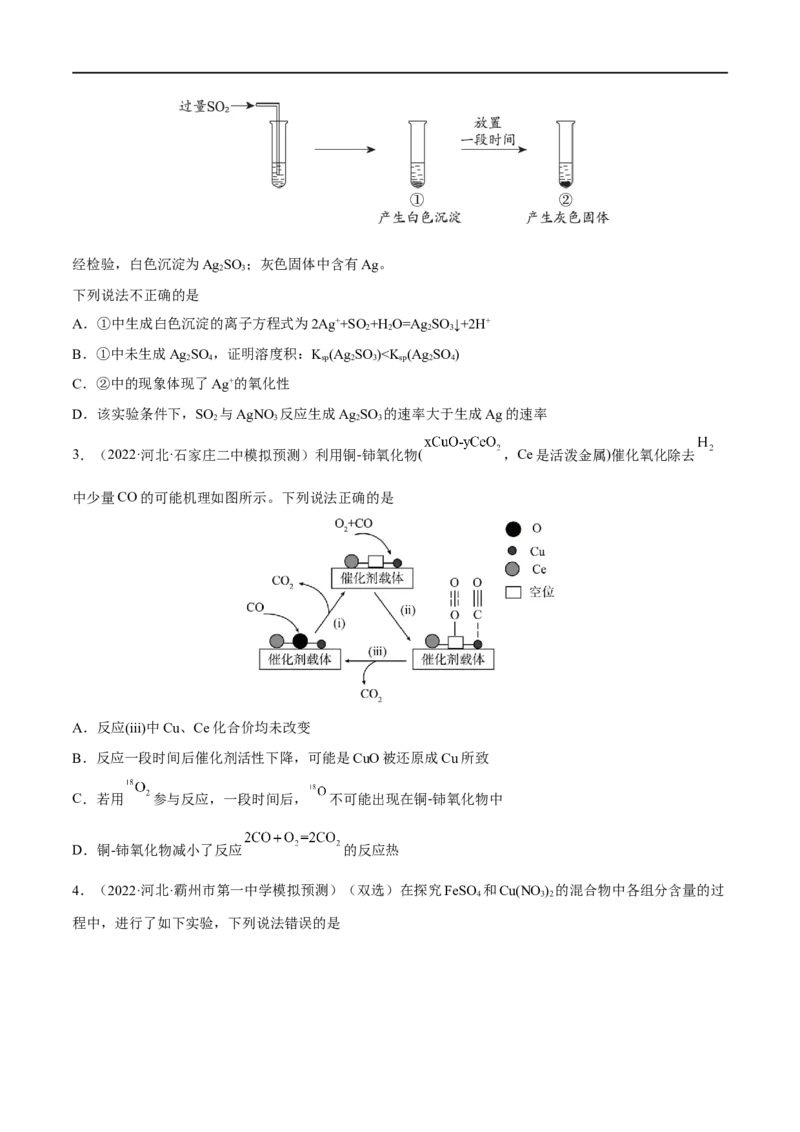
2.(2022·北京海淀·二模)向AgNO 溶液中通入过量SO ,过程和现象如图。
3 2经检验,白色沉淀为Ag SO ;灰色固体中含有Ag。
2 3
下列说法不正确的是
A.①中生成白色沉淀的离子方程式为2Ag++SO+H O=Ag SO ↓+2H+
2 2 2 3
B.①中未生成Ag SO ,证明溶度积:K (Ag SO )