文档内容
高频考点 10 钠、镁、铝及其化合物
1.(2022·江苏卷)少量 与 反应生成 和 。下列说法正确的是( )
A. 的电子式为 B. 的空间构型为直线形
C. 中O元素的化合价为-1 D. 仅含离子键
1.C A.过氧化钠是离子化合物,电子式是 ,A错误;B. 中氧原子的成键
电子对是2,孤电子对是2,根据价层电子对为4,根据价层电子对互斥理论,其空间构型为V形,B错误;
C. 中H显+1价,根据正负化合价为0,可计算出O的化合价为-1,C正确;D. 中O和H之间
是共价键,D错误;故选C。
2.(2022·广东卷)劳动开创未来。下列劳动项目与所述的化学知识没有关联的是( )
选
劳动项目 化学知识
项
A 面包师用小苏打作发泡剂烘焙面包 可与酸反应
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
C 工人将模具干燥后再注入熔融钢水 铁与 高温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
2. A A.小苏打是碳酸氢钠,不是碳酸钠,主要用来做膨松剂,故A符合题意;B.熟石灰是氢氧化钙,
具有碱性,可以用于处理酸性废水,故B不符合题意;C.熔融的铁与水蒸气在高温下反应会生成四氧化
三铁和氢气,因此必须将模具干燥,故C不符合题意;D.钢板上镀铝,保护钢板,金属铝表面形成致密
氧化膜而保护金属铝不被腐蚀,,故D不符合题意。综上所述,答案为A。
3.(2022·湖南卷)铝电解厂烟气净化的一种简单流程如下:下列说法错误的是()
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有 和
D.滤液可回收进入吸收塔循环利用
3.C A.陶瓷的成分中含有SiO ,SiO 能与烟气中的HF发生反应,因此不宜用陶瓷作吸收塔内衬材料,
2 2
故A正确;B.采用溶液喷淋法可增大反应物的接触面积,提高吸收塔内烟气吸收效率,故B正确;C.由
上述分析可知,合成槽内发生反应 ,产物是 和 ,
故C错误;D.由上述分析可知,滤液的主要成分为 ,可进入吸收塔循环利用,故D正确;答案选
C。
4.(2021·湖北卷)金属Na溶解于液氨中形成氨合钠离子和氨合电子,向该溶液中加入穴醚类配体L,得
到首个含碱金属阴离子的金黄色化合物[NaL]+Na-。下列说法错误的是( )
A.Na-的半径比F-的大 B.Na-的还原性比Na的强
C.Na-的第一电离能比H-的大 D.该事实说明Na也可表现出非金属性
4..C A. 核外有3个电子层、 核外有2个电子层,故 的半径比 的大,A项正确;B. 的
半径比Na的大, 中原子核对最外层电子的引力小,易失电子,故 的还原性比Na的强,B项正确;
C. 的1s上有2个电子,为全充满稳定结构,不易失去电子,故 的第一电离能比 的小,C项错误;
D.该事实说明Na可以形成 ,得电子表现出非金属性,D项正确。故选C。
5.(2021·湖南卷)一种工业制备无水氯化镁的工艺流程如下:下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融 制备金属镁
C.“氯化”过程中发生的反应为
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水
5. D A.物质X的作用是使Mg2+转化为Mg(OH) ,工业上常采用CaO,发生CaO+H O=Ca(OH) ,
2 2 2
Ca(OH) +Mg2+=Mg(OH) +Ca2+,A正确;B.Mg是较活泼金属,工业上常用电解熔融 制备金属镁,B
2 2
正确;C.由图可知“氯化”过程反应物为MgO、氯气、C,生成物之一为MgCl ,C在高温下能将二氧化
2
碳还原为CO,则“气体”为CO,反应方程式为 ,C正确;D.“煅烧”
后得到MgO,MgO和盐酸反应得到MgCl 溶液,由于MgCl 在溶液中水解为氢氧化镁和HCl,将所得溶液加
2 2
热蒸发HCl会逸出,MgCl 水解平衡正向移动,得到氢氧化镁,得不到无水MgCl ,D错误;选D。
2 2
6.(2022·烟台高三模拟)下列物质性质和用途均正确且有因果关系的是( )
选项 性质 用途
A ClO 具有还原性 ClO 可用于自来水的杀菌消毒
2 2
B Al(OH) 具有弱碱性 Al(OH) 可用作胃酸中和剂
3 3
C Fe3+具有氧化性 Fe (SO ) 可用作净水剂
2 4 3
D NH HCO 受热易分解 NH HCO 可用作氮肥
4 3 4 3
6.B A.ClO 可用于自来水的杀菌消毒,是因为ClO 具有氧化性,故A错误;
2 2
B.Al(OH) 具有弱碱性,能与盐酸反应生成氯化铝和水,所以Al(OH) 可用作胃酸中和剂,故B正确;C.
3 3Fe (SO ) 可用作净水剂是因为Fe3+水解生成氢氧化铁胶体,吸附水中悬浮杂质,故C错误;D.NH HCO 可
2 4 3 4 3
用作氮肥是因为含有N元素,故D错误;选B。
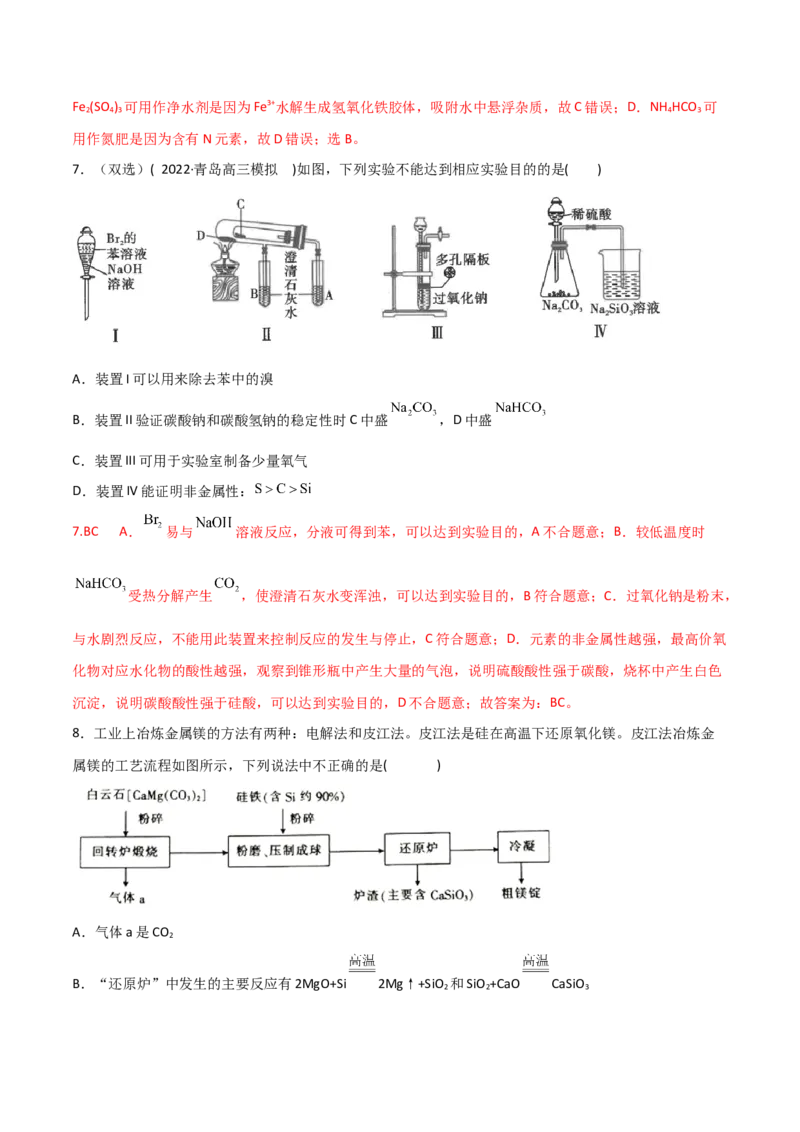
7.(双选)( 2022·青岛高三模拟 )如图,下列实验不能达到相应实验目的的是( )
A.装置I可以用来除去苯中的溴
B.装置II验证碳酸钠和碳酸氢钠的稳定性时C中盛 ,D中盛
C.装置III可用于实验室制备少量氧气
D.装置IV能证明非金属性:
7.BC A. 易与 溶液反应,分液可得到苯,可以达到实验目的,A不合题意;B.较低温度时
受热分解产生 ,使澄清石灰水变浑浊,可以达到实验目的,B符合题意;C.过氧化钠是粉末,
与水剧烈反应,不能用此装置来控制反应的发生与停止,C符合题意;D.元素的非金属性越强,最高价氧
化物对应水化物的酸性越强,观察到锥形瓶中产生大量的气泡,说明硫酸酸性强于碳酸,烧杯中产生白色
沉淀,说明碳酸酸性强于硅酸,可以达到实验目的,D不合题意;故答案为:BC。
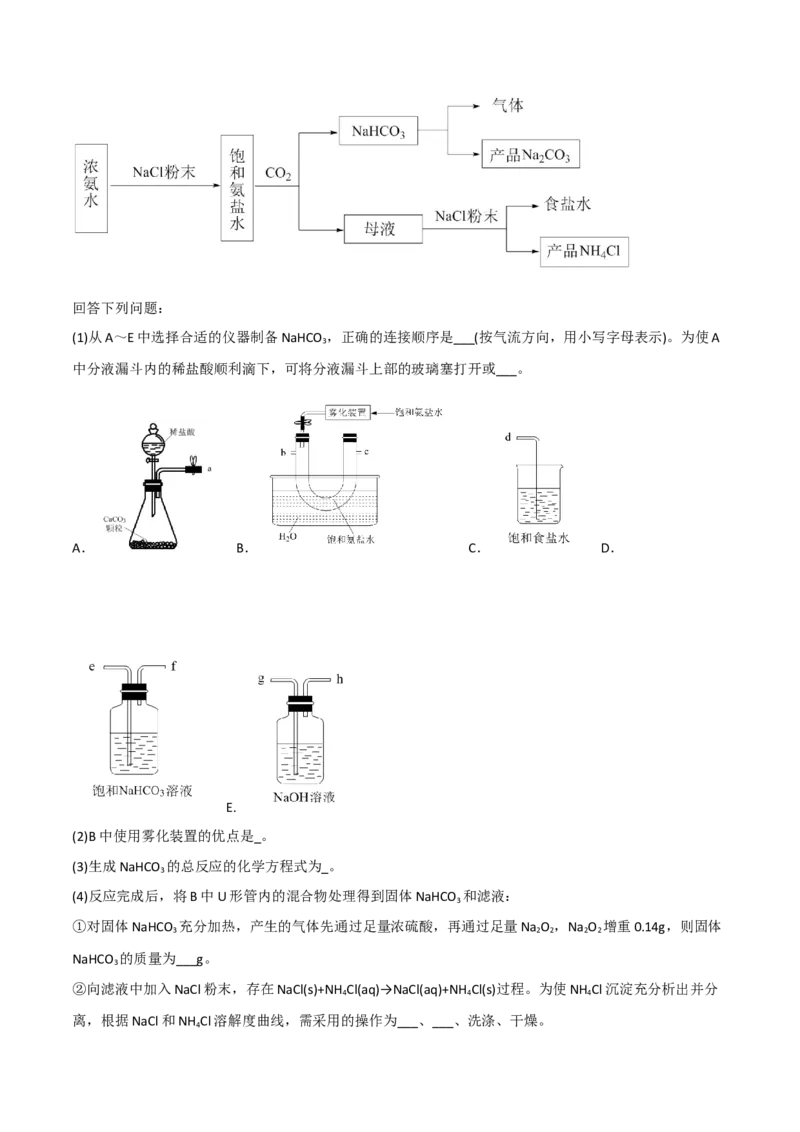
8.工业上冶炼金属镁的方法有两种:电解法和皮江法。皮江法是硅在高温下还原氧化镁。皮江法冶炼金
属镁的工艺流程如图所示,下列说法中不正确的是( )
A.气体a是CO
2
B.“还原炉”中发生的主要反应有2MgO+Si 2Mg↑+SiO 和SiO +CaO CaSiO
2 2 3C.“还原炉”中抽空气到接近真空的原因是防止还原得到的Mg在高温条件下再次被氧化
D.“回转炉煅烧”的产物为CaO和MgO,其中电解法就是电解熔融的氧化镁来制备金属镁
8.D A.根据常见碳酸盐的性质可知白云石高温条件下会分解为氧化钙、氧化镁和二氧化碳,气体a为二
氧化碳,A正确;B.白云石煅烧后得到氧化钙、氧化镁,然后高温条件下用Si还原MgO得到Mg单质,
同时二氧化硅和氧化钙反应得到硅酸钙,发生的反应为2MgO+Si 2Mg↑+SiO 和SiO +CaO CaSiO ,
2 2 3
B正确;C.Mg活泼性较强,易被氧气氧化,所以抽空气到接近真空进行还原,C正确;D.氧化镁的熔点
较高,电解法制备Mg单质,需要电解熔点较低的熔融MgCl ,D错误;综上所述答案为D。
2
9.(2022·江苏启东高三期中))某兴趣小组模拟用粉煤灰(主要含Al O 、SiO 等)制备Al (SO )(OH) 溶液,
2 3 2 2 4 x 6-2x
并用其脱除烟气中的SO ,其流程如下:
2
下列说法错误的是( )
A.浸取时发生反应的离子方程式为Al O +6H+=2Al3++3H O
2 3 2
B.滤渣1和滤渣2的主要成分分别为SiO 和CaSO
2 4
C.为增强SO 的脱除效果,可在现有基础上再加入过量碳酸钙
2
D.若b<a(热分解完全),则循环液的碱性比吸收SO 前溶液的碱性弱
2
9.C A.浸取时氧化铝和硫酸反应生成硫酸铝和水,发生反应的离子方程式为Al O +6H+=2Al3++3H O,故
2 3 2
A正确;B.SiO 和硫酸不反应,所以滤渣1的成分是SiO ,用碳酸钙和硫酸反应调节溶液的pH生成
2 2
CaSO ,滤渣2的主要成分为CaSO ,故B正确;
4 4
C.加入过量碳酸钙会使溶液pH>3.6,生成氢氧化铝沉淀,SO 的脱除效果降低,故C错误;
2
D.若b<a(热分解完全),说明部分SO 没有释放,则氢氧根离子浓度降低,则循环液的碱性比吸收SO 前
2 2
溶液的碱性弱,故D正确;选C。
10.(2021·河北卷)化工专家侯德榜发明的侯氏制碱法为我国纯碱工业和国民经济发展做出了重要贡献,
某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备NaHCO ,进一步处理得到产品Na CO 和NH Cl,实
3 2 3 4
验流程如图:回答下列问题:
(1)从A~E中选择合适的仪器制备NaHCO ,正确的连接顺序是___(按气流方向,用小写字母表示)。为使A
3
中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或___。
A. B. C. D.
E.
(2)B中使用雾化装置的优点是_。
(3)生成NaHCO 的总反应的化学方程式为_。
3
(4)反应完成后,将B中U形管内的混合物处理得到固体NaHCO 和滤液:
3
①对固体NaHCO 充分加热,产生的气体先通过足量浓硫酸,再通过足量Na O ,Na O 增重0.14g,则固体
3 2 2 2 2
NaHCO 的质量为___g。
3
②向滤液中加入NaCl粉末,存在NaCl(s)+NH Cl(aq)→NaCl(aq)+NH Cl(s)过程。为使NH Cl沉淀充分析出并分
4 4 4
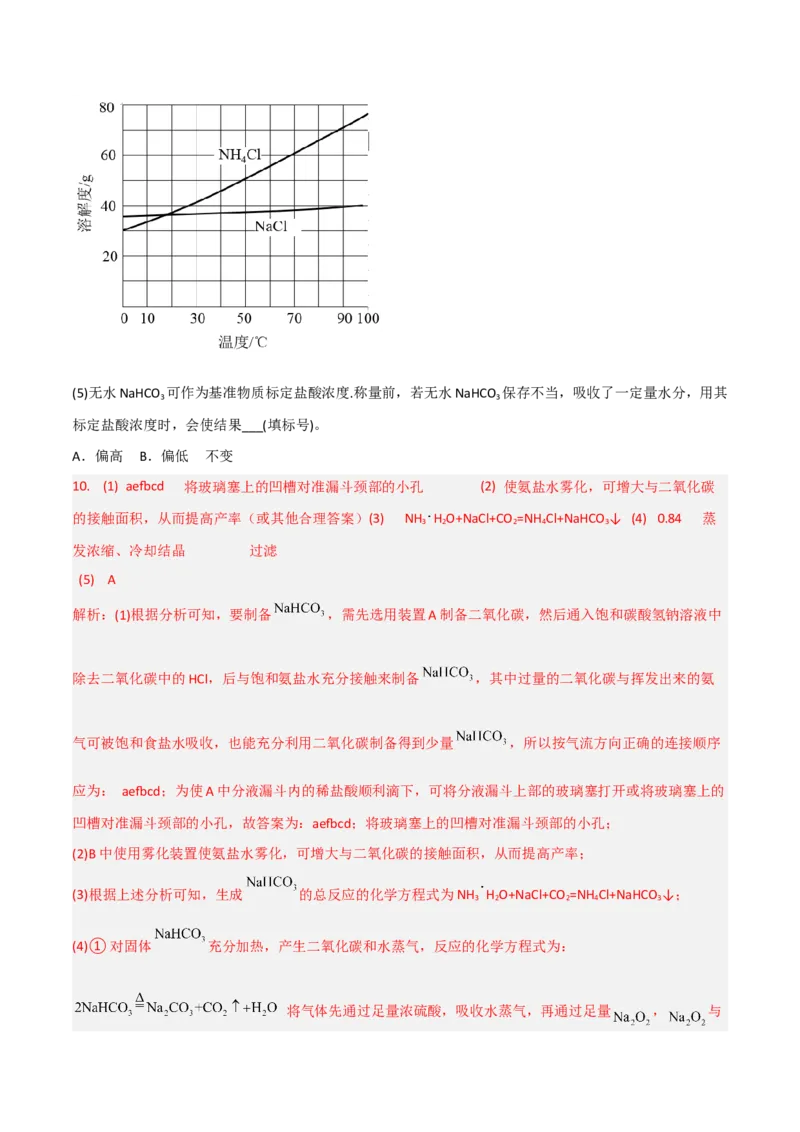
离,根据NaCl和NH Cl溶解度曲线,需采用的操作为___、___、洗涤、干燥。
4(5)无水NaHCO 可作为基准物质标定盐酸浓度.称量前,若无水NaHCO 保存不当,吸收了一定量水分,用其
3 3
标定盐酸浓度时,会使结果___(填标号)。
A.偏高 B.偏低 不变
10. (1) aefbcd 将玻璃塞上的凹槽对准漏斗颈部的小孔 (2) 使氨盐水雾化,可增大与二氧化碳
的接触面积,从而提高产率(或其他合理答案)(3) NH H O+NaCl+CO =NH Cl+NaHCO ↓ (4) 0.84 蒸
3 2 2 4 3
发浓缩、冷却结晶 过滤
(5) A
解析:(1)根据分析可知,要制备 ,需先选用装置A制备二氧化碳,然后通入饱和碳酸氢钠溶液中
除去二氧化碳中的HCl,后与饱和氨盐水充分接触来制备 ,其中过量的二氧化碳与挥发出来的氨
气可被饱和食盐水吸收,也能充分利用二氧化碳制备得到少量 ,所以按气流方向正确的连接顺序
应为: aefbcd;为使A中分液漏斗内的稀盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或将玻璃塞上的
凹槽对准漏斗颈部的小孔,故答案为:aefbcd;将玻璃塞上的凹槽对准漏斗颈部的小孔;
(2)B中使用雾化装置使氨盐水雾化,可增大与二氧化碳的接触面积,从而提高产率;
(3)根据上述分析可知,生成 的总反应的化学方程式为NH H O+NaCl+CO =NH Cl+NaHCO ↓;
3 2 2 4 3
(4)①对固体 充分加热,产生二氧化碳和水蒸气,反应的化学方程式为:
将气体先通过足量浓硫酸,吸收水蒸气,再通过足量 , 与二氧化碳反应生成碳酸钠和氧气,化学方程式为: ,根据方程式可知,根据
差量法可知,当增重 (2CO的质量)时,消耗的二氧化碳的质量为 =0.22g,其物质的量为
,根据关系式 可知,消耗的 的物质的量为2
0.005mol=0.01mol,所以固体 的质量为0.01mol 84g/mol=0.84g;
②根据溶解度虽温度的变化曲线可以看出,氯化铵的溶解度随着温度的升高而不断增大,而氯化钠的溶解
度随着温度的升高变化并不明显,所以要想使 沉淀充分析出并分离,需采用蒸发浓缩、冷却结晶、
过滤、洗涤、干燥的方法,故答案为:蒸发浓缩、冷却结晶、过滤;
(5)称量前,若无水 保存不当,吸收了一定量水分,标准液被稀释,浓度减小,所以用其标定盐酸
浓度时,消耗的碳酸氢钠的体积 会增大,根据c(测)= 可知,最终会使c(测)偏高,A项符合
题意,故答案为:A。