文档内容
高频考点 11 铁及其化合物
题点(一)铁及其化合物的性质
1.(2022·辽宁卷)镀锌铁钉放入棕色的碘水中,溶液褪色;取出铁钉后加入少量漂白粉,溶液恢复棕色;
加入 ,振荡,静置,液体分层。下列说法正确的是( )
A.褪色原因为 被 还原 B.液体分层后,上层呈紫红色
C.镀锌铁钉比镀锡铁钉更易生锈 D.溶液恢复棕色的原因为 被氧化
1.D A. 比 活泼,更容易失去电子,还原性更强,先与 发生氧化还原反应,故溶液褪色原因为
被 还原,A项错误;B.液体分层后, 在 层, 的密度比水大,则下层呈紫红色,B项错误;
C.若镀层金属活泼性大于 ,则 不易生锈,反之,若 活泼性大于镀层金属,则 更易生锈,由于活
泼性: ,则镀锡铁钉更易生锈,C项错误;D.漂白粉的有效成分为 ,其具有强氧化性,
可将 氧化,D项正确;答案选D。
2.(2021·河北卷)“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其《本草经集
注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生
铁熔化灌入熟铁,再锻打成钢。下列说法错误的是( )
A.钢是以铁为主的含碳合金
B.钢的含碳量越高,硬度和脆性越大
C.生铁由于含碳量高,熔点比熟铁高
D.冶炼铁的原料之一赤铁矿的主要成分为Fe O
2 3
2.C A.钢是含碳量低的铁合金,故A正确;B.钢的硬度和脆性与含碳量有关,随着含碳量的增大而增
大,故正确;C.由题意可知,生铁熔化灌入熟铁,再锻打成钢,说明生铁的熔点低于熟铁,故C错误;
D.赤铁矿的主要成分是Fe O ,可用于冶炼铁,故D正确;故选C。
2 3
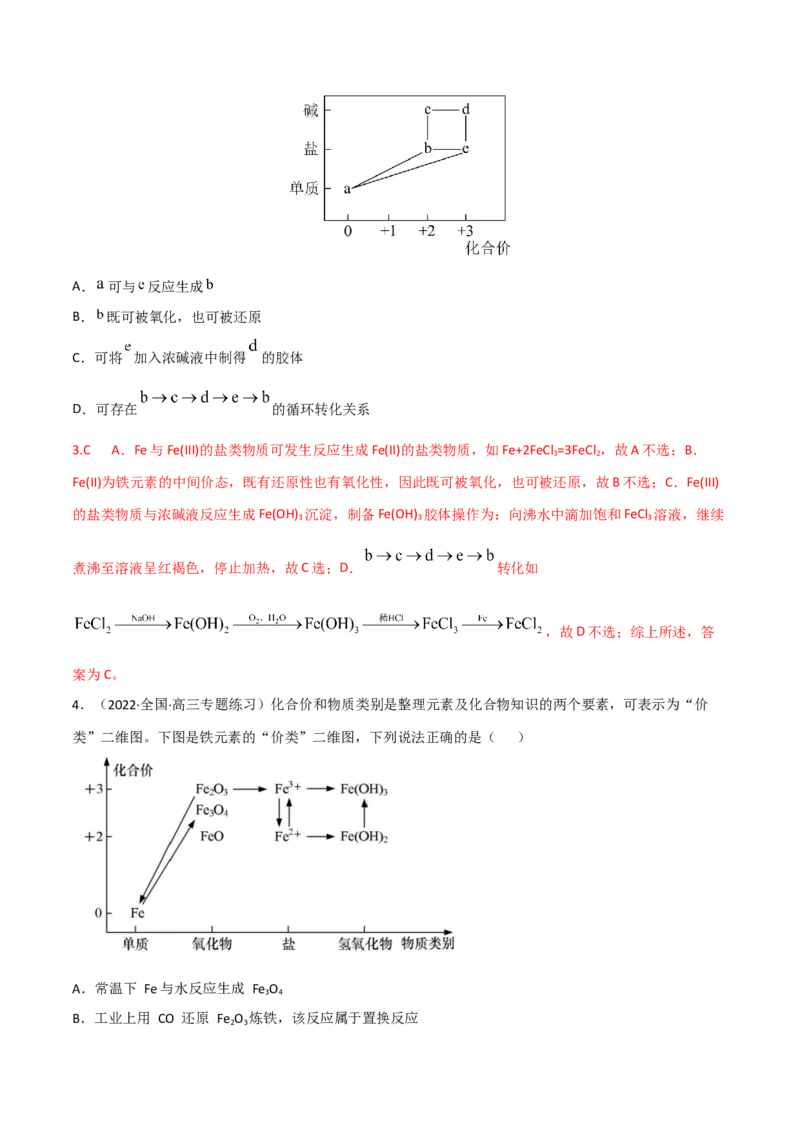
3.(2021·广东卷)部分含铁物质的分类与相应化合价关系如图所示。下列推断不合理的是( )A. 可与 反应生成
B. 既可被氧化,也可被还原
C.可将 加入浓碱液中制得 的胶体
D.可存在 的循环转化关系
3.C A.Fe与Fe(III)的盐类物质可发生反应生成Fe(II)的盐类物质,如Fe+2FeCl =3FeCl ,故A不选;B.
3 2
Fe(II)为铁元素的中间价态,既有还原性也有氧化性,因此既可被氧化,也可被还原,故B不选;C.Fe(III)
的盐类物质与浓碱液反应生成Fe(OH) 沉淀,制备Fe(OH) 胶体操作为:向沸水中滴加饱和FeCl 溶液,继续
3 3 3
煮沸至溶液呈红褐色,停止加热,故C选;D. 转化如
,故D不选;综上所述,答
案为C。
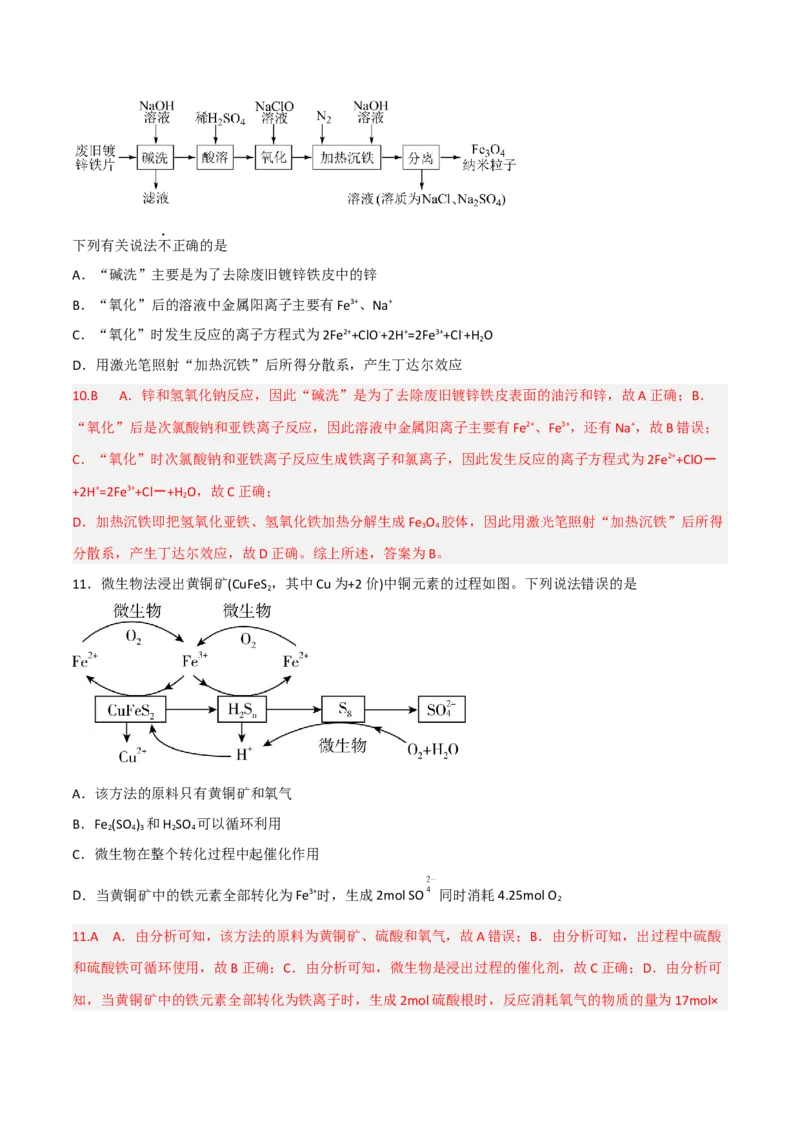
4.(2022·全国·高三专题练习)化合价和物质类别是整理元素及化合物知识的两个要素,可表示为“价
类”二维图。下图是铁元素的“价类”二维图,下列说法正确的是( )
A.常温下 Fe与水反应生成 Fe O
3 4
B.工业上用 CO 还原 Fe O 炼铁,该反应属于置换反应
2 3C.维生素C能将 Fe3+转化为 Fe2+,过程中维生素C做还原剂
D.Fe(OH) 浊液露置于空气中,白色迅速转变为红褐色
2
4.C A.Fe与水在高温条件下才反应生成Fe O ,故A错误;B.CO和Fe O 均为化合物,不符合置换反应
3 4 2 3
的形式,故B错误;C.Fe3+转化为 Fe2+,Fe元素化合价降低被还原,说明维生素C做还原剂,故C正确;
D.Fe(OH) 浊液露置于空气中,白色迅速转变为灰绿色,最终变成红褐色,故D错误;综上所述答案为
2
C。
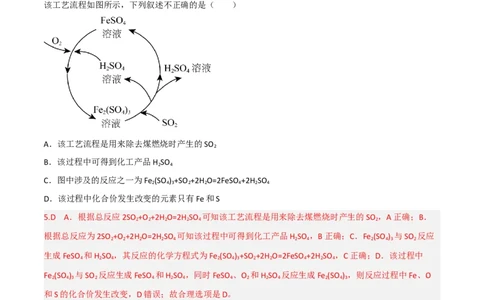
5.含硫煤燃烧会产生大气污染物,为防治该污染,某工厂设计了新的治污方法,同时可得到化工产品,
该工艺流程如图所示,下列叙述不正确的是( )
A.该工艺流程是用来除去煤燃烧时产生的SO
2
B.该过程中可得到化工产品H SO
2 4
C.图中涉及的反应之一为Fe (SO ) +SO +2H O=2FeSO +2H SO
2 4 3 2 2 4 2 4
D.该过程中化合价发生改变的元素只有Fe和S
5.D A.根据总反应2SO +O +2H O=2H SO 可知该工艺流程是用来除去煤燃烧时产生的SO ,A正确;B.
2 2 2 2 4 2
根据总反应为2SO +O +2H O=2H SO 可知该过程中可得到化工产品H SO ,B正确;C.Fe (SO ) 与SO 反应
2 2 2 2 4 2 4 2 4 3 2
生成FeSO 和H SO ,其反应的化学方程式为Fe (SO ) +SO +2H O=2FeSO +2H SO ,C正确;D.该过程中
4 2 4 2 4 3 2 2 4 2 4
Fe (SO ) 与SO 反应生成FeSO 和H SO ,同时FeSO 、O 和H SO 反应生成Fe (SO ) ,则反应过程中Fe、O
2 4 3 2 4 2 4 4 2 2 4 2 4 3
和S的化合价发生改变,D错误;故合理选项是D。
题点(二)与铁及其化合物相关的实验
6.(2022·广东卷)为检验牺牲阳极的阴极保护法对钢铁防腐的效果,将镀层有破损的镀锌铁片放入酸化
的 溶液中。一段时间后,取溶液分别实验,能说明铁片没有被腐蚀的是( )
A.加入 溶液产生沉淀
B.加入淀粉碘化钾溶液无蓝色出现
C.加入 溶液无红色出现D.加入 溶液无蓝色沉淀生成
6.D A.氯化钠溶液中始终存在氯离子,所以加入硝酸银溶液后,不管铁片是否被腐蚀,均会出现白色
沉淀,故A不符合题意;B.淀粉碘化钾溶液可检测氧化性物质,但不论铁片是否被腐蚀,均无氧化性物
质可碘化钾发生反应,故B不符合题意;C.KSCN溶液可检测铁离子的存在,上述现象中不会出现铁离子,
所以无论铁片是否被腐蚀,加入KSCN溶液后,均无红色出现,故C不符合题意;D.K [Fe(CN) ]是用于检
3 6
测Fe2+的试剂,若铁片没有被腐蚀,则溶液中不会生成亚铁离子,则加入K [Fe(CN) ]溶液就不会出现蓝色沉
3 6
淀,故D符合题意。综上所述,答案为D。
7.(2021福建卷)明代《徐光启手迹》记载了制备硝酸的方法,其主要流程(部分产物已省略)如下:
下列说法错误的是( )
A. FeSO 的分解产物X为FeO B. 本流程涉及复分解反应
4
C. HNO 的沸点比H SO 的低 D. 制备使用的铁锅易损坏
3 2 4
7.A A.据图可知FeSO 分解时生成SO 和SO ,部分S元素被还原,则Fe元素应被氧化,X为Fe O ,A错
4 2 3 2 3
误;B.H SO 与KNO 在蒸馏条件下生成HNO 和K SO ,为复分解反应,B正确;C.H SO 与KNO 混合后,
2 4 3 3 2 4 2 4 3
蒸馏过程中生成HNO ,说明HNO 的沸点比H SO 的低,C正确;D.硫酸、硝酸均可以和铁反应,所以制
3 3 2 4
备使用的铁锅易损坏,D正确;综上所述答案为A。
8.通过对实验现象的观察、分析、推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释
正确的是( )
操作、现象 解释
向KI淀粉溶液中加入FeCl 溶液,溶液
A 3 Fe3+能与淀粉发生显色反应
变蓝
把生铁放置于潮湿的空气中,铁表面
B 铁在潮湿的空气中易生成Fe(OH)
有一层红棕色的斑点 3
向稀硝酸中加入少量铁粉,有气泡产 说明Fe置换出溶液中的氢,生成了氢
C
生 气新制Fe(OH) 露置于空气中一段时间,
D 2 说明Fe(OH) 易被O 氧化成Fe(OH)
白色物质变成了红褐色 2 2 3
A.A B.B C.C D.D
8.D A.向KI淀粉溶液中加入FeCl 溶液,碘离子被铁离子氧化成碘单质,从而使溶液变蓝,铁离子不与淀
3
粉反应,故A错误;B.把生铁放置于潮湿的空气中,铁表面有一层红棕色的斑点,铁发生吸氧腐蚀生成
三氧化二铁,不是Fe(OH) ,故B错误;C.少量铁粉与稀硝酸反应生成硝酸铁、NO气体和水,不会生成氢
3
气,故C错误; D.新制Fe(OH) 露置于空气中一段时间,Fe(OH) 易被O 氧化成Fe(OH) ,白色的氢氧化亚
2 2 2 3
铁变成了红褐色的氢氧化铁,故D正确; 故选D。
9.(2022·全国·高三专题练习)高铁酸钾(K FeO )是一种环保、高效、多功能饮用水处理剂,在水处理过程
2 4
中,高铁酸钾转化为Fe(OH) 胶体,制备高铁酸钾流程如图所示。
3
下列叙述不正确的是( )
A.反应I的化学方程式是2Fe+3Cl 2FeCl
2 3
B.用FeCl 溶液吸收反应I中尾气所得产物可再利用
2
C.反应II中氧化剂与还原剂的物质的量之比为2∶3
D.用K FeO 对饮用水杀菌消毒的同时,Fe(OH) 胶体吸附杂质净化水
2 4 3
9.C A.铁与氯气反应生成氯化铁,化学方程式是2Fe+3Cl 2FeCl ,故A正确;
2 3
B.反应Ⅰ中尾气氯气,因此可用 FeCl 溶液作为反应Ⅰ中尾气吸收剂,生成 FeCl ,且反应后溶液进入到
2 3
反应Ⅱ进行反应,故B正确;C.反应中 Cl 元素化合价由 +1 价降低为 −1 价,Fe 元素化合价由 +3 价
升高到 +6 价,则氧化剂与还原剂的物质的量之比为 3:2,故C错误;D.K FeO 中 +6 价铁具有强氧化性,
2 4
用于饮用水杀菌消毒,得到的还原产物铁离子水解生成氢氧化铁胶体,氢氧化铁胶体吸附杂质达到净化水,
故D正确。故答案为C。
10.一种利用废旧镀锌铁皮制备磁性Fe O 纳米粒子的工艺流程如下。
3 4下列有关说法不正确的是
A.“碱洗”主要是为了去除废旧镀锌铁皮中的锌
B.“氧化”后的溶液中金属阳离子主要有Fe3+、Na+
C.“氧化”时发生反应的离子方程式为2Fe2++ClO-+2H+=2Fe3++Cl-+H O
2
D.用激光笔照射“加热沉铁”后所得分散系,产生丁达尔效应
10.B A.锌和氢氧化钠反应,因此“碱洗”是为了去除废旧镀锌铁皮表面的油污和锌,故A正确;B.
“氧化”后是次氯酸钠和亚铁离子反应,因此溶液中金属阳离子主要有Fe2+、Fe3+,还有Na+,故B错误;
C.“氧化”时次氯酸钠和亚铁离子反应生成铁离子和氯离子,因此发生反应的离子方程式为2Fe2++ClO-
+2H+=2Fe3++Cl-+H O,故C正确;
2
D.加热沉铁即把氢氧化亚铁、氢氧化铁加热分解生成Fe O 胶体,因此用激光笔照射“加热沉铁”后所得
3 4
分散系,产生丁达尔效应,故D正确。综上所述,答案为B。
11.微生物法浸出黄铜矿(CuFeS ,其中Cu为+2价)中铜元素的过程如图。下列说法错误的是
2
A.该方法的原料只有黄铜矿和氧气
B.Fe (SO ) 和H SO 可以循环利用
2 4 3 2 4
C.微生物在整个转化过程中起催化作用
D.当黄铜矿中的铁元素全部转化为Fe3+时,生成2mol SO 同时消耗4.25mol O
2
11.A A.由分析可知,该方法的原料为黄铜矿、硫酸和氧气,故A错误;B.由分析可知,出过程中硫酸
和硫酸铁可循环使用,故B正确;C.由分析可知,微生物是浸出过程的催化剂,故C正确;D.由分析可
知,当黄铜矿中的铁元素全部转化为铁离子时,生成2mol硫酸根时,反应消耗氧气的物质的量为17mol×=4.25,故D正确;
故选A。
12.(2021·海南卷)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含
有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 B. 水 C. 水 D. 溶液
(3)操作②是蒸发结晶,加热的同时通入 的目的是___________。
(4)取少量 晶体,溶于水并滴加 溶液,现象是___________。
(5)反应 的化学方程式为___________。
(6)由 转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________,并设计实验验证是
该还原剂将 还原___________。
12.(1)漏斗(2)BD(3)防止水解(4)溶液变为血红色
(5)
(6) 先加盐酸酸化,再加溶液,产生白色沉淀,则是将还原
解析:废铁屑(含有少量碳和SiO 杂质)加入盐酸,铁粉反应生成氯化亚铁,过滤除去少量碳和SiO 杂质,
2 2A(氯化亚铁)加入氧化剂B生成C(氯化铁),蒸发结晶生成 ,通入SOCl 生成FeCl 。
2 3
(1)过滤用到的玻璃仪器有烧杯、玻璃棒和漏斗。
(2)A(氯化亚铁)加入氧化剂B生成C(氯化铁),A、C都引入杂质离子,故选BD。
(3)加热促进氯化铁溶液的水解,会生成氢氧化铁,故加入 的目的是防止水解。
(4)KSCN溶液遇Fe3+变为红色。
(5)根据已知信息氯化亚砜( )熔点-101℃,沸点76℃,易水解,可得 与SOCl 生成
2
FeCl 的化学方程式为 。
3
(6)可能反应中生成的二氧化硫将氯化铁还原为氯化亚铁,若二氧化硫作还原剂,则氧化产物为硫酸盐,故
若加盐酸酸化,再加溶液,产生白色沉淀,则是二氧化硫作还原剂。