文档内容
2017-2018 学年甘肃省白银市白银十中九年级(上)期末化学试
卷
一、选择题(共10小题,每小题2分,共20分)
1.下列是生活中常见的一些现象,其中属于化学变化的是( )
A.石蜡熔化B.瓷碗破碎
C.食物腐败D.潮湿的衣服被晒干了
2.下列化学实验操作正确的是( )
A.
点燃酒精灯B.
给液体加热C.
滴加液体 D.
闻气体气味
3.下列叙述错误的是( )
第1页(共21页)A.分子、原子、离子都是可以直接构成物质
B.原子得到电子形成阳离子
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
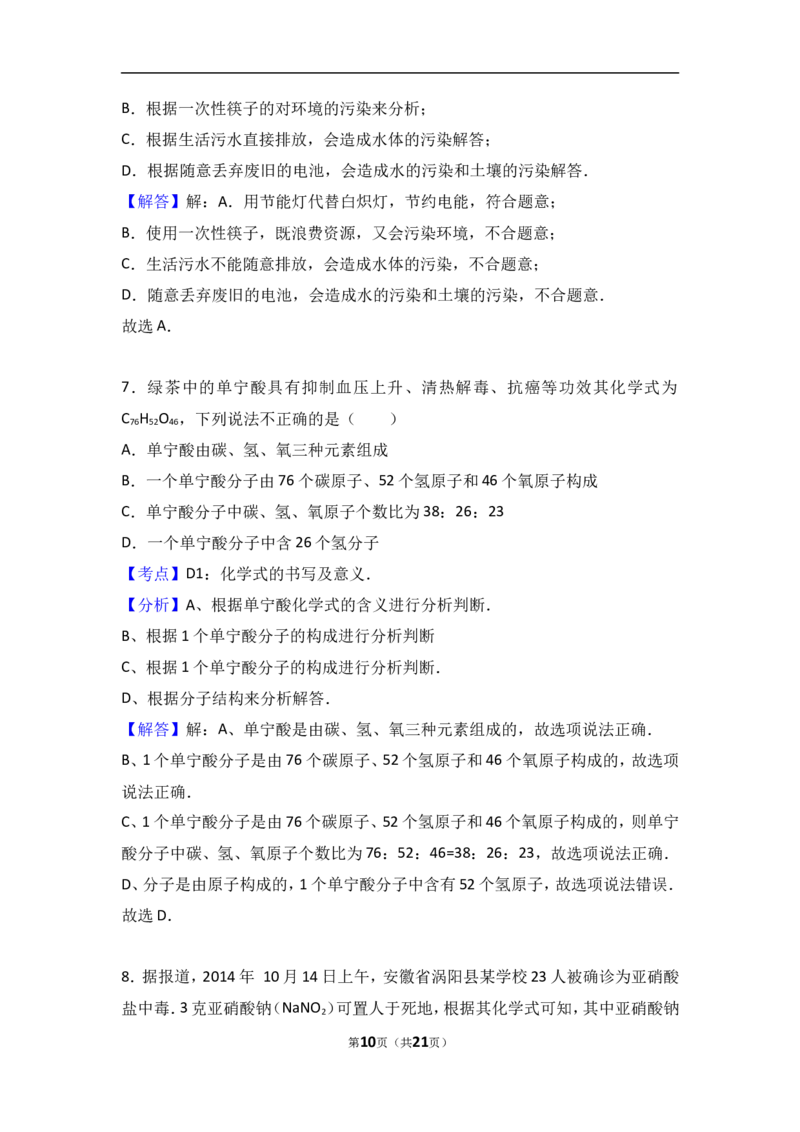
4.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是(
)
A.元素符号为Hg B.属于非金属元素
C.原子核内中子数为80D.相对原子质量是200.6 g
5.下列关于灭火的叙述中错误的是( )
A.炒菜时油锅着火立即盖上锅盖﹣﹣使可燃物与空气隔绝
B.木材着火用水泼灭﹣﹣降低了可燃物的着火点
C.扑灭森林火灾开辟隔离带﹣﹣清除和隔离可燃物
D.不慎将酒精洒到桌面燃烧,用湿布覆盖﹣﹣隔氧又降温
6.6月5日为“世界环境日”,今年我国的主题是“践行绿色生活”.下列做法
符合这一主题的是( )
A.倡导使用节能灯B.使用一次性筷子
C.随意排放生活污水 D.随便丢弃废电池
7.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效其化学式为
C H O ,下列说法不正确的是( )
76 52 46
A.单宁酸由碳、氢、氧三种元素组成
B.一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸分子中碳、氢、氧原子个数比为38:26:23
D.一个单宁酸分子中含26个氢分子
8.据报道,2014年 10月14日上午,安徽省涡阳县某学校23人被确诊为亚硝酸
盐中毒.3克亚硝酸钠(NaNO )可置人于死地,根据其化学式可知,其中亚硝酸钠
2
中氮元素的化合价为( )
第2页(共21页)A.+5 B.+2 C.﹣3 D.+3
9.逻辑推理是一种重要的化学思维方法.以下逻辑合理的是( )
A.离子是带电荷的微粒,所以带电荷的微粒一定是离子
B.氧化物中一定含有氧元素,所以含氧元素的物质一定是氧化物
C.燃烧伴随发光放热的现象,伴随发光放热现象的不一定是燃烧
D.单质中含有一种元素,所以含有一种元素的物质一定是单质
10.X、Y、Z、W四种物质在一定条件下充分反应后,测得反应前后各物质的质量如
下:
物质 X Y Z W
反应前的质量/g 22 34 2 0
反应后的质量/g 40 待测 2 16
下列说法错误的是( )
A.Z在反应中可能是催化剂B.反应中X与Y的质量比是9:17
C.该反应属于化合反应D.该反应中Y全部参加了反应
二、填空题(每空1分,化学方程式一个2分,共24分)
11.元素符号、化学式等是化学用语.以下内容请你用最合适的化学用语填空:
(1)地壳中含量最多的金属元素
(2)两个氢分子
(3)保持氧气化学性质的最小微粒
(4)两个碳酸根离子
(5)硝酸钾中氮元素的化合价 .
12.环境与能源问题是当今社会备受关注的热点.
(1)现在人类以化石燃料为主要能源,常见的化石燃料有:煤、 、天然气;
天然气的主要成分是 ,燃烧的化学方程式为 .
(2)化石燃料的燃烧,会导致很多环境问题.去年我国大范围内出现了雾霾天气,
PM2.5是造成这种天气的“元凶”之一.PM2.5是指大气中直径小于或等于 2.5
微米的颗粒物,也称可入肺颗粒物.下列行为能产生PM2.5的是 .
A.将校园的垃圾堆积起来,就地焚烧 B.为方便出行,提倡大量购买和使用私家
车
第3页(共21页)C.大力发展火力发电 D.节日里燃放鞭炮
(3)化石燃料的燃烧会产生CO ,这是引发温室效应的最主要原因,自然界中消耗
2
CO 的主要途径是 .
2
(4)化石燃料的燃烧对空气质量的影响很大,因此我们要注重开发和使用新能源,
有待开发的新能源有 (写一种即可).
13.下列物质:①食盐水②水银③冰水混合物④液态氮⑤澄清石灰水⑥五氧化二
磷⑦洁净的空气⑧高锰酸钾⑨二氧化锰,用正确序号填空:
属于混合物的是 ;属于纯净物的是 ;
属于单质的是 ;属于化合物的是 .
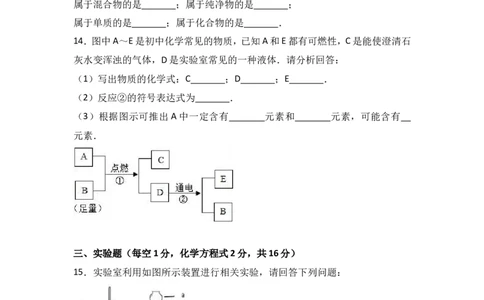
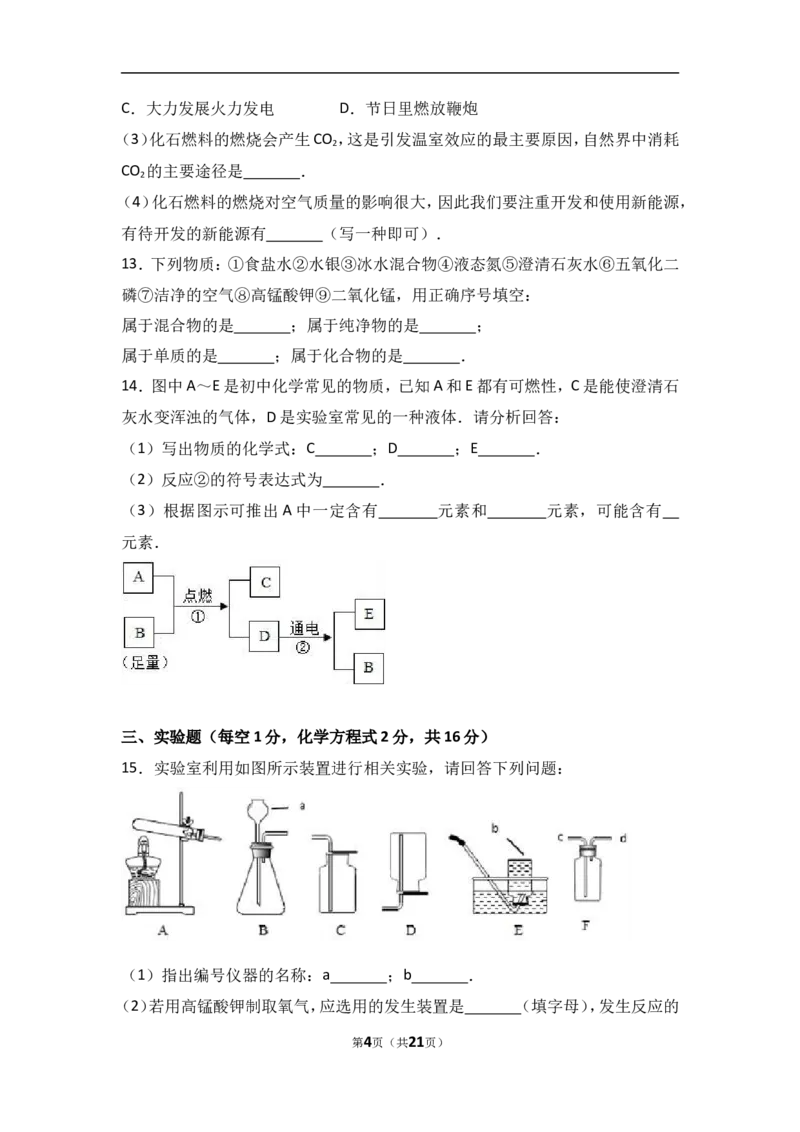
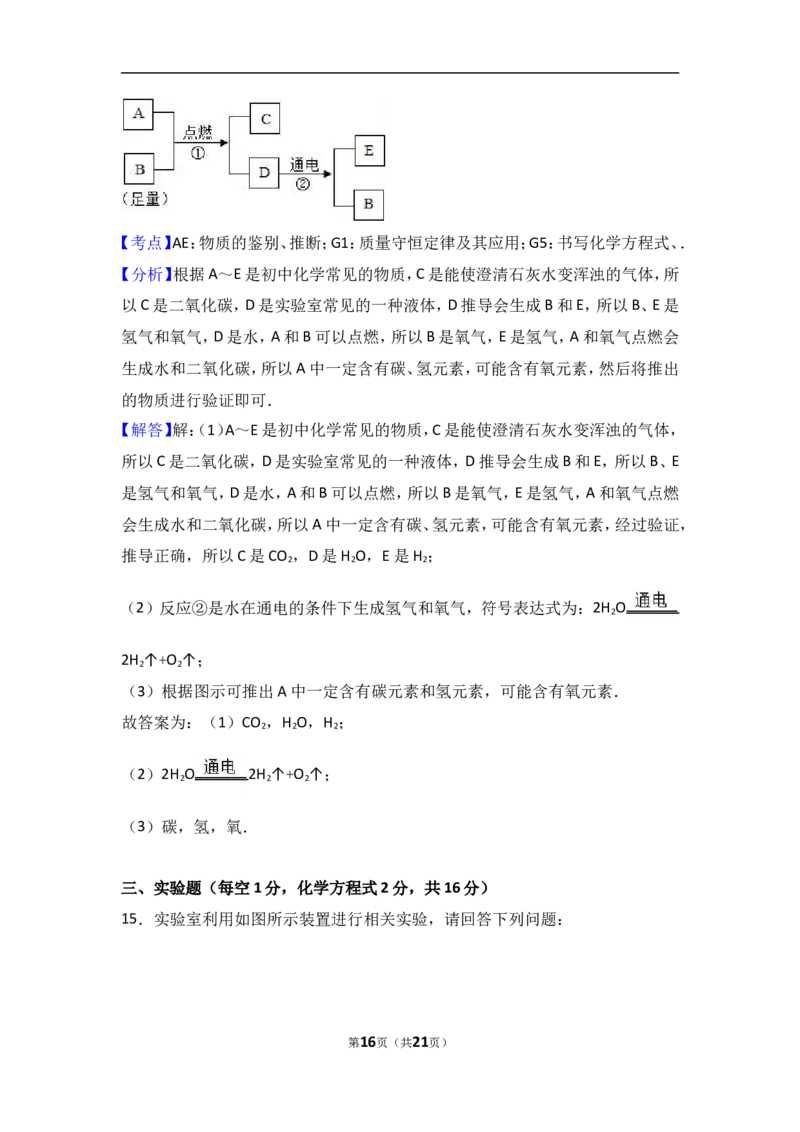
14.图中A~E是初中化学常见的物质,已知A和E都有可燃性,C是能使澄清石
灰水变浑浊的气体,D是实验室常见的一种液体.请分析回答:
(1)写出物质的化学式:C ;D ;E .
(2)反应②的符号表达式为 .
(3)根据图示可推出A中一定含有 元素和 元素,可能含有
元素.
三、实验题(每空1分,化学方程式2分,共16分)
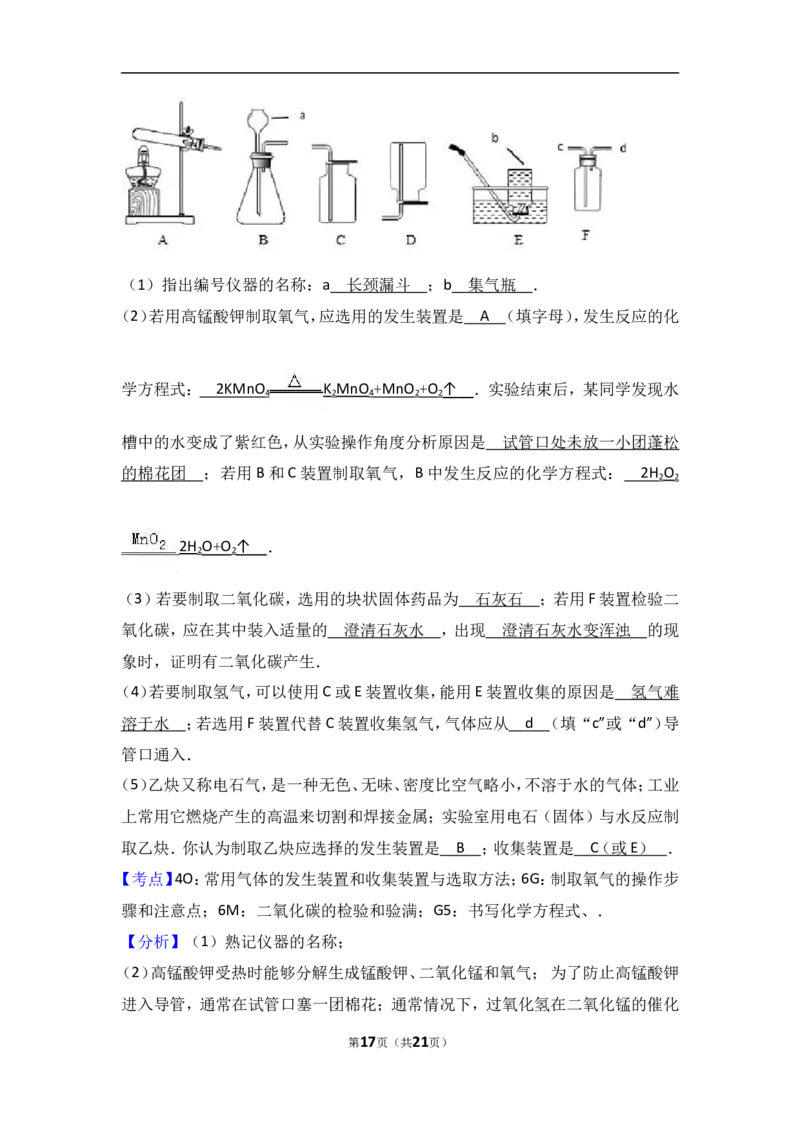
15.实验室利用如图所示装置进行相关实验,请回答下列问题:
(1)指出编号仪器的名称:a ;b .
(2)若用高锰酸钾制取氧气,应选用的发生装置是 (填字母),发生反应的
第4页(共21页)化学方程式: .实验结束后,某同学发现水槽中的水变成了紫红色,从实
验操作角度分析原因是 ;若用B和C装置制取氧气,B中发生反应的化学
方程式: .
(3)若要制取二氧化碳,选用的块状固体药品为 ;若用F装置检验二氧化
碳,应在其中装入适量的 ,出现 的现象时,证明有二氧化碳产生.
(4)若要制取氢气,可以使用C或E装置收集,能用E装置收集的原因是 ;
若选用F装置代替C装置收集氢气,气体应从 (填“c”或“d”)导管口通
入.
(5)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业
上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制
取乙炔.你认为制取乙炔应选择的发生装置是 ;收集装置是 .
四、计算题(共2小题,共10分)
16.苏丹红是一种人工合成的红色染料.最新研究表明,其体内代谢产物有强致
突变性和致癌性,国家正在严查添加有苏丹红的食品.已知最常见的一种苏丹红
的化学式为C H N O,试计算:
16 12 2
(1)苏丹红的相对分子质量;
(2)苏丹红中各元素的质量比;
(3)苏丹红中氮元素的质量分数.
17.乐乐同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石
灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g.试
计算:
(1)该石灰石样品中碳酸钙的质量为多少?
(2)该石灰石样品中碳酸钙的质量分数为多少?(结果精确到0.1%)
第5页(共21页)2017-2018 学年甘肃省白银市白银十中九年级(上)期末
化学试卷
参考答案与试题解析
一、选择题(共10小题,每小题2分,共20分)
1.下列是生活中常见的一些现象,其中属于化学变化的是( )
A.石蜡熔化B.瓷碗破碎
C.食物腐败D.潮湿的衣服被晒干了
【考点】E3:化学变化和物理变化的判别.
【分析】化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变
化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
【解答】解:A、石蜡熔化的过程中没有新物质生成,属于物理变化.
B、瓷碗破碎的过程中没有新物质生成,属于物理变化.
C、食物腐败的过程中有新物质生成,属于化学变化.
D、潮湿的衣服被晒干的过程中没有新物质生成,属于物理变化.
故选C.
2.下列化学实验操作正确的是( )
A.
点燃酒精灯B.
第6页(共21页)给液体加热C.
滴加液体 D.
闻气体气味
【考点】44:加热器皿﹣酒精灯;49:液体药品的取用;4B:给试管里的液体加热.
【分析】A、根据酒精灯的使用方法进行分析判断;
B、根据给液体加热的方法进行分析判断;
C、根据使用胶头滴管的方法进行分析判断;
D、根据闻气体气味的方法进行分析判断.
【解答】解:A、使用酒精灯时要注意“两查、两禁、一不可”,点燃酒精灯要用火
柴点燃,图中所示操作错误;
B、给试管中的液体加热时,用酒精灯的外焰加热试管里的液体,且液体体积不能
超过试管容积的 ,图中所示操作错误;
C、使用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管
内壁.应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错
误;
D、闻气体的气味时,防止气体有毒,应用手扇动,不能直接用鼻子闻,图中所示操
作正确.
故选:D.
3.下列叙述错误的是( )
A.分子、原子、离子都是可以直接构成物质
第7页(共21页)B.原子得到电子形成阳离子
C.化学反应中,分子可分,原子不能再分
D.原子的质量主要集中在原子核上
【考点】B2:分子、原子、离子、元素与物质之间的关系;B4:原子的定义与构成;
B5:分子和原子的区别和联系;B6:原子和离子的相互转化.
【分析】A、根据构成物质的微粒进行解答;
B、根据原子得到电子形成阴离子进行解答;
C、根据分子和原子的区别进行解答;
D、根据原子的质量主要集中在原子核上,而电子的质量可以忽略进行解答.
【解答】解:A、分子、原子、离子都是可以直接构成物质,故A正确;
B、原子得到电子形成阴离子,原子失去电子形成阳离子,故B错误;
C、化学反应中,分子可分,原子不能再分,故C正确;
D、原子的质量主要集中在原子核上,而电子的质量可以忽略,故D正确.
故选:B.
4.在元素周期表中汞元素的某些信息如图所示,下列有关汞的说法正确的是(
)
A.元素符号为Hg B.属于非金属元素
C.原子核内中子数为80D.相对原子质量是200.6 g
【考点】C5:元素周期表的特点及其应用.
【分析】根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符
号、元素种类等,进行分析判断即可.
【解答】解:A、根据元素周期表中的一格中获取的信息,该元素的元素符号是Hg,
故选项说法正确.
B、根据元素周期表中的一格中获取的信息,该元素的名称是汞,属于金属元素,
故选项说法错误.
第8页(共21页)C、根据元素周期表中的一格中获取的信息,该元素的原子序数为80,根据原子序
数=核电荷数=质子数,其核内质子数为80,而不是中子数为80,故选项说法错误.
D、根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为200.6,
相对原子质量单位是“1”,不是“克”,故选项说法错误.
故选:A.
5.下列关于灭火的叙述中错误的是( )
A.炒菜时油锅着火立即盖上锅盖﹣﹣使可燃物与空气隔绝
B.木材着火用水泼灭﹣﹣降低了可燃物的着火点
C.扑灭森林火灾开辟隔离带﹣﹣清除和隔离可燃物
D.不慎将酒精洒到桌面燃烧,用湿布覆盖﹣﹣隔氧又降温
【考点】H1:燃烧与燃烧的条件;H4:灭火的原理和方法.
【分析】灭火的方法有:(1)与空气(或氧气)隔绝.(2)降温到可燃物的着火点以
下.(3)撤走可燃物.
【解答】解:A、炒菜时油锅着火立即盖上锅盖﹣﹣使可燃物与空气隔绝,可以达到
灭火的目的.故选项错误;
B、木材着火用水泼灭﹣﹣降低温度到可燃物的着火点以下,可燃物的着火点不
能降低.故选项正确;
C、扑灭森林火灾开辟隔离带﹣﹣清除和隔离可燃物,可以达到灭火的目的.故选
项错误;
D、不慎将酒精洒到桌面燃烧,用湿布覆盖﹣﹣隔氧又降温,可以达到灭火的目的
故选项错误.
故选B.
6.6月5日为“世界环境日”,今年我国的主题是“践行绿色生活”.下列做法
符合这一主题的是( )
A.倡导使用节能灯B.使用一次性筷子
C.随意排放生活污水 D.随便丢弃废电池
【考点】65:防治空气污染的措施;79:水资源的污染与防治.
【分析】A.根据节能灯能源,光照效果好分析;
第9页(共21页)B.根据一次性筷子的对环境的污染来分析;
C.根据生活污水直接排放,会造成水体的污染解答;
D.根据随意丢弃废旧的电池,会造成水的污染和土壤的污染解答.
【解答】解:A.用节能灯代替白炽灯,节约电能,符合题意;
B.使用一次性筷子,既浪费资源,又会污染环境,不合题意;
C.生活污水不能随意排放,会造成水体的污染,不合题意;
D.随意丢弃废旧的电池,会造成水的污染和土壤的污染,不合题意.
故选A.
7.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效其化学式为
C H O ,下列说法不正确的是( )
76 52 46
A.单宁酸由碳、氢、氧三种元素组成
B.一个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成
C.单宁酸分子中碳、氢、氧原子个数比为38:26:23
D.一个单宁酸分子中含26个氢分子
【考点】D1:化学式的书写及意义.
【分析】A、根据单宁酸化学式的含义进行分析判断.
B、根据1个单宁酸分子的构成进行分析判断
C、根据1个单宁酸分子的构成进行分析判断.
D、根据分子结构来分析解答.
【解答】解:A、单宁酸是由碳、氢、氧三种元素组成的,故选项说法正确.
B、1个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成的,故选项
说法正确.
C、1个单宁酸分子是由76个碳原子、52个氢原子和46个氧原子构成的,则单宁
酸分子中碳、氢、氧原子个数比为76:52:46=38:26:23,故选项说法正确.
D、分子是由原子构成的,1个单宁酸分子中含有52个氢原子,故选项说法错误.
故选D.
8.据报道,2014年 10月14日上午,安徽省涡阳县某学校23人被确诊为亚硝酸
盐中毒.3克亚硝酸钠(NaNO )可置人于死地,根据其化学式可知,其中亚硝酸钠
2
第10页(共21页)中氮元素的化合价为( )
A.+5 B.+2 C.﹣3 D.+3
【考点】D6:有关元素化合价的计算.
【分析】根据在化合物中正负化合价代数和为零,结合亚硝酸钠(NaNO )的化学
2
式进行解答本题.
【解答】解:根据在化合物中正负化合价代数和为零,钠元素显+1,氧元素显﹣2,
设氮元素的化合价是x,可知亚硝酸钠(NaNO )中氮元素的化合价:(+1)+x+(﹣
2
2)×2=0,则x=+3.
故选D.
9.逻辑推理是一种重要的化学思维方法.以下逻辑合理的是( )
A.离子是带电荷的微粒,所以带电荷的微粒一定是离子
B.氧化物中一定含有氧元素,所以含氧元素的物质一定是氧化物
C.燃烧伴随发光放热的现象,伴随发光放热现象的不一定是燃烧
D.单质中含有一种元素,所以含有一种元素的物质一定是单质
【考点】H1:燃烧与燃烧的条件;A3:从组成上识别氧化物;A6:单质和化合物的概
念;B6:原子和离子的相互转化.
【分析】A、据带电的微粒进行解答;
B、根据氧化物的概念考虑;
C、发光放热的现象不一定是燃烧;
D、根据单质是由一种元素组成的纯净物解答.
【解答】解:A、带电荷的微粒不一定是离子,原子核也是带电的微粒,故错误;
B、氧化物是指由两种元素组成,一种元素是氧元素的化合物,含有氧元素的物质,
不一定是由两种元素组成,故错误;
C、发光放热的现象不一定是燃烧,如电灯泡发光就不是燃烧,故正确;
D、含一种元素的物质不一定是单质,如金刚石和石墨的混合物,故错误;
故选:C.
10.X、Y、Z、W四种物质在一定条件下充分反应后,测得反应前后各物质的质量如
下:
第11页(共21页)物质 X Y Z W
反应前的质量/g 22 34 2 0
反应后的质量/g 40 待测 2 16
下列说法错误的是( )
A.Z在反应中可能是催化剂B.反应中X与Y的质量比是9:17
C.该反应属于化合反应D.该反应中Y全部参加了反应
【考点】G1:质量守恒定律及其应用;6J:催化剂的特点与催化作用;FA:反应类型
的判定.
【分析】试题给予了一些数据,要求能通过数据判断四种物质哪些分别属于反应
物、生成物、催化剂.先根据质量守恒定律“在化学反应中,参加反应前各物质的
质量总和等于反应后生成各物质的质量总和”计算出Y反应后的质量,然后根据
图表的数据分析,即可正确选择.
【解答】解:
根据质量守恒定律,由图示数据可知,Y反应后的质量=(2+22+34)g﹣(2+40+16)
g=0g;
A、物质Z的质量在反应前后没有变化,故可判断Z在反应中可能是催化剂.故A
说法正确;
B、该反应中X与Y的质量比是(40g﹣22g):(34g﹣0g)=9:17,故B说法正确;
C、分解反应是一变多的反应,根据图表的数据:Z反应前后不变,X增加了18g,W
增加了16g而Y减少34g,从而判断反应物是Y,而生成物是X、W,由此可定此反
应属于分解反应.故C说法错误;
D、由计算可知,Y反应后的质量为0,故可判断该反应中Y全部参加反应.故D说
法正确.
故选:C.
二、填空题(每空1分,化学方程式一个2分,共24分)
11.元素符号、化学式等是化学用语.以下内容请你用最合适的化学用语填空:
(1)地壳中含量最多的金属元素 A l
(2)两个氢分子 2H
2
(3)保持氧气化学性质的最小微粒 H
2
第12页(共21页)(4)两个碳酸根离子 2CO 2﹣
3
(5)硝酸钾中氮元素的化合价 K O .
3
【考点】DF:化学符号及其周围数字的意义.
【分析】本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对
象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计
量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学
式,才能熟练准确的解答此类题目.
【解答】解:(1)地壳中含量最多的金属元素是铝元素,其符号为:Al;
(2)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前
加上相应的数字,所以2个氢分子可表示为:2H ;
2
(3)保持氧气化学性质的最小微粒是氢分子,其化学式为:H ;
2
(4)离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负
电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.但碳酸根离子是由多
个原子组成的离子,整体带2个单元位的负电荷,表示为CO 2﹣,若表示多个该离
3
子,就在其元素符号前加上相应的数字,故2个碳酸根离子可表示为:2CO 2﹣;
3
(5)元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在
其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以硝酸
钾中氮元素的化合价,故可表示为:K O ;
3
故答案为:(1)Al;(2)2H ;(3)H ;(4)2CO 2﹣;(5)K O ;
2 2 3 3
12.环境与能源问题是当今社会备受关注的热点.
(1)现在人类以化石燃料为主要能源,常见的化石燃料有:煤、 石油 、天然气;
天然气的主要成分是 甲烷 ,燃烧的化学方程式为 CH + 2O CO + 2H O
4 2 2 2
第13页(共21页).
(2)化石燃料的燃烧,会导致很多环境问题.去年我国大范围内出现了雾霾天气,
PM2.5是造成这种天气的“元凶”之一.PM2.5是指大气中直径小于或等于 2.5
微米的颗粒物,也称可入肺颗粒物.下列行为能产生PM2.5的是 ABCD .
A.将校园的垃圾堆积起来,就地焚烧 B.为方便出行,提倡大量购买和使用私家
车
C.大力发展火力发电 D.节日里燃放鞭炮
(3)化石燃料的燃烧会产生CO ,这是引发温室效应的最主要原因,自然界中消耗
2
CO 的主要途径是 绿色植物的光合作用 .
2
(4)化石燃料的燃烧对空气质量的影响很大,因此我们要注重开发和使用新能源,
有待开发的新能源有 太阳能 (写一种即可).
【考点】H7:化石燃料及其综合利用;64:空气的污染及其危害;6I:自然界中的碳
循环;G5:书写化学方程式、;HE:资源综合利用和新能源开发.
【分析】(1)根据常见的化石燃料、化学方程式的书写方法来分析;
(2)根据产生PM2.5的途径来分析;
(3)二氧化碳是植物进行光合作用的原料;
(4)根据新能源的类型解答.
【解答】解:(1)化石燃料包括煤、石油和天然气,天然气的主要成分是甲烷,甲烷
完全燃烧生成水和二氧化碳;故填:石油;甲烷;CH +2O CO +2H O;
4 2 2 2
(2)A、垃圾就地焚烧会产生的烟尘,污染空气;
B、汽车排放的尾气也是造成空气污染的原因之一;
C、火力发电的原料通常使用的是煤炭,煤炭燃烧会产生有害气体和烟尘;
D、节日里燃放鞭炮,会产生有害气体和烟尘,污染空气.
故答案为:ABCD;
(3)二氧化碳是植物进行光合作用的原料,自然界中绿色的植物光合作用能消耗
二氧化碳,故答案为:绿色植物的光合作用;
(4)有待开发的新能源有风能、核能、太阳能、氢能、地热能等,故填:太阳能(答
案合理即可).
第14页(共21页)13.下列物质:①食盐水②水银③冰水混合物④液态氮⑤澄清石灰水⑥五氧化二
磷⑦洁净的空气⑧高锰酸钾⑨二氧化锰,用正确序号填空:
属于混合物的是 ①⑤⑦ ;属于纯净物的是 ②③④⑥⑧⑨ ;
属于单质的是 ②④ ;属于化合物的是 ③⑥⑧⑨ .
【考点】A7:单质和化合物的判别;A5:纯净物和混合物的判别.
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,①食
盐水⑤澄清石灰水⑦洁净的空气都属于混合物;纯净物是由一种物质组成,②水
银③冰水混合物中只有水分子④液态氮⑥五氧化二磷⑧高锰酸钾⑨二氧化锰都
是一种物质,属于纯净物.纯净物又分为单质和化合物.由同种元素组成的纯净
物叫单质,②水银④液态氮都属于单质;由两种或两种以上的元素组成的纯净物
叫化合物,③冰水混合物中只有水分子⑥五氧化二磷⑧高锰酸钾⑨二氧化锰都是
化合物.氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.
【解答】解:混合物是由两种或两种以上的物质组成,①食盐水⑤澄清石灰水⑦洁
净的空气都属于混合物;纯净物是由一种物质组成,②水银③冰水混合物中只有
水分子④液态氮⑥五氧化二磷⑧高锰酸钾⑨二氧化锰都是一种物质,属于纯净物
纯净物又分为单质和化合物.由同种元素组成的纯净物叫单质,②水银④液态氮
都属于单质;由两种或两种以上的元素组成的纯净物叫化合物,③冰水混合物中
只有水分子⑥五氧化二磷⑧高锰酸钾⑨二氧化锰都是化合物;故答案为:①⑤⑦
②③④⑥⑧⑨;②④;③⑥⑧⑨;
14.图中A~E是初中化学常见的物质,已知A和E都有可燃性,C是能使澄清石
灰水变浑浊的气体,D是实验室常见的一种液体.请分析回答:
(1)写出物质的化学式:C CO ;D H O ;E H .
2 2 2
(2)反应②的符号表达式为 2H O 2H ↑ + O ↑ .
2 2 2
(3)根据图示可推出A中一定含有 碳 元素和 氢 元素,可能含有 氧 元
素.
第15页(共21页)【考点】AE:物质的鉴别、推断;G1:质量守恒定律及其应用;G5:书写化学方程式、.
【分析】根据A~E是初中化学常见的物质,C是能使澄清石灰水变浑浊的气体,所
以C是二氧化碳,D是实验室常见的一种液体,D推导会生成B和E,所以B、E是
氢气和氧气,D是水,A和B可以点燃,所以B是氧气,E是氢气,A和氧气点燃会
生成水和二氧化碳,所以A中一定含有碳、氢元素,可能含有氧元素,然后将推出
的物质进行验证即可.
【解答】解:(1)A~E是初中化学常见的物质,C是能使澄清石灰水变浑浊的气体,
所以C是二氧化碳,D是实验室常见的一种液体,D推导会生成B和E,所以B、E
是氢气和氧气,D是水,A和B可以点燃,所以B是氧气,E是氢气,A和氧气点燃
会生成水和二氧化碳,所以A中一定含有碳、氢元素,可能含有氧元素,经过验证,
推导正确,所以C是CO ,D是H O,E是H ;
2 2 2
(2)反应②是水在通电的条件下生成氢气和氧气,符号表达式为:2H O
2
2H ↑+O ↑;
2 2
(3)根据图示可推出A中一定含有碳元素和氢元素,可能含有氧元素.
故答案为:(1)CO ,H O,H ;
2 2 2
(2)2H O 2H ↑+O ↑;
2 2 2
(3)碳,氢,氧.
三、实验题(每空1分,化学方程式2分,共16分)
15.实验室利用如图所示装置进行相关实验,请回答下列问题:
第16页(共21页)(1)指出编号仪器的名称:a 长颈漏斗 ;b 集气瓶 .
(2)若用高锰酸钾制取氧气,应选用的发生装置是 A (填字母),发生反应的化
学方程式: 2KMnO K MnO + MnO + O ↑ .实验结束后,某同学发现水
4 2 4 2 2
槽中的水变成了紫红色,从实验操作角度分析原因是 试管口处未放一小团蓬松
的棉花团 ;若用B和C装置制取氧气,B中发生反应的化学方程式: 2H O
2 2
2H O + O ↑ .
2 2
(3)若要制取二氧化碳,选用的块状固体药品为 石灰石 ;若用F装置检验二
氧化碳,应在其中装入适量的 澄清石灰水 ,出现 澄清石灰水变浑浊 的现
象时,证明有二氧化碳产生.
(4)若要制取氢气,可以使用C或E装置收集,能用E装置收集的原因是 氢气难
溶于水 ;若选用F装置代替C装置收集氢气,气体应从 d (填“c”或“d”)导
管口通入.
(5)乙炔又称电石气,是一种无色、无味、密度比空气略小,不溶于水的气体;工业
上常用它燃烧产生的高温来切割和焊接金属;实验室用电石(固体)与水反应制
取乙炔.你认为制取乙炔应选择的发生装置是 B ;收集装置是 C ( 或 E ) .
【考点】4O:常用气体的发生装置和收集装置与选取方法;6G:制取氧气的操作步
骤和注意点;6M:二氧化碳的检验和验满;G5:书写化学方程式、.
【分析】(1)熟记仪器的名称;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气; 为了防止高锰酸钾
进入导管,通常在试管口塞一团棉花;通常情况下,过氧化氢在二氧化锰的催化
第17页(共21页)作用下,分解生成水和氧气;
(3)根据实验室中制取二氧化碳的反应原理、检验二氧化碳使用澄清的石灰水来
分析;
(4)能用向下排空气法收集的气体说明其密度比空气小且难溶于水;氢气的密度
比空气小,故应从短导管进气;
(5)根据题意,乙炔是一种密度比空气略小,不溶于水的气体,实验室用电石(固
体)与水反应制取乙炔,属于固液常温型,进行分析解答.
【解答】解:(1)仪器a是长颈漏斗,b是集气瓶;故填:长颈漏斗;集气瓶;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,应选用的发生装置是A装
置;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式是:
2KMnO K MnO +MnO +O ↑;从实验操作角度分析其原因是:试管口处未
4 2 4 2 2
放一小团蓬松的棉花团,导致高锰酸钾粉末进入水槽;若用B和C装置制取氧气
是用过氧化氢制取氧气,不需加热,B中发生反应的化学方程式为:2H O
2 2
2H O+O ↑.故填:A;2KMnO K MnO +MnO +O ↑;试管口处未放一小团蓬
2 2 4 2 4 2 2
松的棉花团;2H O 2H O+O ↑;
2 2 2 2
(3)实验室中制取二氧化碳常用大理石或石灰石和稀盐酸反应来制取,若要制取
二氧化碳,选用的块状固体药品为大理石(或石灰石);若用F装置检验二氧化碳
应在其中装入适量的澄清的石灰水,出现澄清的石灰水变浑浊,证明有二氧化碳
产生.故填:石灰石;澄清石灰水;澄清石灰水变浑浊;
(4)能用E装置收集的原因是氢气难溶于水,且不与水反应;氢气的密度比空气
小,故应从短导管进气;故填:氢气难溶于水;d;
(5)乙炔是一种密度比空气略小,不溶于水的气体,可选用C或E装置收集;实验
第18页(共21页)室用电石(固体)与水反应制取乙炔,属于固液常温型,可选用B装置来制取;故
填:B;C(或E).
四、计算题(共2小题,共10分)
16.苏丹红是一种人工合成的红色染料.最新研究表明,其体内代谢产物有强致
突变性和致癌性,国家正在严查添加有苏丹红的食品.已知最常见的一种苏丹红
的化学式为C H N O,试计算:
16 12 2
(1)苏丹红的相对分子质量;
(2)苏丹红中各元素的质量比;
(3)苏丹红中氮元素的质量分数.
【考点】D8:相对分子质量的概念及其计算;D9:元素质量比的计算;DA:元素的质
量分数计算.
【分析】(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,进
行解答;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,
(3)根据物质中某元素的质量分数= ×100%,进
行解答.
【解答】解:(1)根据相对分子的质量为组成分子的各原子的相对原子质量之和,
可得苏丹红的相对分子质量=12×16+l×12+14×2+16=248;
(2)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得
苏丹红中各元素的质量比为:
(12×16):(1×12):(14×2):16=48:3:7:4;
(3)根据物质中某元素的质量分数= ×100%,可
得苏丹红中氮氮元素的质量分数= ×100%≈11.3%;
答:(1)苏丹红的相对分子质量为248;
第19页(共21页)(2)苏丹红中碳、氢、氮、氧四种元素的质量比为48:3:7:4;
(3)苏丹红中氮元素的质量分数为11.3%.
17.乐乐同学为测定某石灰石中碳酸钙的质量分数(杂质不与酸反应),向6.0g石
灰石样品中逐滴加入稀盐酸至不再产生气泡为止,共生成二氧化碳气体2.2g.试
计算:
(1)该石灰石样品中碳酸钙的质量为多少?
(2)该石灰石样品中碳酸钙的质量分数为多少?(结果精确到0.1%)
【考点】G6:根据化学反应方程式的计算.
【分析】利用碳酸钙与盐酸反应的化学方程式,根据二氧化碳的质量求出碳酸钙
的质量,再根据质量分数的计算公式求出石灰石样品中碳酸钙的质量分数即可.
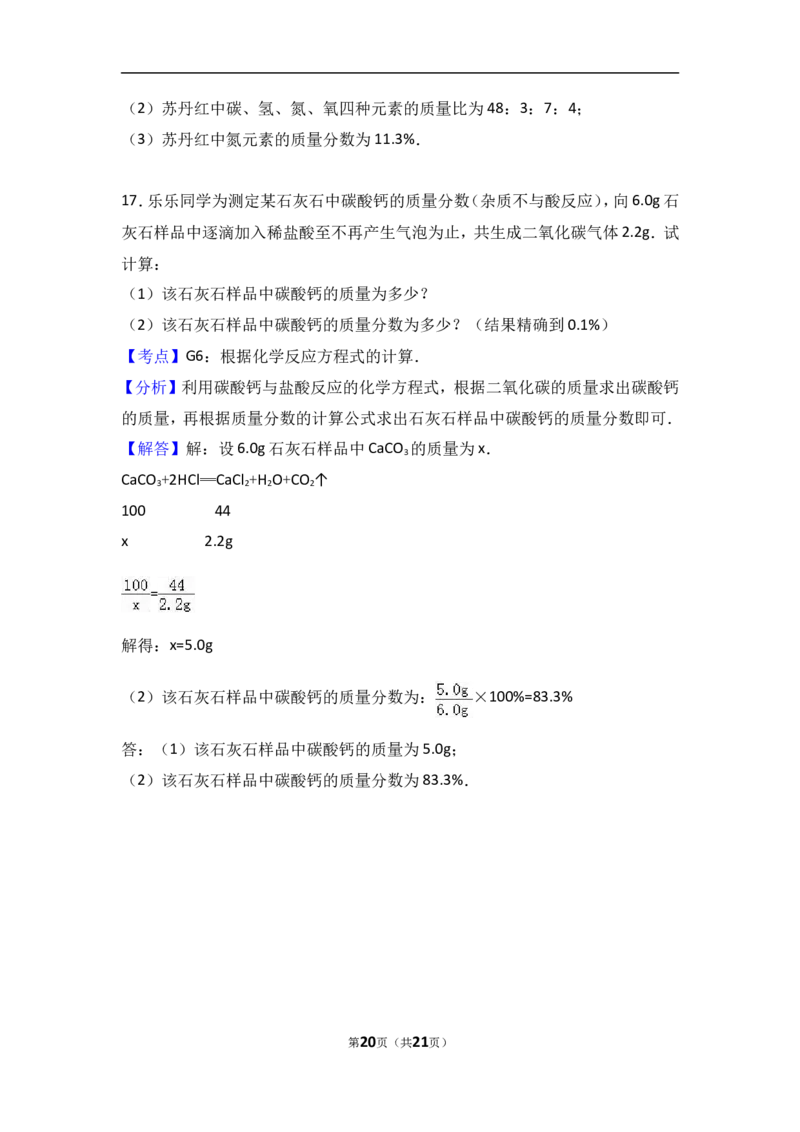
【解答】解:设6.0g石灰石样品中CaCO 的质量为x.
3
CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
100 44
x 2.2g
=
解得:x=5.0g
(2)该石灰石样品中碳酸钙的质量分数为: ×100%=83.3%
答:(1)该石灰石样品中碳酸钙的质量为5.0g;
(2)该石灰石样品中碳酸钙的质量分数为83.3%.
第20页(共21页)2017年7月4日
第21页(共21页)