文档内容
一、选择题(每小题1分,共12分)
1.生活中的下列变化,属于化学变化的是( )
A.汽油挥发 B.粮食酿酒 C.滴水成冰 D.石墨导电
2.下列物质中,属于混合物的是( )
A.氧气 B.高锰酸钾 C.澄清石灰水 D.冰水混合物
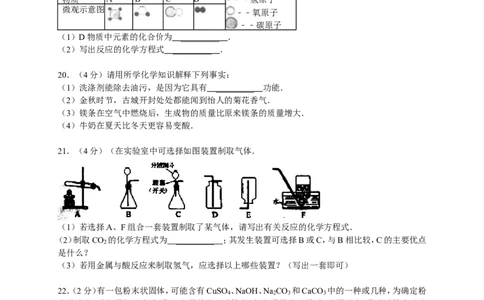
3.下列实验操作中,错误的是( )
4.下列生活中的认识或做法,错误的是( )
A.减少CO 的排放有助于控制“温室效应”
2
B.室内起火,不要急于打开所有门窗
C.氮气可做保护气
D.霉变的食品只要煮熟就可以食用
5.水是生命之源,下列关于水的说法正确的是( )
A.水是由氢气和氧气组成的
B.水是最常见的溶剂
C.煮沸和蒸馏都能让自来水变成纯净水
D.纯净水比矿泉水的营养价值高
6.生活中常见到“含铁酱油”、“高钙牛奶”、“富硒茶叶”等,这里的铁、钙、硒指的是( )
A.元素 B.原子 C.离子 D.分子
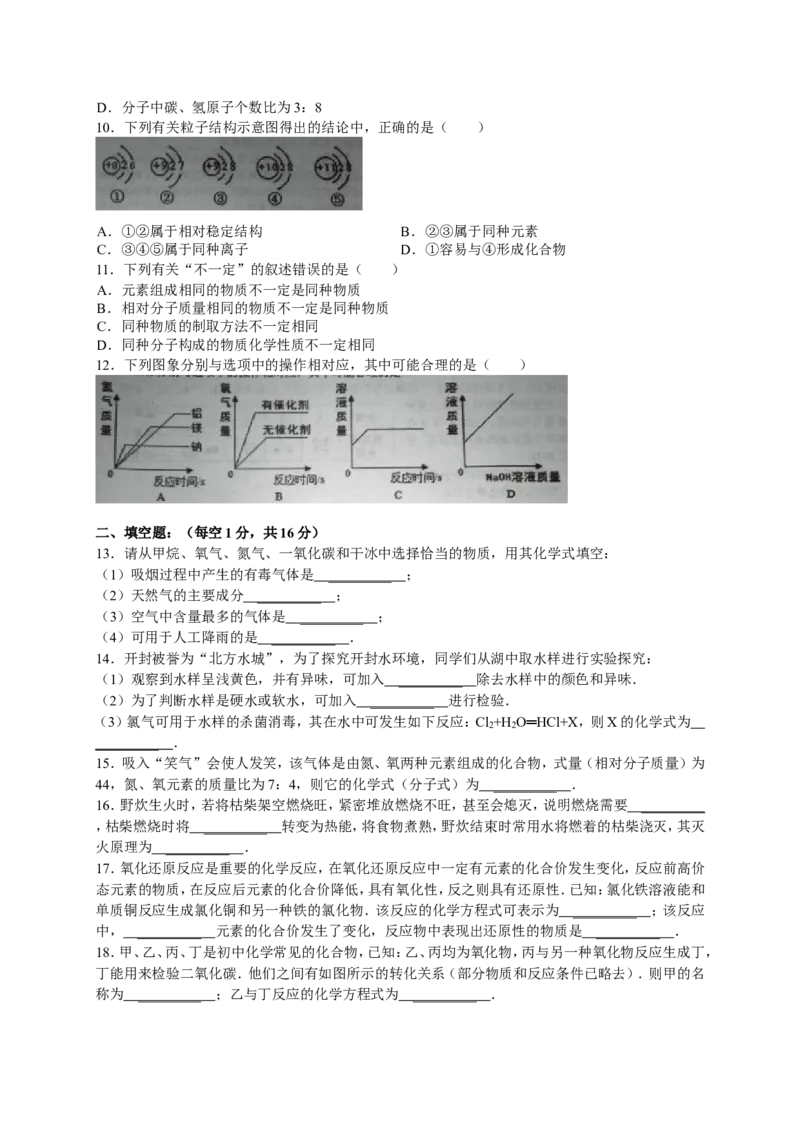
7.如图是甲、乙两种固体的溶解度曲线,下列说法正确的是( )
A.甲的溶解度等于乙的溶解度
B.升高温度可将甲的不饱和溶液变为饱和溶液
C.20℃时,100g乙的饱和溶液中溶质质量是30g
D.40℃时,分别用100g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
8.先将二氧化碳气体通入试管里的紫色石蕊溶液中,然后再加热,溶液颜色变化情况是( )
A.先变红后变蓝 B.先变红后变紫 C.不变色 D.变红后不再变色
9.已知4.4g某纯净完全燃烧生成13.2g二氧化碳和7.2g水,有关该物质判断正确的是( )
A.一定含有碳、氢元素,可能含有氧元素
B.一定含有碳、氢、氧三种元素
C.含碳元素的质量分数为42%D.分子中碳、氢原子个数比为3:8
10.下列有关粒子结构示意图得出的结论中,正确的是( )
A.①②属于相对稳定结构 B.②③属于同种元素
C.③④⑤属于同种离子 D.①容易与④形成化合物
11.下列有关“不一定”的叙述错误的是( )
A.元素组成相同的物质不一定是同种物质
B.相对分子质量相同的物质不一定是同种物质
C.同种物质的制取方法不一定相同
D.同种分子构成的物质化学性质不一定相同
12.下列图象分别与选项中的操作相对应,其中可能合理的是( )
二、填空题:(每空1分,共16分)
13.请从甲烷、氧气、氮气、一氧化碳和干冰中选择恰当的物质,用其化学式填空:
(1)吸烟过程中产生的有毒气体是 ________ _ ;
(2)天然气的主要成分 ________ _ ;
(3)空气中含量最多的气体是 ________ _ ;
(4)可用于人工降雨的是 ________ _ .
14.开封被誉为“北方水城”,为了探究开封水环境,同学们从湖中取水样进行实验探究:
(1)观察到水样呈浅黄色,并有异味,可加入 ________ _ 除去水样中的颜色和异味.
(2)为了判断水样是硬水或软水,可加入 ________ _ 进行检验.
(3)氯气可用于水样的杀菌消毒,其在水中可发生如下反应:Cl +H O═HCl+X,则X的化学式为
2 2
_________ .
15.吸入“笑气”会使人发笑,该气体是由氮、氧两种元素组成的化合物,式量(相对分子质量)为
44,氮、氧元素的质量比为7:4,则它的化学式(分子式)为 ________ _ .
16.野炊生火时,若将枯柴架空燃烧旺,紧密堆放燃烧不旺,甚至会熄灭,说明燃烧需要 ________ _
,枯柴燃烧时将 ________ _ 转变为热能,将食物煮熟,野炊结束时常用水将燃着的枯柴浇灭,其灭
火原理为 ________ _ .
17.氧化还原反应是重要的化学反应,在氧化还原反应中一定有元素的化合价发生变化,反应前高价
态元素的物质,在反应后元素的化合价降低,具有氧化性,反之则具有还原性.已知:氯化铁溶液能和
单质铜反应生成氯化铜和另一种铁的氯化物.该反应的化学方程式可表示为 ________ _ ;该反应
中, ________ _ 元素的化合价发生了变化,反应物中表现出还原性的物质是 ________ _ .
18.甲、乙、丙、丁是初中化学常见的化合物,已知:乙、丙均为氧化物,丙与另一种氧化物反应生成丁,
丁能用来检验二氧化碳.他们之间有如图所示的转化关系(部分物质和反应条件已略去).则甲的名
称为 ________ _ ;乙与丁反应的化学方程式为 ________ _ .三、简答题:
19.(2分)“航天梦”是实现“中国梦”的具体体现,2013年12月14日“嫦娥三号”在月球成功登
陆,对月球进行探测.“嫦娥三号”使用“长三乙”运载火箭发射,“常三乙”的第三级火箭使用液
氢燃料.如表是某种制备氢气的反应,已知A与B在高温和有催化剂的条件下反应,生成C和D.
物质 A B C D ﹣﹣氢原子
微观示意图
﹣﹣氧原子
﹣﹣碳原子
(1)D物质中元素的化合价为 ________ _ .
(2)写出反应的化学方程式 ________ _ .
20.(4分)请用所学化学知识解释下列事实:
(1)洗涤剂能除去油污,是因为它具有 ________ _ 功能.
(2)金秋时节,古城开封处处都能闻到怡人的菊花香气 .
(3)镁条在空气中燃烧后,生成物的质量比原来镁条的质量增大 .
(4)牛奶在夏天比冬天更容易变酸.
21.(4分)(在实验室中可选择如图装置制取气体.
(1)若选择A、F组合一套装置制取了某气体,请写出有关反应的化学方程式.
(2)制取CO 的化学方程式为 ________ _ ;其发生装置可选择B或C,与B相比较,C的主要优点
2
是什么?
(3)若用金属与酸反应来制取氢气,应选择以上哪些装置?(写出一套即可)
22.(2分)有一包粉末状固体,可能含有CuSO 、NaOH、Na CO 和CaCO 中的一种或几种,为确定粉
4 2 3 3
末的成分,进行了如下实验:取一定量粉末于试管中,加入足量水溶解后,静置观察,发现试管内溶液
为无色,试管底部有白色固体出现,用手触摸试管外壁明显感到发烫.请回答:
(1)这包粉末状固体中肯定有什么物质?
(2)为确定可能含有的物质是否存在,还需做什么实验?请简要写出实验操作和观察要点.
四、综合应用题:
23.(10分)金属盒金属化合物是重要的资源,生活、工业、农业生产都离不开金属盒金属化合物.
(1)如图是铝在元素周期表中的某些信息,下列根据该信息进行分析并得出的结论中,不正确的是
_________ .
A.原子序数为13 B.核外电子数为13C.在地壳中含量为26.98% D.在化学反应中易失电子
(2)现代社会使用大量的钢铁,写出工业上用赤铁矿(主要成分是氧化铁)冶铁的化学方程式
_________ ;钢铁与空气中的 ________ _ 接触容易生锈,为什么常常将铝粉涂刷在钢铁制品表面
来防止铁制品锈蚀? ________ _
(3)在Cu(NO )、AgNO 和Zn(NO )的混合溶液中加入一定量和铁粉,充分反应后过滤,向滤出的
3 2 3 3 2
固体中滴加稀硫酸,有气泡产生,则:
①滤出的固体中一定含有 ________ _ ,滤液中一定含有的溶质的化学式为 ________ _ ;
②写出一个上述过程中有关反应的化学方程式: ________ _ .
(4)钛(Ti)和钛合金被认为是21世纪的重要金属材料,生产金属钛常用镁和四氯化钛在高温条件下
发生置换反应来制取.计算:要制取10t的金属钛,消耗镁的质量是多少?参考答案
一、选择题(每小题1分,共12分)
1.B
2.C
3.C
4.D
5.B
6.A
7.D
8.B
9.D
10.B
11.D
12.A
二、填空题:(每空1分,共16分)
13.(1) C 0 ;(2) CH ;(3)空 N ; (4)可 CO .
4 2 2
14.(1) 活性炭 (2)为 肥皂水 (3) HClO .
15. N O .
2
16. 氧气 , 化学能 , 降低温度到枯柴的着火点以下 .
17. 2FeC l +Cu═CuCl +2FeCl ;该反应中, F e 、 C u 元素的化合价发生了变化,反应物中表现出
3 2 2
还原性的物质是 C u .
18.甲的名称为 碳酸钙 ;乙与丁反应的化学方程式为 C a ( OH ) +CO =CaCO ↓+H O .
2 2 3 2
三、简答题:
19、 解:依据ABCD四物质的分子结构情况可知四物质的化学式分别是CH 、H O、CO、H .则该
4 2 2
反应的方程式为:CH +H O CO+3H ;
4 2 2
D是氢气属于单质,故氢元素的化合价为0价;
故答案为:(1)0;(2)CH +H O CO+3H ;
4 2 2
20. 解:(1)洗涤剂能除去油污是由于洗涤剂把大颗粒的油污分解成小的颗粒的油污,便于被水冲
掉,属于乳化原理;
(2)分子是不断运动的,菊花中含有香味的分子不断运动,向四周扩散,所以人们能闻到香味;
(3)反应物为镁条和空气中的氧气,生成物为氧化镁,根据质量守恒定律,氧化镁的质量等于
参加反应的镁条和氧气的质量之和,所以比原来镁条的质量增大了.
(4)温度越高,化学反应速率越快;牛奶在夏天比冬天更容易变酸,这说明化学反应速率与温
度有关.
故答案为:(1)乳化
(2)分子是不断运动的,菊花中含有香味的分子不断运动,向四周扩散,所以人们能闻到香味
(3)反应物为镁条和空气中的氧气,生成物为氧化镁,根据质量守恒定律,氧化镁的质量等于
参加反应的镁条和氧气的质量之和,所以比原来镁条的质量增大了.
(4)温度越高,化学反应速率越快
21. 解:(1)若选择A、F组合一套装置,是需要加热的装置,因此可以用高锰酸钾或氯酸钾制氧
气,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;故答案为:2KMnO
4
K MnO +MnO +O ↑ (或 2KClO 2KC1+3O ↑)
2 4 2 2 3 2(2)碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,配平即可;其发生装置可选择B
或C,与B相比较,C的主要优点是:C用的是分液漏斗,可通过分液漏斗的开关控制液体的滴
加速率和滴加量,来控制反应的速度;故答案为:CaCO +2HC1=CaCl +CO ↑+H O;可通过分液
3 2 2 2
漏斗的开关控制液体的滴加速率和滴加量,来控制反应的速度.
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,氢气难溶于水,密度比空气的密度小,
因此可以用排水法和向下排空气法收集;故答案为:发生装置选B(或C),收集装置选E(或
F).
22. 解:取一定量粉末于试管中,加入足量水溶解后,静置观察,发现试管内溶液为无色,试管底部
有白色固体出现,则可以知道固体中不会存在显蓝色的硫酸铜,则一定含有难溶性的碳酸钙;
用手触摸试管外壁明显感到发烫,说明含有氢氧化钠固体,碳酸钠是否含有不能确定;因此:
(1)这包粉末状固体中肯定有难溶性的碳酸钙和溶解放热的氢氧化钠,故答案为:碳酸钙、氢
氧化钠;
(2)可能含有碳酸钠,可以取上层清液滴加稀盐酸,若产生气泡,则含有碳酸钠,否则不含有碳
酸钠;故答案为:取上层清液滴加稀盐酸,若产生气泡,则含有碳酸钠,否则不含有碳酸钠.
四、综合应用题:
23. 解:(1)A、铝元素的原子序数为13,故正确;
B、根据原子序数=质子数=核外电子数可知,铝原子核外电子数为13,故正确;
C、26.98是铝元素的相对原子质量,故错误;
D、铝元素原子最外层有3个电子,在化学反应中易失电子,故正确;
故选:C;
(2)氧化铁和一氧化碳反应的化学方程式为:3CO+Fe O 2Fe+3CO ;钢铁与空气中的
2 3 2
水、氧气接触容易生锈;铝易和空气中的氧气反应生成一层致密的氧化铝薄膜,因此常常将铝
粉涂刷在钢铁制品表面来防止铁制品锈蚀,故答案为:3CO+Fe O 2Fe+3CO ;水、氧
2 3 2
气;铝易和空气中的氧气反应生成一层致密的氧化铝薄膜;
(3)加入酸有气体,证明有铁剩余,则铜和银全部被置换出来,因此滤出的固体中一定含有
Fe、Cu、Ag;反应后的溶液中即滤液不再含的Cu(NO )、AgNO ,而是含有生成的Fe(NO );
3 2 3 3 2
由于Zn(NO )不与Fe发生反应,所以滤液中还含有Zn(NO );该过程中共发现两个反应:
3 2 3 2
铁和硝酸铜的置换反应,铁和硝酸银的置换反应,故答案为:Fe、Cu、Ag;Zn(NO )、Fe(NO )
3 2 3
;Fe+Cu(NO ) =Fe(NO ) +Cu;
2 3 2 3 2
(4)设需要镁的质量为x,则
TiCl +2Mg Ti+2MgCl
4 2
48 48
x 10t
= ,解得x=10t,
答:需要镁的质量为10t.