文档内容
九年级化学
2014 . 1
(满分:100分;考试时间:100分钟)
1.所有的试题都必须在专用的“答题卡”上作答,选择题用2B铅笔作答、非选择题在指定位置用0. 5毫
米黑色水笔作答。在试卷或草稿纸上答题无效
2.可能用到的相对原子质量:
H-1 C-12 O-16 N-14 K -39 I -127 Fe-56 Zn-65 Cu-64
第Ⅰ卷(选择题共40分)
[来源:Zxxk.Com]
一、选择题(每题只有1个选项符合题意,每题2分,共30分)
1.PM2.5是形成灰霾天气的最大元凶,它是指大气中直径小于或等于2.5微米的颗粒物,也称为可吸入颗
粒物。针对灰霾天气,下列做法不合理的是
A.举行“地球一小时"熄灯活动
B.灰霾天出门戴N95专业口罩(过滤孔径在0.1微米左右)
C.香烟烟雾颗粒的直径大多在0.1至1.0微米,提倡不吸烟或少吸烟
D.为了减小PM2.5对环境的影响,禁止家庭使用私家车
2.下面是几种人体重要体液的正常pH范围,其中酸性最强的是
A.胆汁(6.8~7.4) B.唾液(6.6~7.1) C.血液(7.35~7.45)D.胃液(0.8~1.5)
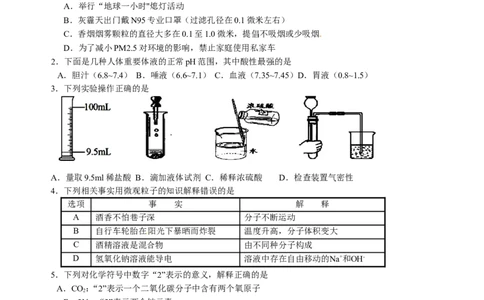
3.下列实验操作正确的是
A.量取9.5ml稀盐酸 B.滴加液体试剂 C.稀释浓硫酸 D.检查装置气密性
4.下列相关事实用微观粒子的知识解释错误的是
选项 事 实 解 释
A 酒香不怕巷子深 分子不断运动
B 自行车轮胎在阳光下暴晒而炸裂 温度升高,分子体积变大
C 酒精溶液是混合物 由不同种分子构成
D 氢氧化钠溶液能导电 溶液中存在自由移动的Na+和OH-
5.下列对化学符号中数字“2”表示的意义,解释正确的是
A.CO:“2”表示一个二氧化碳分子中含有两个氧原子
2
B.2Na:“2”表示两个钠元素
+
C. 2M g :“+2”表示每个镁离子带两个单位正电荷
D.S 2 - : “2–”表示硫元素的化合价为负二价
6.下列实验,可能达到预期目的的是
①用托盘天平称取2.5 g NaCl;
②用10 mL水和10 mL 36%浓盐酸制成20 mL 18%的稀盐酸
③20℃时,配制溶质质量分数为31.6%的硝酸钾溶液(已知20℃时,KNO 的溶解度是31.6g);
3
④用广泛的pH试纸测出肥皂水的pH为8
A.②③ B.①②④ C.①③④ D.①④
7.区分下列物质的方法中不可行的是
A.用燃烧的木条区别氧气和二氧化碳 B.用酚酞区分石灰水和肥皂水C.用二氧化锰区分双氧水和蒸馏水 D.用稀硫酸区分黄铜(Cu、Zn)和黄金
8.CO 和H 可在一定条件下反应,生成一种重要的化工原料甲醇:
2 2
钌-膦铬合物
CO 2 +3H 2 加 压 CH 3 OH+H 2 O,下列有关该反应的说法正确的是
A.为CO 的利用创造了一种新途径 B.钌-膦铬合物的质量在反应前后发生了变化
2
C.反应前后分子的数目没有改变 D.属于置换反应
9.下列关于金属及合金的说法正确的是
A.铝是人类最早利用的金属材料
B.铁是目前世界年产量最高的金属
C.大多数金属元素在自然界中以单质形式存在
D.多数合金的熔点高于组成它的成分金属
10.右图是元素周期表中的一格,从中获取的信息不正确的是
A.该元素的原子序数为18 B.该元素原子的核外有18个电子
C.该元素属于金属元素 D.该元素的相对原子质量为39.95
11.下列实验现象描述错误的是
A.加热“铜绿“时,绿色固体会变成黑色,管壁出现小水珠
B.镁条燃烧时,产生耀眼的白光,同时生成一种黑色粉末状固体
[来源:Zxxk.Com]
C.铁丝在氧气中燃烧时,会火星四射,放出热量,生成一种黑色固体
D.白磷在空气中燃烧产生大量的白烟,放出热量
12.下列实验、生产和生活安全的做法不正确的是
A.洒在实验桌上的少量酒精着火,迅速用湿布盖灭
B.家用电器着火,迅速切断电源
C.油库、面粉厂、纺织厂、煤矿矿井内都要严禁烟火
D.夜间厨房发生煤气泄漏时,应立即开灯检查并打开门窗通风
13.下列说法正确的是
A.冬天在汽车的水箱中加入乙二醇做防冻剂,是因为乙二醇溶于水能放出大量的热
B.煮沸的汤比煮沸的水烫,是因为汤中溶解了食盐等物质而使溶液的沸点升高
C.从饱和溶液中析出晶体后,溶质质量分数一定减小
D.将饱和的硝酸钾溶液变成不饱和溶液,其溶质质量分数一定减小
14.欲将粗盐提纯并用所得精盐配制一定质量分数的氯化钠溶液。下列说法正确的是
A.粗盐提纯时,用玻璃棒搅拌可加快过滤的速度
B.蒸发滤液时,待蒸发皿中液体蒸干时停止加热
C.配制溶液时,仰视量筒读数,会导致配制的溶液偏稀
D.配制溶液时,必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
15.在密闭容器内有X 、Y 、Z、Q四种物质,在一定条件下使它们充分反应,测得反应前后各物质的质量如
下表,下列说法不正确的是
物 质 X Y Z Q
反应前质量/g 8 2 20 5
反应后质量/g 待测 10 8 13
A.反应后X的质量为4 g B.若X是氧气,该反应为氧化反应
C.参加反应的X、Z的质量比是1:3 D.Y、Q的相对分子质量之比一定为1:1
二、选择题(每题有1~2个正确答案。错选、多选不给分,漏选一个给1分。每题2分,共10分)
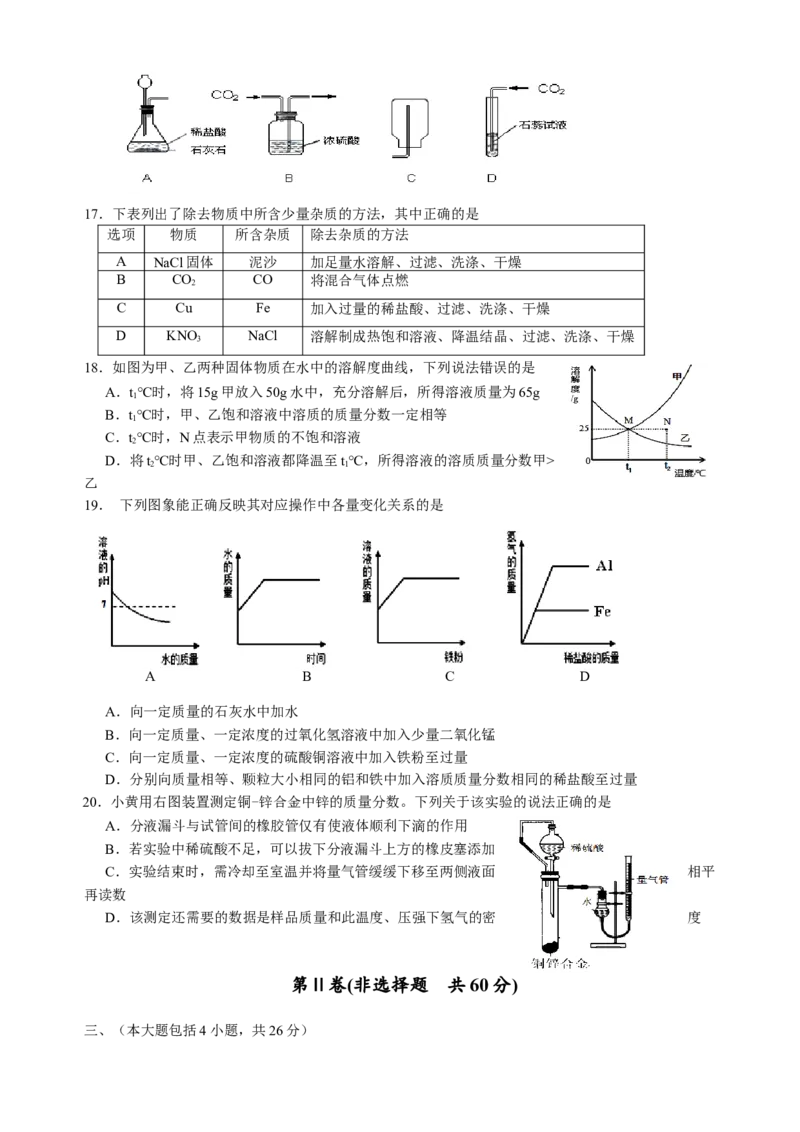
16.下图分别是二氧化碳的制取、干燥、收集和性质检验的装置图,其中正确的是17.下表列出了除去物质中所含少量杂质的方法,其中正确的是
选项 物质 所含杂质 除去杂质的方法
A NaCl固体 泥沙 加足量水溶解、过滤、洗涤、干燥
B CO CO 将混合气体点燃
2
C Cu Fe 加入过量的稀盐酸、过滤、洗涤、干燥
D KNO NaCl 溶解制成热饱和溶液、降温结晶、过滤、洗涤、干燥
3
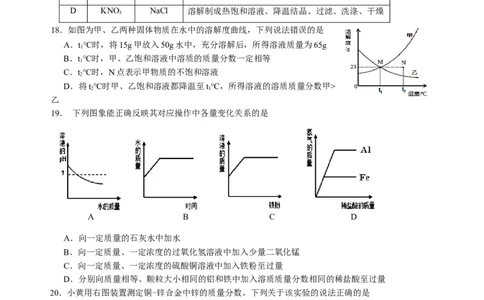
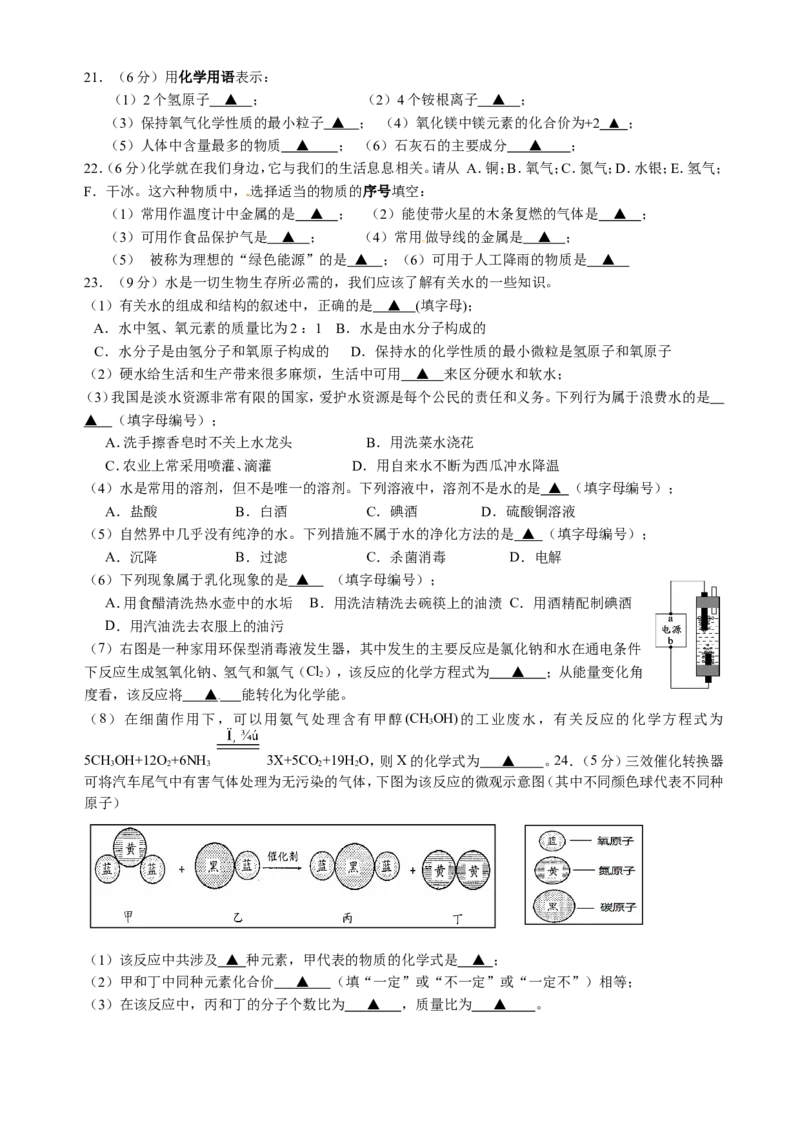
18.如图为甲、乙两种固体物质在水中的溶解度曲线,下列说法错误的是
A.t℃时,将15g甲放入50g水中,充分溶解后,所得溶液质量为65g
1
B.t℃时,甲、乙饱和溶液中溶质的质量分数一定相等
1
C.t℃时,N点表示甲物质的不饱和溶液
2
D.将t℃时甲、乙饱和溶液都降温至t℃,所得溶液的溶质质量分数甲>
2 1
乙
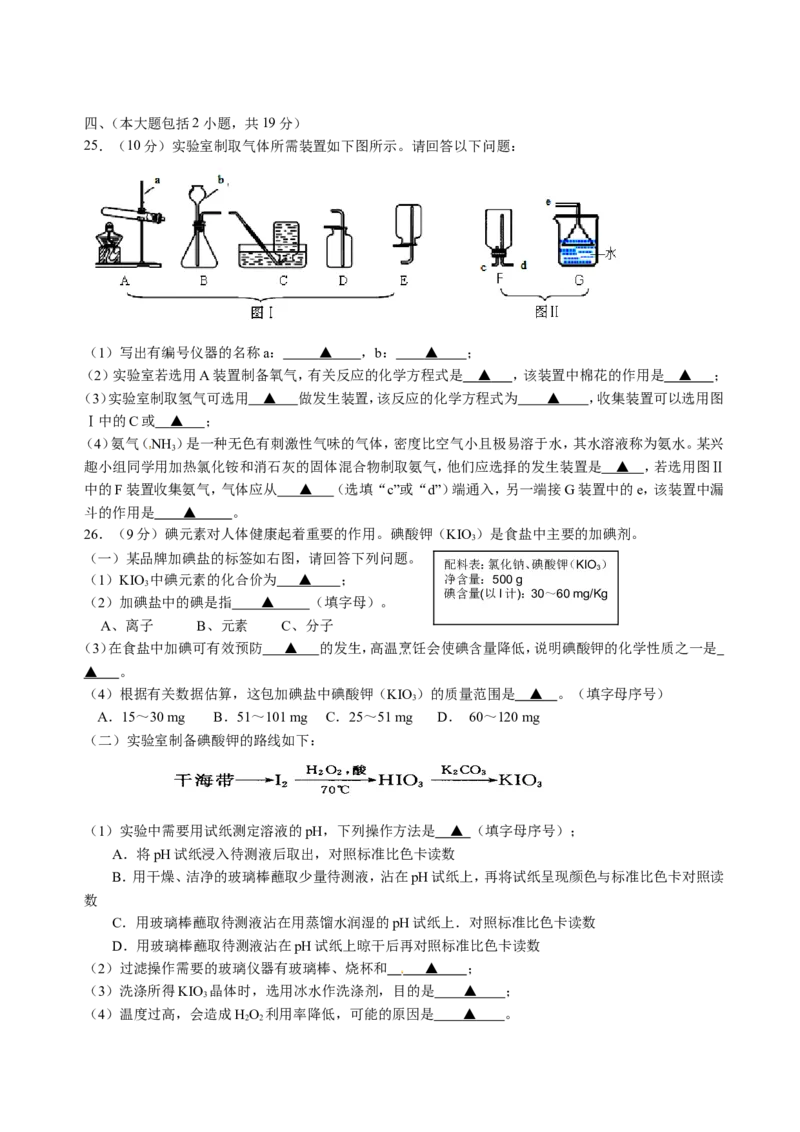
19. 下列图象能正确反映其对应操作中各量变化关系的是
[来源:学科网]
A B C D
A.向一定质量的石灰水中加水
B.向一定质量、一定浓度的过氧化氢溶液中加入少量二氧化锰
C.向一定质量、一定浓度的硫酸铜溶液中加入铁粉至过量
D.分别向质量相等、颗粒大小相同的铝和铁中加入溶质质量分数相同的稀盐酸至过量
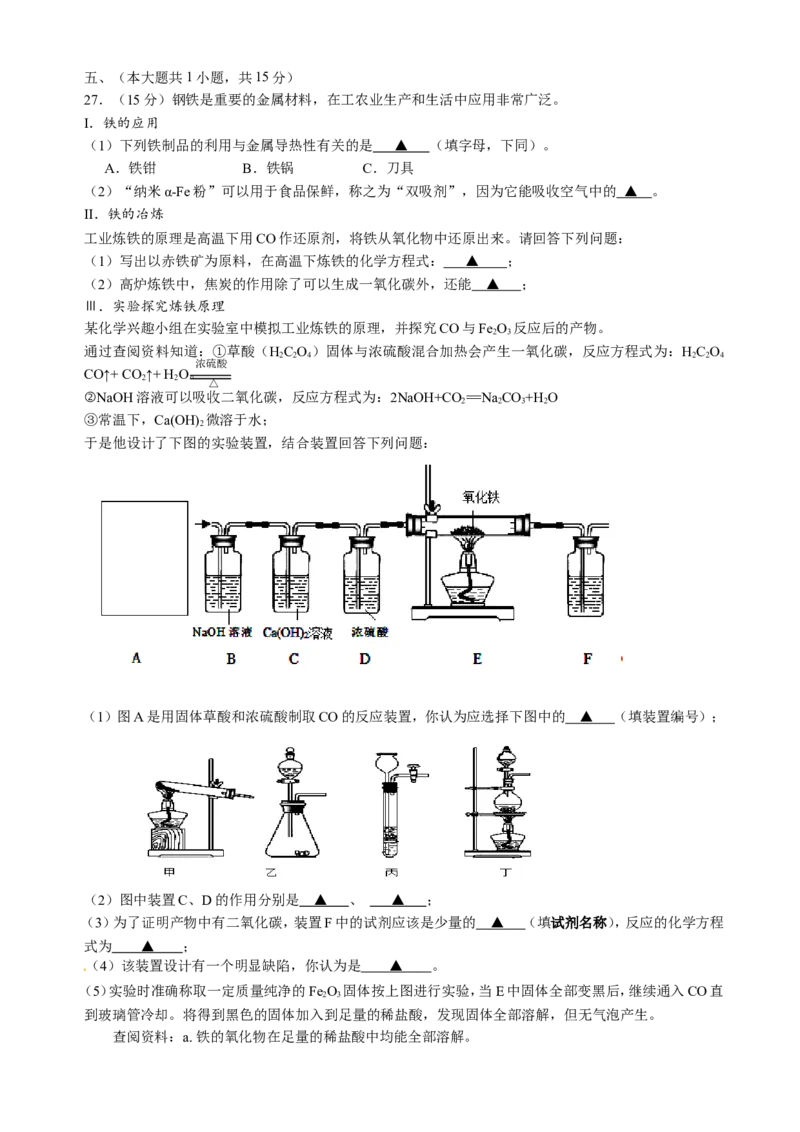
20.小黄用右图装置测定铜-锌合金中锌的质量分数。下列关于该实验的说法正确的是
A.分液漏斗与试管间的橡胶管仅有使液体顺利下滴的作用
B.若实验中稀硫酸不足,可以拔下分液漏斗上方的橡皮塞添加
C.实验结束时,需冷却至室温并将量气管缓缓下移至两侧液面 相平
再读数
D.该测定还需要的数据是样品质量和此温度、压强下氢气的密 度
第Ⅱ卷(非选择题 共60分)
三、(本大题包括4小题,共26分)21.(6分)用化学用语表示:
(1)2个氢原子 ▲ ; (2)4个铵根离子 ▲ ;
(3)保持氧气化学性质的最小粒子 ▲ ; (4)氧化镁中镁元素的化合价为+2 ▲ ;
(5)人体中含量最多的物质 ▲ ; (6)石灰石的主要成分 ▲ ;
22.(6分)化学就在我们身边,它与我们的生活息息相关。请从 A.铜;B.氧气;C.氮气;D.水银;E.氢气;
F.干冰。这六种物质中,选择适当的物质的序号填空:
(1)常用作温度计中金属的是 ▲ ; (2)能使带火星的木条复燃的气体是 ▲ ;
(3)可用作食品保护气是 ▲ ; (4)常用做导线的金属是 ▲ ;
(5) 被称为理想的“绿色能源”的是 ▲ ;(6)可用于人工降雨的物质是 ▲
23.(9分)水是一切生物生存所必需的,我们应该了解有关水的一些知识。
(1)有关水的组成和结构的叙述中,正确的是 ▲ (填字母);
A.水中氢、氧元素的质量比为2 :1 B.水是由水分子构成的
C.水分子是由氢分子和氧原子构成的 D.保持水的化学性质的最小微粒是氢原子和氧原子
(2)硬水给生活和生产带来很多麻烦,生活中可用 ▲ 来区分硬水和软水;
(3)我国是淡水资源非常有限的国家,爱护水资源是每个公民的责任和义务。下列行为属于浪费水的是
▲ (填字母编号);
A.洗手擦香皂时不关上水龙头 B.用洗菜水浇花
C.农业上常采用喷灌、滴灌 D.用自来水不断为西瓜冲水降温
(4)水是常用的溶剂,但不是唯一的溶剂。下列溶液中,溶剂不是水的是 ▲ (填字母编号);
A.盐酸 B.白酒 C.碘酒 D.硫酸铜溶液
(5)自然界中几乎没有纯净的水。下列措施不属于水的净化方法的是 ▲ (填字母编号);
A.沉降 B.过滤 C.杀菌消毒 D.电解
(6)下列现象属于乳化现象的是 ▲ (填字母编号);
A.用食醋清洗热水壶中的水垢 B.用洗洁精洗去碗筷上的油渍 C.用酒精配制碘酒
D.用汽油洗去衣服上的油污
(7)右图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件
下反应生成氢氧化钠、氢气和氯气(Cl),该反应的化学方程式为 ▲ ;从能量变化角
2
度看,该反应将 ▲ 能转化为化学能。
(8)在细菌作用下,可以用氨气处理含有甲醇(CHOH)的工业废水,有关反应的化学方程式为
3
5CHOH+12O +6NH 3X+5CO+19H O,则X的化学式为 ▲ 。24.(5分)三效催化转换器
3 2 3 2 2
可将汽车尾气中有害气体处理为无污染的气体,下图为该反应的微观示意图(其中不同颜色球代表不同种
原子)
(1)该反应中共涉及 ▲ 种元素,甲代表的物质的化学式是 ▲ ;
(2)甲和丁中同种元素化合价 ▲ (填“一定”或“不一定”或“一定不”)相等;
(3)在该反应中,丙和丁的分子个数比为 ▲ ,质量比为 ▲ 。四、(本大题包括2小题,共19分)
25.(10分)实验室制取气体所需装置如下图所示。请回答以下问题:
(1)写出有编号仪器的名称a: ▲ ,b: ▲ ;
(2)实验室若选用A装置制备氧气,有关反应的化学方程式是 ▲ ,该装置中棉花的作用是 ▲ ;
(3)实验室制取氢气可选用 ▲ 做发生装置,该反应的化学方程式为 ▲ ,收集装置可以选用图
Ⅰ中的C或 ▲ ;
(4)氨气(NH )是一种无色有刺激性气味的气体,密度比空气小且极易溶于水,其水溶液称为氨水。某兴
3
趣小组同学用加热氯化铵和消石灰的固体混合物制取氨气,他们应选择的发生装置是 ▲ ,若选用图Ⅱ
中的F装置收集氨气,气体应从 ▲ (选填“c”或“d”)端通入,另一端接G装置中的e,该装置中漏
斗的作用是 ▲ 。
26.(9分)碘元素对人体健康起着重要的作用。碘酸钾(KIO )是食盐中主要的加碘剂。
3
(一)某品牌加碘盐的标签如右图,请回答下列问题。
配料表:氯化钠、碘酸钾(KIO)
3
(1)KIO 中碘元素的化合价为 ▲ ; 净含量:500 g
3
碘含量(以I计):30~60 mg/Kg
(2)加碘盐中的碘是指 ▲ (填字母)。
A、离子 B、元素 C、分子
(3)在食盐中加碘可有效预防 ▲ 的发生,高温烹饪会使碘含量降低,说明碘酸钾的化学性质之一是
▲ 。
(4)根据有关数据估算,这包加碘盐中碘酸钾(KIO )的质量范围是 ▲ 。(填字母序号)
3
A.15~30 mg B.51~101 mg C.25~51 mg D. 60~120 mg
(二)实验室制备碘酸钾的路线如下:
(1)实验中需要用试纸测定溶液的pH,下列操作方法是 ▲ (填字母序号);
A.将pH试纸浸入待测液后取出,对照标准比色卡读数
B.用干燥、洁净的玻璃棒蘸取少量待测液,沾在pH试纸上,再将试纸呈现颜色与标准比色卡对照读
数
C.用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数
D.用玻璃棒蘸取待测液沾在pH试纸上晾干后再对照标准比色卡读数
(2)过滤操作需要的玻璃仪器有玻璃棒、烧杯和 ▲ ;
(3)洗涤所得KIO 晶体时,选用冰水作洗涤剂,目的是 ▲ ;
3
(4)温度过高,会造成HO 利用率降低,可能的原因是 ▲ 。
2 2五、(本大题共1小题,共15分)
27.(15分)钢铁是重要的金属材料,在工农业生产和生活中应用非常广泛。
I.铁的应用
(1)下列铁制品的利用与金属导热性有关的是 ▲ (填字母,下同)。
A.铁钳 B.铁锅 C.刀具
(2)“纳米α-Fe粉”可以用于食品保鲜,称之为“双吸剂”,因为它能吸收空气中的 ▲ 。
II.铁的冶炼
工业炼铁的原理是高温下用CO作还原剂,将铁从氧化物中还原出来。请回答下列问题:
(1)写出以赤铁矿为原料,在高温下炼铁的化学方程式: ▲ ;
(2)高炉炼铁中,焦炭的作用除了可以生成一氧化碳外,还能 ▲ ;
Ⅲ.实验探究炼铁原理
某化学兴趣小组在实验室中模拟工业炼铁的原理,并探究CO与Fe O 反应后的产物。
2 3
通过查阅资料知道:①草酸(HC O )固体与浓硫酸混合加热会产生一氧化碳,反应方程式为:HC O
2 2 4 2 2 4
浓硫酸
CO↑+ CO
2
↑+ H
2
O。
△
②NaOH溶液可以吸收二氧化碳,反应方程式为:2NaOH+CO =NaCO+H O
2 2 3 2
③常温下,Ca(OH) 微溶于水;
2
于是他设计了下图的实验装置,结合装置回答下列问题:
(1)图A是用固体草酸和浓硫酸制取CO的反应装置,你认为应选择下图中的 ▲ (填装置编号);
(2)图中装置C、D的作用分别是 ▲ 、 ▲ ;
(3)为了证明产物中有二氧化碳,装置F中的试剂应该是少量的 ▲ (填试剂名称),反应的化学方程
式为 ▲ ;
(4)该装置设计有一个明显缺陷,你认为是 ▲ 。
(5)实验时准确称取一定质量纯净的Fe O 固体按上图进行实验,当E中固体全部变黑后,继续通入CO直
2 3
到玻璃管冷却。将得到黑色的固体加入到足量的稀盐酸,发现固体全部溶解,但无气泡产生。
查阅资料:a. 铁的氧化物在足量的稀盐酸中均能全部溶解。b. Fe O 与CO反应的固体生成物可能情况如下:
2 3
根据“无气泡”猜想,黑色粉末可能是:① Fe O ;② ▲ ③ ▲ 。
3 4
(6)定量分析 用电子天平称量得部分数据如下:
根据
玻璃管质量 玻璃管及其中固体的质量 装置F及其中物质的总质量
上述 [来源:Z§xx§k.Com] 数据,
反应前 33.00 g 300.0 g
纯净 28.20 g [来源:学科网] 的
反应后 32.84 g 300.4 g
Fe O 固
2 3
体质量为 ▲ g,请选择有效的数据,推断出反应后黑色固体的成分。(写出计算过程) ▲ 。
根据推断结果,写出该实验中玻璃管内发生的化学反应方程式: ▲扬州中学教育集团2013–2014学年第一学期期末考试
九年级化学参考答案
一、 选择题
D D C B A; D B A B C; B D B C D; D CD A BD CD
+2
21. 2H 4NH + O MgO H O CaCO
4 2 2 3
22. D B C A E F
23.(1)B (2)肥皂水 (3)AD (4)C (5)D (6)B
(7) 2NaCl+2H O 通电 2NaOH+H ↑+Cl ↑ 电
2 2 2
(8)N
2
24.(1)三 NO (2)一定不 (3)4:1 44:7
2
25.(1)铁架台 长颈漏斗 (2)略 防止固体粉末堵塞导管(合理即可)
(3)B 略 E (4)A d 防倒吸
26.(一)
(1)+5 (2)B (3)甲状腺疾病(或大脖子病 ) 热稳定性差(或受热易分解等)
(4)C
(二)
(1)B (2)漏斗 (3)降低(或减少)晶体损耗 (4)H O 受热易分解
2 2
27.I.铁的应用
(1) B (2)氧气和水(或O 和H O)
2 2
II.铁的冶炼
(1)略 (2)提供热源,维持炉温
Ⅲ.实验探究炼铁原理
(1) 丁 (2)证明CO 已经除尽 吸收水分(或干燥CO)
2
(3)澄清的石灰水(或氢氧化钙溶液) 略 (4)缺少尾气处理装置
(5)FeO Fe O 和FeO
3 4
(6)4.8 Fe O ((计算过程略) CO+3Fe O △ 2Fe O +CO
3 4 2 3 3 4 2