文档内容
北京景山学校 2019~2020 学年第二学期
高一年级化学期末考试试卷
事项:
(1)请用蓝色或黑色圆珠笔、钢笔或签字笔答题,不得使用铅笔或红笔答卷。
(2)认真审题,字迹工整,卷面整洁注意。
(3)本试卷共8页,共有2道大题,35道小题。考试时间90分钟。其中35题为附加题,该
题为4、5班必做题,1、2、3班选做题。
(4)请将试题答案填写在答题纸上。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Cl-35.5 Fe-56
第一部分(选择题共60分)
一、选择题(本题包括30小题,每小题2分,共60分,每小题只有一个选项符合题意)。
1.下列有关氧气的摩尔质量表示正确的是
A. 32 B. 32 g C. 32 mol D. 32 g/mol
2.当光束通过下列分散系时,能观察到丁达尔效应的是( )
A. 泥浆 B. CuSO 溶液 C. Fe(OH) 胶体 D. 酒精溶液
4 3
3. 下列物质属于电解质且能导电的是
A. 金属铜 B. 碳酸钠晶体 C. 硝酸钠溶液 D. 熔融氯化钠
4. 下列金属在冷、浓的硝酸或硫酸中,能形成致密氧化膜的是( )
A. Mg B. Fe C. Cu D. Na
5. 下列物质中,可用于治疗胃酸过多的是( )
A. 氢氧化铝 B. 氯化钠 C. 氢氧化钠 D. 硫酸钠
6.下列物质中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①Al ②Al O ③Ca(OH) ④Al(OH) ⑤NaCO ⑥NaHCO
2 3 2 3 2 3 3
A. ①②③⑤ B. ①②④⑥ C. ①②⑤⑥ D. ②③④⑥
7.用化学方法区别NaCl、MgCl 、AlCl 、CuCl 、FeCl 和NH Cl六种溶液(必要时可加热),下列试剂中
2 3 2 3 4
可选用的是( )
A. KSCN溶液 B. AgNO 溶液 C. BaCl 溶液 D. NaOH溶液
3 2
8.下列离子方程式书写正确的是( )
A. 铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+
B. 氯化铝溶液与过量的氢氧化钠溶液反应:Al3++3OH-=Al(OH)↓
3
C. 氯气与氢氧化钠溶液反应:Cl+2OH-=Cl-+ClO-+HO
2 2D. 碳酸氢钠溶液与稀盐酸反应:2H++CO2-=CO↑+HO
3 2 2
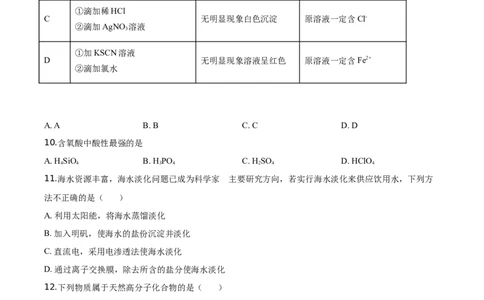
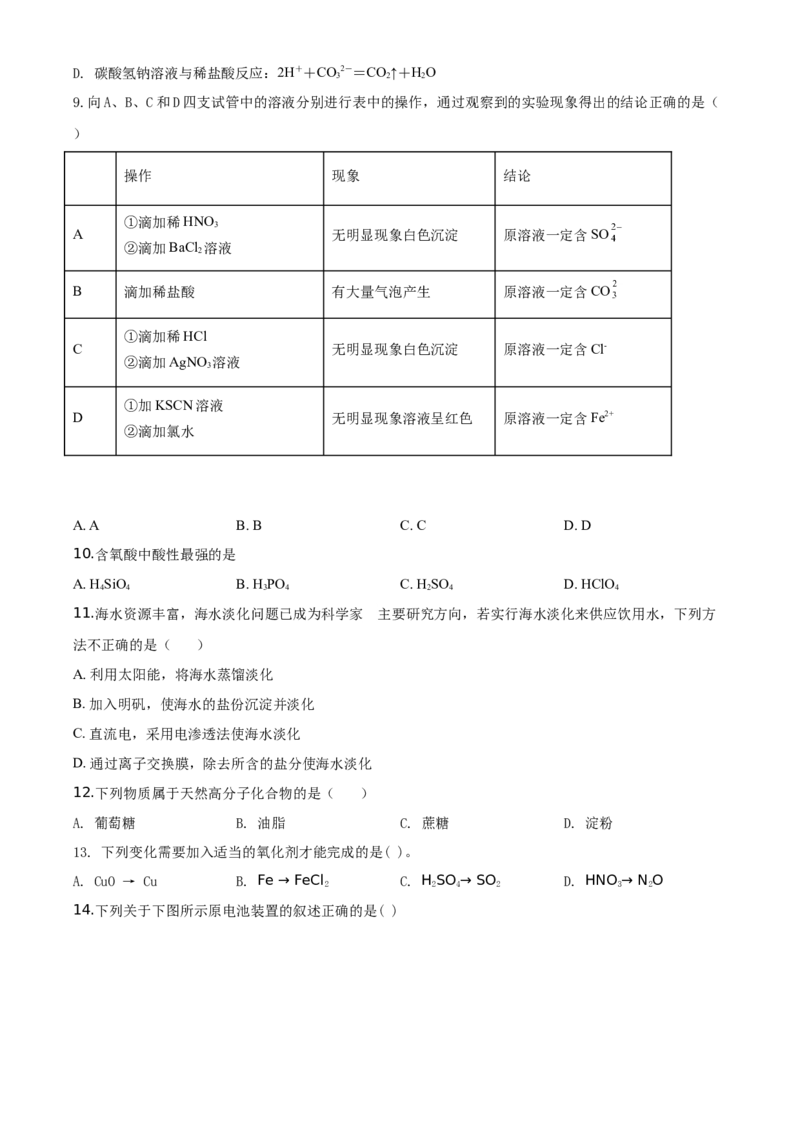
9.向A、B、C和D四支试管中的溶液分别进行表中的操作,通过观察到的实验现象得出的结论正确的是(
)
操作 现象 结论
①滴加稀HNO
3
A 无明显现象白色沉淀 原溶液一定含SO
②滴加BaCl 溶液
2
B 滴加稀盐酸 有大量气泡产生 原溶液一定含CO
①滴加稀HCl
C 无明显现象白色沉淀 原溶液一定含Cl-
②滴加AgNO 溶液
3
①加KSCN溶液
D 无明显现象溶液呈红色 原溶液一定含Fe2+
②滴加氯水
A. A B. B C. C D. D
10.含氧酸中酸性最强的是
A. H SiO B. HPO C. HSO D. HClO
4 4 3 4 2 4 4
11.海水资源丰富,海水淡化问题已成为科学家 的主要研究方向,若实行海水淡化来供应饮用水,下列方
法不正确的是( )
A. 利用太阳能,将海水蒸馏淡化
B. 加入明矾,使海水的盐份沉淀并淡化
C. 直流电,采用电渗透法使海水淡化
D. 通过离子交换膜,除去所含的盐分使海水淡化
12.下列物质属于天然高分子化合物的是( )
A. 葡萄糖 B. 油脂 C. 蔗糖 D. 淀粉
13. 下列变化需要加入适当的氧化剂才能完成的是( )。
A. CuO → Cu B. Fe → FeCl C. HSO→ SO D. HNO→ N O
2 2 4 2 3 2
14.下列关于下图所示原电池装置的叙述正确的是( )A. 铜片是负极 B. 铜片质量逐渐减少
C. 氢离子在铜片表面被还原 D. 电流从锌片经导线流向铜片
15.用铁片与稀硫酸反应制氢气时,下列措施不能使反应速率加快的是( )
A. 加热
B. 不用稀硫酸,改用98%的浓硫酸
C. 滴加少量CuSO 溶液
4
D. 不用铁片,改用铁粉
16.元素性质呈现周期性变化的根本原因是( )
A. 元素的原子量逐渐增大
B. 核外电子排布呈周期性变化
C. 核电荷数逐渐增大
D. 元素化合价呈周期性变化
17.下列单质中,按最高正价递增的顺序排列的是( )
A. C、N、O、F B. F、Cl、Br、O C. K、Mg、C、S D. Li、Na、K、Rb
18.下列元素中,原子半径最大的是( )
A. Na B. Mg C. Al D. C
19.下列关于化学键的叙述正确的是( )
A. 离子化合物中只含离子键
B. 共价化合物一定不含离子键
C. 离子化合物一定不含共价键
D. 共价化合物可能含有离子键
20.“1998年中国十大科技成果”之一是合成一维纳米氮化镓。已知氮化镓中镓是第ⅢA族元素,则氮化镓
的化学式可能为( )
A. GaN B. GaN C. GaN D. GaN
2 3 3 2 2
21.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。下列说法正确的是( )
X Y
Z WA. 原子半径:X>Y>Z>W
B. 若它们都能形成气态氢化物,则Z的氢化物稳定性最强
C. 若常温下它们的单质中只有Z为固态,则W单质的水溶液具有漂白性
D. 若X与W形成的化合物的电子式是 ,则Y属于第ⅣA族
22.2002年多国科学家通过离子加速器进行实验,获得了6个罕见的 Fe原子,并且观测到这6个原子中
有4个发生了双质子衰变,即由一个原子核同时放出两个质子的衰变方式。下列关于 Fe的说法正确的是
( )
A. 该原子的中子数与质子数之差为3
B. 是一种新元素
.
C Fe与 Fe化学性质几乎相同
D. 这种铁原子衰变放出两个质子后变成 Fe
23.已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
A. 该反应为吸热反应
B. A物质能量一定低于C物质能量
C. 该反应只有 在加热条件下才能进行
D. 反应物的总能量高于生成物的总能量
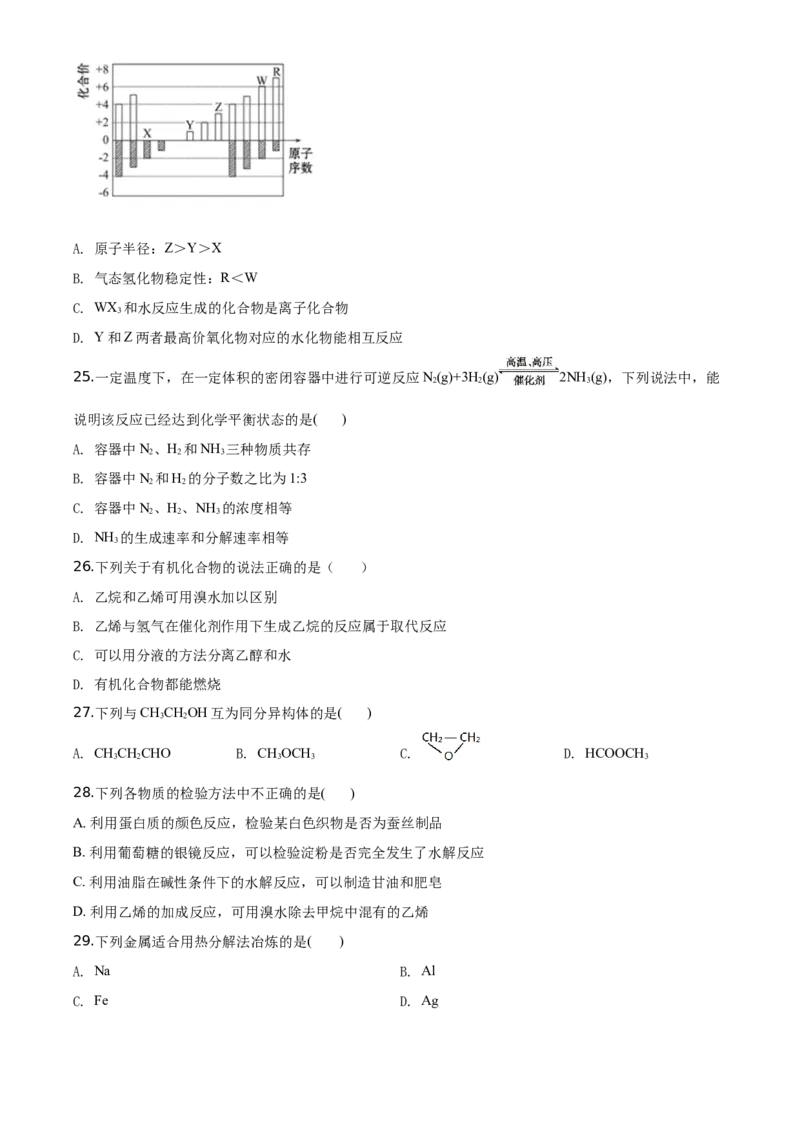
24.图中是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )A. 原子半径:Z>Y>X
B. 气态氢化物稳定性:R<W
C. WX 和水反应生成的化合物是离子化合物
3
D. Y和Z两者最高价氧化物对应的水化物能相互反应
25.一定温度下,在一定体积的密闭容器中进行可逆反应N(g)+3H(g) 2NH (g),下列说法中,能
2 2 3
说明该反应已经达到化学平衡状态的是( )
A. 容器中N、H 和NH 三种物质共存
2 2 3
B. 容器中N 和H 的分子数之比为1:3
2 2
C. 容器中N、H、NH 的浓度相等
2 2 3
D. NH 的生成速率和分解速率相等
3
26.下列关于有机化合物的说法正确的是( )
A. 乙烷和乙烯可用溴水加以区别
B. 乙烯与氢气在催化剂作用下生成乙烷的反应属于取代反应
C. 可以用分液的方法分离乙醇和水
D. 有机化合物都能燃烧
27.下列与CHCHOH互为同分异构体的是( )
3 2
A. CHCHCHO B. CHOCH C. D. HCOOCH
3 2 3 3 3
28.下列各物质的检验方法中不正确的是( )
A. 利用蛋白质的颜色反应,检验某白色织物是否为蚕丝制品
B. 利用葡萄糖的银镜反应,可以检验淀粉是否完全发生了水解反应
C. 利用油脂在碱性条件下的水解反应,可以制造甘油和肥皂
D. 利用乙烯的加成反应,可用溴水除去甲烷中混有的乙烯
29.下列金属适合用热分解法冶炼的是( )
A. Na B. Al
C. Fe D. Ag30.食盐中所加的碘以碘酸钾(KIO )形式存在。根据反应:IO +I-+H+→I+H O(未配平),可用KI淀粉试
3 2 2
纸和食醋进行实验,证明加碘食盐中存在IO 。下列说法不正确的是( )
A. 上述反应中氧化剂和还原剂的物质的量之比为1∶5
B. 实验时可观察到试纸变蓝
C. 实验可证明该条件下I-的还原性强于Cl-
D. 食醋中含有的乙酸是强酸,它能提供反应所需的H+
第二部分(非选择题共40分)
二、填空题(本题包括4道小题,共40分)
31.将下列物质进行分类:
① H与 H;②O 与O;③乙醇(C HOH)与甲醚(CH—O—CH );④正戊烷(CHCHCHCHCH)与异丁烷
2 3 2 5 3 3 3 2 2 2 3
( )
(1)互为同位素的是_____(填序号、下同);
(2)互为同系物的是_____;
(3)互为同分异构体的是_____。
32.来自石油的有机化工原料A,可以发生如下转化:
已知:E是具有果香味的有机物,F是一种高分子化合物。请回答下列问题。
(1)A 的分子式是_____,C的名称是_____。
(2)D分子中的官能团名称是_____。
(3)反应③的化学方程式是_____,该反应属于_____反应。反应④的化学方程式是_____,该反应属于
_____反应。
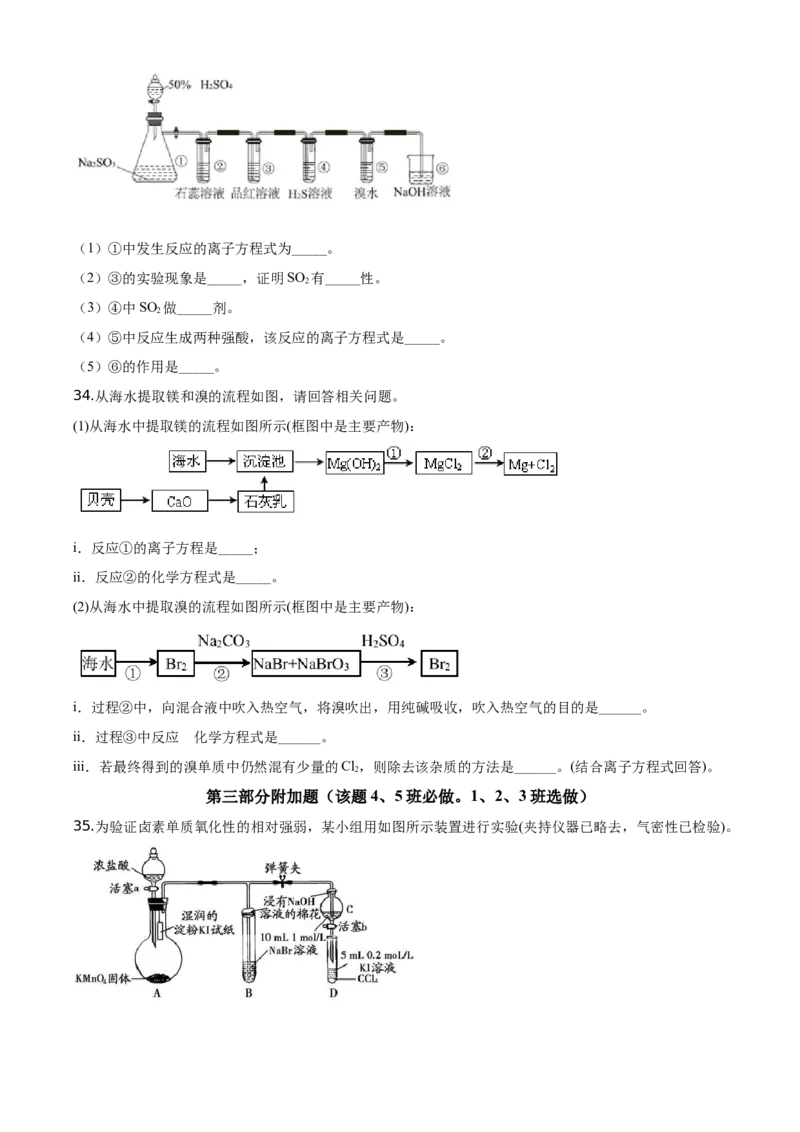
33.如图是实验室制取SO 并验证SO 某些性质的装置图。若观察到装置④中的有淡黄色沉淀生成,⑤中的
2 2
溴水褪色(已知因含有Br 而溴水呈红棕色),请回答:
2(1)①中发生反应的离子方程式为_____。
(2)③的实验现象是_____,证明SO 有_____性。
2
(3)④中SO 做_____剂。
2
(4)⑤中反应生成两种强酸,该反应的离子方程式是_____。
(5)⑥的作用是_____。
34.从海水提取镁和溴的流程如图,请回答相关问题。
(1)从海水中提取镁的流程如图所示(框图中是主要产物):
i.反应①的离子方程是_____;
ii.反应②的化学方程式是_____。
(2)从海水中提取溴的流程如图所示(框图中是主要产物):
i.过程②中,向混合液中吹入热空气,将溴吹出,用纯碱吸收,吹入热空气的目的是______。
ii.过程③中反应 的化学方程式是______。
iii.若最终得到的溴单质中仍然混有少量的Cl,则除去该杂质的方法是______。(结合离子方程式回答)。
2
第三部分附加题(该题4、5班必做。1、2、3班选做)
35.为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.……
(1)A中产生黄绿色气体,其电子式是_____。
(2)验证氯气的氧化性强于碘的实验现象是____。
(3)B中溶液发生反应的离子方程式是______。
(4)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是_____。
(5)过程Ⅲ实验的目的是______。