文档内容
高频考点 13 无机化工流程题
1.(2022·山东卷)高压氢还原法可直接从溶液中提取金属粉。以硫化铜精矿(含Zn、Fe元素的杂质)为主
要原料制备Cu粉的工艺流程如下,可能用到的数据见下表。
开始沉淀pH 1.9 4.2 6.2
沉淀完全pH 3.2 6.7 8.2
下列说法错误的是( )
A.固体X主要成分是 和S;金属M为Zn
B.浸取时,增大 压强可促进金属离子浸出
C.中和调pH的范围为3.2~4.2
D.还原时,增大溶液酸度有利于Cu的生成
1.D A.经过上述分析可知固体X主要成分是S、Fe(OH) ,金属M为Zn,A正确;
3
B.CuS难溶于硫酸,在溶液中存在沉淀溶解平衡CuS(s) Cu2+(aq)+S2-(aq),增大O 的浓度,可以反应消耗
2
S2-,使之转化为S,从而使沉淀溶解平衡正向移动,从而可促进金属离子的浸取,B正确;C.根据流程图
可知:用NH 调节溶液pH时,要使Fe3+转化为沉淀,而Cu2+、Zn2+仍以离子形式存在于溶液中,结合离子
3
沉淀的pH范围,可知中和时应该调节溶液pH范围为3.2~4.2,C正确;D.在用H 还原Cu2+变为Cu单质
2
时,H 失去电子被氧化为H+,与溶液中OH-结合形成H O,若还原时增大溶液的酸度,c(H+)增大,不利于
2 2
H 失去电子还原Cu单质,因此不利于Cu的生成,D错误;故合理选项是D。
2
2.(2021·河北卷)BiOCl是一种具有珠光泽的材料,利用金属Bi制备BiOCl的工艺流程如图:下列说法错误的是( )
A.酸浸工序中分次加入稀HNO 可降低反应剧烈程度
3
B.转化工序中加入稀HCl可抑制生成BiONO
3
C.水解工序中加入少量CH COONa(s)可提高Bi3+水解程度
3
D.水解工序中加入少量NH NO (s)有利于BiOCl的生成
4 3
2.D A.硝酸为强氧化剂,可与金属铋反应,酸浸工序中分次加入稀 ,反应物硝酸的用量减少,
可降低反应剧烈程度,A正确;B.金属铋与硝酸反应生成的硝酸铋会发生水解反应生成 ,水解
的离子方程式为 ,转化工序中加入稀 ,使氢离子浓度增大,根
据勒夏特列原理分析,硝酸铋水解平衡左移,可抑制生成 ,B正确;C.氯化铋水解生成
的离子方程式为 ,水解工序中加入少量 ,醋酸根会结合
氢离子生成弱电解质醋酸,使氢离子浓度减小,根据勒夏特列原理分析,氯化铋水解平衡右移,促进
水解,C正确;D.氯化铋水解生成 的离子方程式为 ,水解工序中
加入少量 ,铵根离子水解生成氢离子,使氢离子浓度增大,根据勒夏特列原理分析,氯化铋
水解平衡左移,不利于生成 ,且部分铋离子与硝酸根、水也会发生反应
,也不利于生成 ,综上所述,D错误;故选D。
3.(双选)(2022·江苏省如皋中学高三开学考试)氯酸镁[Mg(ClO )]常做催熟剂、除草剂等。实验室利用
3
卤块(主要成分为MgCl •6H O,含有MgSO 、FeCl 等杂质)制备少量Mg(ClO ) 的工艺流程如图:
2 2 4 2 3 2部分氢氧化物开始沉淀及沉淀完全的pH如表所示:
氢氧化物 Fe(OH) Fe(OH) Mg(OH)
3 2 2
开始沉淀的pH 1.5 6.5 8.9
沉淀完全的pH 3.2 9.7 10.9
下列说法正确的是( )
A.反应I的离子方程式为MnO +5Fe2++4H O=Mn2++5Fe3++8OH-
2
B.反应II后溶液中大量存在的离子是Mg2+、Ba2+、Fe3+、SO 、Cl-
C.调pH时应控制溶液的pH在3.2~8.9
D.反应III属于复分解反应,能够发生的原因是因为生成溶解度相对较小的Mg(ClO )
3 2
3.CD A.反应环境为酸性环境,故离子方程式为:MnO +5Fe2++8H+=Mn2++5Fe3++4H O,A错误;B.钡离
2
子和硫酸根离子会生成硫酸钡沉淀,不能大量共存,B错误;C.由分析可知,调节pH的目的是为了让三
价铁形成沉淀,同时镁离子不沉淀,根据表格中的数据可知,pH应该在3.2~8.9,C正确;D.过滤后溶液
主要存在的金属阳离子是镁离子,根据流程图可知,镁离子和氯酸根离子反应生成氯酸镁沉淀,属于复分
解反应,就是因为氯酸镁难溶于水,D正确;故选CD。
4.(2022·江苏省上冈高级中学高三开学考试)用硫酸渣(主要成分为Fe O 、SiO )制备铁基颜料铁黄
2 3 2
(FeOOH)的一种工艺流程如图。
已知:“还原”时,发生反应FeS +14Fe3++8H O=2 +15Fe2++16H+;FeS 与H SO 不反应。下列有关说法
2 2 2 2 4
不正确的是( )A.“酸溶”时适当提高硫酸浓度可加快反应速率
B.“还原”时氧化产物与还原产物质的物质的量之比为1∶7
C.“过滤I”所得滤液中存在的阳离子主要有Fe2+、Fe3+和H+
D.“沉降、氧化”时发生反应的离子方程式:4Fe2++8NH •H O+O =8NH +4FeOOH↓+2H O
3 2 2 2
4.C A.适当提高硫酸浓度,增大氢离子浓度,可增大反应速率,A正确;B.有关的离子方程式为
FeS +14Fe3++8H O=2 +15Fe2++16H+,反应中FeS 的Fe元素化合价不变,S元素化合价升高,则 为氧
2 2 2
化产物,Fe3+转化为Fe2+,化合价降低,Fe2+为还原产物,则“还原”时氧化产物与还原产物质的物质的量
之比为2∶14=1∶7,B正确;C.滤液中含有硫酸亚铁和过量的硫酸,且生成氢离子,则“过滤I”所得滤液中
存在的阳离子主要有Fe2+和H+,C错误;D.滤液中通入空气氧化,同时加入氨水调节pH生成FeOOH沉淀,
发生的离子方程式为4Fe2++8NH •H O+O =8NH +4FeOOH↓+2H O,D正确;故选C。
3 2 2 2
5.(2022·哈尔滨三中高三阶段练习)以高硫铝土矿(主要成分为Fe O 、Al O 、SiO ,少量FeS 和硫酸盐)
2 3 2 3 2 2
为原料制备聚合硫酸铁[Fe (OH)(SO )] 和明矾的部分工艺流程如下,下列说法错误的是( )
2 x 4 y n
已知:赤泥液的主要成分为Na CO 。
2 3
A.聚合硫酸铁可用于净化自来水,与其组成中的Fe3+具有氧化性有关
B.赤泥液的作用是吸收“焙烧”阶段中产生的SO
2
C.在“聚合”阶段,若增加Fe O 用量,会使[Fe (OH)(SO )] 中x变大
2 3 2 x 4 y n
D.从“滤液”到“明矾”的过程中还应有“除硅”步骤
5.A A.聚合硫酸铁可用于净水,原理是聚合硫酸铁中的Fe3+水解生成的Fe(OH) 胶体可吸附水中的悬浮物
3
和杂质,与Fe3+的氧化性无关,故A项错误;B.赤泥液主要成分是Na CO ,可吸收焙烧产生的SO ,故B项
2 3 2
正确;C.聚合硫酸铁中的OH-来源于Fe O ,因此增加Fe O 用量会使[Fe (OH)(SO )] 中x变大,故C项正确;
2 3 2 3 2 x 4 y n
D.制备明矾的滤液中含有 ,应预先除去,故D项正确。故答案选:A。
6.(2022·江苏南通·高三开学考试)用低品铜矿(主要含CuS、FeO)制备 的一种工艺流程如下:下列说法正确的是( )
A.“酸浸”过程中CuS发生反应的离子方程式为:
B.已知酸浸液中含 ,为检验是否含有 ,可先加入KSCN溶液,再加氯水观察现象
C.1个 晶胞(如图)中含4个氧原子
D.水合肼浓度过大, 产率下降,可能的原因是 进一步被还原成单质铜
6.D A.CuS是难溶物,“酸浸”过程中CuS发生反应的离子方程式为:
,故A错误;B.已知酸浸液中含 ,为检验是否含有 ,
可先加入KSCN溶液,再加氯水观察现象,都是一样的现象,应加入酸性高锰酸钾溶液,酸性高锰酸钾与
亚铁离子反应,看溶液是否褪色,故B错误;C. 晶胞中白球为2个,黑球为4个,因此1个 晶
胞中含2个氧原子,故C错误;D.水合肼浓度过大, 产率下降,由于氧化亚铜中铜为+1价,具有氧
化性,因此可能的原因是 与水合肼进一步被还原成单质铜,故D正确。综上所述,答案为D。
7.以低品位粉煤灰(主要成分为 ,还含有少量 杂质)为原料制备 的工艺流程如下,
下列说法错误的是( )A.“酸浸”时,适当增大盐酸浓度可提高金属离子的浸出速率
B.应选择蒸馏水对得到的 粗品进行洗涤
C.“母液”经一系列操作后可重新获得
D.与在HCl气流中蒸发结晶相比,盐析结晶对设备的要求较低
7.B A.酸浸时,适当增大盐酸浓度,可增大溶液中氢离子浓度,有利于提高金属离子的浸出速率,故A
正确;B.六水氯化铝晶体易溶于水,用蒸馏水洗涤会使晶体溶解造成产率降低,应选择浓盐酸或乙醇洗
涤,故B错误;C.由分析可知,母液的主要成分是氯化亚铁,经一系列操作后可重新获得四水氯化亚铁
晶体循环使用,故C正确;D.氯化亚铁溶液的酸性较弱,与盐酸相比,对设备腐蚀程度较小,且盐析结
晶在常温下进行,所以与在氯化氢气流中蒸发结晶相比,盐析结晶对设备的要求较低,故D正确;故选
B。
8.(2022·全国乙卷)废旧铅蓄电池的铅膏中主要含有 、 、 和Pb。还有少量Ba、Fe、Al
的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质
一定条件下,一些金属氢氧化物沉淀时的 如下表:
金属氢氧化物
开始沉淀的pH 2.3 6.8 3.5 7.2
完全沉淀的pH 3.2 8.3 4.6 9.1
回答下列问题:(1)在“脱硫”中 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择 的原因
________。
(2)在“脱硫”中,加入 不能使铅膏中 完全转化,原因是________。
(3)在“酸浸”中,除加入醋酸( ),还要加入 。
(ⅰ)能被 氧化的离子是________;
(ⅱ) 促进了金属Pb在醋酸中转化为 ,其化学方程式为________;
(ⅲ) 也能使 转化为 , 的作用是________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
8. (1) PbSO (s)+CO (aq)= PbCO (s)+SO (aq) 反应PbSO (s)+CO (aq)= PbCO (s)+SO (aq)的平衡常数K=
4 3 4 3
=3.4 105>105,PbSO 可以比较彻底的转化为PbCO
4 3
(2)反应BaSO (s)+CO (aq)= BaCO (s)+SO (aq)的平衡常数K= =0.04<<105,反应正向进行的程度有限
4 3
(3) Fe2+ Pb+H O +2HAc=Pb(Ac) +2H O 作还原剂
2 2 2 2
(4)Fe(OH) 、Al(OH)
3 3
(5)Ba2+、Na+
解析:(1)“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO (s)+CO
4
(aq)= PbCO (s)+SO (aq),由一些难溶电解质的溶度积常数的数据可知,K (PbCO )=7.4 10-14,
3 sp 3
K (PbSO )=2.5 10-8,反应PbSO (s)+CO (aq)= PbCO (s)+SO (aq)的平衡常数K= = =
sp 4 4 3= ≈3.4 105>105,说明可以转化的比较彻底,且转化后生成的碳酸铅可由酸浸进入溶
液中,减少铅的损失。
(2)反应BaSO (s)+CO (aq)= BaCO (s)+SO (aq)的平衡常数K= = = =
4 3
≈0.04<<105,说明该反应正向进行的程度有限,因此加入碳酸钠不能使铅膏中的BaSO 完全转化。
4
(3)(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac) ,过氧化氢与Pb、HAc发生氧还原反应生成Pb(Ac)
2 2
和H O,依据得失电子守恒和原子守恒可知,反应的化学方程式为:Pb+H O +2HAc=Pb(Ac) +2H O。
2 2 2 2 2
(iii)过氧化氢也能使PbO 转化为Pb(Ac) ,铅元素化合价由+4价降低到了+2价,PbO 是氧化剂,则过氧
2 2 2
化氢是还原剂。
(4)酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁。
(5)依据分析可知,加入碳酸钠不能使铅膏中的BaSO 完全转化,铁离子、铝离子转化为了氢氧化铁、氢氧
4
化铝沉淀,铅转化为了氢氧化铅、最终变为了氧化铅,因此沉铅的滤液中,金属离子有Ba2+和加入碳酸钠、
氢氧化钠时引入的Na+。
9.(2022·山东卷)工业上以氟磷灰石[ ,含 等杂质]为原料生产磷酸和石膏,工艺流程如
下:
回答下列问题:
(1)酸解时有 产生。氢氟酸与 反应生成二元强酸 ,离子方程式为_______。
(2)部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比 加入 脱氟,充分反应后, _______ ;再分批加入一定量的 ,首先转化为沉淀的离子是_______。
(3) 浓度(以 计)在一定范围时,石膏存在形式与温度、 浓度(以 计)的关系如图甲所示。
酸解后,在所得 、 为45的混合体系中,石膏存在形式为_______(填化学式);洗涤时使用一定
浓度的硫酸溶液而不使用水,原因是_______,回收利用洗涤液X的操作单元是_______;一定温度下,石
膏存在形式与溶液中 和 的关系如图乙所示,下列条件能实现酸解所得石膏结晶转化的是
_______(填标号)。
A. 、 、 B. 、 、
C. 、 、 D. 、 、
9.(1)6HF+SiO =2H++ +2H O
2 2
(2)
(3) CaSO •0.5H O 抑制CaSO 的溶解,提高产品石膏的产率 酸解 AD
4 2 4
解析:氟磷灰石用硫酸溶解后过滤,得到粗磷酸和滤渣,滤渣经洗涤后结晶转化为石膏;粗磷酸以精制I脱氟、除硫酸根离子和 ,过滤,滤液经精制II等一系列操作得到磷酸。
(1)氢氟酸与SiO 反应生成二元强酸H SiF ,该反应的离子方程式为6HF+SiO =2H++ +2H O。
2 2 6 2 2
(2)精制1中,按物质的量之比n(Na CO ):n( )= 1:1加入Na CO 脱氟,该反应的化学方程式为H SiF +
2 3 2 3 2 6
Na CO = Na SiF ↓+CO ↑+ H O,充分反应后得到沉淀Na SiF ,溶液中有饱和的Na SiF ,且c(Na+)=2c(
2 3 2 6 2 2 2 6 2 6
),根据Na SiF 的溶度积可知Ksp= c2(Na+)• c( )=4c3( ),c( ) = mol•L-1,因
2 6
此c(Na+)=2c( )= mol•L-1;同时,粗磷酸中还有硫酸钙的饱和溶液,c(Ca2+)=c( )=
mol•L-1;分批加入一定量的BaCO ,当BaSiF 沉淀开始生成时,c(Ba2+)=
3 6
mol•L-1,当BaSO 沉淀开始生成时,c(Ba2+)= mol•L-1,因此,首先
4
转化为沉淀的离子是 ,然后才是 。
(3)根据图中的坐标信息,酸解后,在所得100℃、P O %为45的混合体系中,石膏存在形式为
2 5
CaSO •0.5H O;CaSO 在硫酸中的溶解度小于在水中的,因此,洗涤时使用一定浓度的硫酸溶液而不使用水
4 2 4
的原因是:减少CaSO 的溶解损失,提高产品石膏的产率;洗涤液X中含有硫酸,其具有回收利用的价值,
4
由于酸解时使用的也是硫酸,因此,回收利用洗涤液X的操作单元是:酸解。由图甲信息可知,温度越低,
越有利于实现酸解所得石膏结晶的转化,由图乙信息可知,体系温度为65℃时,位于65℃线上方的晶体全
部以CaSO •0.5H O形式存在,位于65℃线下方的晶体全部以CaSO •2H O。体系温度为80℃时,位于80℃
4 2 4 2
线下方的晶体全部以CaSO •2H O形式存在,位于80℃线上方的晶体全部以CaSO •0.5H O形式存在,据此
4 2 4 2
分析:
A. P O %= l5、SO %= 15,由图乙信息可知,该点坐标位于65℃线以下,晶体以CaSO •2H O形式存在,
2 5 3 4 2
可以实现石膏晶体的转化,A符合题意;
B. P O %= 10、SO %= 20,由图乙信息可知,该点坐标位于80℃线的上方,晶体全部以CaSO •0.5H O形
2 5 3 4 2式存在,故不能实现晶体的转化, B不符合题意;
C.P O %= 10、SO %= 30,由图乙信息可知,该点坐标位于65℃线上方,晶体全部以CaSO •0.5H O形式存
2 5 3 4 2
在,故不能实现晶体转化, C不符合题意;
D. P O %=10、SO %= 10,由图乙信息可知,该点坐标位于80℃线下方,晶体全部以CaSO •2H O形式存
2 5 3 4 2
在,故能实现晶体的完全转化,D符合题意;
综上所述,能实现酸解所得石膏结晶转化的是AD。
10.(2022·河北衡水高三模拟)以黄铁矿为原料制硫酸会产生大量的废渣,合理利用废渣可以减少环境污
染,变废为宝。工业上利用废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备高档颜料铁红(Fe O )和回收
2 3
(NH ) SO ,具体生产流程如图:
4 2 4
(1)在废渣溶解操作时,应选用___溶解(填字母)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2)为了提高废渣的浸取率,可采用的措施有哪些?___(至少写出两点)。
(3)物质A是一种氧化剂,工业上最好选用___(供选择使用的有:空气、Cl 、MnO )。氧化过程中发生反
2 2
应的离子方程式为___。
(4)根据如图有关数据,你认为工业上氧化操作时应控制的条件(从温度、pH和氧化时间三方面说明)是:
___。
(5)铵黄铁矾的化学式可表示为(NH )Fe(SO )(OH) ,其化学式可通过下列实验测定:
4 x y 4 z w
①称取一定质量的样品加入稀硝酸充分溶解,将所得溶液转移至容量瓶并配制成100.00mL溶液A。
②量取25.00mL溶液A,加入盐酸酸化的BaCl 溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体
2
9.32g。③量取25.00mL溶液A,加入足量NaOH溶液,加热,收集到标准状况下气体448mL,同时有红褐色沉淀生
成。
④将步骤③所得沉淀过滤、洗涤、灼烧,最终得固体4.80g。
通过计算,可确定铵黄铁矾的化学式为___。(已知铵黄铁矾的摩尔质量为960g•mol-1,计算过程中不考虑
固体损失和气体溶解。)
10.(1)D
(2)将废渣粉碎、加热、搅拌等
(3)空气 4Fe2++O +4H+=4Fe3++2H O
2 2
(4)溶液温度控制在80℃,pH控制在1.5,氧化时间4-6之间
(5)(NH ) Fe (SO ) (OH)
4 2 6 4 4 12
解析:(1)结合流程可知,废渣中含有Fe2+、Fe3+的硫酸盐及少量CaO和MgO,故废渣溶解操作时,应选
用硫酸溶解比较合适。
(2)为了提高废渣的浸取率,可以将废渣进一步粉碎,以增大固体的表面积提高反应速率,还可以采用
加热、搅拌等方法。
(3)废渣溶解后,加入氧化剂将Fe2+氧化为Fe3+,提供的三种氧化剂中只有空气(O )是绿色氧化剂;反应
2
化学方程式为:4Fe2++O +4H+=4Fe3++2H O。
2 2
(4)由三条曲线可得,相同时间内,80℃、pH=1.5时,Fe2+的转化率最高,故应选该条件,浸取4小时之
后再延长时间转化率提高不大,故浸取4小时较合适,综上分析,工业上氧化操作时应控制的条件是:溶
液温度控制在80℃,pH控制在1.5,氧化时间为4h左右。
( 5 ) 由 ② 得 , n(SO )=n(BaSO )=0.04mol ; 由 ③ 得 , n(NH )=n(NH )=0.02mol ; 由 ④ 得 ,
4 3
n(Fe)=2n(Fe O )=0.06mol;所以,结合(NH )Fe(SO )(OH) ,可设为(NH )Fe (SO ) (OH) ,由正负化合价代数
2 3 4 x y 4 z w 4 x 3x 4 2x w
和为0得:w=6x,又因为(NH )Fe(SO )(OH) 的摩尔质量为960g•mol-1,其化学式为:(NH ) Fe (SO ) (OH)
4 x y 4 z w 4 2 6 4 4 12
11.(2022·潍坊高三期中)钒有“工业维生素”之称。我国是世界上主要的钒相关产品出口国。一种以钒
矿粉(含+3、+4、+5价钒,同时还含有SiO 、Fe O 、铝硅酸盐等)为原料制备NH VO 的工艺流程如图。
2 3 4 4 3
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+开始沉淀pH 1.9 7.0 3.0 8.1
完全沉淀pH 3.2 9.0 4.7 10.1
已知:Al(OH) 在pH>12时溶解。回答下列问题:
3
(1)NH VO 中V的化合价为_______价;“酸浸氧化”时,可以提高反应速率的方法有很多,请写出其中
4 3
两点:_______、_______。
(2)“酸浸氧化”中,VO+和VO2+被氧化成VO 。VO2+转化为VO 反应的离子方程式为_______。
(3)“中和沉淀”中加入的NaOH溶液与过量H SO 发生的反应为_______(填“吸热”或“放热”)反应。
2 4
从“中和沉淀”的条件看,“滤渣②”中除了含有V O ·xH O外,还含有的物质的化学式为_______。
2 5 2
(4)“沉淀转溶”时将V O ·xH O转化为钒酸盐,该反应的离子方程式为_______,同时溶解的还有
2 5 2
_______(填化学式)。
(5)“沉钒”时,加入的NH Cl应过量,其原因是_______;检验“滤液⑤”中金属阳离子的方法是
4
_______。
11.(1)+5 适当升高温度 搅拌
(2)2VO2++MnO =2VO +Mn2+
2
(3)放热 Fe(OH) 、Al(OH)
3 3
(4)V O ·xH O+2OH-=2VO +(1+x)H O Al(OH)
2 5 2 2 3
(5)使NH VO 充分析出 焰色试验
4 3
解析:(1)根据化合物中元素化合价代数和为0计算可知NH VO 中V的化合价为+5价;提高温度,搅拌,
4 3
可以提高“酸浸氧化”时的反应速率;答案为:+5;适当升高温度;搅拌;
(2)“酸浸氧化”中,二氧化锰做氧化剂,可以将VO+、VO2+氧化成VO ,氧化VO2+的离子方程式为
2VO2++MnO =2VO +Mn2+,答案为:2VO2++MnO =2VO +Mn2+;
2 2
(3)酸碱中和反应是放热反应;通过表格信息可知三价铁离子在pH=3.2时已经完全沉淀,铝离子在
pH=3.0时开始沉淀,所以 “滤渣②”中除了含有V O ·xH O外,还含有Fe(OH) 、Al(OH) ,答案为:放热;
2 5 2 3 3
Fe(OH) 、Al(OH) ;
3 3(4)“沉淀转溶”时将V O ·xH O转化为钒酸盐,反应的离子方程式为V O ·xH O+2OH-=2VO +(1+x)H O;
2 5 2 2 5 2 2
Al(OH) 在强碱性环境下也可以溶解,所以同时溶解的还有Al(OH) ;答案为:V O ·xH O+2OH-=2VO
3 3 2 5 2
+(1+x)H O;Al(OH) ;
2 3
(5)“沉钒”时,加入的NH Cl应过量,可以利用同离子效应使NH VO 充分析出;“滤液⑤”中金属阳
4 4 3
离子为钠离子,可以采用焰色试验进行检验;答案为:使NH VO 充分析出;焰色试验。
4 3
12.(2022·全国·高三专题练习)三氧化二(Co O )主要用作颜料、釉料、磁性材料,催化剂和氧化剂等。
2 3
以含钴废料(主要成分为Co O ,含有少量MnO ,NiO、Fe O )为原料制备Co O 的流程如图所示:
2 3 2 3 4 2 3
已知:
Ⅰ.“酸浸”后的浸出液中含的阳离子有H+、Co2+、Fe3+、Ni2+。
Ⅱ.部分阳离子以氢氧化物形式完全沉淀时溶液的pH如表:
沉淀物 Fe(OH) Co(OH) Ni(OH)
3 2 2
完全沉淀时的pH 3.7 9.0 9.2
回答下列问题:
(1)“滤渣1”的化学式为__,“酸浸”时Co O 发生的反应的化学方程式是__。
2 3
(2)“酸浸”时加入H O 的目的是__。生产过程中发现实际消耗双氧水的量大于理论值,可能的原因是__。
2 2
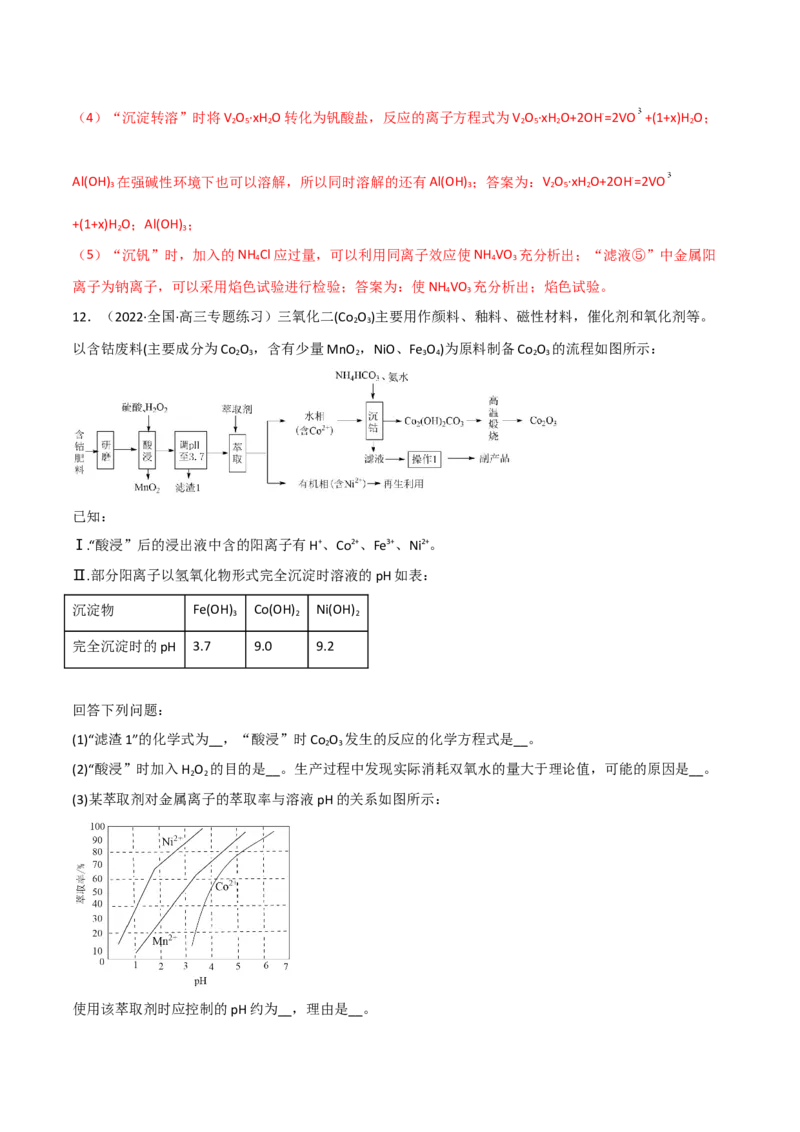
(3)某萃取剂对金属离子的萃取率与溶液pH的关系如图所示:
使用该萃取剂时应控制的pH约为__,理由是__。(4)“操作1”所得副产品的一种用途为__。已知该物质的溶液加热到100℃时会变质,该物质的溶解度见表:
温度/℃ 0 10 20 30 40 50 60
溶解
70.6 73.0 75.4 78.0 81.0 84.5 88.0
度/g
操作1是__(填字母)。
A.蒸发结晶 B.降温结晶 C.减压蒸发结晶
(5)“沉钴”时发生反应的离子方程式为__。
(6)有机相提取的Ni2+再生时可用于制备氢电池,该电池充电时的总反应为Ni(OH) +M=NiOOH+MH。则放电
2
时负极的电极反应式为__。
12.(1)
(2) 将+3价的钴还原为 ,将 氧化为 ,便于后续调节pH后除去 酸浸反应放热,使
双氧水分解;废料中的 或生成的 催化双氧水分解
(3) 2.5~3.3 萃取剂在该pH时对 、 萃取率差别大,能分离 、 两种离子
(4) 做氮肥 c
(5)
(6)
解析:(1)由已知I可知,酸浸后浸出液中含有的阳离子为 、 、 、 ,再由已知II可知,
当调节pH至3.7时, 会先以沉淀的形式析出,所以“滤渣1”的化学式为 ;酸浸时
在酸性条件下与 发生氧化还原反应生成 、氧气和水,依据得失电子守恒、质量守恒,化学方程
式为: 。
(2)由分析可知,加入过氧化氢的目的是酸性条件下,氧化钴与过氧化氢发生氧化还原反应生成 ,四氧化三铁中的 与过氧化氢发生氧化还原反应生成 ;过氧化氢的稳定性差,酸浸时,反应放热,
放出的热量能使过氧化氢分解,同时,废料中的二氧化锰或溶液中的 也可以做过氧化氢分解的催化剂,
加快过氧化氢的分解,导致实际消耗的过氧化氢的量大于理论值。
(3)使用该萃取剂萃取 ,单纯从萃取率考虑,萃取率越高越好,但同时还要考虑到 尽可能的不
被萃取,两方面综合考虑,pH应控制在2.5~3.3;因为萃取剂在该pH时对 、 萃取率差别大,能分
离 、 两种离子。
(4)整个过程中加入的物质有:硫酸、过氧化氢、氨水和碳酸氢铵,过氧化氢和碳酸氢根在反应过程中
反应完全,依据质量守恒,溶液中还有的物质为硫酸铵,可用作氮肥;从溶解度角度看,硫酸铵的溶解度
随温度升高有所增大,但变化量不大,且硫酸铵受热易分解,因此操作1应采取减压蒸发结晶,选c。
(5)沉钴时发生的反应为向水相中加入氨水和碳酸氢铵溶液,亚钴离子转化为 沉淀,钴元素
化合价不变,因此发生非氧化还原反应,离子方程式为: 。
(6)由电池充电时的总反应可知,放电时负极为MH,失电子化合价升高,发生氧化反应生成M,因此放
电时负极电极反应式为: 。