文档内容
高频考点 15 氯气及其化合物
题点(一)氯气及其化合物的性质
1.(2022·北京卷)已知: 。下列说法不正确的是 ( )
A. 分子的共价键是 键, 分子的共价键是 键
B.燃烧生成的 气体与空气中的水蒸气结合呈雾状
C.停止反应后,用蘸有浓氨水的玻璃棒靠近集气瓶口产生白烟
D.可通过原电池将 与 反应的化学能转化为电能
1.A A.H 分子里的共价键H-H键是由两个s电子重叠形成的,称为s-s σ键,Cl 分子里的共价键Cl-Cl键
2 2
是由两个p电子重叠形成的,称为p-p σ键,故A错误;
B.HCl气体极易溶于水,遇到空气中的水蒸气后立即形成盐酸小液滴,即白雾,故B正确;C.浓氨水易
挥发,挥发的氨气和HCl气体互相反应,化学方程式NH +HCl=NH Cl,生成NH Cl氯化铵固体小颗粒,固体
3 4 4
粉末就是烟,故C正确;D. 与 的反应是能够自发进行的氧化还原反应,可通过原电池将 与
反应的化学能转化为电能,故D正确;故选A。
2.(2021·河北卷)关于非金属含氧酸及其盐的性质,下列说法正确的是( )
A.浓H SO 具有强吸水性,能吸收糖类化合物中的水分并使其炭化
2 4
B.NaClO、KClO 等氯的含氧酸盐的氧化性会随溶液的pH减小而增强
3
C.加热NaI与浓H PO 混合物可制备HI,说明H PO 比HI酸性强
3 4 3 4
D.浓HNO 和稀HNO 与Cu反应的还原产物分别为NO 和NO,故稀HNO 氧化性更强
3 3 2 3
2.B A.浓硫酸能使蔗糖炭化,体现的是其脱水性,而不是吸水性,A错误;B.NaClO在水溶液中会发生水解,离子方程式为: ,pH减小,则酸性增强,会促使平衡向正反应方向
移动,生成氧化性更强的HClO, 在酸性条件下可生成具有强氧化性的氯气、二氧化氯等气体,增强
氧化能力,B正确;C.HI的沸点低,易挥发加热 与浓 混合物发生反应生成 利用的是高沸点
酸制备低沸点酸的原理,C错误;D.相同条件下根据铜与浓硝酸、稀硝酸反应的剧烈程度可知,浓硝酸的
氧化性大于稀硝酸的氧化性,D错误;故选B。
3.(2022·全国·高三专题练习)在Cl 与金属、非金属的反应中,下列说法正确的是( )
2
A.与金属反应时一定表现氧化性 B.与非金属反应时表现还原性
C.与金属反应时表现酸性 D.在与非金属的化合物中均表现负价
3.A A.氯气与金属反应生成氯化物时氯的化合价降低,均表现氧化性,选项A正确;B.氯气与非金属
反应时也大多表现氧化性,如生成氯化氢等,选项B错误;C.氯气与金属反应时均表现氧化性,而不是
酸性,选项C错误;D.氯气在与非金属的化合物中也可显正价,如在ClO 中氯元素表现+4价,选项D错
2
误;答案选A。
4. 某实验小组利用下图装置进行实验。下列说法不正确的是( )
A.滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔
B.蘸有淀粉KI溶液的棉花变蓝,说明氯气的氧化性强于碘
C.蘸有品红溶液的棉花褪色,说明氯气具有漂白性
D.蘸有紫色石蕊溶液的棉花上出现的现象是棉花先变红后褪色
4.C A.滴加浓盐酸时需将分液漏斗上端玻璃塞上的凹槽对准漏斗上的小孔,A正确;
B.蘸有淀粉KI溶液的棉花变蓝,说明Cl 与KI溶液发生了反应:Cl +2KI=2KCl+I ,I2遇淀粉溶液变为蓝色。
2 2 2
在该反应中Cl 为氧化剂,I 为氧化产物,所以氯气的氧化性强于碘,B正确;C.氯气本身没有漂白性,氯
2 2
气与水反应生成的次氯酸具有漂白性,能够使品红溶液褪色,C错误;D.浓盐酸与KMnO 溶液反应产生
4Cl ,Cl 溶于蘸有紫色石蕊溶液中,反应产生HCl、HClO,酸使紫色石蕊试液变为红色,HClO同时具有强氧
2 2
化性,又将红色物质氧化变为无色,因此看到蘸有紫色石蕊溶液的棉花上出现的现象是先变红后褪色,D
正确;故合理选项是C。
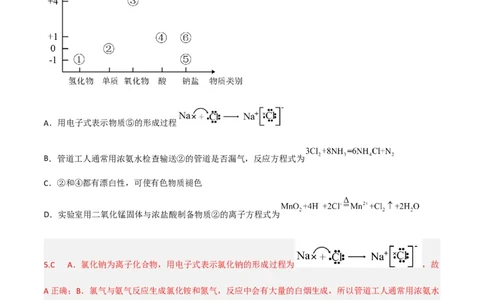
5.部分含氯物质的分类与相应氯元素的化合价的关系如图所示。下列说法不正确的是( )
A.用电子式表示物质⑤的形成过程
B.管道工人通常用浓氨水检查输送②的管道是否漏气,反应方程式为
C.②和④都有漂白性,可使有色物质褪色
D.实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式为
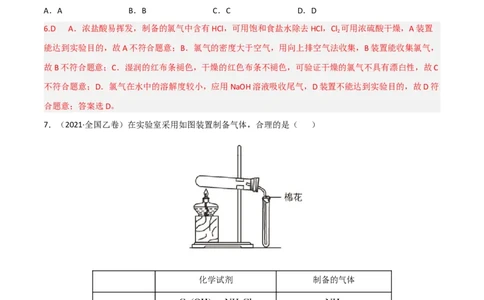
5.C A.氯化钠为离子化合物,用电子式表示氯化钠的形成过程为 ,故
A正确;B.氯气与氨气反应生成氯化铵和氮气,反应中会有大量的白烟生成,所以管道工人通常用浓氨水
检查输送氯气的管道是否漏气,反应的化学方程式为 ,故B正确;C.氯气没有漂
白性,不能使干燥的有色物质褪色,故C错误;D.实验室用二氧化锰固体与浓盐酸制备物质氯气的反应
为,二氧化锰与浓盐酸共热反应生成氯化锰、氯气和水,反应的离子方程式为
,故D正确;故选C。题点(二)氯气的实验室制法
6.(2022·广东卷)实验室用 和浓盐酸反应生成 后,按照净化、收集、性质检验及尾气处理的顺
序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
A.A B.B C.C D.D
6.D A.浓盐酸易挥发,制备的氯气中含有HCl,可用饱和食盐水除去HCl,Cl 可用浓硫酸干燥,A装置
2
能达到实验目的,故A不符合题意;B.氯气的密度大于空气,用向上排空气法收集,B装置能收集氯气,
故B不符合题意;C.湿润的红布条褪色,干燥的红色布条不褪色,可验证干燥的氯气不具有漂白性,故C
不符合题意;D.氯气在水中的溶解度较小,应用NaOH溶液吸收尾气,D装置不能达到实验目的,故D符
合题意;答案选D。
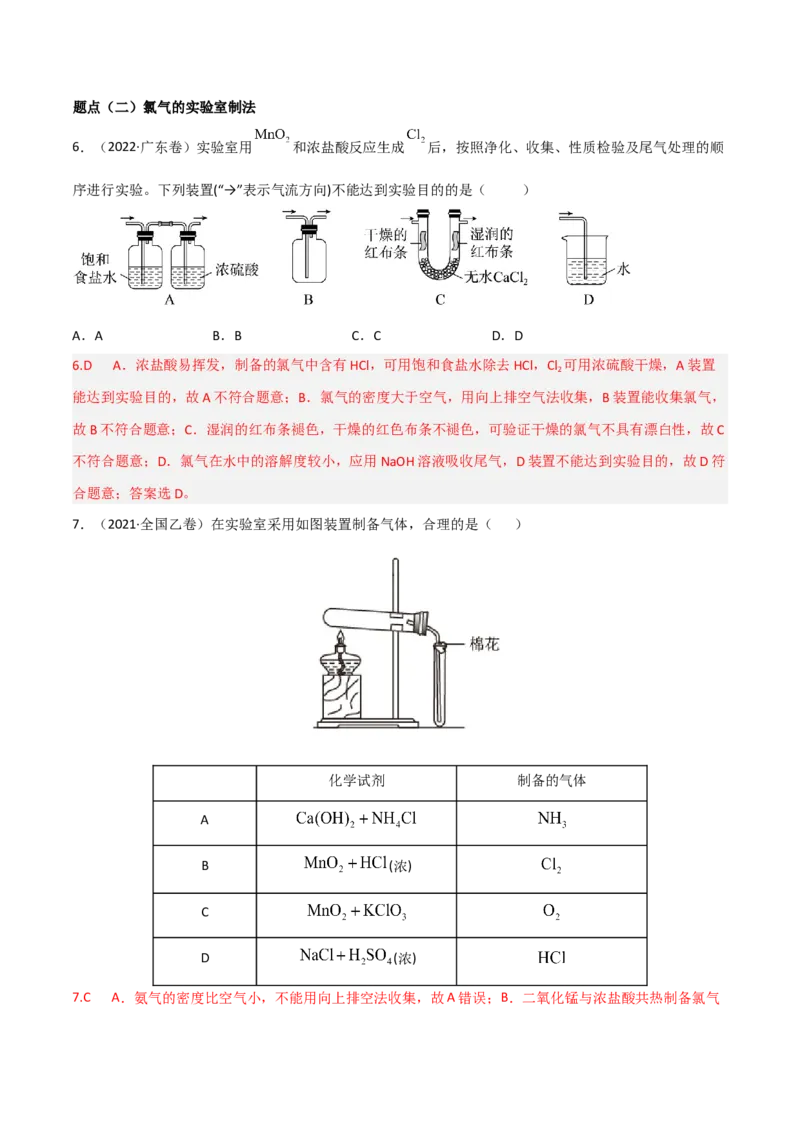
7.(2021·全国乙卷)在实验室采用如图装置制备气体,合理的是( )
化学试剂 制备的气体
A
B (浓)
C
D (浓)
7.C A.氨气的密度比空气小,不能用向上排空法收集,故A错误;B.二氧化锰与浓盐酸共热制备氯气为固液加热反应,需要选用固液加热装置,不能选用固固加热装置,故B错误;C.二氧化锰和氯酸钾共
热制备氧气为固固加热的反应,能选用固固加热装置,氧气的密度大于空气,可选用向上排空气法收集,
故C正确;D.氯化钠与浓硫酸共热制备为固液加热反应,需要选用固液加热装置,不能选用固固加热装
置,故D错误;故选C。
8.(2022·烟台市第一中学一模)1971年,John.J.Bishop等通过3Mg2++4ClO-+2Cl-
+2H O=Mg(ClO) ·2Mg(OH) +2Cl ↑反应制得Mg(ClO) ·2Mg(OH) (BMHs,微溶于水),而1921年,
2 2 2 2 2 2
Georg.Kereszty等将Cl 通入Mg(OH) 悬浊液进行制备BMHs却宣告失败。用下列装置制取BMHs,相关叙述
2 2
错误的是()
A.向装置a烧瓶中滴入浓盐酸之前,应打开K
B.装置b的广口瓶盛放的是饱和食盐水
C.开始时,不断搅拌下先向三口烧瓶中加入MgCl 溶液,然后通入Cl
2 2
D.从反应完成后的三口烧瓶中分离得到BMHs,需经过过滤、洗涤及干燥等操作
8.C A.打开K可使浓盐酸顺利滴入烧瓶并使气体进入后续装置,A正确;B.浓盐酸具有挥发性,得到
氯气中含有氯化氢杂质,用饱和食盐水除去氯气中的氯化氢,B正确;C.先加入 会生成
悬浊液,由题给信息, 难以与 反应,几乎得不到 ,C错误; D.由于 微溶于水,
先过滤,再经洗涤和干燥得到产品,D正确;故选C。
9.(2021·广东卷)含氯物质在生产生活中有重要作用。1774年,舍勒在研究软锰矿(主要成分是 )的
过程中,将它与浓盐酸混合加热,产生了一种黄绿色气体。1810年,戴维确认这是一种新元素组成的单质,
并命名为chlorine(中文命名“氯气”)。
(1)实验室沿用舍勒的方法制取 的化学方程式为_______。(2)实验室制取干燥 时,净化与收集 所需装置的接口连接顺序为_______。
(3) 某氯水久置后不能使品红溶液褪色,可推测氯水中_______已分解。检验此久置氯水中 存在的操作
及现象是_______。
9.(1) MnO +4HCl(浓) MnCl +Cl ↑+2H O (2) c-d-b-a-e (3) HClO 取少量溶液于试管中,
2 2 2 2
加入过量稀硝酸,防止溶液中含有C 、HC 等,再加入少量AgNO 溶液,若有白色沉淀生成,则证明
3
原溶液中含有Cl-
解析:(1)实验室通常采用浓盐酸和MnO 制取 ,化学方程式为:MnO +4HCl(浓) MnCl +Cl ↑+2H O,故
2 2 2 2 2
答案为:MnO +4HCl(浓) MnCl +Cl ↑+2H O;
2 2 2 2
(2)根据化学方程式可知,制取的氯气中混有氯化氢、水蒸气,氯气有毒,必须进行尾气处理,因此使用饱
和食盐水吸收氯化氢气体,浓硫酸除去水蒸气,最后用NaOH溶液吸收尾气,因此接口连接顺序为c-d-b-a-
e,故答案为:c-d-b-a-e;
(3)久置后不能使品红溶液褪色,说明HClO已分解;检验 的方法:取少量溶液于试管中,加入过量稀硝
酸,防止溶液中含有C 、HC 等,再加入少量AgNO 溶液,若有白色沉淀生成,则证明原溶液中含有
3
Cl-,故答案为:HClO;向溶液中加入过量稀硝酸,防止溶液中含有C 、HC 等,再加入少量AgNO 溶
3液,若有白色沉淀生成,则证明原溶液中含有Cl-;
10. (2021·山东卷)六氯化钨(WCl )可用作有机合成催化剂,熔点为283℃,沸点为340℃,易溶于CS ,
6 2
极易水解。实验室中,先将三氧化钨(WO )还原为金属钨(W)再制备WCl ,装置如图所示(夹持装置略)。回
3 6
答下列问题:
(1)检查装置气密性并加入WO 。先通N ,其目的是___;一段时间后,加热管式炉,改通H ,对B处逸出
3 2 2
的H 进行后续处理。仪器A的名称为___,证明WO 已被完全还原的现象是___。
2 3
(2)WO 完全还原后,进行的操作为:①冷却,停止通H ;②以干燥的接收装置替换E;③在B处加装盛有
3 2
碱石灰的干燥管;④……;⑤加热,通Cl ;⑥……。碱石灰的作用是___;操作④是___,目的是___。
2
10.(1) 排除装置中的空气 直形冷凝管 不再有水凝结 吸收多余氯气,防止
污染空气;防止空气中的水蒸气进入E (2) 再次通入N 排除装置中的H
2 2
解析:(1)用H 还原WO 制备W,装置中不能有空气,所以先通N ,其目的是排除装置中的空气;由仪器
2 3 2
构造可知仪器A的名称为直形冷凝管;当WO 被完全还原后,不再有水生成,则可观察到的现象为锥形瓶
3
中不再有液滴滴下,即不再有水凝结。故答案为:不再有水凝结;
(2) 由信息可知WCl 极易水解,W与Cl 反应制取WCl 时,要在B处加装盛有碱石灰的干燥管,防止空气
6 2 6
中的水蒸气进入E中,所以碱石灰的作用其一是吸收多余氯气,防止污染空气;其二是防止空气中的水蒸
气进入E;在操作⑤加热,通Cl 之前,装置中有多余的H ,需要除去,所以操作④是再次通入N ,目的是
2 2 2
排除装置中的H ,故答案为:吸收多余氯气,防止污染空气;防止空气中的水蒸气进入E;再次通入N ;
2 2
排除装置中的H ;
2