文档内容
高频考点 16 卤族元素
题点(一)卤族元素及化合物的性质
1.(2021·浙江卷)下列说法不正确的是( )
A.应避免铵态氮肥与草木灰混合施用
B.工业上可用离子交换法提高海带中碘的提取率
C.电解饱和食盐水可以得到金属钠和氯气
D.将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢
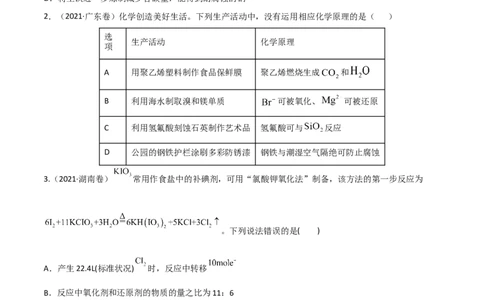
2.(2021·广东卷)化学创造美好生活。下列生产活动中,没有运用相应化学原理的是( )
选
生产活动 化学原理
项
A 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成 和
B 利用海水制取溴和镁单质 可被氧化、 可被还原
C 利用氢氟酸刻蚀石英制作艺术品 氢氟酸可与 反应
D 公园的钢铁护栏涂刷多彩防锈漆 钢铁与潮湿空气隔绝可防止腐蚀
3.(2021·湖南卷) 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
。下列说法错误的是( )
A.产生22.4L(标准状况) 时,反应中转移
B.反应中氧化剂和还原剂的物质的量之比为11:6
C.可用石灰乳吸收反应产生的 制备漂白粉
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在
4.(2022·黑龙江·哈师大附中高三期末)实验室保存下列药品的方法,正确的是( )
A.氢氟酸贮存在细口玻璃瓶里
B.盛液溴的试剂瓶里加一些水来防止溴挥发
C.氯水保存在无色玻璃瓶中,液氯贮存在钢瓶里D.盛放浓硫酸的广口瓶应当用磨口玻璃塞,不能用橡皮塞
5.(2022·全国·高三专题练习)下列说法正确的是( )
A.FeSO 、Fe(OH) 都可以通过化合反应制得
4 3
B.往海带灰的浸泡液中加入过量的氯水,保证I-完全氧化为I
2
C.氨气、溴中毒时,要立即到室外呼吸新鲜空气,必要时进行人工呼吸
D.AgBr见光易分解,故可用于人工降雨
6.碘在地壳中主要以 的形式存在,在海水中主要以 的形式存在,几种粒子之间的转化关系如图所
示。下列说法不正确的是( )
A.用淀粉-KI试纸和食醋检验加碘盐时淀粉-KI试纸会变蓝
B.足量Cl 能使湿润的、已变蓝的淀粉-KI试纸褪色的原因可能
2
C.途径Ⅱ中若生成1mol ,则反应中转移10mol电子
D.由题图可知氧化性的强弱顺序为
题点(二)溴和碘的提取实验
7.(2022·河北卷) 溶液可作为替代氟利昂的绿色制冷剂。合成 工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的 用 溶液吸收,吸收液直接返回还原工序
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为
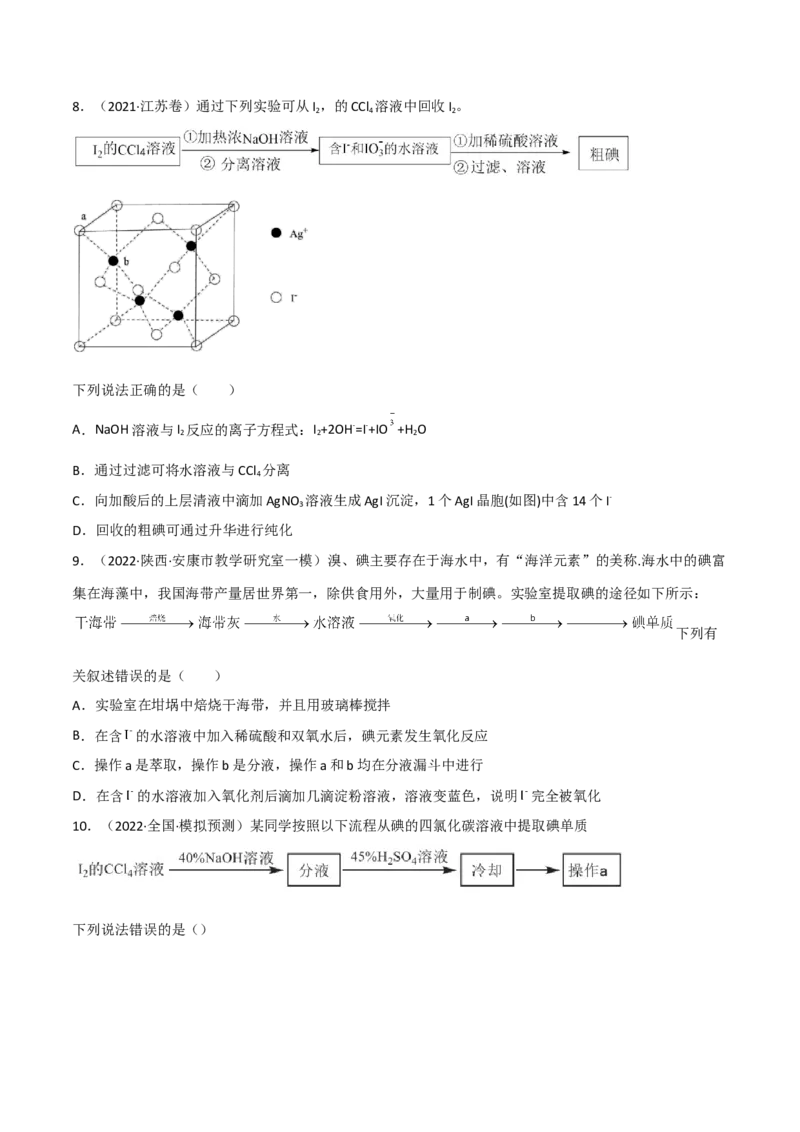
D.参与反应的 为1∶1∶18.(2021·江苏卷)通过下列实验可从I ,的CCl 溶液中回收I 。
2 4 2
下列说法正确的是( )
A.NaOH溶液与I 反应的离子方程式:I +2OH-=I-+IO +H O
2 2 2
B.通过过滤可将水溶液与CCl 分离
4
C.向加酸后的上层清液中滴加AgNO 溶液生成AgI沉淀,1个AgI晶胞(如图)中含14个I-
3
D.回收的粗碘可通过升华进行纯化
9.(2022·陕西·安康市教学研究室一模)溴、碘主要存在于海水中,有“海洋元素”的美称.海水中的碘富
集在海藻中,我国海带产量居世界第一,除供食用外,大量用于制碘。实验室提取碘的途径如下所示:
下列有
关叙述错误的是( )
A.实验室在坩埚中焙烧干海带,并且用玻璃棒搅拌
B.在含 的水溶液中加入稀硫酸和双氧水后,碘元素发生氧化反应
C.操作a是萃取,操作b是分液,操作a和b均在分液漏斗中进行
D.在含 的水溶液加入氧化剂后滴加几滴淀粉溶液,溶液变蓝色,说明 完全被氧化
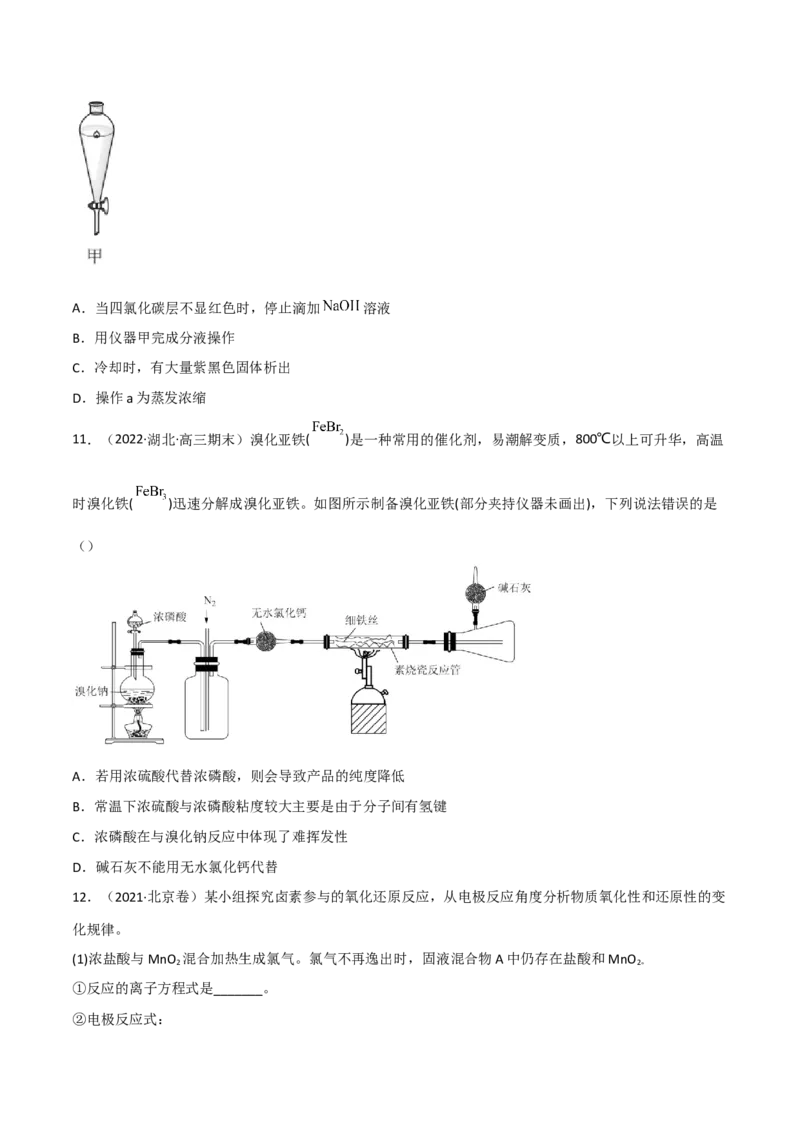
10.(2022·全国·模拟预测)某同学按照以下流程从碘的四氯化碳溶液中提取碘单质
下列说法错误的是()A.当四氯化碳层不显红色时,停止滴加 溶液
B.用仪器甲完成分液操作
C.冷却时,有大量紫黑色固体析出
D.操作a为蒸发浓缩
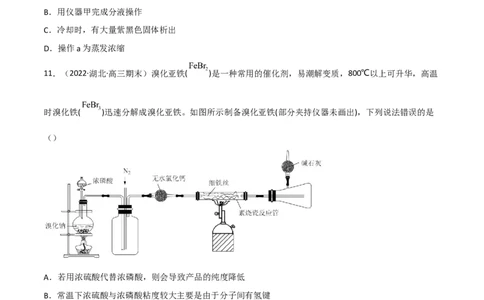
11.(2022·湖北·高三期末)溴化亚铁( )是一种常用的催化剂,易潮解变质,800℃以上可升华,高温
时溴化铁( )迅速分解成溴化亚铁。如图所示制备溴化亚铁(部分夹持仪器未画出),下列说法错误的是
()
A.若用浓硫酸代替浓磷酸,则会导致产品的纯度降低
B.常温下浓硫酸与浓磷酸粘度较大主要是由于分子间有氢键
C.浓磷酸在与溴化钠反应中体现了难挥发性
D.碱石灰不能用无水氯化钙代替
12.(2021·北京卷)某小组探究卤素参与的氧化还原反应,从电极反应角度分析物质氧化性和还原性的变
化规律。
(1)浓盐酸与MnO 混合加热生成氯气。氯气不再逸出时,固液混合物A中仍存在盐酸和MnO
2 2。
①反应的离子方程式是_______。
②电极反应式:i.还原反应:MnO +2e-+4H+=Mn2++2H O
2 2
ii.氧化反应:_______。
③根据电极反应式,分析A中仍存在盐酸和MnO 的原因。
2
i.随c(H+)降低或c(Mn2+)浓度升高,MnO 氧化性减弱。
2
ii.随c(Cl-)降低,_______。
④补充实验证实了③中的分析。
实验操作 试剂 产物
I 较浓H SO 有氯气
2 4
II a 有氯气
III a+b 无氯气
a是_______,b是_______。
(2)利用c(H+)浓度对MnO 氧化性的影响,探究卤素离子的还原性。相同浓度的KCl、KBr和KI溶液,能与
2
MnO 反应所需的最低c(H+)由大到小的顺序是_______,从原子结构角度说明理由______________。
2
(3)根据(1)中结论推测:酸性条件下,加入某种化合物可以提高溴的氧化性,将Mn2+氧化为MnO 。经实验
2
证实了推测,该化合物是_______。
(4)Ag分别与1mol·L1的盐酸、氢溴酸和氢碘酸混合,Ag只与氢碘酸发生置换反应,试解释原因:_______。
(5)总结:物质氧化性和还原性变化的一般规律是_______。