文档内容
高频考点 27 化学平衡移动原理
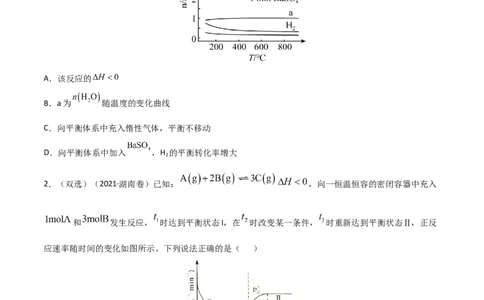
1.(2022·广东卷)恒容密闭容器中, 在不同温度下达平衡时,
各组分的物质的量(n)如图所示。下列说法正确的是( )
A.该反应的
B.a为 随温度的变化曲线
C.向平衡体系中充入惰性气体,平衡不移动
D.向平衡体系中加入 ,H 的平衡转化率增大
2
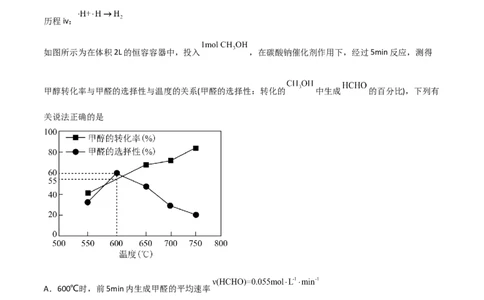
2.(双选)(2021·湖南卷)已知: ,向一恒温恒容的密闭容器中充入
和 发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态Ⅱ,正反
应速率随时间的变化如图所示。下列说法正确的是( )
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件:向容器中加入CC.平衡时A的体积分数 :
D.平衡常数K:
3.(2021·辽宁卷)某温度下,在恒容密闭容器中加入一定量X,发生反应 ,一段时间
后达到平衡。下列说法错误的是( )
A.升高温度,若 增大,则
B.加入一定量Z,达新平衡后 减小
C.加入等物质的量的Y和Z,达新平衡后 增大
D.加入一定量氩气,平衡不移动
4.CH 与CO 重整生成H 和CO的过程中主要发生下列反应
4 2 2
CH (g)+CO (g)=2H (g)+2CO(g) ΔH=247.1 kJ·mol-1
4 2 2
H (g)+CO (g)=H O(g)+CO(g) ΔH=41.2 kJ·mol-1
2 2 2
在恒压、反应物起始物质的量比n(CH )∶n(CO )=1∶1条件下,CH 和CO 的平衡转化率随温度变化的曲线如图
4 2 4 2
所示。下列有关说法正确的是()
A.升高温度、增大压强均有利于提高CH 的平衡转化率
4
B.曲线B表示CH 的平衡转化率随温度的变化
4
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH )∶n(CO )=1∶1条件下,反应至CH 转化率达到X点的值,改变除温度外的特定条件继
4 2 4
续反应,CH 转化率不能达到Y点的值
4
5.(2022·江苏杭州高级中学高三开学考试)甲醛在木材加工、医药等方面有重要用途。甲醇利用脱氢法可制备甲醛,主要反应为: 。 是甲醇脱氢制甲
醛的催化剂,有研究指出,催化反应的部分机理如下:
历程ⅰ:
历程ⅱ:
历程ⅲ:
历程iv:
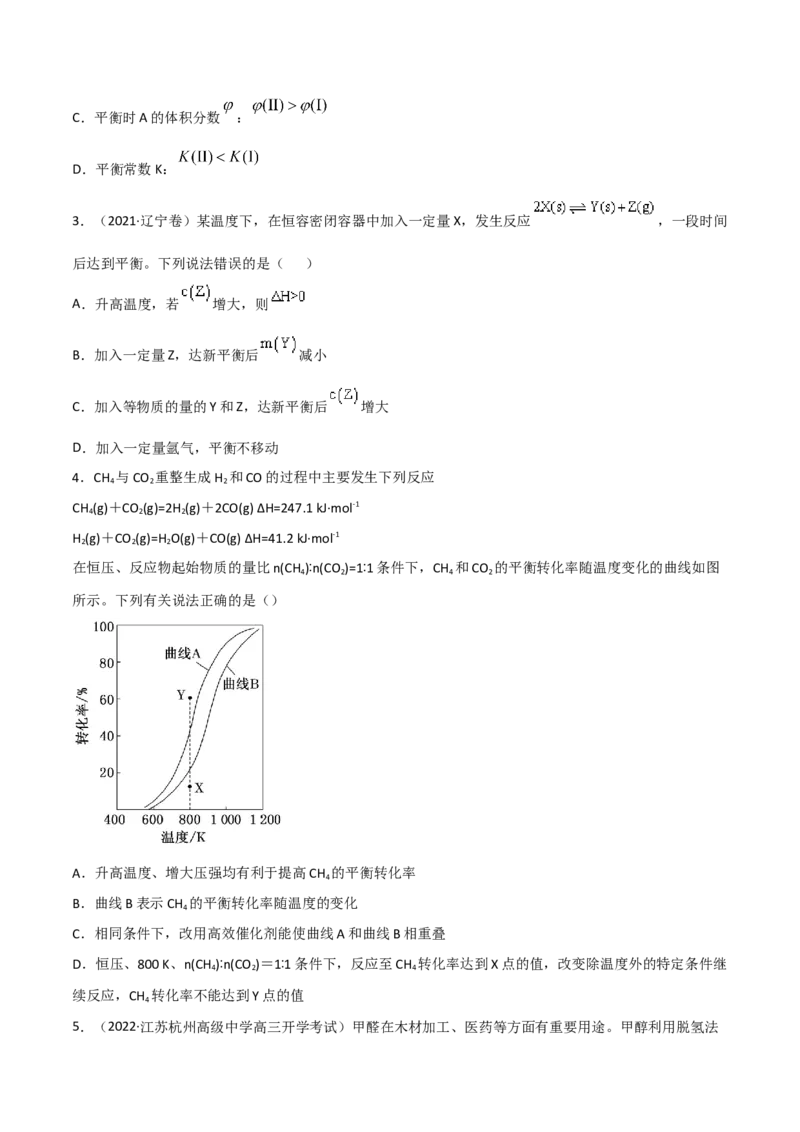
如图所示为在体积2L的恒容容器中,投入 ,在碳酸钠催化剂作用下,经过5min反应,测得
甲醇转化率与甲醛的选择性与温度的关系(甲醛的选择性:转化的 中生成 的百分比),下列有
关说法正确的是
A.600℃时,前5min内生成甲醛的平均速率
B.700℃时,反应历程ⅱ的速率大于反应历程ⅲ的速率
C.脱氢法制甲醛中,在高温高压条件下更有利于提高平衡产率
D.反应历程ⅰ的活化能小于 的活化能
6.(双选)(2022·江苏南京·高三阶段练习)将金红石(TiO )转化为TiCl 是生产金属钛的关键步骤。在
2 4
1.0×105Pa,将TiO 、C、Cl 以物质的量比1:2:2进行反应,平衡体系中主要物质的物质的量分数(x)随温
2 2
度变化理论计算结果如图所示。下列说法不正确的是( )
A.200~1600℃反应达到平衡时,TiO 的转化率均已接近100%
2
B.将400℃时的平衡体系加热至800℃,平衡C(s)+CO (g) 2CO(g)向逆反应方向移动
2
C.1000℃时,测得某时刻x(TiCl )=0.2.其他条件不变,延长反应时间能使x(TiCl )超过该温度下平衡时的
4 4
x(TiCl )
4
D.实际生产时反应温度选择900℃而不选择200℃,其主要原因是:900℃比200℃时化学反应速率更快,
生产效益更高
7.(2022·河北·二模)通过“CO →合成气→高附加值产品”的工艺路线,可有效实现CO 的资源化利用。
2 2
CO 加氢制合成气(CO、H )时发生下列反应:
2 2
I.CO (g)+H (g) CO(g)+H O(g) H =+41kJ·mol-1
2 2 2 1
△
II.CO (g)+4H (g) CH (g)+2H O(g) H
2 2 4 2 2
△
III.CO (g)+CH (g) 2CO(g)+2H (g) H =+247kJ·mol-1
2 4 2 3
△
(1)据此计算 H =____;反应III能自发进行的原因为____。
2
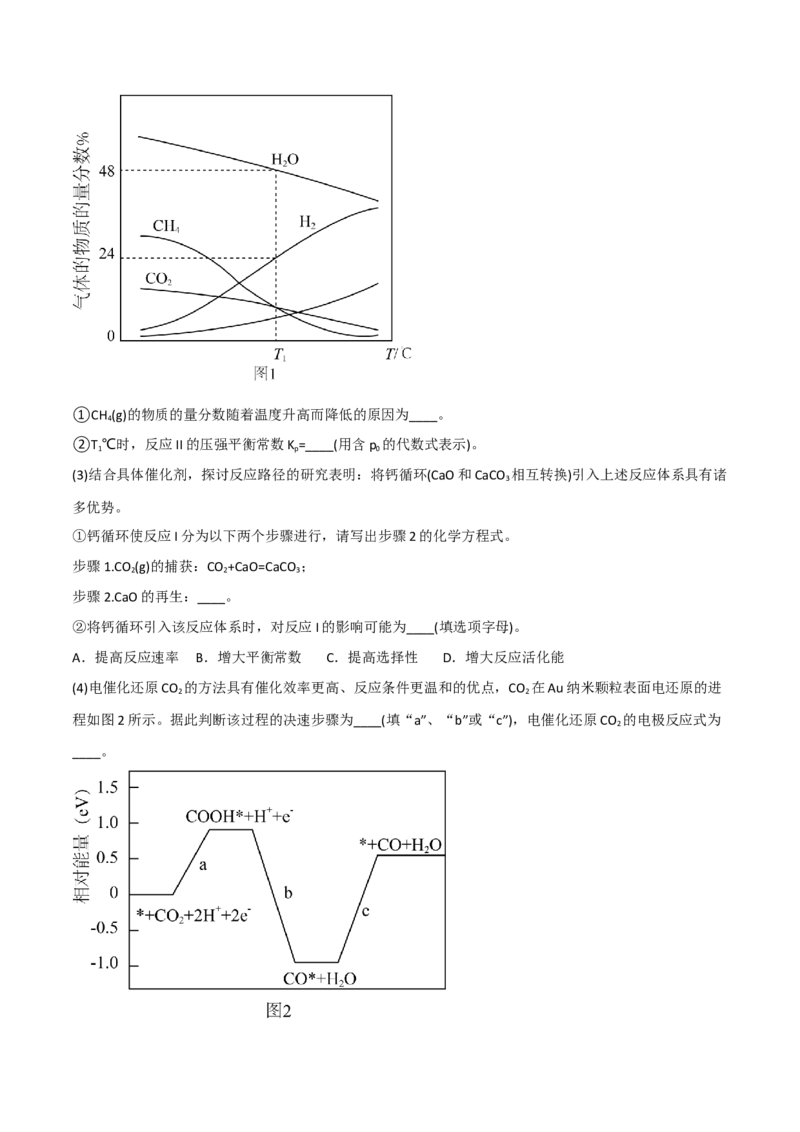
(2)在压强为△p 的恒压密闭容器中,按一定物质的量之比充入H (g)和CO (g)发生反应,平衡体系中气体的物
0 2 2
质的量分数随温度变化如图1所示:①CH (g)的物质的量分数随着温度升高而降低的原因为____。
4
②T ℃时,反应II的压强平衡常数K=____(用含p 的代数式表示)。
1 p 0
(3)结合具体催化剂,探讨反应路径的研究表明:将钙循环(CaO和CaCO 相互转换)引入上述反应体系具有诸
3
多优势。
①钙循环使反应I分为以下两个步骤进行,请写出步骤2的化学方程式。
步骤1.CO (g)的捕获:CO +CaO=CaCO ;
2 2 3
步骤2.CaO的再生:____。
②将钙循环引入该反应体系时,对反应I的影响可能为____(填选项字母)。
A.提高反应速率 B.增大平衡常数 C.提高选择性 D.增大反应活化能
(4)电催化还原CO 的方法具有催化效率更高、反应条件更温和的优点,CO 在Au纳米颗粒表面电还原的进
2 2
程如图2所示。据此判断该过程的决速步骤为____(填“a”、“b”或“c”),电催化还原CO 的电极反应式为
2
____。8.(2022·潍坊高三模拟)碳以及碳的化合物在生活中应用广泛。利用CO 合成甲醇不仅能够使二氧化碳
2
得到有效合理的利用,也能解决日益严重的能源危机。由CO 合成甲醇的过程可能涉及如下反应:
2
反应I:CO (g)+3H (g) CH OH(g)+H O(g) ΔH =-49.58 kJ·mol-1
2 2 3 2 1
反应II:CO (g)+H (g) CO(g)+H O(g) ΔH =+41.19 kJ·mol-1
2 2 2 2
反应III:CO(g)+2H (g) CH OH(g) ΔH
2 3 3
回答下列问题:
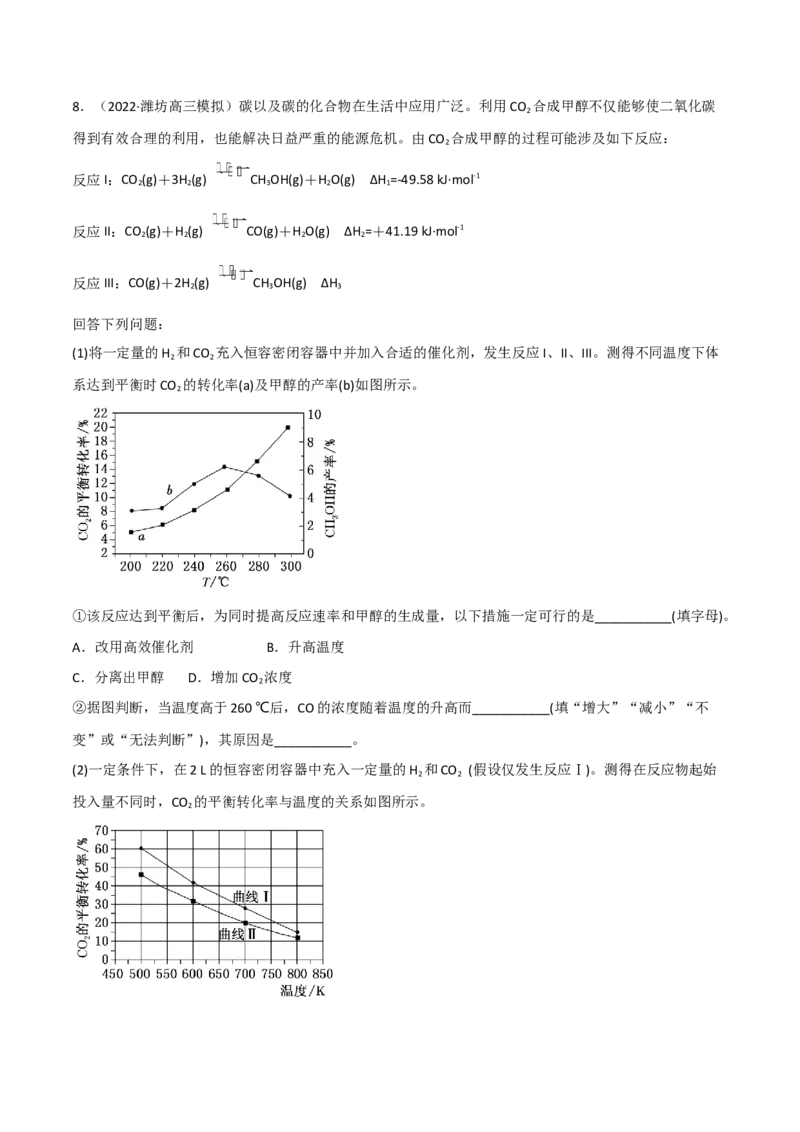
(1)将一定量的H 和CO 充入恒容密闭容器中并加入合适的催化剂,发生反应I、II、III。测得不同温度下体
2 2
系达到平衡时CO 的转化率(a)及甲醇的产率(b)如图所示。
2
①该反应达到平衡后,为同时提高反应速率和甲醇的生成量,以下措施一定可行的是___________(填字母)。
A.改用高效催化剂 B.升高温度
C.分离出甲醇 D.增加CO 浓度
2
②据图判断,当温度高于260 ℃后,CO的浓度随着温度的升高而___________(填“增大”“减小”“不
变”或“无法判断”),其原因是___________。
(2)一定条件下,在2 L的恒容密闭容器中充入一定量的H 和CO (假设仅发生反应Ⅰ)。测得在反应物起始
2 2
投入量不同时,CO 的平衡转化率与温度的关系如图所示。
2反应物起始投入量:
曲线I:n(H )=3 mol,n(CO )=1.5 mol
2 2
曲线II:n(H )=3 mol,n(CO )=2 mol
2 2
①根据图中数据判断,要使CO 平衡转化率大于40%,以下条件中最合理的是___________。
2
A.n(H )=3 mol,n(CO )=2.5 mol;550 K
2 2
B.n(H )=3 mol,n(CO )=1.6 mol;550 K
2 2
C.n(H )=3 mol,n(CO )=1.9 mol;600 K
2 2
D.n(H )=3 mol,n(CO )=1.5 mol;650 K
2 2
②请选择图中数据计算500 K时反应I的平衡常数K=___________。