文档内容
高频考点 37 原子结构与性质
1.(2022·辽宁卷)理论化学模拟得到一种 离子,结构如图。下列关于该离子的说法错误的是( )
A.所有原子均满足8电子结构 B.N原子的杂化方式有2种
C.空间结构为四面体形 D.常温下不稳定
1.B A .由 的结构式可知,所有N原子均满足8电子稳定结构,A正确;B.中心N原子为 杂化,
与中心N原子直接相连的N原子为 杂化,与端位N原子直接相连的N原子为 杂化,端位N原子为
杂化,则N原子的杂化方式有3种,B错误;C.中心N原子为 杂化,则其空间结构为四面体形,C正
确;D. 中含叠氮结构( ),常温下不稳定,D正确;故答案选B。
2.(2022·江苏卷)工业上电解熔融 和冰晶石 的混合物可制得铝。下列说法正确的是(
)
A.半径大小: B.电负性大小:
C.电离能大小: D.碱性强弱:
2.A A.核外电子数相同时,核电荷数越大半径越小,故半径大小为 ,故A正确;B.同
周期元素核电荷数越大电负性越大,故 ,故B错误;C.同周期从左往右第一电离能呈增大趋势,
同主族从上往下第一电离能呈减小趋势,故电离能大小为 ,故C错误;D.元素金属性越强,其最高价氧化物对应水化物的碱性越强,故碱性强弱为 ,故D错误;故选A。
3.(2022·海南·高考真题)钠和钾是两种常见金属,下列说法正确的是( )
A.钠元素的第一电离能大于钾 B.基态钾原子价层电子轨道表示式为
C.钾能置换出NaCl溶液中的钠 D.钠元素与钾元素的原子序数相差18
3.A A.同一主族元素的第一电离能从上到下依次减小,金属性越强的元素,其第一电离能越小,因此,
钠元素的第一电离能大于钾,A说法正确;B.基态钾原子价层电子为4s1,其轨道表示式为 ,B说法不
正确;C.钾和钠均能与水发生置换反应,因此,钾不能置换出 NaC1溶液中的钠,C说法不正确;D.钠
元素与钾元素的原子序数分别为11和19,两者相差8,D说法不正确;综上所述,本题选A。
4.(2021·辽宁卷)某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态
Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是()
A.氢化物沸点: B.原子半径:
C.第一电离能: D.阴、阳离子中均有配位键
4.D 由题干信息可知,基态Z原子的电子填充了3个能级,其中有2个未成对电子,故Z为C或者O,根
据多孔储氢材料前驱体结构图可知Y周围形成了4个单键,再结合信息M、W、X、Y、Z五种元素原子序数
依次增大,故Y为N,故Z为O,M只形成一个单键,M为H,X为C,则W为B,据此分析解题。A.由分
析可知,X、Y的氢化物分别为:CH 和NH ,由于NH 存在分子间氢键,故氢化物沸点: ,A错误;
4 3 3
B.根据同一周期从左往右主族元素的原子半径依次减小,同一主族从上往下依次增大,故原子半径:
,B错误;C.根据同一周期从左往右元素的第一电离能呈增大趋势,IIA与IIIA,VA与VIA反常,
故第一电离能: ,C错误;
D.由于阳离子中的Y原子是N原子,形成了类似于铵根离子的阳离子,故存在配位键,阴离子中的W为
B,最外层上只有3个电子,能形成3个共价键,现在形成了4个共价键,故还有一个配位键,D正确;故
答案为:D。5.(2021·山东卷)X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物能
以[XY ]+[XY ]-的形式存在。下列说法错误的是( )
4 6
A.原子半径:X>Y B.简单氢化物的还原性:X>Y
C.同周期元素形成的单质中Y氧化性最强 D.同周期中第一电离能小于X的元素有4种
5.D Y位于第三周期,且最高正价与最低负价的代数和为6,则Y是Cl元素,由X、Y形成的阴离子和阳
离子知,X与Y容易形成共价键,根据化合物的形式知X是P元素。A.P与Cl在同一周期,则P半径大,
即X>Y,A项不符合题意;B.两者对应的简单氢化物分别是PH 和HCl,半径是P3->Cl-,所以PH 的失电子
3 3
能力强,还原性强,即X>Y,B项不符合题意;C.同周期元素从左往右,金属性减弱,非金属性增强,各
元素对应的金属单质还原性减弱,非金属单质的氧化性增强,所以Cl 的氧化性最强,C项不符合题意;
2
D.同一周期,从左到右,第一电离能呈现增大的趋势,第VA族元素的第一电离能大于相邻元素的第一电
离能;所以第三周期第一电离能从小到大依次为Na、Al、Mg、Si、S、P、Cl,所以有5种,D项符合题意;
故选D。
6.(2022·广东佛山·一模)某药物的一种成分均由短周期主族元素组成,其结构如图所示。元素X、Y、
Z、W、E的原子序数依次增大,X与其它几种元素不同周期,W与E原子的基态价电子排布均为 。
下列说法中错误的是( )
A.原子半径:W<E B.简单氢化物的沸点:Z>Y
C.第一电离能:Z>W D.最高价氧化物对应的水化物的酸性:E>Y
6.C X、Y、Z、W、E的原子序数依次增大,W与E原子的基态价电子排布均为 ,则W为F原子、E
为Cl元素;X与其它几种元素不同周期,则X为H元素;由药物的结构示意图可知,Y、Z形成共价键的数
目为4、2,则Y为C元素、X为O元素。A.氢原子的原子半径小于氯原子,故A正确;B.水分子能形成
分子间氢键,甲烷不能形成分子间氢键,则水的分子间作用力大于甲烷,水的沸点高于甲烷,故B正确;
C.同周期元素,从左到右第一电离能呈增大趋势,则氟元素的第一电离能大于Y元素,故C错误;D.元
素的非金属性越强,最高价氧化物对应的水化物的酸性越强,氯元素的非金属性强于碳元素,则高氯酸的
酸性强于碳酸,故D正确;故选C。7.(2022·广东深圳·一模)已知X、Y、Z、W、M为原子序数依次递增的短周期元素,其中X、Y、Z元素
同周期, Y与W元素同主族,它们可以形成一种重要化合物甲。其结构如图所示。下列说法正确的是(
)
A.原子半径:M>W>Z B.第一电离能:Y>Z>X
C.氢化物的沸点:Z>Y>X D.甲中W的杂化方式为sp2
7.B 已知X、Y、Z、W、M为原子序数依次递增的短周期元素,其中X、Y、Z元素同周期,X形成四个共
价键,则X特征最外层有4个电子,X是C元素;Y形成3个共价键,Y 原子最外层有5个电子,Y是N元
素;Z形成2个共价键,则Z最外层有6个电子,Y与W元素同主族,则W是P元素,M原子序数比P大,
可形成1个共价键,则M 最外层有7个电子,M是Cl元素,然后根据元素周期律及物质的性质分析解答。
根据上述分析可知:X是C,Y是N,Z是O,W是P,M是Cl元素。A.同一周期族元素从左到右原子半径
逐渐减小,所以原子半径P>Cl,不同周期元素,原子核外电子层数越多,原子半径越大,则原子半径大
小关系为: W(P)>M(Cl)>Z(O),A错误;B.一般情况下同一周期元素的第一电离能随原子序数的增大而
增强,但当元素处于第ⅡA|diⅤA时,原子核外电子处于全满、半满的稳定状态,其第一电离能大于同一
周期相邻元素,由于N的2p轨道处于半满状态,较稳定,所以第一电离能:N>O>C,B正确;C.碳的
氢化物种类较多,物质分子中含有的C原子数目多少不同,物质沸点高低不同,因此无法确定X、Y、Z三
种元素的氢化物熔沸点高低,C错误;D.W是P,P原子价层电子对数是3+ =4,元素甲中W的杂化
方式为sp3杂化,D错误;故合理选项是B。
8.(2022·江苏泰州·模拟预测)我国“祝融号”火星车成功着陆火星,其矿脉中含有原子序数依次增大的
短周期主族元素W、X、Y、Z。已知W、Z同主族,且Z的原子序数是W的2倍,X的氢化物可用于蚀刻玻
璃,Y与Z最外层电子数之和等于8。下列说法正确的是( )
A.离子半径:Z>Y>W>X
B.同周期第一电离能小于Z的元素有4种
C.X与Y可形成共价化合物YX
2
D.简单氢化物的还原性:W的氢化物>Z的氢化物
8.B 原子序数依次增大的短周期主族元素W、X、Y、Z,已知W、Z同主族,且Z的原子序数是W的2倍,
则W为O,Z为S;X的氢化物可用于蚀刻玻璃,则X为F元素,Y与Z最外层电子数之和等于8,Y的最外
层电子数为8-6=2,Y的原子序数大于F,则Y为Mg元素,以此解答。A.离子的核外电子层结构相同,核电荷数越大离子半径越小,电子层数越多,离子半径越大,则离子半径Z>W>X>Y,A错误;B.同周期主族
元素随原子序数增大第一电离能呈增大趋势,但是第ⅡA族和ⅤA族比相邻元素的大,则同一周期小于Z
的元素有Na、Mg、Al、Si,B正确;C.X和Y形成的化合物为MgF ,含有离子键,属于离子化合物,C错
2
误;D.非金属性W>Z,则简单氢化物的还原性:W的氢化物W>X
C.物质R吸收微波时,分子内的σ键会断裂
D.简单气态氢化物的还原性:W>Y
9.D X、Y、Q、W、Z是原子序数依次增大的短周期主族元素,其中Y原子最外层电子数是其内层电子数
的2倍,则Y为C元素;W与Y位于同一主族,则W为Si元素;Q元素单质可用作铝热反应的引燃剂,则
Q为Mg元素;结合物质的结构式可知,X可形成1对共用电子对,则X为H元素,Z可形成2个共价单键,
则根据满8电子稳定原则可知,Z最外层电子数为6,且位于第三周期,所以Z为S元素。A.同周期元素,
从左到右第一电离能呈增大趋势,镁原子的3s轨道为稳定的全充满结构,元素的第一电离能大于相邻元素,
则钠元素、铝元素的第一电离能小于镁元素,故A错误;B.硅元素的电负性小于氢元素,故B错误;C.
σ键比π键牢固,所以物质R吸收微波时,分子内的π键会断裂,故C错误;D.元素的非金属性越强,简
单氢化物的热稳定性越强、还原性越弱,碳元素的非金属性强于硅元素,所以硅烷的还原性强于甲烷,故
D正确;故选D。
10.(2022·全国甲卷节选)2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,
实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯(CH =CH )与四氟乙烯(CF =CF )的共聚物(ETFE)制成。
2 2 2 2
回答下列问题:
(1)基态F原子的价电子排布图(轨道表示式)为_______。
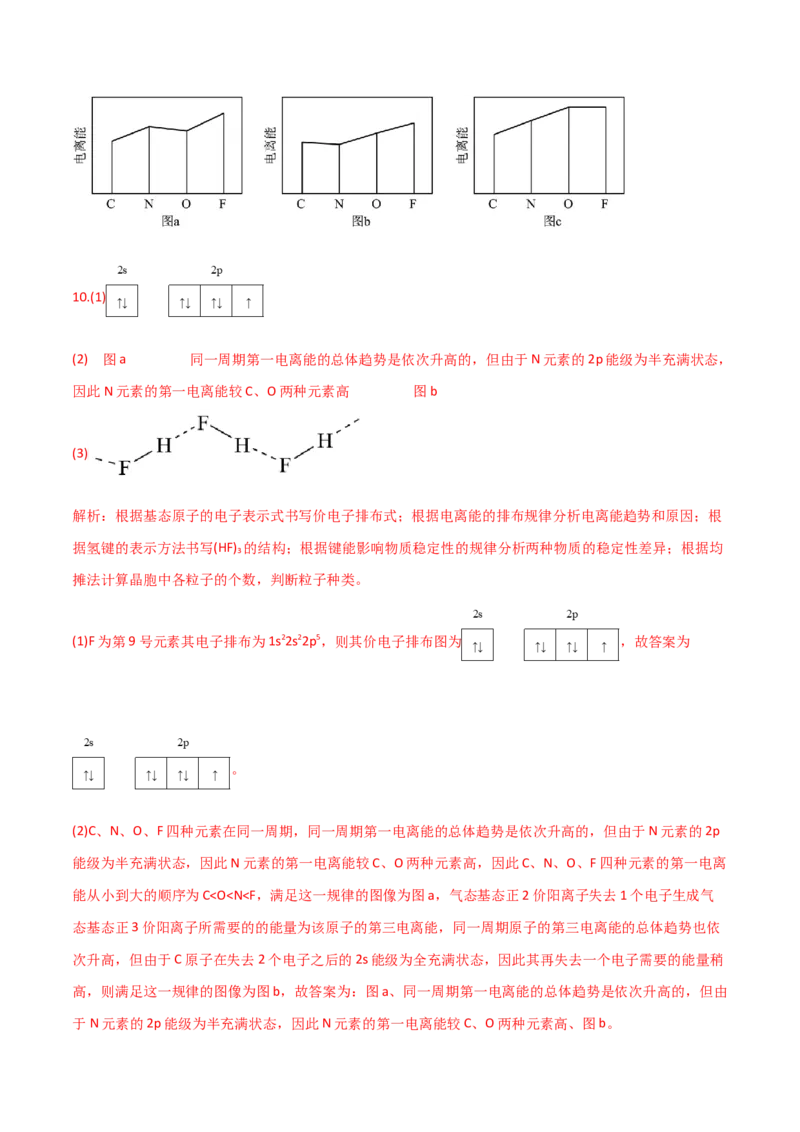
(2)图a、b、c分别表示C、N、O和F的逐级电离能Ⅰ变化趋势(纵坐标的标度不同)。第一电离能的变化图
是_______(填标号),判断的根据是_______;第三电离能的变化图是_______(填标号)。10.(1)
(2) 图a 同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p能级为半充满状态,
因此N元素的第一电离能较C、O两种元素高 图b
(3)
解析:根据基态原子的电子表示式书写价电子排布式;根据电离能的排布规律分析电离能趋势和原因;根
据氢键的表示方法书写(HF) 的结构;根据键能影响物质稳定性的规律分析两种物质的稳定性差异;根据均
3
摊法计算晶胞中各粒子的个数,判断粒子种类。
(1)F为第9号元素其电子排布为1s22s22p5,则其价电子排布图为 ,故答案为
。
(2)C、N、O、F四种元素在同一周期,同一周期第一电离能的总体趋势是依次升高的,但由于N元素的2p
能级为半充满状态,因此N元素的第一电离能较C、O两种元素高,因此C、N、O、F四种元素的第一电离
能从小到大的顺序为C