文档内容
高频考点 39 晶体结构与性质
1.(2022·北京卷)由键能数据大小,不能解释下列事实的是( )
化学键
键能/ 411 318 799 358 452 346 222
A.稳定性: B.键长:
C.熔点: D.硬度:金刚石>晶体硅
1.C A.键能越大越稳定, 键能大于 ,所以稳定性: ,故不选A;
B.键能越大,键长越短, 键能大于 ,所以键长: ,故不选B;
C.CO 是分子晶体,熔点由分子间作用力决定,SiO 是共价晶体,所以熔点 ,不能用键能解释
2 2
熔点 ,故选C;D.金刚石、晶体硅都是共价晶体,共价晶体中键能越大,晶体的硬度越大,
的键能大于 ,所以硬度:金刚石>晶体硅,故不选D;选C。
2.(2021·天津卷)下列各组物质的晶体类型相同的是( )
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
2.C A.SiO 为原子晶体,SO 为分子晶体,晶体类型不同,故A错误;B.I 为分子晶体,NaCl为离子晶
2 3 2
体,晶体类型不同,故B错误;C.Cu和Ag都为金属晶体,晶体类型相同,故C正确;D.SiC为原子晶体,
MgO为离子晶体,晶体类型不同,故D错误;
故选C。
3.(2021·海南卷)关于 性质的解释合理的是( )
选项 性质 解释
A 比 容易液化 分子间的范德华力更大
B 熔点高于 键的键能比 大
能与 以配位键结
C 中氮原子有孤电子对
合D 氨水中存在 是离子化合物
A.A B.B C.C D.D
3.C A. 和 都属于同一主族是氢化物,分子晶体的沸点与其相对分子质量成正比,但氨气中含有
氢键, PH 不含氢键,氢键的存在导致氨气的沸点升高,故A错误;
3
B. 熔点高于 ,是因为氨气中含有氢键,氢键的存在导致氨气的熔点升高,不是 键的键能比
大,故B错误;C. 中氮原子有孤电子对,使 和 以配位键结合形成[Ag(NH ) ]+,故C正确;
3 2
D. 是共价化合物,是弱碱,在水溶液中部分电离出 和OH-,故D错误;答案选C。
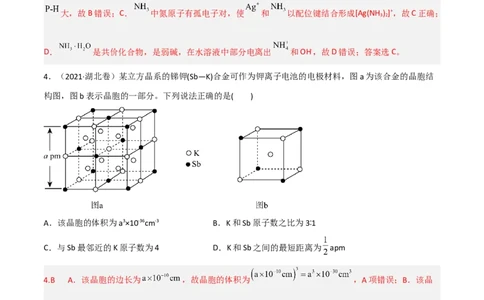
4.(2021·湖北卷)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结
构图,图b表示晶胞的一部分。下列说法正确的是( )
A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1
C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
4.B A.该晶胞的边长为 ,故晶胞的体积为 ,A项错误;B.该晶
胞中K的个数为 ,Sb的个数为 ,故K和Sb原子数之比为3∶1,B项正确;C.
以面心处Sb为研究对象,与Sb最邻近的K原子数为8,C项错误;D.K和Sb的最短距离为晶胞体对角线
长度的 ,即 ,D项错误。故选B。
5.(2022·河北沧州·高三开学考试)金属铜的晶胞结构如图所示,已知金属铜的密度为ρg•cm-3,N 表示
A阿伏加德罗常数的值。下列说法中正确的是()
A.基态Cu原子的核外电子排布式为[Ar]3d94s2
B.金属铜的晶胞是体心立方堆积
C.每个晶胞中Cu原子个数为6
D.距离最近的两个铜原子之间的距离为 cm
5.D A.Cu为29号元素,基态原子的核外电子排布式为[Ar]3d104s1,故A错误;B.金属铜的晶胞是面心
立方堆积,故B错误;C.每个晶胞中Cu原子个数为 =4,故C错误;D .Cu为面心立方堆积,
处于晶胞面对角线上Cu原子紧密相邻,晶胞棱长等于Cu原子之间距离的 倍,晶胞中Cu原子数目
=4,晶胞质量= g,设最近的两个Cu原子之间距离为r,则晶胞棱长为 r,故
g=ρg•cm-3×( r)3,解得r= cm,故D正确;故选:D。
6.(双选)(2022·广东·汕头市第一中学高三阶段练习)FeS 晶体的晶胞结构如图所示。下列说法正确的
2
是()A.阴阳离子个数比为2∶1
B.阳离子位于阴离子构成的正八面体空隙中
C.阳离子的配位数为12
D.若晶胞边长为a,则阳离子间的最短距离为 a
6.BD A. 的个数为 ,Fe2+的个数为 ,阴阳离子个数比为1∶1,故A错误;B.由晶
胞结构可知,晶胞中心的阳离子位于阴离子构成的正八面体的中心,故B正确;C.由晶胞结构可知,每
个阳离子周围距离最近且相等的阴离子有6个,故阳离子的配位数为6,故C错误;D.通过晶胞中阳离子
的位置分析,若晶胞边长为a,则阳离子间的最短距离为 ,故D正确;故答案为BD
7.锌与硫所形成化合物晶体的晶胞如图所示。下列判断不正确的是( )
A.氧化锌的熔点低于硫化锌 B.该晶胞中 和 数目相等
C.晶胞中 周围最靠近的 共有4个 D.该晶体属于离子晶体
7.A A.氧化锌和硫化锌阴阳离子所带电荷量相等,但氧离子半径小于硫离子,因此氧化锌的熔点高于
硫化锌,A错误;B.依据均摊法,锌离子个数为8 +6 =4,硫离子个数为4,锌离子和硫离子数目相等,B正确;C.由晶胞图可知,晶胞中锌离子周围最近的硫离子共4个,C正确;D.硫化锌是由锌离子
和硫离子构成的离子化合物,属于离子晶体,D正确;答案选A。
8.(双选))某超导材料属于离子晶体,其晶胞结构如图所示。下列说法正确的是()
A.该超导材料的最简化学式为
B.Ni位于元素周期表中的ds区
C.晶胞中S的配位数为4
D.若该晶体的密度为 ,则阿伏伽德罗常数
8.AC A.晶胞中K原子位于顶点和体内,一个晶胞中原子数目为 ;Ni原子位于晶胞面上,一
个晶胞中原子数目为 ;S原子位于晶胞棱上和体内,一个晶胞中原子数目为 ;故该超导
材料的最简化学式为 ,A正确;B.镍为28号元素,位于第四周期第Ⅷ族,是元素周期表中的d区,
B错误;C.由图可知,以晶胞内硫为例,最近等距的Ni位于面上共4个,故晶胞中S的配位数为4,C正
确;D.一个晶胞中K、Ni、S的数目分别为2、4、4,则晶胞质量为 ;密度为 ,则 ;D错误;故选AC。
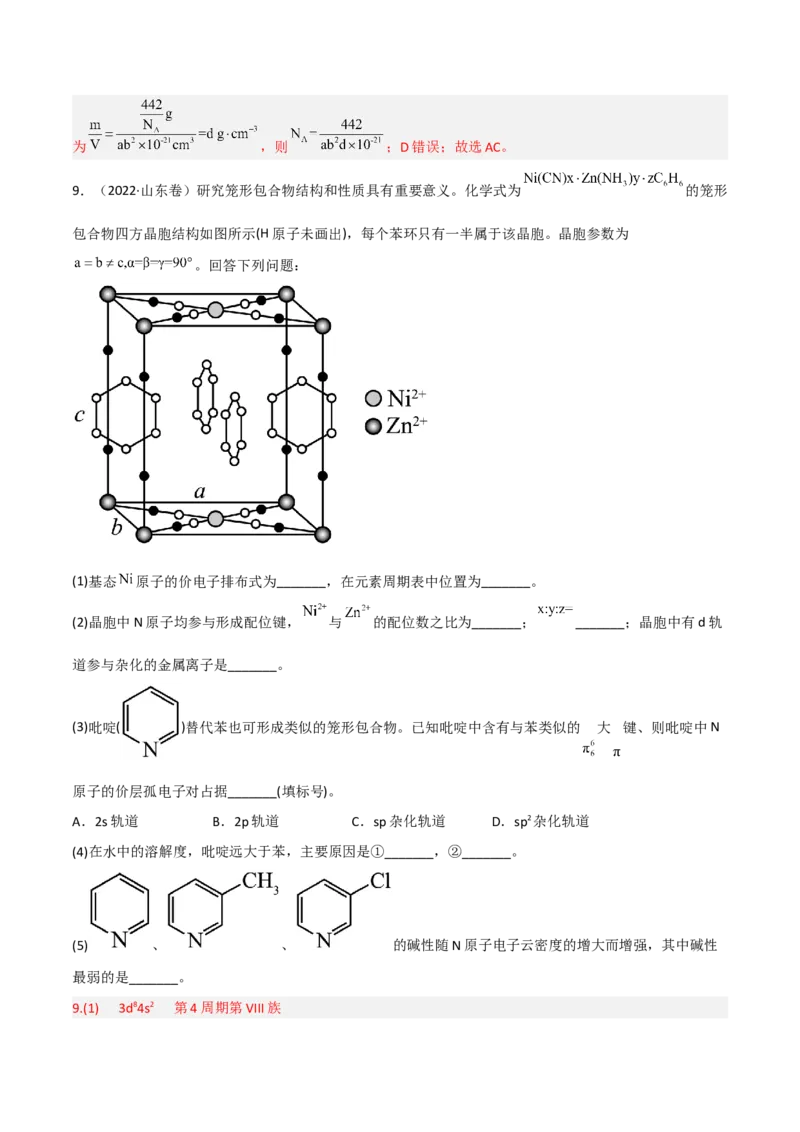
9.(2022·山东卷)研究笼形包合物结构和性质具有重要意义。化学式为 的笼形
包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为
。回答下列问题:
(1)基态 原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键, 与 的配位数之比为_______; _______;晶胞中有d轨
道参与杂化的金属离子是_______。
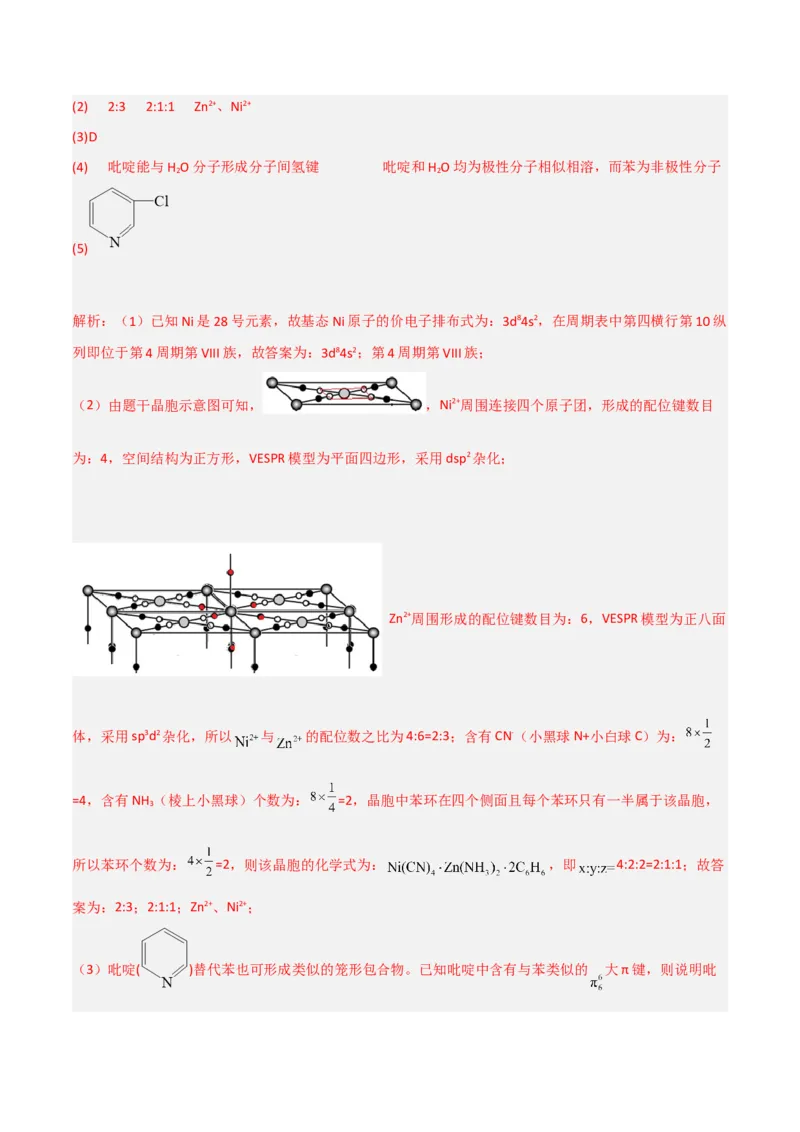
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大 键、则吡啶中N
原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱性
最弱的是_______。
9.(1) 3d84s2 第4周期第VIII族(2) 2:3 2:1:1 Zn2+、Ni2+
(3)D
(4) 吡啶能与H O分子形成分子间氢键 吡啶和H O均为极性分子相似相溶,而苯为非极性分子
2 2
(5)
解析:(1)已知Ni是28号元素,故基态Ni原子的价电子排布式为:3d84s2,在周期表中第四横行第10纵
列即位于第4周期第VIII族,故答案为:3d84s2;第4周期第VIII族;
(2)由题干晶胞示意图可知, ,Ni2+周围连接四个原子团,形成的配位键数目
为:4,空间结构为正方形,VESPR模型为平面四边形,采用dsp2杂化;
Zn2+周围形成的配位键数目为:6,VESPR模型为正八面
体,采用sp3d2杂化,所以 与 的配位数之比为4:6=2:3;含有CN-(小黑球N+小白球C)为:
=4,含有NH (棱上小黑球)个数为: =2,晶胞中苯环在四个侧面且每个苯环只有一半属于该晶胞,
3
所以苯环个数为: =2,则该晶胞的化学式为: ,即 4:2:2=2:1:1;故答
案为:2:3;2:1:1;Zn2+、Ni2+;
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大π键,则说明吡啶中N原子也是采用sp2杂化,杂化轨道只用于形成σ键和存在孤电子对,则吡啶中N原子的价层孤电子
对占据sp2杂化轨道,故答案为:D;
(4)已知苯分子为非极性分子,H O分子为极性分子,且吡啶中N原子上含有孤电子对能与H O分子形成
2 2
分子间氢键,从而导致在水中的溶解度,吡啶远大于苯,故答案为:吡啶能与H O分子形成分子间氢键;
2
吡啶和H O均为极性分子相似相溶,而苯为非极性分子;
2
(5)已知-CH 为推电子基团,-Cl是吸电子基团,则导致N原子电子云密度大小顺序为: >
3
> ,结合题干信息可知,其中碱性最弱的为: ,故答案为:
。
10.环烷酸金属(Cu、Ni、Co、Sn、Zn)盐常作为合成聚氨酯过程中的有效催化剂。回答下列问题:
(1)基态Co原子的价电子排布式为_______。
(2)镍的氨合离子[Ni(NH ) ]2+中存在的化学键有_______。
3 6
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(3)Cu、Zn的第二电离能比较I (Cu)_______I (Zn)(填“>”、“=”或“<”)
2 2
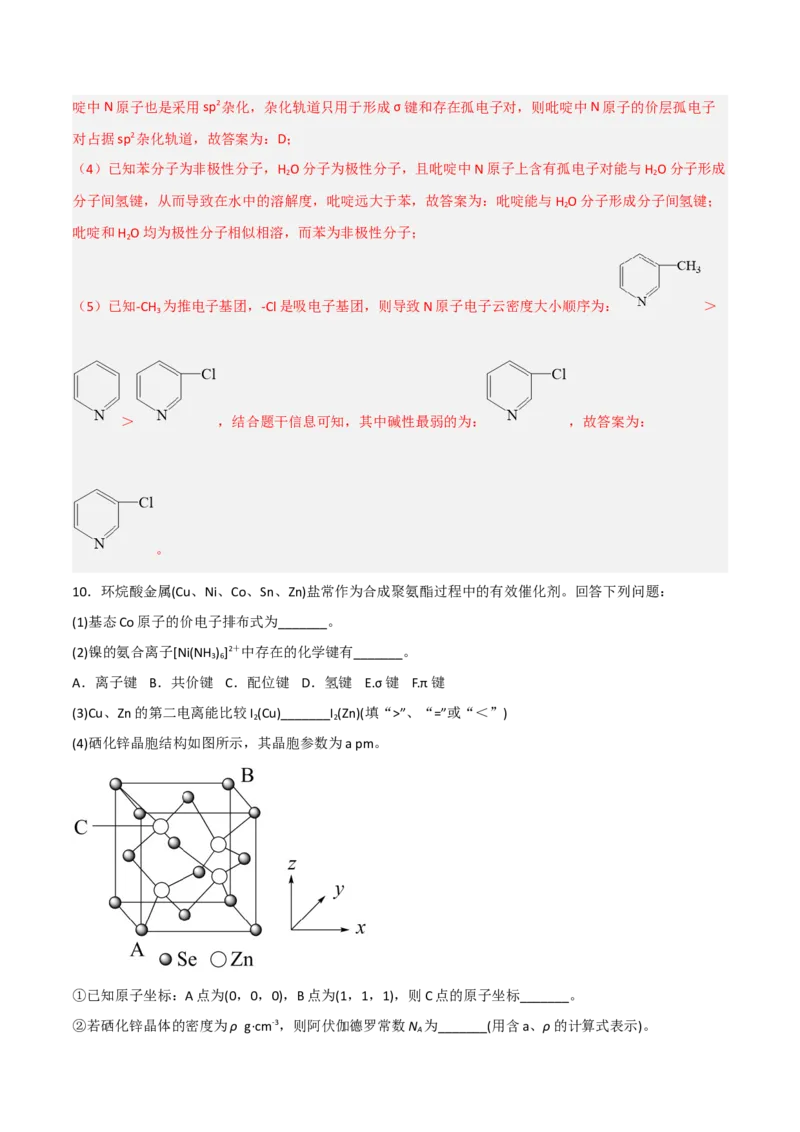
(4)硒化锌晶胞结构如图所示,其晶胞参数为a pm。
①已知原子坐标:A点为(0,0,0),B点为(1,1,1),则C点的原子坐标_______。
②若硒化锌晶体的密度为ρ g·cm-3,则阿伏伽德罗常数N 为_______(用含a、ρ的计算式表示)。
A10.(1)3d74s2(2)BCE(3)>(4) ( , , )
解析:(1)Co的原子序数为27,核外电子排布式为1s22s22p63s23p63d74s2,价电子排布式为3d74s2。
(2)在镍的氨合离子[Ni(NH ) ]2+中,N和H之间存在共价单键,也是σ键,Ni2+和NH 之间存在配位键,故
3 6 3
选BCE。
(3)Cu的价电子排布式为3d104s1,Zn的价电子排布式为3d104s2,铜失去一个电子后达到全充满的稳定结
构,再失去一个电子需要的能量高,所以铜的第二电离能大于锌的第二电离能。
(4)①根据原子坐标:A点为(0,0,0),B点为(1,1,1),C点位于把晶胞分为8个等大的小立方体后,
居于左上后方的小立方体的体心,则C点的原子坐标为( )。
②在硒化锌晶胞中,硒位于顶点和面心,共4个,锌位于晶胞内部,共4个,所以一个晶胞的质量为
,晶胞的体积为(a×10-10)3cm3=a3×10-30cm3,晶胞密度为ρ g·cm-3,则ρ g·cm-3×a3×10-30cm3=
,可求出N = 。。
A
11.(2022·河北·廊坊市第十五中学模拟预测)氮、磷、氯、溴、铁、铜等元素及其化合物在现代农业、
科技和国防建设中有着许多独特的用途。LiFePO 是新型锂离子电池的电极材料,可利用FeCl 、NH H PO 、
4 3 4 2 4
LiC1和苯胺( )等原料来制备。回答下列问题。
(1)铁元素在元素周期表中的位置为_______,基态Fe2+的价层电子排布图(轨道表达式)为_______。
(2)NH H PO 中,除氢元素外,其余三种元素第一电离能最大的是_______(填元素符号)。
4 2 4
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点明显比甲苯的高,原因是_______。
(4)红磷在氯气中燃烧可以得到PCl 和PCl ,其中气态PCl 分子的立体构型为_______。研究发现固态PCl 和
3 5 3 5
PBr 的结构分别为 和 ,则它们的晶体类型为_______。
5
(5)已知NH 分子中H-N-H的键角为107.3°,则配合物[Cu(NH ) ]SO 中H-N-H的键角_______107.3°(填“大
3 3 4 4于”“小于”“等于”)。
(6)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构以及各原子的投影位置如图所示。
已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为( , −m, −n),则3号Fe原子的空间
坐标为_______,若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用N 表示,则该晶体的密度
A
为_______g·cm−3(列出表达式)。
11.(1) 第四周期第Ⅷ族 (2)N
(3)苯胺和甲苯都是分子晶体,苯胺分子间形成氢键,其熔点偏高
(4) 三角锥形 离子晶体
(5)大于
(6) ( , +m, )
解析:(1)铁元素在元素周期表中位于第四周期第VIII族,基态Fe2+的价层电子排布图(轨道表达式)为
。
(2)同一周期元素,元素第一电离能随着原子序数增大而呈增大趋势,但第IIA族、第VA族元素第一电
离能大于其相邻元素,所以这三种元素第一电离能大小顺序是N>O>C。
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点明显比甲苯的高,原因是:苯胺和甲苯都是分子晶体,
苯胺分子间形成氢键,其熔点偏高。
(4)P为中心原子,提供5个价电子,Cl作为周围原子,1个Cl提供1个价电子,共8个价电子(4对),所
以P为sp3杂化,价电子构型为四面体形。因为只有3个P-Cl,所以分子构型是三角锥形,有1对孤对电子;
研究发现固态PCl 和PBr 的结构分别为[PCl ]+[PCl ]−和[PBr ]+Br−,这两种结构都属于离子晶体结构,结构存
5 5 4 6 4在差异是因为溴原子半径较大,P周围无法容纳6个溴原子,斥力太大不稳定,故晶体类型为:离子晶体。
(5)对于NH 分子中N原子的价层电子对数=3+ =4,所以NH 的VSEPR模型为正四面体形;孤电子
3 3
对与成键电子对之间的排斥力大于成键电子对之间的排斥力,氨气分子中含有1对孤电子对,而
[Cu(NH ) ]2+离子中N原子上的孤电子对与铜离子形成配位键,所以[Cu(NH ) ]2+离子中H-N-H键角大于
3 4 3 4
107.3°。
(6)晶胞中Y的个数为8 ,Fe的个数为2,O的个数为8 ,铁酸钇的化学式为
YFeO ;已知1号O原子空间坐标为(0, 0, ),2号O原子空间坐 标为( , -m, -n),则3号Fe原
3
子空间坐标为( , +m, );若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用N 表示,则
A
该晶体的密度为 。
12.(2022·广东茂名·高三期中)锰、铬、钴、铁的单质及其化合物在科研和生产中有着重要用途。回答
下列问题:
(1)基态锰原子的价电子排布式为_______。
(2) 和 均为离子化合物, 的熔点高于 熔点的原因为_______。
(3)化学式为 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种
化合物中, 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得
沉淀的物质的量之比为3∶2∶1。
①呈暗绿色的配合物,其内界的离子符号为_______。
② 分子的 模型为_______。
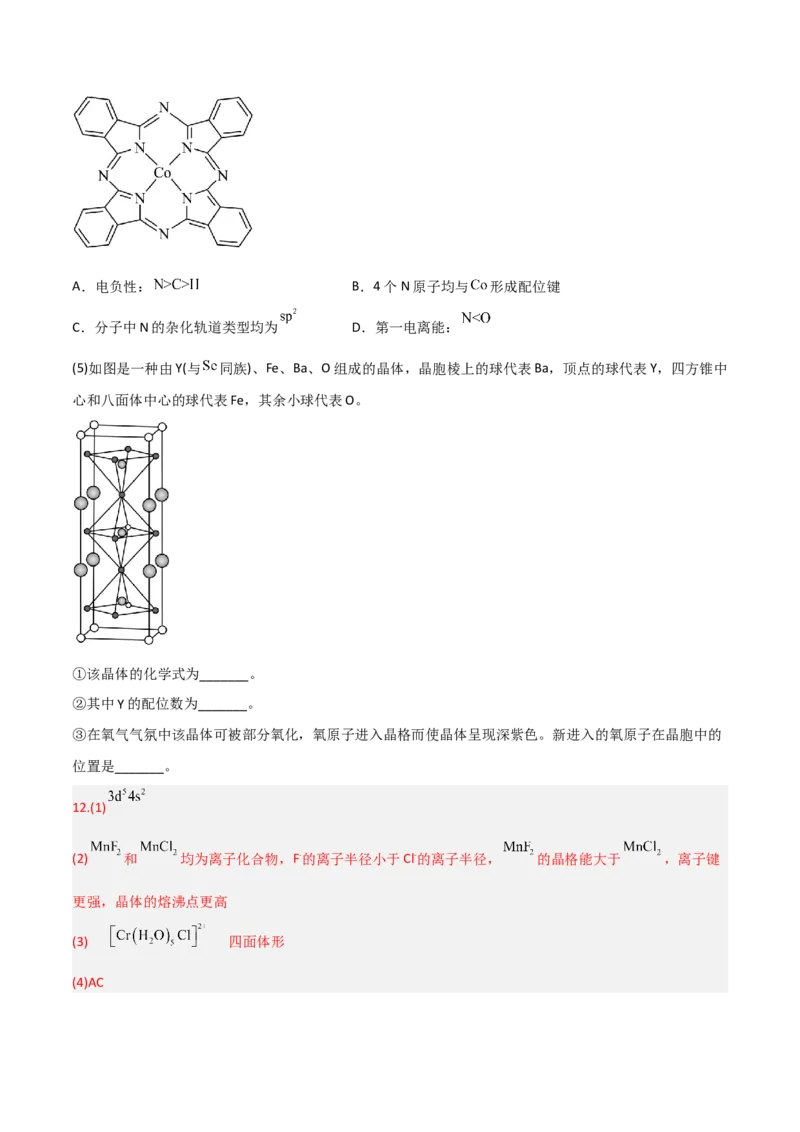
(4)如图为酞菁钴分子的平面结构,下列说法正确的是_______(填标号)。A.电负性: B.4个N原子均与 形成配位键
C.分子中N的杂化轨道类型均为 D.第一电离能:
(5)如图是一种由Y(与 同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中
心和八面体中心的球代表Fe,其余小球代表O。
①该晶体的化学式为_______。
②其中Y的配位数为_______。
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。新进入的氧原子在晶胞中的
位置是_______。
12.(1)
(2) 和 均为离子化合物,F-的离子半径小于Cl-的离子半径, 的晶格能大于 ,离子键
更强,晶体的熔沸点更高
(3) 四面体形
(4)AC(5) 8 晶胞顶面和底面的面心位置
解析:(1)Mn原子核外有25个电子,基态Mn原子的核外电子排布式为1s22s22p63s23p63d54s2,价电子排
布式为3d54s2。
(2) 和 均为离子化合物, 的熔点高于 熔点的原因为 和 均为离子化合
物,F-的离子半径小于Cl-的离子半径, 的晶格能大于 ,离子键更强,晶体的熔沸点更高。
(3)
①由相同物质的量的甲、乙、丙的水溶液中加入足量的AgNO 溶液,析出AgCl的物质的量之比分别为3:
3
2:1可知,暗绿色配合物的6个配体为1个氯离子和5个水分子,则暗绿色的配合物内界的化学式为[Cr
(H O) C1]2+;
2 5
②水分子中氧原子的价层电子对数为2+ =4,O原子为sp3杂化,则水分子的VSEPR模型为四面体形。
(4)A.酞菁钴中三种非金属原子为C、N、H,同周期自左而右电负性增大,非金属性越强电负性越大,
故电负性N>C>H,故A正确;
B.N原子最外层有5个电子,有1个孤电子对,含有孤对电子的N原子与Co原子以配位键结合;含有双
键的N原子与Co原子形成的才是配位键;形成3个单键的N原子与Co原子形成的是普通共价键;所以与
Co原子相连的4个N原子中只有2个N原子形成配位键,故B错误;
C.根据分子结构简式,碳碳双键和苯的结构都为平面形结构,其中的碳原子和N原子的杂化轨道类型为
sp2,故C正确;
D.同周期,从左至右,元素的原子半径逐渐减小,元素的第一电离能逐渐增大,但第ⅡA族和第ⅤA族
的p轨道为全空和半满结构,第一电离能反常,大于相邻周期的元素,所以第一电离能:N>O,故D错误。
(5)①如图是一种由Y(与Sc同族)、Ba、Fe、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,
四方锥中心和八面体中心的球代表Fe,小球代表O;从晶胞可知,Y位于顶点,原子数为: ×8=1;Ba位
于棱上,原子数为: ×8=2;O原子有12个位于面上,2个位于晶胞内,原子数为: ×12+2=8;3个Fe
原子位于晶胞内,该晶体的化学式为YBa Fe O ;
2 3 8
②从晶胞结构知Y位于晶胞棱柱顶点,距离Y最近的原子共有8个,即Y的配位数为8;
③氧原子进入晶格而使晶体呈现深紫色,新进入的氧原子在晶胞中的位置是晶胞顶面和底面的面心位置。13.(2022·江西·会昌县第五中学高三模拟)“愚人金”的主要成分是 ,它是炼铜的主要矿物,冶
炼中的反应之一为 。
(1)基态 的核外电子排布式为___________,铜元素的焰色为绿色,产生此焰色过程中电子会
___________(填“吸收”或“释放”)出能量;上述反应涉及的几种元素中,第一电离能由大到小的顺序是
___________。
(2) (八元环状结构)、 、 、 、 五种粒子中每个原子均达到8电子稳定结构,则中心原子
杂化类型为 的是___________, 的立体构型为___________,属于非极性分子的是___________。
(3)已知 、 的熔点分别为 、 ,导致这种差异的主要原因是___________,热稳定性:
,从结构角度上看,其原因是___________。
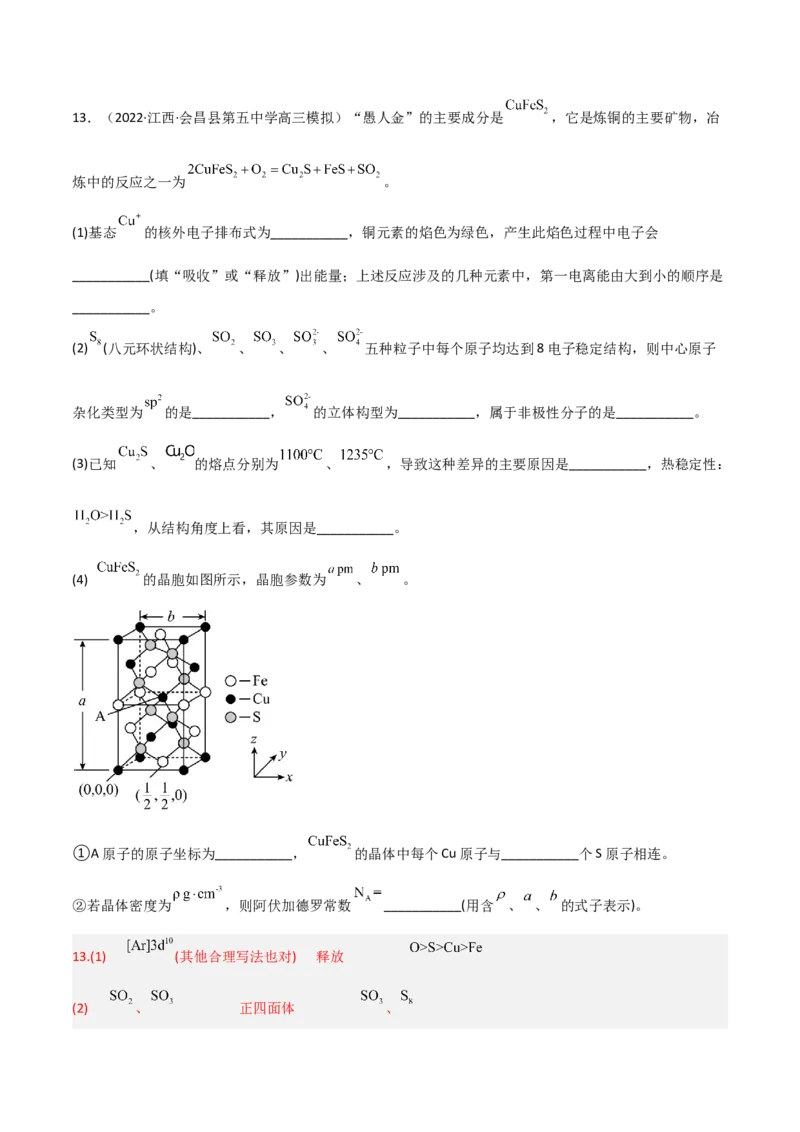
(4) 的晶胞如图所示,晶胞参数为 、 。
①A原子的原子坐标为___________, 的晶体中每个Cu原子与___________个S原子相连。
②若晶体密度为 ,则阿伏加德罗常数 ___________(用含 、 、 的式子表示)。
13.(1) (其他合理写法也对) 释放
(2) 、 正四面体 、(3) 两种物质均是离子晶体,离子所带电荷数相同,但半径: ,故 中离子键较强 键
能: 键 键
(4) 4
解析:(1)Cu+是Cu失去4s1上的电子后形成的,Cu的核外电子排布式为1s22s22p63s23p63d104s1,故Cu+的
电子排布式为 。焰色为发射光谱,粒子从激发态到基态,能量通过光能释放,从而产生焰色。由
第一电离能递变规律及非金属元素的第一电离能通常比金属元素的大知,几种元素第一电离能大小顺序为
。答案为 、释放、 。
(2) 中每个硫原子形成了2个σ键,另有2个孤电子对,硫为sp3杂化,属于非极性分子; 、
中硫原子均有4个价层电子对,均为sp3杂化, 为正四面体结构;SO 、SO 中硫原子各有3个价层电子
2 3
对,均为sp2杂化,前者的立体构型为V形,为极性分子,后者的立体构型为平面三角形,为非极性分子。
答案为SO SO 、正四面体、SO S 。
2 3 3 8
(3)Cu S、Cu O均是离子晶体,离子间是靠离子键结合在一起的,离子所带的电荷数相同,但半径:
2 2
,故Cu O中离子键较强,Cu O的熔点高。分子的热稳定性是由键能的相对大小决定的,键能越大
2 2
分子越稳定, 键键长比 键键长短,键能大,故热稳定性: 。
(4)①由已经给出的两个原子坐标及 原子的位置知其原子坐标为 。观察晶胞图知,位于面上
的铜原子与一个晶胞内的2个硫原子相连,面上的原子为两个晶胞共用,故晶体中每个铜原子与4个硫原
子相连。观察晶胞图知,晶胞中有4个“CuFeS ”,质量为 ,晶胞的体积为 ,
2, 。