文档内容
高频考点 39 晶体结构与性质
1.(2022·北京卷)由键能数据大小,不能解释下列事实的是( )
化学键
键能/ 411 318 799 358 452 346 222
A.稳定性: B.键长:
C.熔点: D.硬度:金刚石>晶体硅
2.(2021·天津卷)下列各组物质的晶体类型相同的是( )
A.SiO 和SO B.I 和NaCl C.Cu和Ag D.SiC和MgO
2 3 2
3.(2021·海南卷)关于 性质的解释合理的是( )
选项 性质 解释
A 比 容易液化 分子间的范德华力更大
B 熔点高于 键的键能比 大
能与 以配位键结
C 中氮原子有孤电子对
合
D 氨水中存在 是离子化合物
A.A B.B C.C D.D
4.(2021·湖北卷)某立方晶系的锑钾(Sb—K)合金可作为钾离子电池的电极材料,图a为该合金的晶胞结
构图,图b表示晶胞的一部分。下列说法正确的是( )
A.该晶胞的体积为a3×10-36cm-3 B.K和Sb原子数之比为3∶1C.与Sb最邻近的K原子数为4 D.K和Sb之间的最短距离为 apm
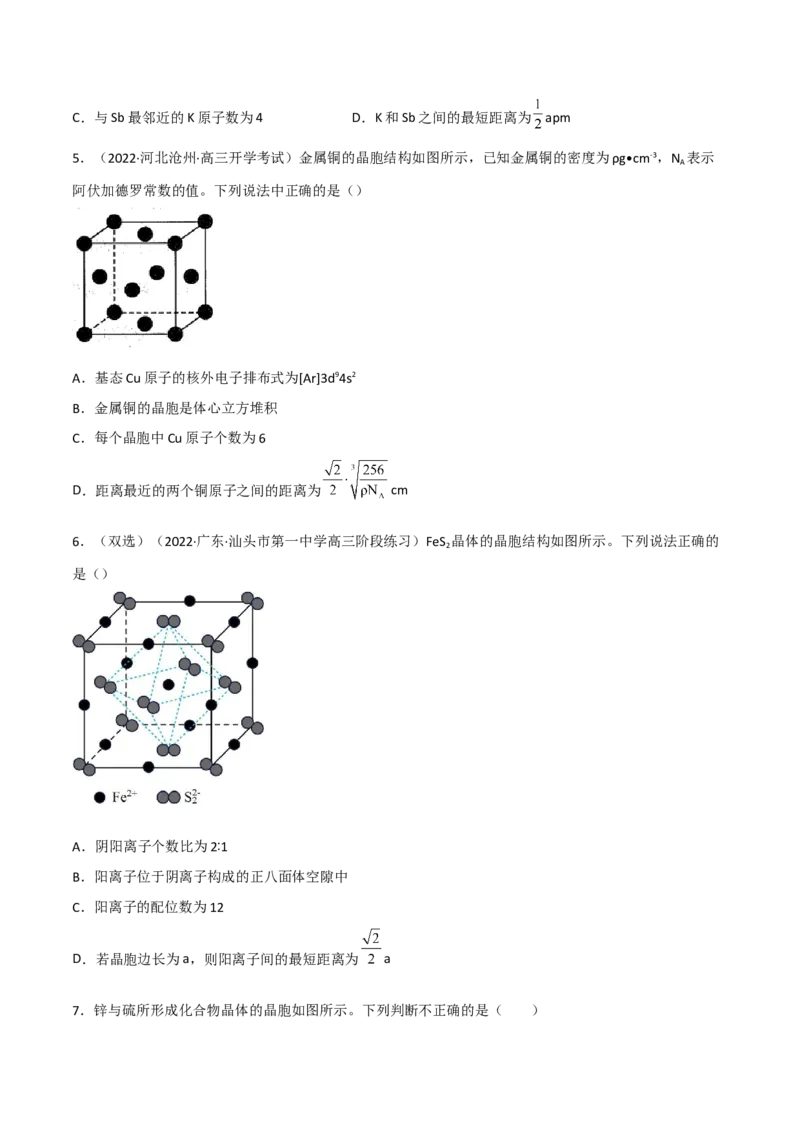
5.(2022·河北沧州·高三开学考试)金属铜的晶胞结构如图所示,已知金属铜的密度为ρg•cm-3,N 表示
A
阿伏加德罗常数的值。下列说法中正确的是()
A.基态Cu原子的核外电子排布式为[Ar]3d94s2
B.金属铜的晶胞是体心立方堆积
C.每个晶胞中Cu原子个数为6
D.距离最近的两个铜原子之间的距离为 cm
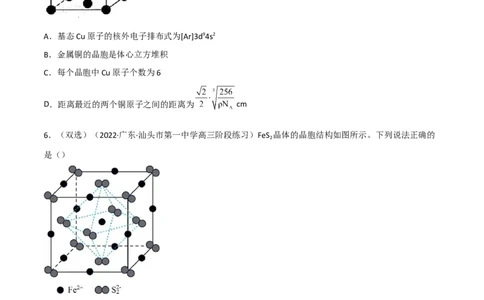
6.(双选)(2022·广东·汕头市第一中学高三阶段练习)FeS 晶体的晶胞结构如图所示。下列说法正确的
2
是()
A.阴阳离子个数比为2∶1
B.阳离子位于阴离子构成的正八面体空隙中
C.阳离子的配位数为12
D.若晶胞边长为a,则阳离子间的最短距离为 a
7.锌与硫所形成化合物晶体的晶胞如图所示。下列判断不正确的是( )A.氧化锌的熔点低于硫化锌 B.该晶胞中 和 数目相等
C.晶胞中 周围最靠近的 共有4个 D.该晶体属于离子晶体
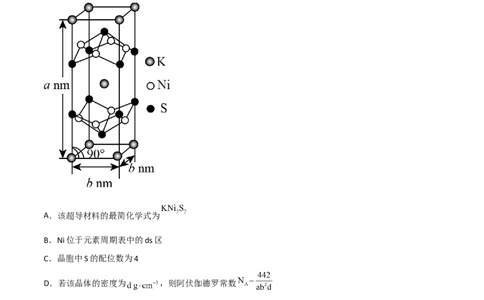
8.(双选))某超导材料属于离子晶体,其晶胞结构如图所示。下列说法正确的是()
A.该超导材料的最简化学式为
B.Ni位于元素周期表中的ds区
C.晶胞中S的配位数为4
D.若该晶体的密度为 ,则阿伏伽德罗常数
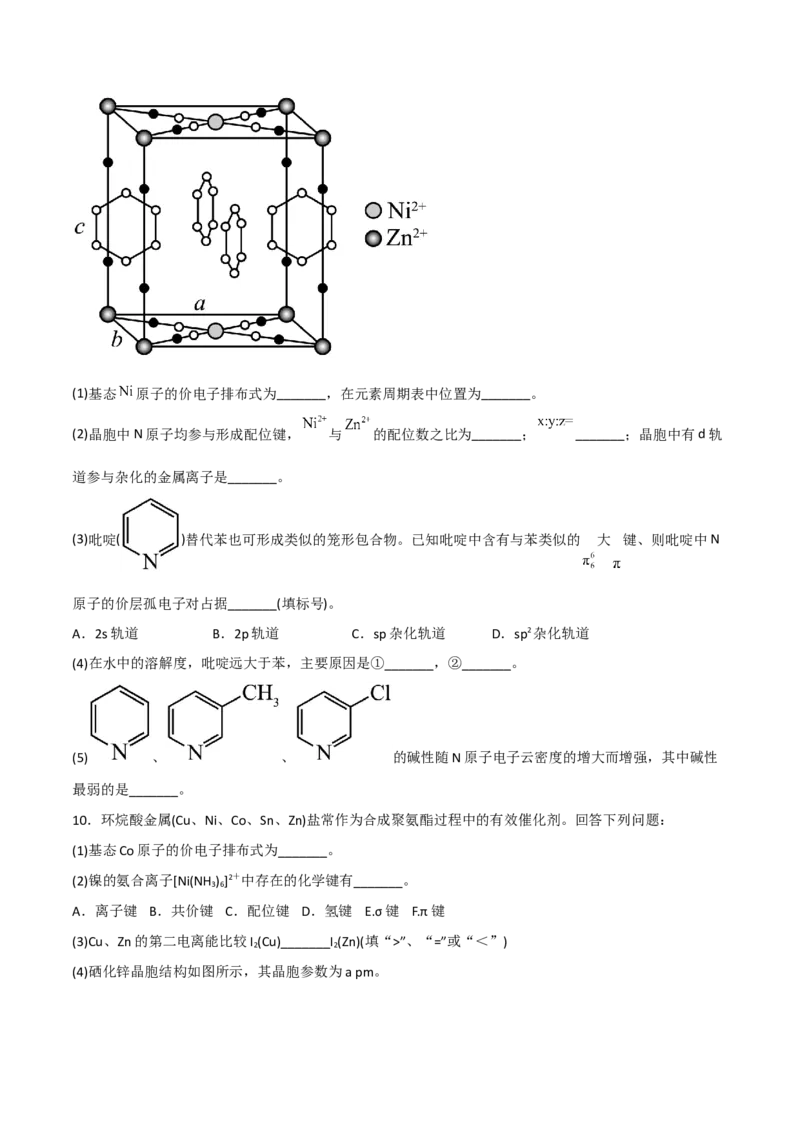
9.(2022·山东卷)研究笼形包合物结构和性质具有重要意义。化学式为 的笼形
包合物四方晶胞结构如图所示(H原子未画出),每个苯环只有一半属于该晶胞。晶胞参数为
。回答下列问题:(1)基态 原子的价电子排布式为_______,在元素周期表中位置为_______。
(2)晶胞中N原子均参与形成配位键, 与 的配位数之比为_______; _______;晶胞中有d轨
道参与杂化的金属离子是_______。
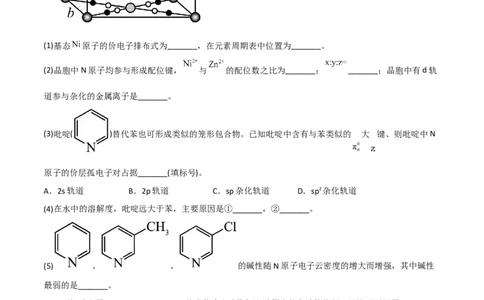
(3)吡啶( )替代苯也可形成类似的笼形包合物。已知吡啶中含有与苯类似的 大 键、则吡啶中N
原子的价层孤电子对占据_______(填标号)。
A.2s轨道 B.2p轨道 C.sp杂化轨道 D.sp2杂化轨道
(4)在水中的溶解度,吡啶远大于苯,主要原因是①_______,②_______。
(5) 、 、 的碱性随N原子电子云密度的增大而增强,其中碱性
最弱的是_______。
10.环烷酸金属(Cu、Ni、Co、Sn、Zn)盐常作为合成聚氨酯过程中的有效催化剂。回答下列问题:
(1)基态Co原子的价电子排布式为_______。
(2)镍的氨合离子[Ni(NH ) ]2+中存在的化学键有_______。
3 6
A.离子键 B.共价键 C.配位键 D.氢键 E.σ键 F.π键
(3)Cu、Zn的第二电离能比较I (Cu)_______I (Zn)(填“>”、“=”或“<”)
2 2
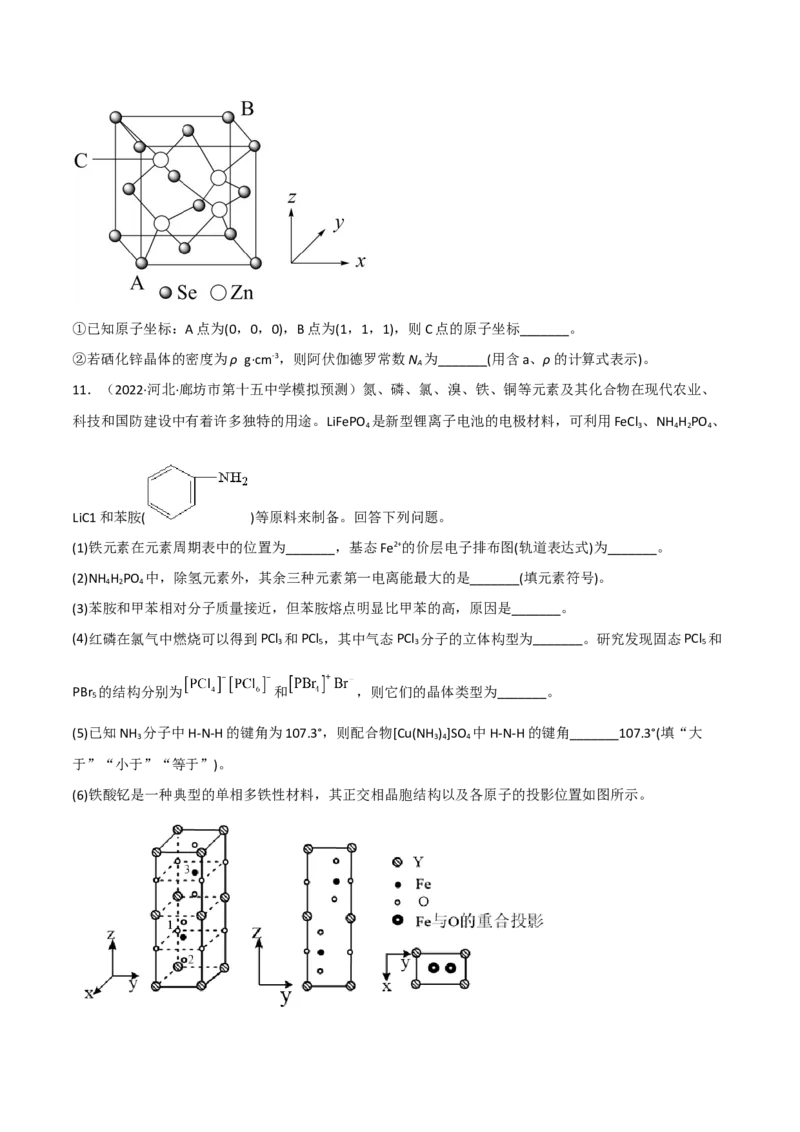
(4)硒化锌晶胞结构如图所示,其晶胞参数为a pm。①已知原子坐标:A点为(0,0,0),B点为(1,1,1),则C点的原子坐标_______。
②若硒化锌晶体的密度为ρ g·cm-3,则阿伏伽德罗常数N 为_______(用含a、ρ的计算式表示)。
A
11.(2022·河北·廊坊市第十五中学模拟预测)氮、磷、氯、溴、铁、铜等元素及其化合物在现代农业、
科技和国防建设中有着许多独特的用途。LiFePO 是新型锂离子电池的电极材料,可利用FeCl 、NH H PO 、
4 3 4 2 4
LiC1和苯胺( )等原料来制备。回答下列问题。
(1)铁元素在元素周期表中的位置为_______,基态Fe2+的价层电子排布图(轨道表达式)为_______。
(2)NH H PO 中,除氢元素外,其余三种元素第一电离能最大的是_______(填元素符号)。
4 2 4
(3)苯胺和甲苯相对分子质量接近,但苯胺熔点明显比甲苯的高,原因是_______。
(4)红磷在氯气中燃烧可以得到PCl 和PCl ,其中气态PCl 分子的立体构型为_______。研究发现固态PCl 和
3 5 3 5
PBr 的结构分别为 和 ,则它们的晶体类型为_______。
5
(5)已知NH 分子中H-N-H的键角为107.3°,则配合物[Cu(NH ) ]SO 中H-N-H的键角_______107.3°(填“大
3 3 4 4
于”“小于”“等于”)。
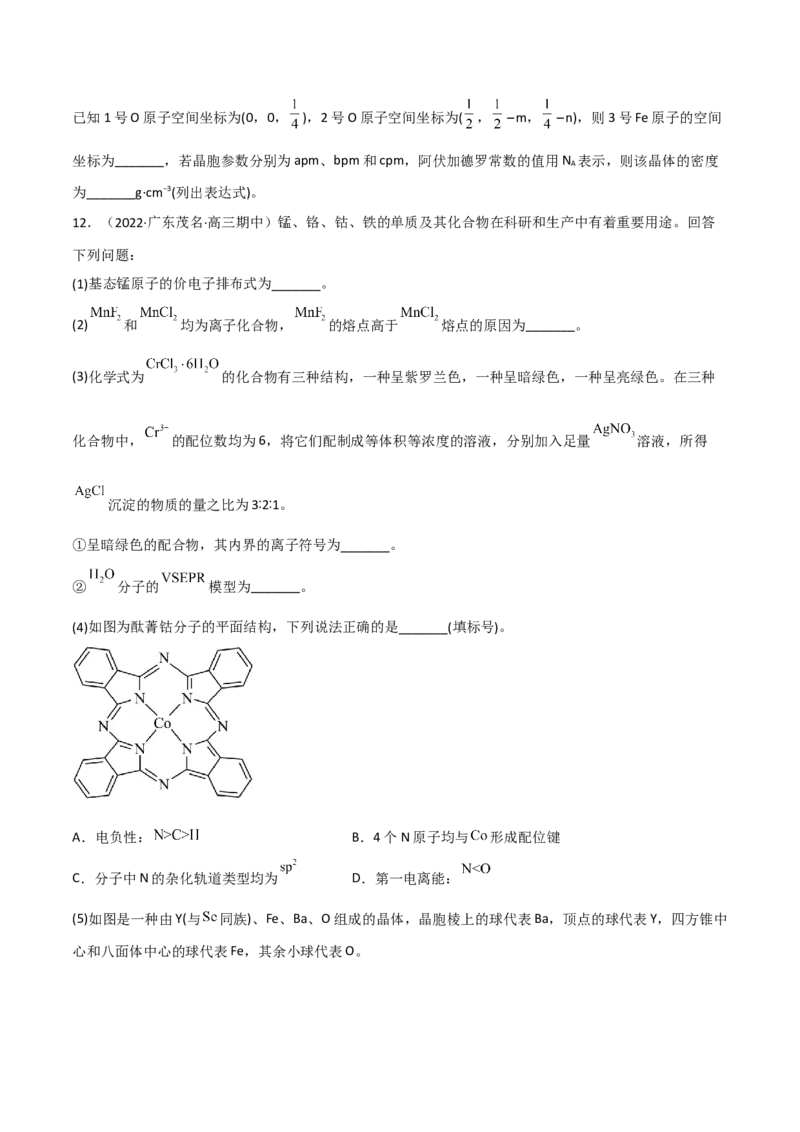
(6)铁酸钇是一种典型的单相多铁性材料,其正交相晶胞结构以及各原子的投影位置如图所示。已知1号O原子空间坐标为(0,0, ),2号O原子空间坐标为( , −m, −n),则3号Fe原子的空间
坐标为_______,若晶胞参数分别为apm、bpm和cpm,阿伏加德罗常数的值用N 表示,则该晶体的密度
A
为_______g·cm−3(列出表达式)。
12.(2022·广东茂名·高三期中)锰、铬、钴、铁的单质及其化合物在科研和生产中有着重要用途。回答
下列问题:
(1)基态锰原子的价电子排布式为_______。
(2) 和 均为离子化合物, 的熔点高于 熔点的原因为_______。
(3)化学式为 的化合物有三种结构,一种呈紫罗兰色,一种呈暗绿色,一种呈亮绿色。在三种
化合物中, 的配位数均为6,将它们配制成等体积等浓度的溶液,分别加入足量 溶液,所得
沉淀的物质的量之比为3∶2∶1。
①呈暗绿色的配合物,其内界的离子符号为_______。
② 分子的 模型为_______。
(4)如图为酞菁钴分子的平面结构,下列说法正确的是_______(填标号)。
A.电负性: B.4个N原子均与 形成配位键
C.分子中N的杂化轨道类型均为 D.第一电离能:
(5)如图是一种由Y(与 同族)、Fe、Ba、O组成的晶体,晶胞棱上的球代表Ba,顶点的球代表Y,四方锥中
心和八面体中心的球代表Fe,其余小球代表O。①该晶体的化学式为_______。
②其中Y的配位数为_______。
③在氧气气氛中该晶体可被部分氧化,氧原子进入晶格而使晶体呈现深紫色。新进入的氧原子在晶胞中的
位置是_______。
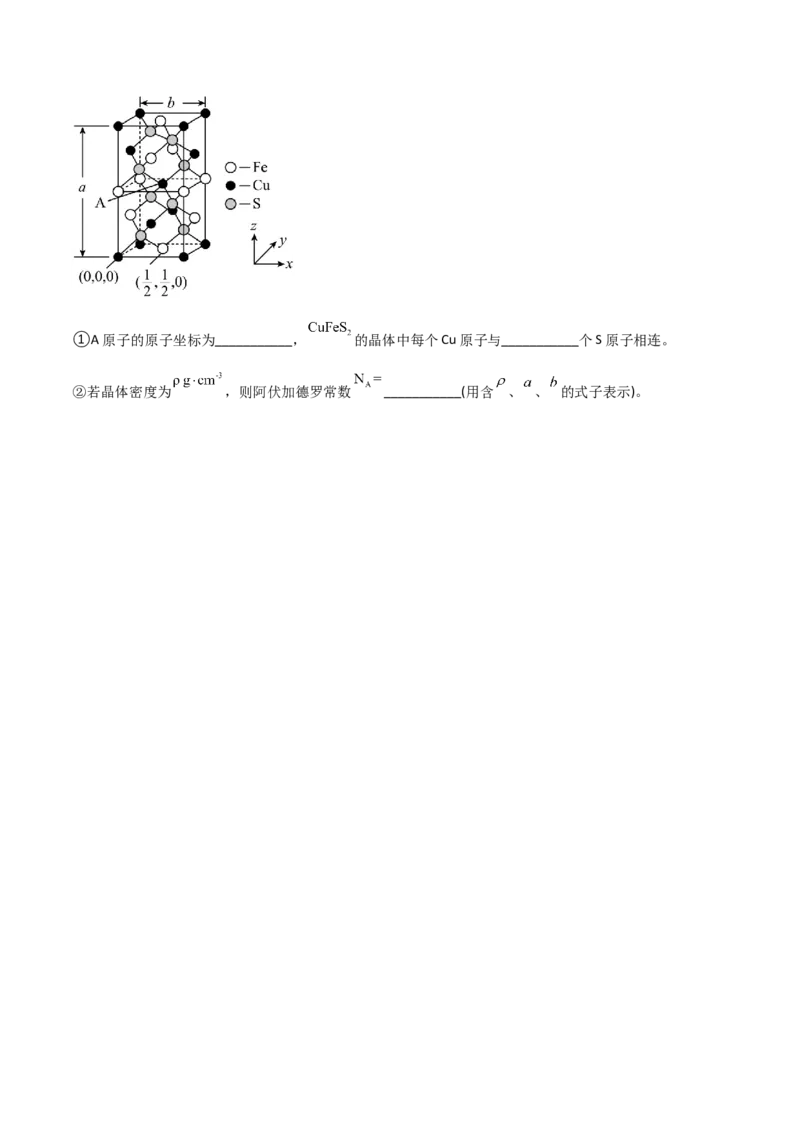
13.(2022·江西·会昌县第五中学高三模拟)“愚人金”的主要成分是 ,它是炼铜的主要矿物,冶
炼中的反应之一为 。
(1)基态 的核外电子排布式为___________,铜元素的焰色为绿色,产生此焰色过程中电子会
___________(填“吸收”或“释放”)出能量;上述反应涉及的几种元素中,第一电离能由大到小的顺序是
___________。
(2) (八元环状结构)、 、 、 、 五种粒子中每个原子均达到8电子稳定结构,则中心原子
杂化类型为 的是___________, 的立体构型为___________,属于非极性分子的是___________。
(3)已知 、 的熔点分别为 、 ,导致这种差异的主要原因是___________,热稳定性:
,从结构角度上看,其原因是___________。
(4) 的晶胞如图所示,晶胞参数为 、 。①A原子的原子坐标为___________, 的晶体中每个Cu原子与___________个S原子相连。
②若晶体密度为 ,则阿伏加德罗常数 ___________(用含 、 、 的式子表示)。