文档内容
高频考点 38 分子结构与性质
1.(2022·湖北卷)磷酰三叠氮是一种高能分子,结构简式为 。下列关于该分子的说法正确的
是( )
A.为非极性分子 B.立体构型为正四面体形
C.加热条件下会分解并放出 D.分解产物 的电子式为
1.C A.磷酰三叠氮分子不是对称结构,分子中的正负电荷重心是不重合的,是极性分子,A项错误;B.
磷酰三叠氮分子含有三个P-N键及一个P=O双键,则立体构型为四面体构型,B项错误;C.磷酰三叠氮是
一种高能分子,加热条件下会分解并放出 ,C项正确;D. 为共价化合物,则电子式为 ,
D项错误;答案选C。
2.(双选)(2022·海南卷)已知 , 的酸性比
强。下列有关说法正确的是( )
A.HCl的电子式为 B.Cl-Cl键的键长比I-I键短
C. 分子中只有σ键 D. 的酸性比 强
2.BD A.HCl为共价化合物,H原子和Cl原子间形成共用电子对,其电子式为 ,A错误;B.原子
半径Cl<I,故键长:Cl—Cl<I—I,B正确;C.CH COOH分子中,羧基的碳氧双键中含有π键,C错误;
3
D.电负性Cl>I,-Cl能使-COOH上的H原子具有更大的活动性,因此ClCH COOH的酸性比ICH COOH强,D
2 2
正确;答案选BD。
3.(2021·江苏卷)N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产HNO ;
2 3 3
HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反应生成
3 2 2
NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO 和水体中过量
2 2 2 x的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化为N ,也可将水体
2
中的NO -转化为N 。下列有关NH 、NH 、NO 的说法正确的是( )
3 2 3
A.NH 能形成分子间氢键
3
B.NO 的空间构型为三角锥形
C.NH 与NH 中的键角相等
3
D.NH 与Ag+形成的[Ag(NH ) ]+中有6个配位键
3 3 2
3.A A.NH 能形成分子间氢键,氨分子是一个极性分子,氮原子带有部分负电荷,氢原子带有部分正电荷,
3
当氨分子互相靠近时,由于取向力的作用,带有部分正电荷的氢原子与另外一个氨分子中的带有部分负电
荷的氮原子发生异性电荷的吸引进一步靠拢,A正确;B.硝酸根离子的空间构型是个标准的正三角形,N
在中间,O位于三角形顶点,N和O都是sp2杂化,B错误;C.NH 和NH 都是sp3杂化,但NH 中存在一
3 3
个孤电子对,是三角锥结构,而NH 为标准的正四面体,所以键角是不一样的,NH 中每两个N—H键之间
3
夹角为107°18',正四面体为109°28',C错误;D.N-H为σ键,配位键也为σ键,则[Ag(NH ) ]+中含有8
3 2
个σ键,2个配位键,D错误;答案选A。
4.(2021·湖北卷)下列有关N、P及其化合物的说法错误的是( )
A.N的电负性比P的大,可推断NCl 分子的极性比PCl 的大
3 3
B.N与N的π键比P与P的强,可推断N≡N的稳定性比P≡P的高
C.NH 的成键电子对间排斥力较大,可推断NH 的键角比PH 的大
3 3 3
D.HNO 的分子间作用力较小,可推断HNO 的熔点比H PO 的低
3 3 3 4
4.A A.P和Cl的电负性差值比N和Cl的电负性差值大,因此PCl 分子的极性比NCl 分子极性大,A项错
3 3
误;B.N与N的 键比P与P的强,故 的稳定性比 的高,B项正确;C.N的电负性比P大,
NH 中成键电子对距离N比PH 中成键电子对距离P近,NH 中成键电子对间的斥力大,因此NH 的键角比
3 3 3 3
PH 的大,C项正确;
3
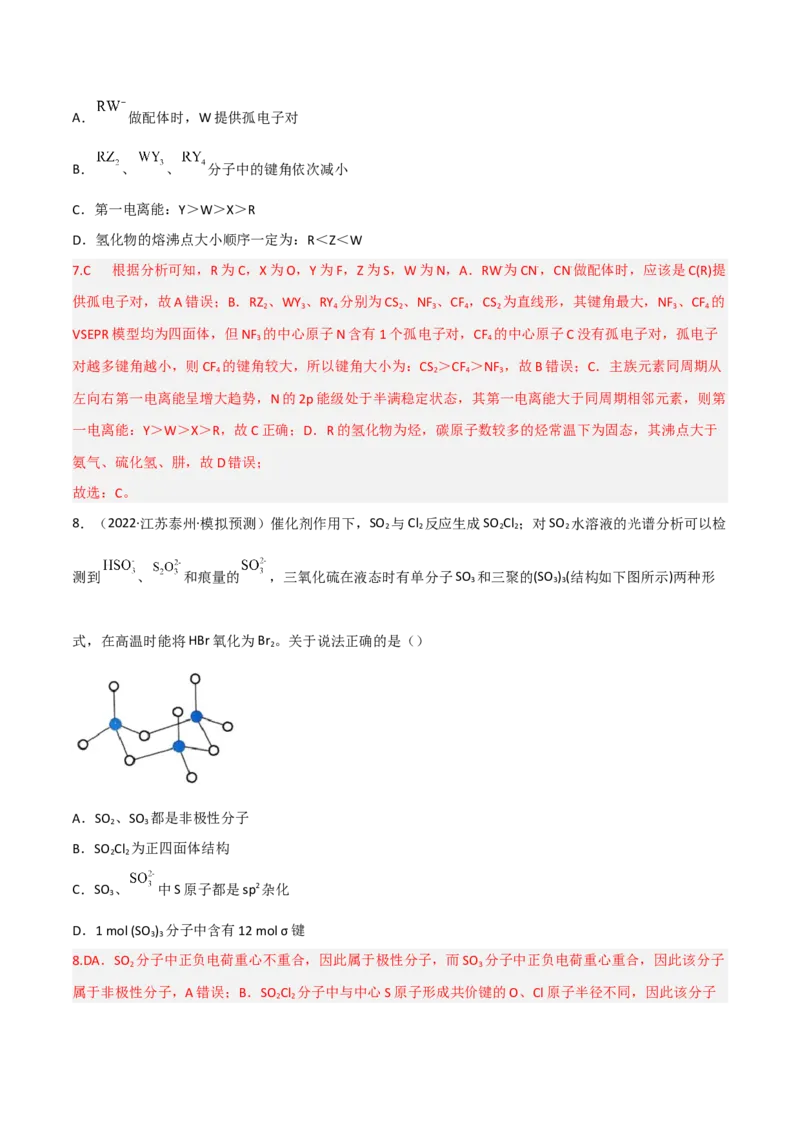
D.相对分子质量:HNO 一氯乙烯>一氯乙炔 Cl参与形成的大π键越多,形成的C-Cl键的键长越
短
(3) CsCl CsCl为离子晶体,ICl为分子晶体
(4) 电解质
解析:(1)F的原子序数为9,其基态原子电子排布式为1s22s22p5,a.1s22s22p43s1,基态氟原子2p能级
上的1个电子跃迁到3s能级上,属于氟原子的激发态,a正确;b.1s22s22p43d2,核外共10个电子,不是
氟原子,b错误;
c.1s22s12p5,核外共8个电子,不是氟原子,c错误;d.1s22s22p33p2,基态氟原子2p能级上的2个电子
跃迁到3p能级上,属于氟原子的激发态,d正确;
答案选ad;而同一原子3p能级的能量比3s能级的能量高,因此能量最高的是1s22s22p33p2,答案选d;(2)①一氯乙烯的结构式为 ,碳为双键碳,采取sp2杂化,因此C的一个sp2杂化轨道与Cl的
3p 轨道形成C-Clσ键;
x
②C的杂化轨道中s成分越多,形成的C-Cl键越强,C-Cl键的键长越短,一氯乙烷中碳采取sp3杂化,一氯
乙烯中碳采取sp2杂化,一氯乙炔中碳采取sp杂化,sp杂化时p成分少,sp3杂化时p成分多,因此三种物
质中C-Cl键键长顺序为:一氯乙烷>一氯乙烯>一氯乙炔,同时Cl参与形成的大π键越多,形成的C-Cl键的
键长越短,一氯乙烯中Cl的3p 轨道与C的2p 轨道形成3中心4电子的大π键( ),一氯乙炔中Cl的3p
z z z
轨道与C的2p 轨道形成2套3中心4电子的大π键( ),因此三种物质中C-Cl键键长顺序为:一氯乙烷>
z
一氯乙烯>一氯乙炔;
(3)CsICl 发生非氧化还原反应,各元素化合价不变,生成无色晶体和红棕色液体,则无色晶体为CsCl,
2
红棕色液体为ICl,而CsCl为离子晶体,熔化时,克服的是离子键,ICl为分子晶体,熔化时,克服的是分
子间作用力,因此CsCl的熔点比ICl高;
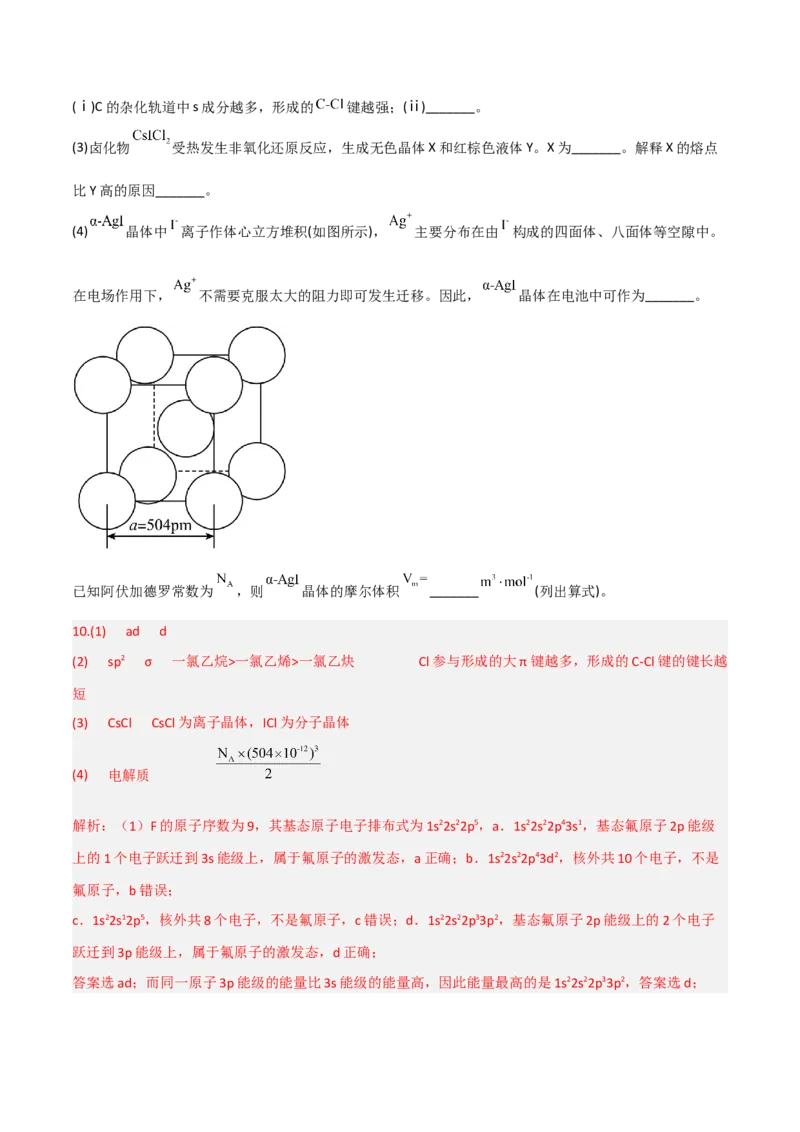
(4)由题意可知,在电场作用下,Ag+不需要克服太大阻力即可发生迁移,因此α-AgI晶体是优良的离子导
体,在电池中可作为电解质;每个晶胞中含碘离子的个数为8 +1=2个,依据化学式AgI可知,银离子个
数也为2个,晶胞的物质的量n= mol= mol,晶胞体积V=a3pm3=(504 10-12)3m3,则α-AgI晶体的摩尔
体积V = = = m3/mol。
m
11.(2022·海南·高三专题练习)材料是人类进步的基石,深入认识物质的结构有助于进一步开发新的材
料。回答下列问题:
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl 。杂化前,处于激发态的B原子
3
的价电子轨道表示式为_______ ( 选填标号)。
A. B.C. D.
(2)已知:第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色。下列离子形成的水合
离子为无色的是_______。
A.Sc3+ B.Cr3+ C.Fe3+ D.Zn2+
(3)K [Fe(CN) ]中所含元素电负性由大到小的顺序为_______,lmol K [Fe(CN) ]含有_______ molσ键;Ti3+能形
3 6 3 6
成化合物[TiCl(H O) ]Cl ·H O,该化合物中Ti3+的配位数为_______。
2 5 2 2
(4)Ni(CO) 常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl 、苯等有机溶剂的原因:
4 4
_______。
(5)纯水电离产生H O+、OH-,研究发现在某些水溶液中还存在 、 等微粒。
3
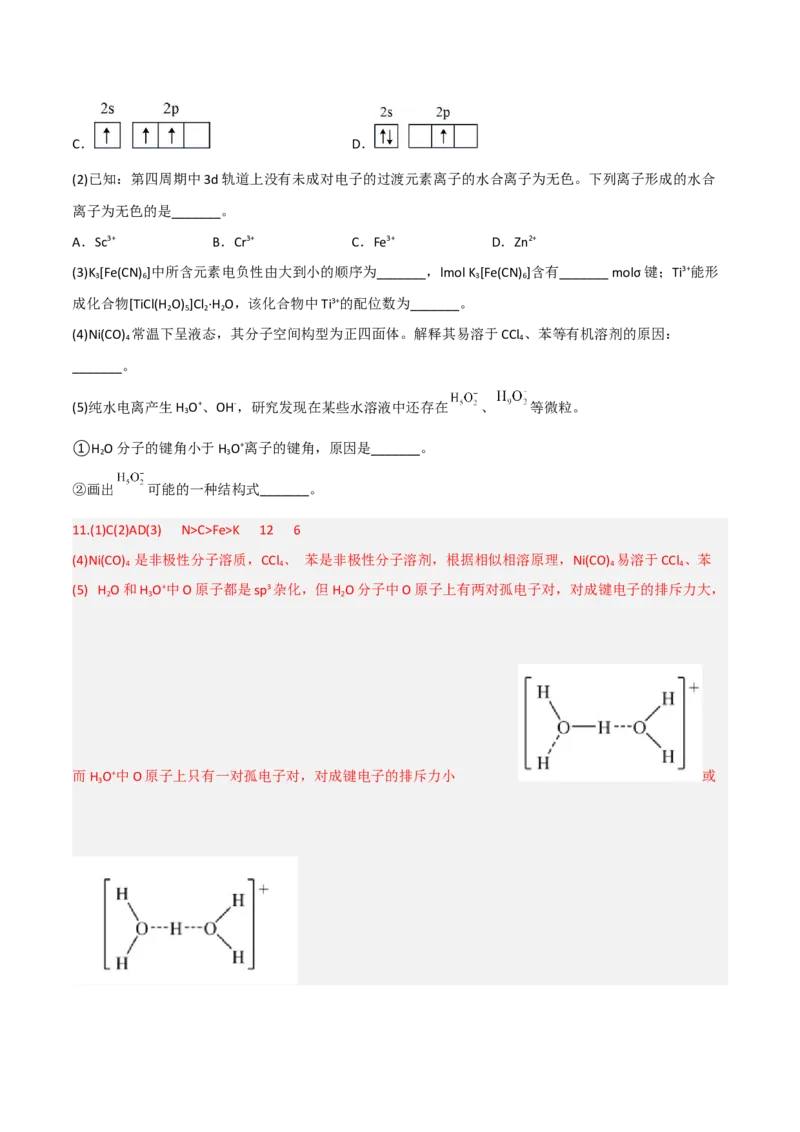
①H O分子的键角小于H O+离子的键角,原因是_______。
2 3
②画出 可能的一种结构式_______。
11.(1)C(2)AD(3) N>C>Fe>K 12 6
(4)Ni(CO) 是非极性分子溶质,CCl 、 苯是非极性分子溶剂,根据相似相溶原理,Ni(CO) 易溶于CCl 、苯
4 4 4 4
(5) H O和H O+中O原子都是sp3杂化,但H O分子中O原子上有两对孤电子对,对成键电子的排斥力大,
2 3 2
而H O+中O原子上只有一对孤电子对,对成键电子的排斥力小 或
3(6)
解析:(1)按照杂化轨道理论,基态B原子的价电子2s22p1先激发,再杂化组成sp2三个杂化轨道,成键形成
BCl 。杂化前,处于激发态的B原子的价电子轨道表示式为C. ,故答案为:C;
3
(2)A. Sc3+核外电子排布是:1s22s22p63s23p6,没有3d电子,则其水合离子为无颜色;B. Cr3+核外电子排布是:
1s22s22p63s23p63d3,有未成对d电子,其水合离子为有颜色;C. Fe3+核外电子排布是:1s22s22p63s23p63d5,
有未成对d电子,其水合离子为有颜色; D. Zn2+核外电子排布是:1s22s22p63s23p63d10,没有未成对d电子,
其水合离子为无色;故答案为:AD;
(3)周期表中同主族从下到上,同周期从左到右,元素的非金属性增强,电负性增大,K [Fe(CN) ]中所含元
3 6
素电负性由大到小的顺序为N>C>Fe>K,K [Fe(CN) ]分子中铁和CN-形成6个配位键,6个C-N共价键,lmol
3 6
K [Fe(CN) ]含有12 molσ键;Ti3+能形成化合物[TiCl(H O) ]Cl ·H O,该化合物中Ti3+的配位数为5+1=6。故答案
3 6 2 5 2 2
为:N>C>Fe>K;12;6;
(4)Ni(CO) 常温下呈液态,其分子空间构型为正四面体,说明Ni(CO) 属于分子晶体。其易溶于CCl 、苯等有
4 4 4
机溶剂的原因:Ni(CO) 是非极性分子溶质,CCl 、 苯是非极性分子溶剂,根据相似相溶原理,Ni(CO) 易溶
4 4 4
于CCl 、苯。故答案为:Ni(CO) 是非极性分子溶质,CCl 、 苯是非极性分子溶剂,根据相似相溶原理,
4 4 4
Ni(CO) 易溶于CCl 、苯;
4 4
(5)①H O分子的键角小于H O+离子的键角,原因是H O和H O+中O原子都是sp3杂化,但H O分子中O原
2 3 2 3 2
子上有两对孤电子对,对成键电子的排斥力大,而H O+中O原子上只有一对孤电子对,对成键电子的排斥
3
力小。故答案为:H O和H O+中O原子都是sp3杂化,但H O分子中O原子上有两对孤电子对,对成键电
2 3 2
子的排斥力大,而H O+中O原子上只有一对孤电子对,对成键电子的排斥力小;
3
②画出 可能的一种结构式 或 。
12. 以 、ZnO等半导体材料制作的传感器和芯片具有能耗低、效率高的优势。回答问题:
(1)基态O原子的电子排布式_______,其中未成对电子有_______个。
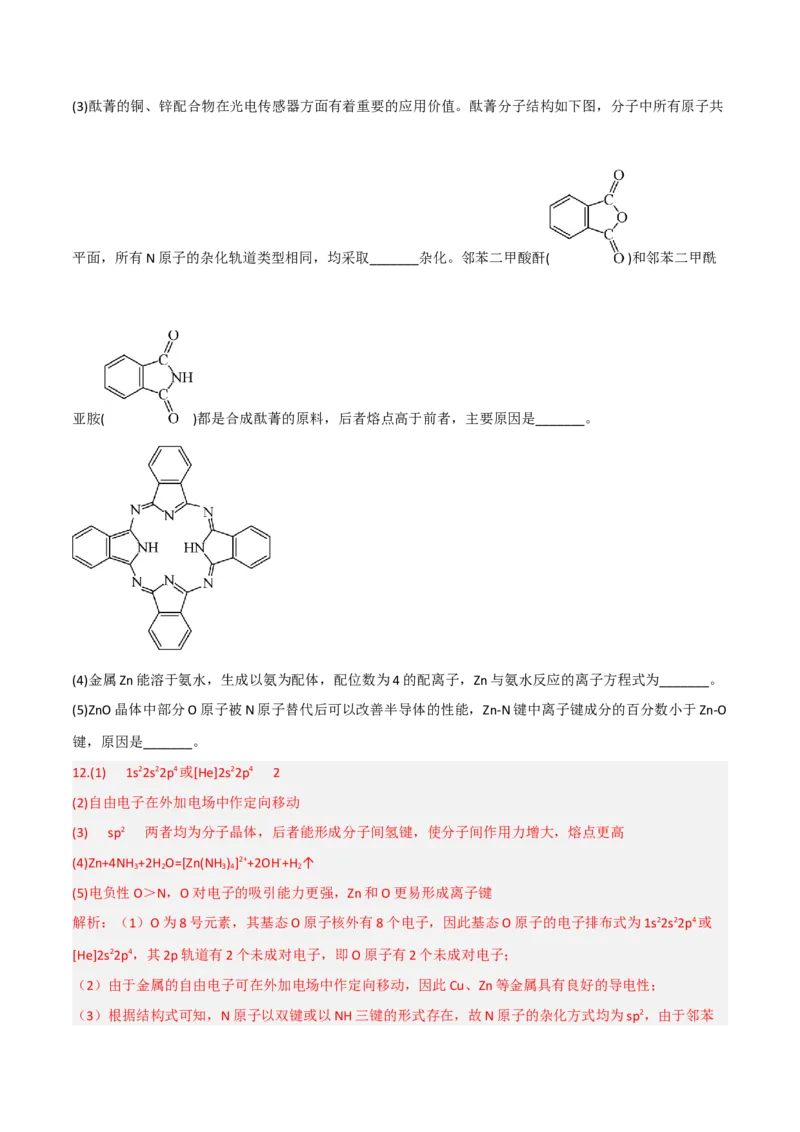
(2)Cu、Zn等金属具有良好的导电性,从金属键的理论看,原因是_______。(3)酞菁的铜、锌配合物在光电传感器方面有着重要的应用价值。酞菁分子结构如下图,分子中所有原子共
平面,所有N原子的杂化轨道类型相同,均采取_______杂化。邻苯二甲酸酐( )和邻苯二甲酰
亚胺( )都是合成酞菁的原料,后者熔点高于前者,主要原因是_______。
(4)金属Zn能溶于氨水,生成以氨为配体,配位数为4的配离子,Zn与氨水反应的离子方程式为_______。
(5)ZnO晶体中部分O原子被N原子替代后可以改善半导体的性能,Zn-N键中离子键成分的百分数小于Zn-O
键,原因是_______。
12.(1) 1s22s22p4或[He]2s22p4 2
(2)自由电子在外加电场中作定向移动
(3) sp2 两者均为分子晶体,后者能形成分子间氢键,使分子间作用力增大,熔点更高
(4)Zn+4NH +2H O=[Zn(NH ) ]2++2OH-+H ↑
3 2 3 4 2
(5)电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键
解析:(1)O为8号元素,其基态O原子核外有8个电子,因此基态O原子的电子排布式为1s22s22p4或
[He]2s22p4,其2p轨道有2个未成对电子,即O原子有2个未成对电子;
(2)由于金属的自由电子可在外加电场中作定向移动,因此Cu、Zn等金属具有良好的导电性;
(3)根据结构式可知,N原子以双键或以NH三键的形式存在,故N原子的杂化方式均为sp2,由于邻苯二甲酸酐和邻苯二甲酰亚胺均为分子晶体,而后者能形成分子间氢键,使分子间作用力增大,因此熔点更
高;
(4)金属Zn与氨水反应可生成[Zn(NH ) ](OH) 和H ,反应的离子方程式为Zn+4NH +2H O=[Zn(NH ) ]2++2OH-
3 4 2 2 3 2 3 4
+H ↑;
2
(5)由于电负性O>N,O对电子的吸引能力更强,Zn和O更易形成离子键,因此Zn—N键中离子键成分
的百分数小于Zn—O键;