文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N14 O 16 F 19 Al 27 Si 28 Cl 35.5 Co 59
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.2023年5月10日,我国天舟六号发射成功,空间站建设过程中化学学科发挥着重要作用,下列有关叙
述错误的是
A.核心舱离子推进器用氙气作为推进剂,氙位于元素周期表0族
B.机械臂用到的铝合金、钛合金属于金属材料
C.实验舱采用砷化镓( )太阳能电池,砷和镓位于元素周期表第四周期
D.宇航服用到的聚酰胺纤维属于天然有机高分子材料
2.西汉长信宫灯通高48厘米,通体鎏金,是河北博物院收藏的珍贵文物。鎏金又称火法镀金,其工艺是
将黄金溶于汞中形成的金汞齐均匀地涂到干净的金属器物表面,加热使汞挥发,黄金与金属表面固结,
形成光亮的金黄色镀层。已知铜和金是第ⅠB族元素,汞是第ⅡB族元素。下列说法错误的是
A.铜、金、汞均为ds区元素
B.常温下的金汞齐是金属晶体
C.应将宫灯保存在干燥的环境中
D.铜腐蚀后生成的 属于盐
3.7−羟基香豆素是香豆素家族的天然产物,是一种荧光化合物,可用作防晒剂和药物;它的结构简式如
图所示。下列说法错误的是
A.分子式为C HO
9 6 3
B.该物质的官能团是碳碳双键、羟基、酯基
C.1 mol该物质与足量H 反应,最多消耗4 mol H
2 2
D.该物质不能发生取代反应
4.能正确表示下列反应的离子方程式为
A.臭碱(硫化钠)溶液中滴加足量的稀硝酸:S2−+2H+=H S↑
2
B.氯化铝溶液中通入过量的氨气:Al3++4NH+4H O= +4NH
3 2
C.石钟乳(CaCO)溶于醋酸:CaCO +2H+=Ca2++H O+CO↑
3 3 2 2
D.1.5 mol Cl 通入到含1 mol FeI 的溶液中:2Fe2++4I−+3Cl=2Fe3++6Cl−+2I
2 2 2 2
5.下列由实验操作及现象所得结论正确的是
选项 实验操作和现象 实验结论将适量蔗糖与稀硫酸反应,加热后加碱中和,再加
A 证明蔗糖完全水解
入新制Cu(OH) 浊液加热,有红色沉淀生成
2
向2 mL 0.1 mol·L−1硝酸银溶液中,加入1 mL等浓
B 度NaCl溶液,出现白色沉淀,再加入几滴等浓度的 K (AgCl)>K (Ag S)
sp sp 2
NaS溶液,有黑色沉淀生成
2
某溶液中加盐酸,产生使澄清石灰水变浑浊的无色
C 原溶液中一定存在
无味气体
向碘水中加入等体积CCl ,振荡后静置,上层接近 I 在CCl 中的溶解度大于
4 2 4
D
无色,下层显紫红色 在水中的溶解度
6.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.1 mol金属钠生成NaO,转移的电子数为2N
2 2 A
B.60 g二氧化硅晶体中含有N 个SiO 分子
A 2
C.乙烯和丙烯的混合物共28 g,含有的氢原子数为4N
A
D.由1 mol CHCOONa和少量CHCOOH形成的中性溶液中,CHCOO−数目小于N
3 3 3 A
7.用下图所示装置及药品进行实验,能达到对应实验目的的是
A.检查装置的气密 B.实验室制 C.配制一定物质的量浓 D.制备 胶
性 取氯气 度的硫酸
体
8.TCCA是一种高效消毒剂,由原子序数依次增大的W、X、Y、Z四种元素构成,且位于两个不同短周
期。W元素的K层电子数与其p能级上的电子数相等,基态Y原子s能级电子总数与p能级电子总数
相等,其原子半径小于W原子,Z元素的原子半径为同周期主族元素最小。下列叙述正确的是
A.电负性大小:X>Y>W
B.简单离子半径:Z>Y>X
C.Y的氢化物的沸点一定高于W的氢化物
D.化合物WY 中,W的杂化方式为sp,为非极性分子
2
9.下列说法不正确的是
A. 的VSEPR模型:
B.蔗糖和氨易溶于水,难溶于四氯化碳,可用“相似相溶”规律解释C.金属晶体存在“电子气”,具有良好的导电性和导热性
D.水晶研成粉末摄取的 射线衍射图谱为分立的斑点或明锐的衍射峰
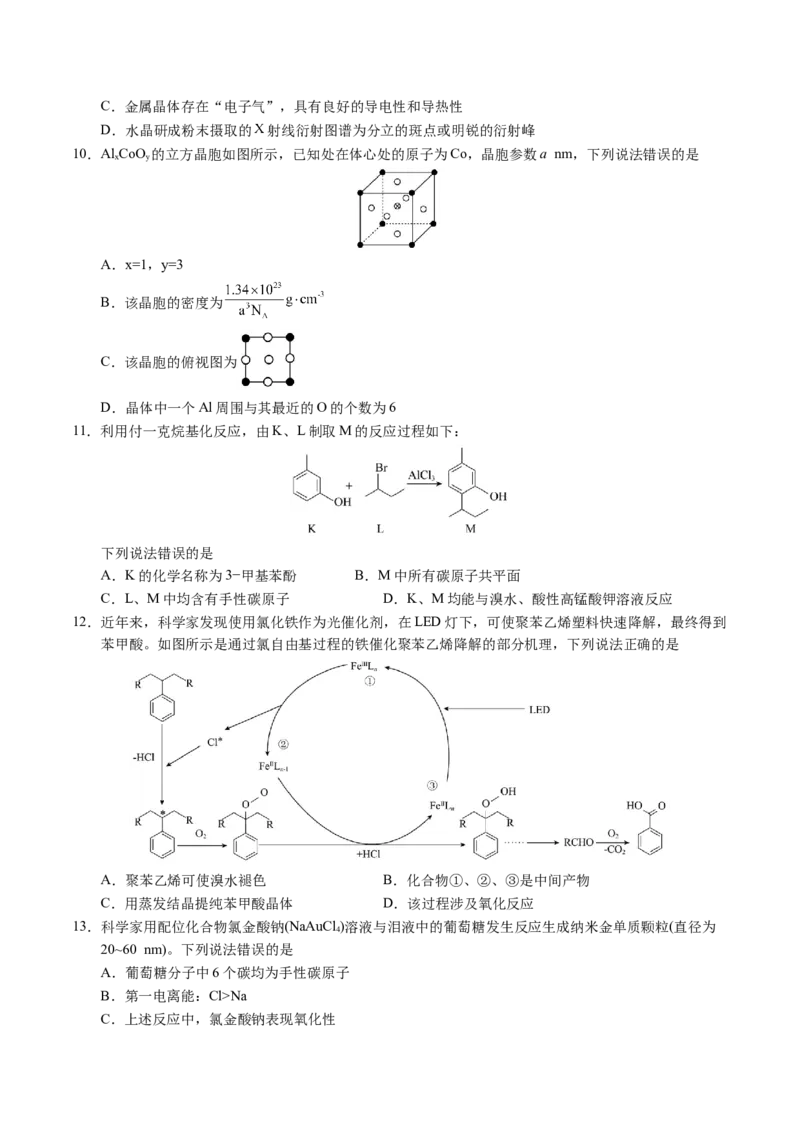
10.Al CoO 的立方晶胞如图所示,已知处在体心处的原子为Co,晶胞参数a nm,下列说法错误的是
x y
A.x=1,y=3
B.该晶胞的密度为
C.该晶胞的俯视图为
D.晶体中一个Al周围与其最近的O的个数为6
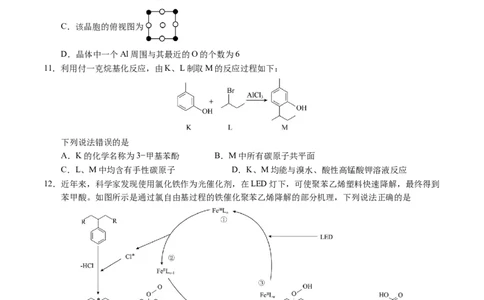
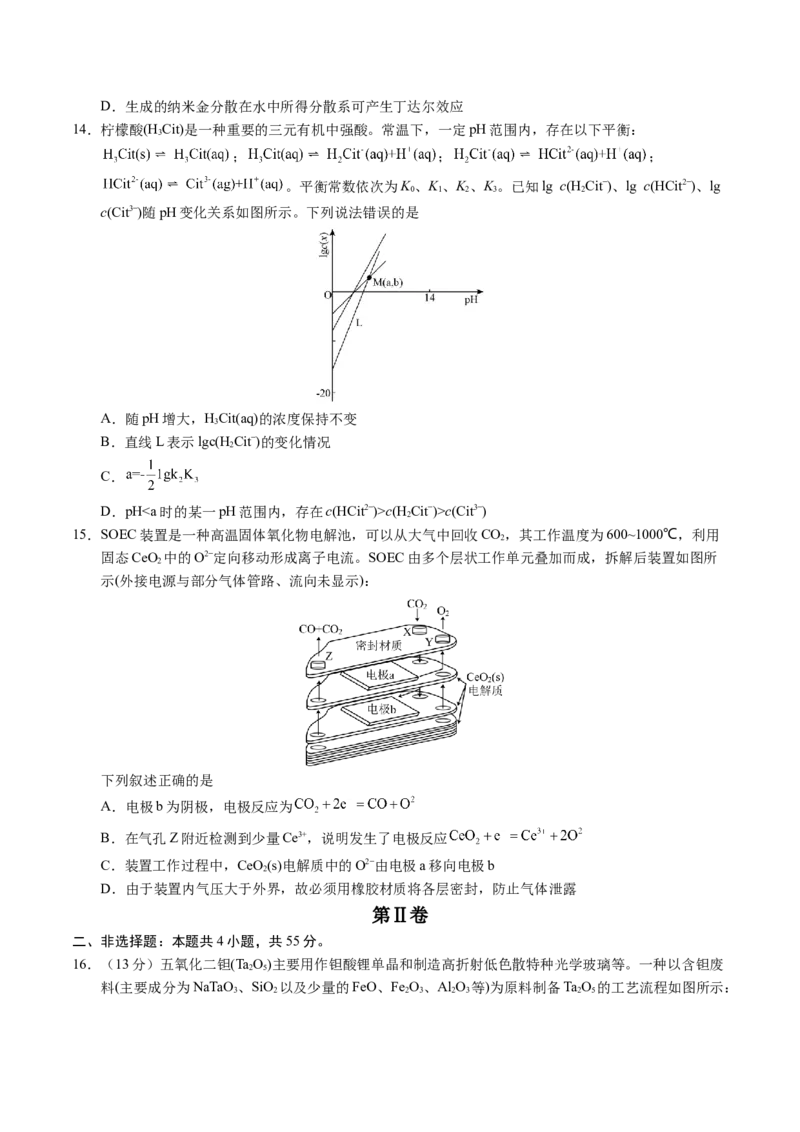
11.利用付一克烷基化反应,由K、L制取M的反应过程如下:
下列说法错误的是
A.K的化学名称为3−甲基苯酚 B.M中所有碳原子共平面
C.L、M中均含有手性碳原子 D.K、M均能与溴水、酸性高锰酸钾溶液反应
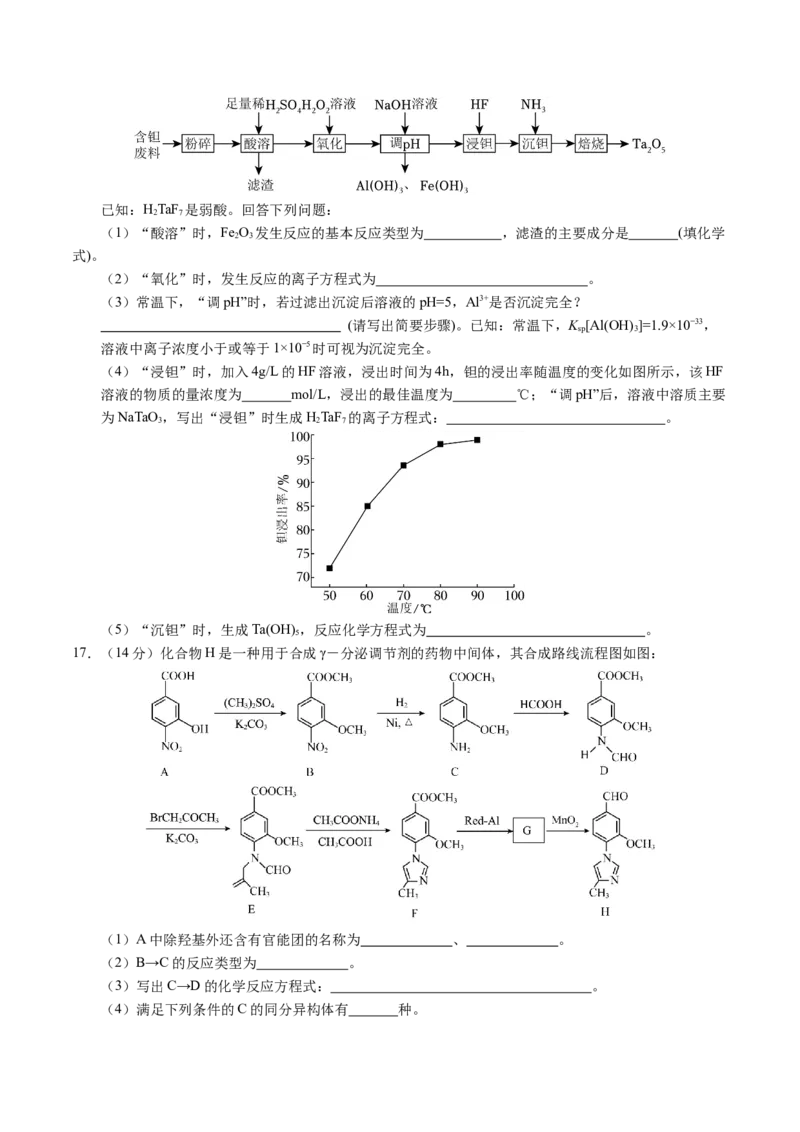
12.近年来,科学家发现使用氯化铁作为光催化剂,在LED灯下,可使聚苯乙烯塑料快速降解,最终得到
苯甲酸。如图所示是通过氯自由基过程的铁催化聚苯乙烯降解的部分机理,下列说法正确的是
A.聚苯乙烯可使溴水褪色 B.化合物①、②、③是中间产物
C.用蒸发结晶提纯苯甲酸晶体 D.该过程涉及氧化反应
13.科学家用配位化合物氯金酸钠(NaAuCl )溶液与泪液中的葡萄糖发生反应生成纳米金单质颗粒(直径为
4
20~60 nm)。下列说法错误的是
A.葡萄糖分子中6个碳均为手性碳原子
B.第一电离能:Cl>Na
C.上述反应中,氯金酸钠表现氧化性D.生成的纳米金分散在水中所得分散系可产生丁达尔效应
14.柠檬酸(H Cit)是一种重要的三元有机中强酸。常温下,一定pH范围内,存在以下平衡:
3
; ; ;
。平衡常数依次为K 、K 、K 、K 。已知lg c(H Cit−)、lg c(HCit2−)、lg
0 1 2 3 2
c(Cit3−)随pH变化关系如图所示。下列说法错误的是
A.随pH增大,HCit(aq)的浓度保持不变
3
B.直线L表示lgc(H Cit−)的变化情况
2
C.
D.pHc(H Cit−)>c(Cit3−)
2
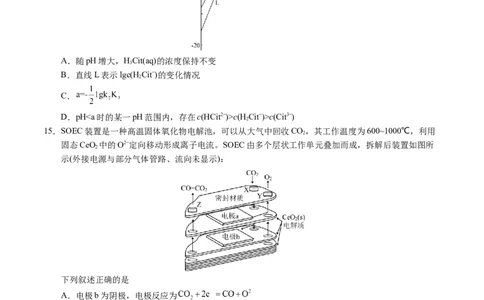
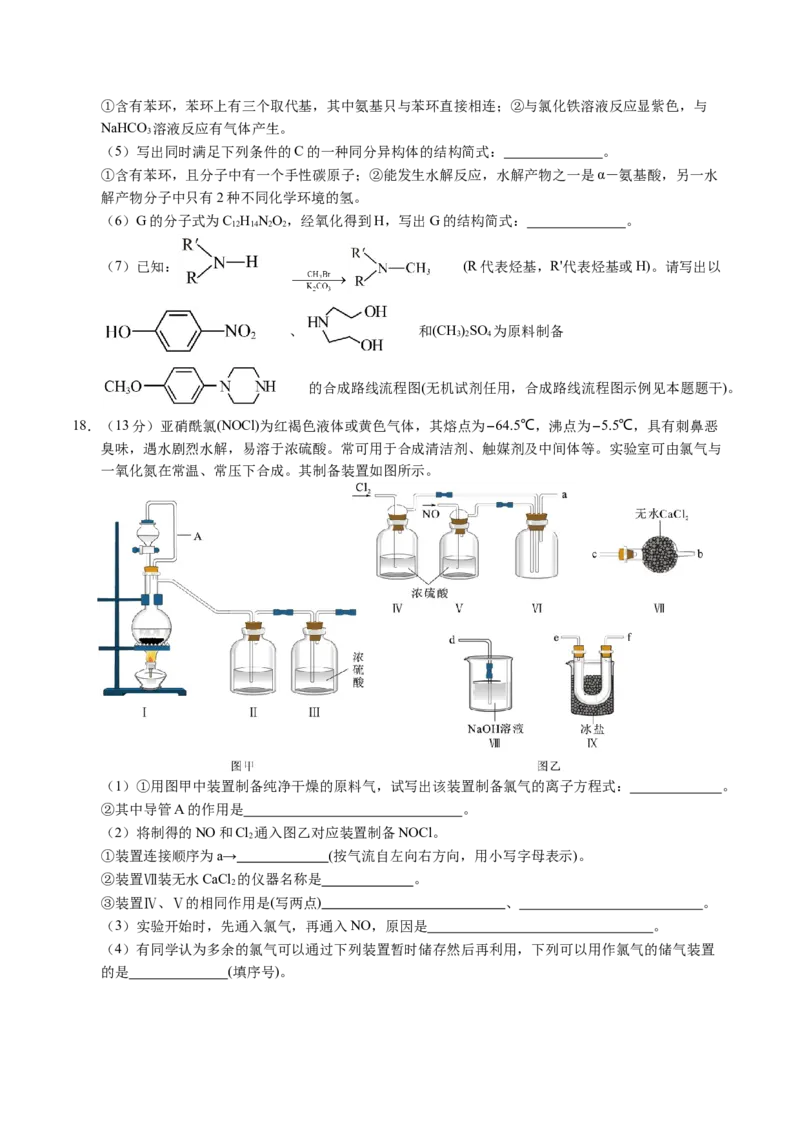
15.SOEC装置是一种高温固体氧化物电解池,可以从大气中回收CO,其工作温度为600~1000℃,利用
2
固态CeO 中的O2−定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所
2
示(外接电源与部分气体管路、流向未显示):
下列叙述正确的是
A.电极b为阴极,电极反应为
B.在气孔Z附近检测到少量Ce3+,说明发生了电极反应
C.装置工作过程中,CeO(s)电解质中的O2−由电极a移向电极b
2
D.由于装置内气压大于外界,故必须用橡胶材质将各层密封,防止气体泄露
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.(13分)五氧化二钽(TaO)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废
2 5
料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO 的工艺流程如图所示:
3 2 2 3 2 3 2 5已知:HTaF 是弱酸。回答下列问题:
2 7
(1)“酸溶”时,Fe O 发生反应的基本反应类型为 ,滤渣的主要成分是 (填化学
2 3
式)。
(2)“氧化”时,发生反应的离子方程式为 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全?
(请写出简要步骤)。已知:常温下,K [Al(OH) ]=1.9×10−33,
sp 3
溶液中离子浓度小于或等于1×10−5时可视为沉淀完全。
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF
溶液的物质的量浓度为 mol/L,浸出的最佳温度为 ℃;“调pH”后,溶液中溶质主要
为NaTaO ,写出“浸钽”时生成HTaF 的离子方程式: 。
3 2 7
(5)“沉钽”时,生成Ta(OH),反应化学方程式为 。
5
17.(14分)化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如图:
(1)A中除羟基外还含有官能团的名称为 、 。
(2)B→C的反应类型为 。
(3)写出C→D的化学反应方程式: 。
(4)满足下列条件的C的同分异构体有 种。①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;②与氯化铁溶液反应显紫色,与
NaHCO 溶液反应有气体产生。
3
(5)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
①含有苯环,且分子中有一个手性碳原子;②能发生水解反应,水解产物之一是α-氨基酸,另一水
解产物分子中只有2种不同化学环境的氢。
(6)G的分子式为C H NO,经氧化得到H,写出G的结构简式: 。
12 14 2 2
(7)已知: (R代表烃基,R'代表烃基或H)。请写出以
、 和(CH)SO 为原料制备
3 2 4
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
18.(13分)亚硝酰氯(NOCl)为红褐色液体或黄色气体,其熔点为−64.5℃,沸点为−5.5℃,具有刺鼻恶
臭味,遇水剧烈水解,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与
一氧化氮在常温、常压下合成。其制备装置如图所示。
(1)①用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式: 。
②其中导管A的作用是 。
(2)将制得的NO和Cl 通入图乙对应装置制备NOCl。
2
①装置连接顺序为a→ (按气流自左向右方向,用小写字母表示)。
②装置Ⅶ装无水CaCl 的仪器名称是 。
2
③装置Ⅳ、Ⅴ的相同作用是(写两点) 、 。
(3)实验开始时,先通入氯气,再通入NO,原因是 。
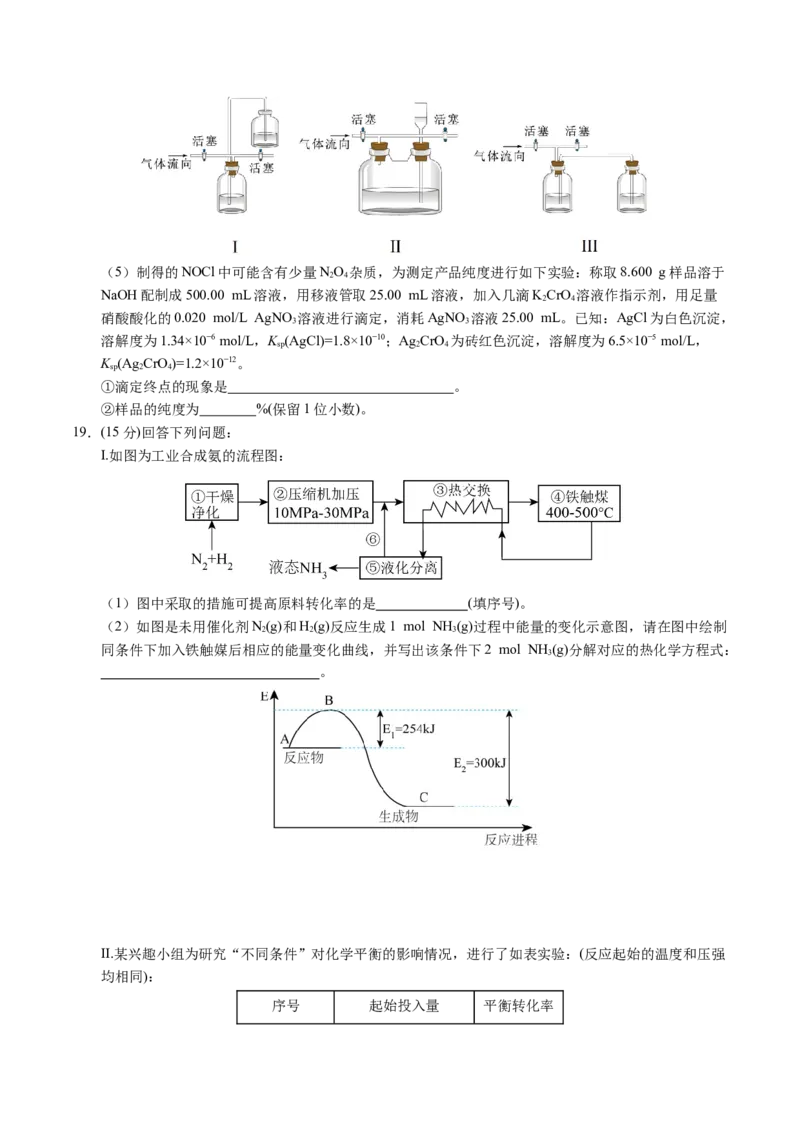
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置
的是 (填序号)。(5)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度进行如下实验:称取8.600 g样品溶于
2 4
NaOH配制成500.00 mL溶液,用移液管取25.00 mL溶液,加入几滴KCrO 溶液作指示剂,用足量
2 4
硝酸酸化的0.020 mol/L AgNO 溶液进行滴定,消耗AgNO 溶液25.00 mL。已知:AgCl为白色沉淀,
3 3
溶解度为1.34×10−6 mol/L,K (AgCl)=1.8×10−10;Ag CrO 为砖红色沉淀,溶解度为6.5×10−5 mol/L,
sp 2 4
K (Ag CrO)=1.2×10−12。
sp 2 4
①滴定终点的现象是 。
②样品的纯度为 %(保留1位小数)。
19.(15分)回答下列问题:
I.如图为工业合成氨的流程图:
(1)图中采取的措施可提高原料转化率的是 (填序号)。
(2)如图是未用催化剂N(g)和H(g)反应生成1 mol NH (g)过程中能量的变化示意图,请在图中绘制
2 2 3
同条件下加入铁触媒后相应的能量变化曲线,并写出该条件下2 mol NH (g)分解对应的热化学方程式:
3
。
II.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如表实验:(反应起始的温度和压强
均相同):
序号 起始投入量 平衡转化率N H NH
2 2 3
①恒温恒容 1mol 3mol 0 α
1
②绝热恒容 1mol 3mol 0 α
2
③恒温恒压 2mol 6mol 0 α
3
(3)则:α α 、α α (填“>”、“=”或“<”)。
1 2 1 3
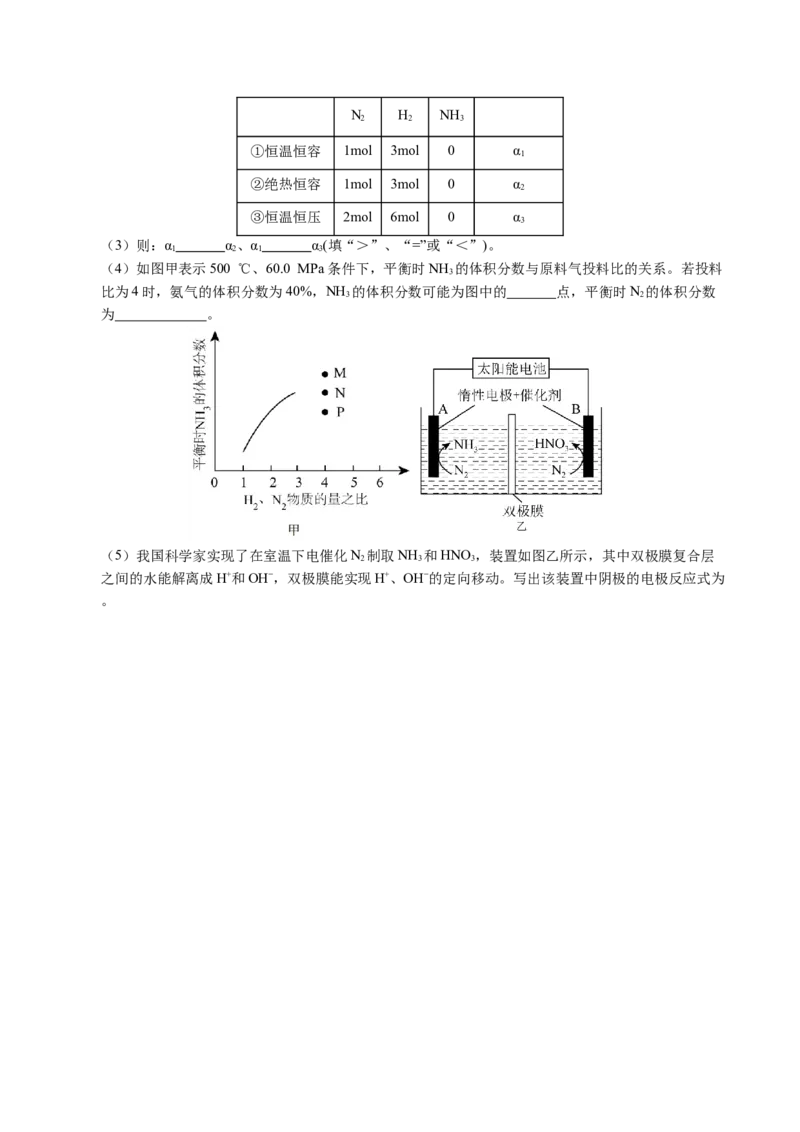
(4)如图甲表示500 ℃、60.0 MPa条件下,平衡时NH 的体积分数与原料气投料比的关系。若投料
3
比为4时,氨气的体积分数为40%,NH 的体积分数可能为图中的 点,平衡时N 的体积分数
3 2
为 。
(5)我国科学家实现了在室温下电催化N 制取NH 和HNO,装置如图乙所示,其中双极膜复合层
2 3 3
之间的水能解离成H+和OH−,双极膜能实现H+、OH−的定向移动。写出该装置中阴极的电极反应式为
。