文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(湖北专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N14 O 16 F 19 Al 27 Si 28 Cl 35.5 Co 59
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1.2023年5月10日,我国天舟六号发射成功,空间站建设过程中化学学科发挥着重要作用,下列有关叙
述错误的是
A.核心舱离子推进器用氙气作为推进剂,氙位于元素周期表0族
B.机械臂用到的铝合金、钛合金属于金属材料
C.实验舱采用砷化镓( )太阳能电池,砷和镓位于元素周期表第四周期
D.宇航服用到的聚酰胺纤维属于天然有机高分子材料
【答案】D
【解析】A.氙是稀有气体元素,故核心舱离子推进器用氙气作为推进剂,氙位于元素周期表0族,A正
确;B.金属单质和合金均属于金属材料,即机械臂用到的铝合金、钛合金属于金属材料,B正确;C.实
验舱采用砷化镓( )太阳能电池,已知Ga为31号元素,As为33号元素,故砷和镓位于元素周期表第
四周期,C正确;D.宇航服用到的聚酰胺纤维是合成纤维,不属于天然有机高分子材料,D错误;故答
案为:D。
2.西汉长信宫灯通高48厘米,通体鎏金,是河北博物院收藏的珍贵文物。鎏金又称火法镀金,其工艺是
将黄金溶于汞中形成的金汞齐均匀地涂到干净的金属器物表面,加热使汞挥发,黄金与金属表面固结,
形成光亮的金黄色镀层。已知铜和金是第ⅠB族元素,汞是第ⅡB族元素。下列说法错误的是
A.铜、金、汞均为ds区元素
B.常温下的金汞齐是金属晶体
C.应将宫灯保存在干燥的环境中
D.铜腐蚀后生成的 属于盐
【答案】B
【解析】A.铜和金是第ⅠB族元素,汞是第ⅡB族元素,则铜、金、汞均为ds区元素,A正确;B.常温下的金汞齐是液态物质,不是金属晶体,B错误;C.在潮湿的环境中,铜制的宫灯会发生电化学腐蚀,
将宫灯保存在干燥的环境中,有利于减缓腐蚀,C正确;D.铜腐蚀后生成 ,该物质属于盐,
是一种碱式盐,D正确;故选B。
3.7−羟基香豆素是香豆素家族的天然产物,是一种荧光化合物,可用作防晒剂和药物;它的结构简式如
图所示。下列说法错误的是
A.分子式为C HO
9 6 3
B.该物质的官能团是碳碳双键、羟基、酯基
C.1 mol该物质与足量H 反应,最多消耗4 mol H
2 2
D.该物质不能发生取代反应
【答案】D
【解析】A.观察其结构简式知,一分子含9个C,6个H,3个O,故分子式为C HO,A不符合题意;
9 6 3
B.观察其结构简式知,该物质的官能团是碳碳双键、羟基、酯基,B不符合题意;C.7−羟基香豆素结构
中含一个苯环、一个碳碳双键,分别可与三分子氢气、一分子氢气发生加成反应,故1mol该物质与足量
H 反应时最多消耗4molH ,C不符合题意;D.由于含酚羟基,可与浓溴水发生取代反应;所含的酯基可
2 2
以发生水解反应,也属于取代反应,D符合题意;故选D。
4.能正确表示下列反应的离子方程式为
A.臭碱(硫化钠)溶液中滴加足量的稀硝酸:S2−+2H+=H S↑
2
B.氯化铝溶液中通入过量的氨气:Al3++4NH+4H O= +4NH
3 2
C.石钟乳(CaCO)溶于醋酸:CaCO +2H+=Ca2++H O+CO↑
3 3 2 2
D.1.5 mol Cl 通入到含1 mol FeI 的溶液中:2Fe2++4I−+3Cl=2Fe3++6Cl−+2I
2 2 2 2
【答案】D
【解析】A.臭碱(硫化钠)溶液中滴加足量的稀硝酸不发生复分解反应,硝酸具有强氧化性,可以将 氧
化为S单质,自身根据其浓度大小被还原为NO或 ,A错误;B.氢氧化铝不溶于氨水, 与氨水
反应生成 , B错误;C.醋酸是弱酸,碳酸钙与醋酸反应的离子方程式2CHCOOH+CaCO =Ca2+
3 3+2CH COO−+H O+CO↑, C错误;D.1.5mol 通入到含1mol 的溶液中,可将 全部氧化,
3 2 2
离子方程式:2Fe2++4I−+3Cl=2Fe3++6Cl−+2I ,D正确;选D。
2 2
5.下列由实验操作及现象所得结论正确的是
选项 实验操作和现象 实验结论
将适量蔗糖与稀硫酸反应,加热后加碱中和,再加
A 证明蔗糖完全水解
入新制Cu(OH) 浊液加热,有红色沉淀生成
2
向2 mL 0.1 mol·L−1硝酸银溶液中,加入1 mL等浓
B 度NaCl溶液,出现白色沉淀,再加入几滴等浓度的 K (AgCl)>K (Ag S)
sp sp 2
NaS溶液,有黑色沉淀生成
2
某溶液中加盐酸,产生使澄清石灰水变浑浊的无色
C 原溶液中一定存在
无味气体
向碘水中加入等体积CCl ,振荡后静置,上层接近 I 在CCl 中的溶解度大于
D 4 2 4
无色,下层显紫红色 在水中的溶解度
【答案】D
【解析】A.蔗糖在稀硫酸催化下加热,发生水解反应产生葡萄糖、果糖,然后加入NaOH溶液中和催化
剂硫酸,使溶液显碱性,再加入新制Cu(OH) 悬浊液,加热煮沸,有红色沉淀生成,只能证明蔗糖发生了
2
水解反应产生了葡萄糖,但不能证明蔗糖完全水解,A错误;B.根据反应方程式
AgNO+NaCl=AgCl↓+NaNO 中二者反应关系,结合加入的二者相对量可知:AgNO 过量,再向其中加入
3 3 3
几滴等浓度的NaS溶液时,过量的AgNO 与NaS反应产生Ag S黑色沉淀,不能证明溶度积常数
2 3 2 2
K (AgCl)>K (Ag S),B错误;C.某溶液中加盐酸,产生使澄清石灰水变浑浊的无色无味气体,该气体
sp sp 2
是CO,则原溶液中可能含有 ,也可能含有 ,C错误;D.CCl 是无色液体,与水互不相溶,
2 4
密度比水大。向碘水中加入等体积CCl ,振荡后静置,上层接近无色,下层显紫红色,说明I 在CCl 中的
4 2 4
溶解度大于在水中的溶解度,CCl 起到了萃取作用,D正确;故合理选项是D。
4
6.设N 为阿伏加德罗常数的值。下列叙述正确的是
A
A.1 mol金属钠生成NaO,转移的电子数为2N
2 2 A
B.60 g二氧化硅晶体中含有N 个SiO 分子
A 2
C.乙烯和丙烯的混合物共28 g,含有的氢原子数为4N
A
D.由1 mol CHCOONa和少量CHCOOH形成的中性溶液中,CHCOO−数目小于N
3 3 3 A
【答案】C
【解析】A.1molNa完全反应失去1mol电子,无论产物为氧化钠还是过氧化钠,转移的电子数都为1mol,转移电子总数N 个,A错误;B.二氧化硅为共价晶体,不存在二氧化硅分子,B错误;C.乙烯
A
和丙烯的最简式均为CH,混合物共28g可以认为有2molCH ,含有的氢原子数为4N ,C正确;D.由
2 2 A
1mol CHCOONa和少量CHCOOH形成的中性溶液中,含有1mol钠离子;溶液为中性,氢离子与氢氧根
3 3
离子物质的量相等,根据电荷守恒,则钠离子与CHCOO−的物质的量相等,所以溶液中含有CHCOO−的
3 3
物质的量为1mol,含有的CHCOO−数目为N 个,D错误;故选C。
3 A
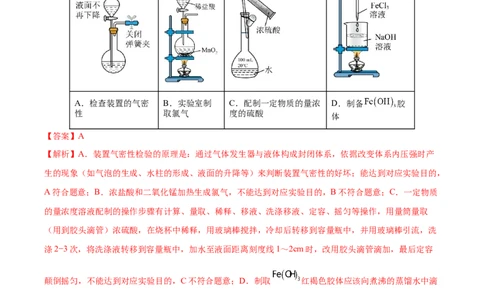
7.用下图所示装置及药品进行实验,能达到对应实验目的的是
A.检查装置的气密 B.实验室制 C.配制一定物质的量浓 D.制备 胶
性 取氯气 度的硫酸
体
【答案】A
【解析】A.装置气密性检验的原理是:通过气体发生器与液体构成封闭体系,依据改变体系内压强时产
生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性的好坏;能达到对应实验目的,
A符合题意;B.浓盐酸和二氧化锰加热生成氯气,不能达到对应实验目的,B不符合题意;C.一定物质
的量浓度溶液配制的操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取
(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到容量瓶中,并用玻璃棒引流,洗
涤2−3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容
颠倒摇匀,不能达到对应实验目的,C不符合题意;D.制取 红褐色胶体应该向煮沸的蒸馏水中滴
加饱和氯化铁溶液至溶液变红褐色;不能达到对应实验目的,D不符合题意;故选A。
8.TCCA是一种高效消毒剂,由原子序数依次增大的W、X、Y、Z四种元素构成,且位于两个不同短周
期。W元素的K层电子数与其p能级上的电子数相等,基态Y原子s能级电子总数与p能级电子总数
相等,其原子半径小于W原子,Z元素的原子半径为同周期主族元素最小。下列叙述正确的是
A.电负性大小:X>Y>W
B.简单离子半径:Z>Y>X
C.Y的氢化物的沸点一定高于W的氢化物D.化合物WY 中,W的杂化方式为sp,为非极性分子
2
【答案】D
【分析】原子序数依次增大的W、X、Y、Z四种元素构成,且位于两个不同短周期。W元素的K层电子
数与其p能级上的电子数相等,则W为碳;基态Y原子s能级电子总数与p能级电子总数相等,其原子半
径小于碳原子,则Y与碳同周期,为氧,那么X原子序数位于碳氧之间,X为氮;Z元素的原子半径为同
周期主族元素最小,为第三周期的氯;
【解析】A.同周期从左到右,金属性减弱,非金属性变强,元素的电负性变强;同主族由上而下,金属
性增强,非金属性逐渐减弱,元素电负性减弱;电负性大小:O>N>C,A错误;B.电子层数越多半径
越大,电子层数相同时,核电荷数越大,半径越小;简单离子半径:Cl−>N3−>O2−,B错误;C.碳可以
形成相对分子质量很大的高聚物氢化物,故氧的的氢化物的沸点不一定高于碳的氢化物,C错误;D.化
合物CO 中分子构型为直线形,碳的杂化方式为sp,分子正负电荷中心重合,为非极性分子,D正确;故
2
选D。
9.下列说法不正确的是
A. 的VSEPR模型:
B.蔗糖和氨易溶于水,难溶于四氯化碳,可用“相似相溶”规律解释
C.金属晶体存在“电子气”,具有良好的导电性和导热性
D.水晶研成粉末摄取的 射线衍射图谱为分立的斑点或明锐的衍射峰
【答案】A
【解析】A.SO 的成键电子对数是2,孤电子对数是1,价层电子对数为3,VSEPR模型为平面三角形,
2
A错误;B.蔗糖和氨是极性分子,易溶于水,四氯化碳是非极性分子,难溶于四氯化碳,B正确;C.金
属晶体存在的“电子气”, 电子气在外电场作用下定向移动,金属有良好的导电性;金属受热,加速自
由电子与金属离子之间的能量交换将热能从一端传递到另一端而使金属有良好的导热性,C正确;D.水
晶为晶态二氧化硅,X射线衍射图谱上有分立的斑点或明锐的衍射峰,D正确;故选A。
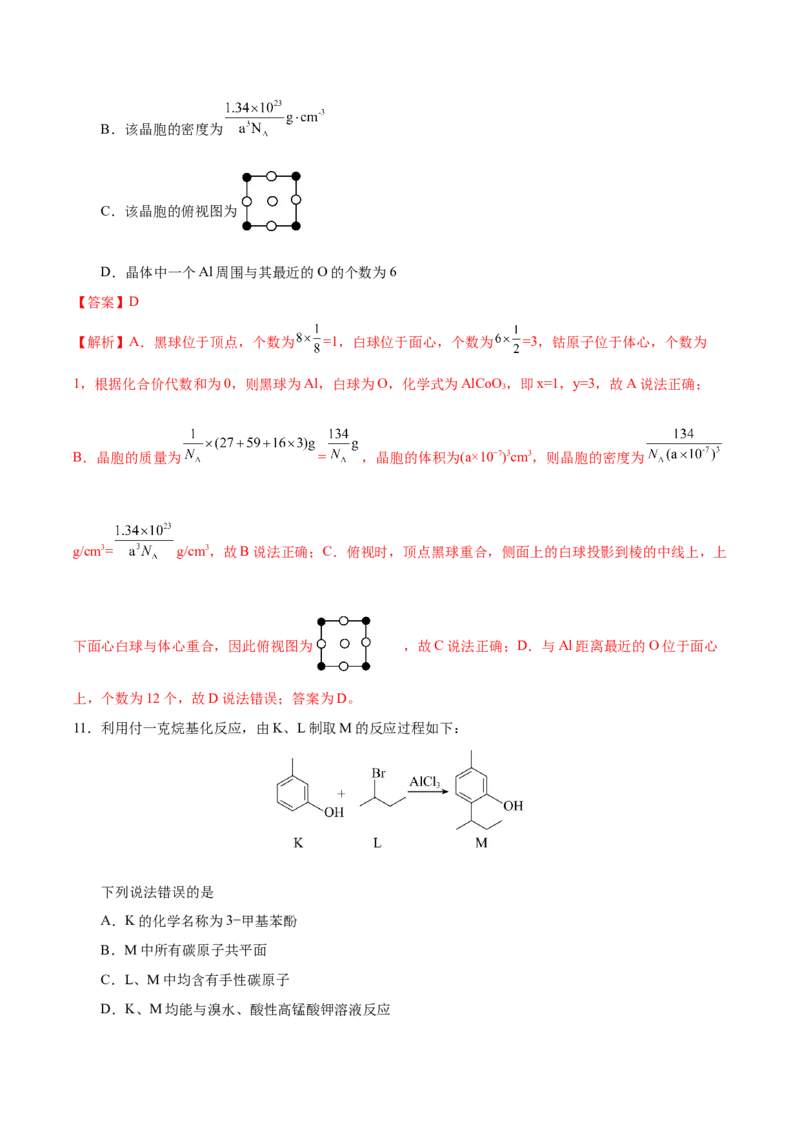
10.Al CoO 的立方晶胞如图所示,已知处在体心处的原子为Co,晶胞参数a nm,下列说法错误的是
x y
A.x=1,y=3B.该晶胞的密度为
C.该晶胞的俯视图为
D.晶体中一个Al周围与其最近的O的个数为6
【答案】D
【解析】A.黑球位于顶点,个数为 =1,白球位于面心,个数为 =3,钴原子位于体心,个数为
1,根据化合价代数和为0,则黑球为Al,白球为O,化学式为AlCoO,即x=1,y=3,故A说法正确;
3
B.晶胞的质量为 = ,晶胞的体积为(a×10−7)3cm3,则晶胞的密度为
g/cm3= g/cm3,故B说法正确;C.俯视时,顶点黑球重合,侧面上的白球投影到棱的中线上,上
下面心白球与体心重合,因此俯视图为 ,故C说法正确;D.与Al距离最近的O位于面心
上,个数为12个,故D说法错误;答案为D。
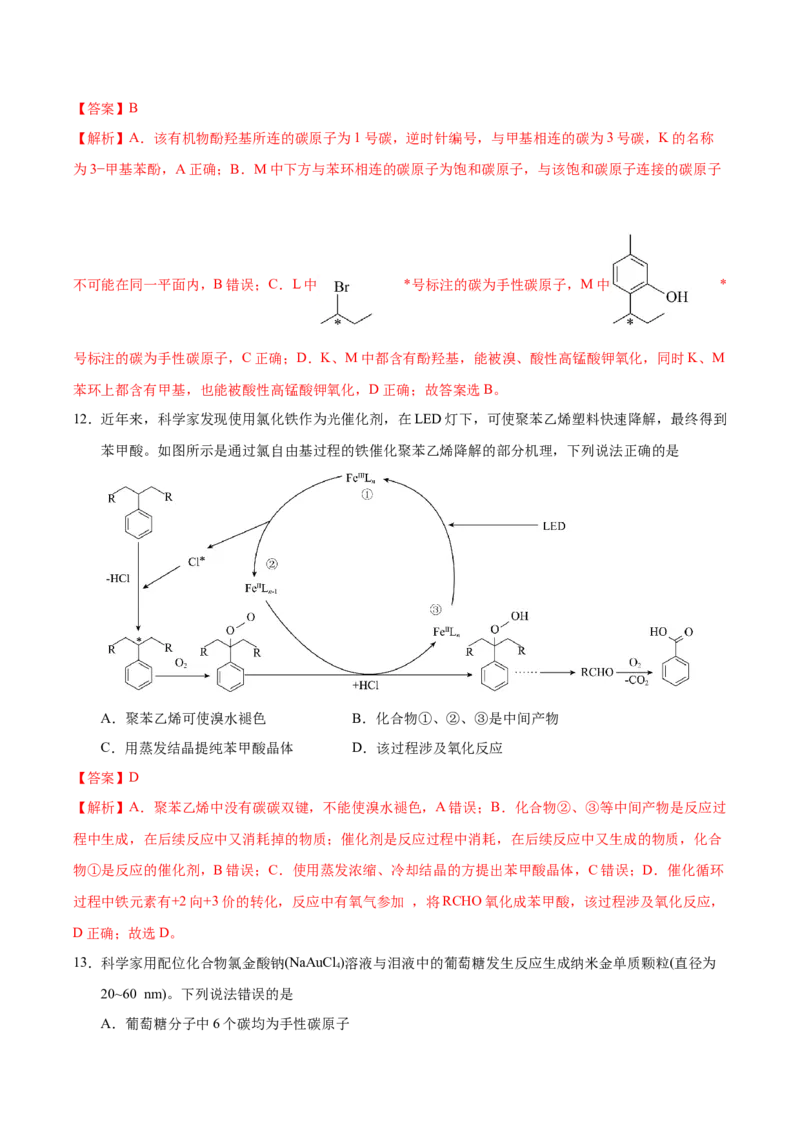
11.利用付一克烷基化反应,由K、L制取M的反应过程如下:
下列说法错误的是
A.K的化学名称为3−甲基苯酚
B.M中所有碳原子共平面
C.L、M中均含有手性碳原子
D.K、M均能与溴水、酸性高锰酸钾溶液反应【答案】B
【解析】A.该有机物酚羟基所连的碳原子为1号碳,逆时针编号,与甲基相连的碳为3号碳,K的名称
为3−甲基苯酚,A正确;B.M中下方与苯环相连的碳原子为饱和碳原子,与该饱和碳原子连接的碳原子
不可能在同一平面内,B错误;C.L中 *号标注的碳为手性碳原子,M中 *
号标注的碳为手性碳原子,C正确;D.K、M中都含有酚羟基,能被溴、酸性高锰酸钾氧化,同时K、M
苯环上都含有甲基,也能被酸性高锰酸钾氧化,D正确;故答案选B。
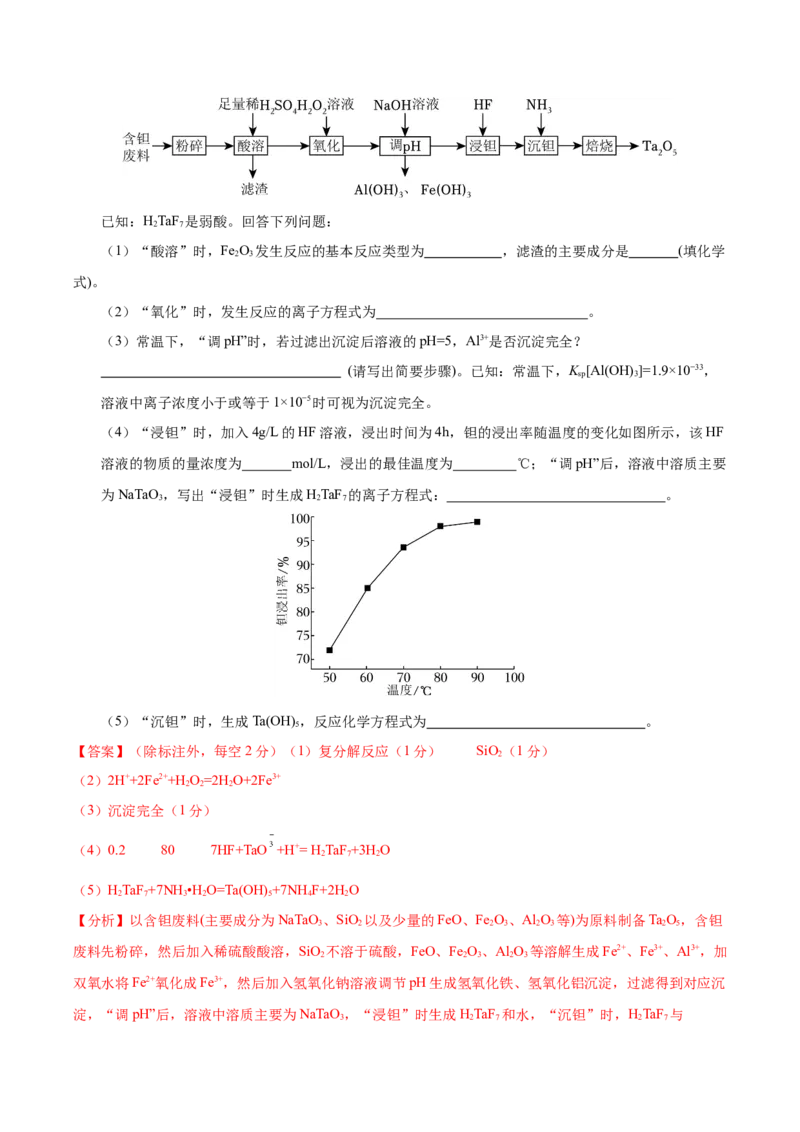
12.近年来,科学家发现使用氯化铁作为光催化剂,在LED灯下,可使聚苯乙烯塑料快速降解,最终得到
苯甲酸。如图所示是通过氯自由基过程的铁催化聚苯乙烯降解的部分机理,下列说法正确的是
A.聚苯乙烯可使溴水褪色 B.化合物①、②、③是中间产物
C.用蒸发结晶提纯苯甲酸晶体 D.该过程涉及氧化反应
【答案】D
【解析】A.聚苯乙烯中没有碳碳双键,不能使溴水褪色,A错误;B.化合物②、③等中间产物是反应过
程中生成,在后续反应中又消耗掉的物质;催化剂是反应过程中消耗,在后续反应中又生成的物质,化合
物①是反应的催化剂,B错误;C.使用蒸发浓缩、冷却结晶的方提出苯甲酸晶体,C错误;D.催化循环
过程中铁元素有+2向+3价的转化,反应中有氧气参加 ,将RCHO氧化成苯甲酸,该过程涉及氧化反应,
D正确;故选D。
13.科学家用配位化合物氯金酸钠(NaAuCl )溶液与泪液中的葡萄糖发生反应生成纳米金单质颗粒(直径为
4
20~60 nm)。下列说法错误的是
A.葡萄糖分子中6个碳均为手性碳原子B.第一电离能:Cl>Na
C.上述反应中,氯金酸钠表现氧化性
D.生成的纳米金分散在水中所得分散系可产生丁达尔效应
【答案】A
【解析】A.连有4个不同原子或原子团的碳为手性碳,葡萄糖分子中6个碳中4个碳为手性碳原子,A项
错误;B.同周期从左到右,元素第一电离能整体呈增大的趋势,则第一电离能;Nac(H Cit−)>c(Cit3−)
2
【答案】B【分析】由已知信息,K =c[HCit(aq)],常温下,K 为常数,因此原溶液中c[HCit(aq)]始终不变。
0 3 0 3
, , ;
, ,
, ,
,
。因此,lg c(H Cit−)、lg c(HCit2−)、lg c(Cit3−)与pH的变化关系直
2
线的斜率分别为1、2、3。
【解析】A.由分析可知,pH在一定范围内增大,HCit(aq)的浓度是不变的,A正确;B.由分析可知,
3
直线L的斜率最大,表示lgc(Cit3−)的变化情况,B错误;C.由分析可知,M点存在
,即 ,整理得
,C正确;D.由分析可知,从图像来看,pHc(H Cit−)>c(Cit3−)大小关系,D正确;故答案为:B。
2
15.SOEC装置是一种高温固体氧化物电解池,可以从大气中回收CO,其工作温度为600~1000℃,利用
2
固态CeO 中的O2−定向移动形成离子电流。SOEC由多个层状工作单元叠加而成,拆解后装置如图所
2
示(外接电源与部分气体管路、流向未显示):下列叙述正确的是
A.电极b为阴极,电极反应为
B.在气孔Z附近检测到少量Ce3+,说明发生了电极反应
C.装置工作过程中,CeO(s)电解质中的O2−由电极a移向电极b
2
D.由于装置内气压大于外界,故必须用橡胶材质将各层密封,防止气体泄露
【答案】A
【分析】由题干图示信息可知,CO 经导管X进入电极b中,发生反应CO+2e−=CO+O2−,未反应的CO 和
2 2 2
生成的CO经Z导管流出,O2−经固态CeO 定向移动到a电极,在a电极上放电,发生2O2− − 4e−=O ↑,产
2 2
生的O 经导管Y流出。
2
【解析】A.由分析可知,CO 经导管X进入电极b中,发生反应CO+2e−=CO+O2−,发生还原反应,故电
2 2
极b为阴极,A正确;B.在气孔Z附近检测到少量Ce3+,不能说明发生了电极反应CeO+e−=Ce3++2O2−,
2
也可能是高温下CO将CeO 还原为Ce3+,B错误;C.由分析可知,电极a为阳极,b为阴极,电解池中电
2
解质中阴离子流向阳极,故装置工作过程中,CeO(s)电解质中的O2−由电极b移向电极a,C错误;D.由
2
题干信息可知,装置内气压等于外界,由于产生有毒气体CO,故必须用橡胶材质将各层密封,防止气体
泄露,D错误;故答案为:A。
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.(13分)五氧化二钽(TaO)主要用作钽酸锂单晶和制造高折射低色散特种光学玻璃等。一种以含钽废
2 5
料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO 的工艺流程如图所示:
3 2 2 3 2 3 2 5已知:HTaF 是弱酸。回答下列问题:
2 7
(1)“酸溶”时,Fe O 发生反应的基本反应类型为 ,滤渣的主要成分是 (填化学
2 3
式)。
(2)“氧化”时,发生反应的离子方程式为 。
(3)常温下,“调pH”时,若过滤出沉淀后溶液的pH=5,Al3+是否沉淀完全?
(请写出简要步骤)。已知:常温下,K [Al(OH) ]=1.9×10−33,
sp 3
溶液中离子浓度小于或等于1×10−5时可视为沉淀完全。
(4)“浸钽”时,加入4g/L的HF溶液,浸出时间为4h,钽的浸出率随温度的变化如图所示,该HF
溶液的物质的量浓度为 mol/L,浸出的最佳温度为 ℃;“调pH”后,溶液中溶质主要
为NaTaO ,写出“浸钽”时生成HTaF 的离子方程式: 。
3 2 7
(5)“沉钽”时,生成Ta(OH),反应化学方程式为 。
5
【答案】(除标注外,每空2分)(1)复分解反应(1分) SiO(1分)
2
(2)2H++2Fe2++H O=2H O+2Fe3+
2 2 2
(3)沉淀完全(1分)
(4)0.2 80 7HF+TaO +H+= H TaF +3H O
2 7 2
(5)HTaF +7NH•H O=Ta(OH) +7NHF+2HO
2 7 3 2 5 4 2
【分析】以含钽废料(主要成分为NaTaO 、SiO 以及少量的FeO、Fe O、Al O 等)为原料制备TaO,含钽
3 2 2 3 2 3 2 5
废料先粉碎,然后加入稀硫酸酸溶,SiO 不溶于硫酸,FeO、Fe O、Al O 等溶解生成Fe2+、Fe3+、Al3+,加
2 2 3 2 3
双氧水将Fe2+氧化成Fe3+,然后加入氢氧化钠溶液调节pH生成氢氧化铁、氢氧化铝沉淀,过滤得到对应沉
淀,“调pH”后,溶液中溶质主要为NaTaO ,“浸钽”时生成HTaF 和水,“沉钽”时,HTaF 与
3 2 7 2 7NH •H O反应生成Ta(OH),焙烧得TaO。
3 2 5 2 5
【解析】(1)“酸溶”时,Fe O 发生Fe O+3H SO =Fe (SO )+3H O反应,属于复分解反应,SiO 不溶于
2 3 2 3 2 4 2 4 3 8 2
硫酸,滤渣的主要成分是SiO,故答案为:复分解反应;SiO;
2 6
(2)加双氧水将Fe2+氧化成Fe3+,发生反应的离子方程式为2H++2Fe2++H O=2H O+2Fe3+;
2 2 2
(3)常温下,“调pH=5”时,此时溶液中c(OH−)=1×10−9mol/L,可得c(Al3+)=
,Al7+沉淀完全;
(4)HF溶液的物质的量浓度c(HF)= = =2.2mol/L,由图可知,浸出的最佳温度为80℃,温度过
低,浸出率低,温度过高,Ta浸出率变化不大,但耗能增大;“调pH”后,溶液中溶质主要为NaTaO ,
3
“浸钽”时生成HTaF 和水,离子方程式:7HF+TaO +H+= H TaF +3H O,
2 7 2 7 2
故答案为:0.2;80;7HF+TaO +H+= H TaF +3H O;
2 7 2
(5)“沉钽”时通入氨气,生成了一水合氨,HTaF 与NH •H O反应生成Ta(OH),反应化学方程式为
2 7 3 2 5
HTaF +7NH•H O=Ta(OH) +7NHF+2HO。
2 7 3 2 5 4 2
17.(14分)化合物H是一种用于合成γ-分泌调节剂的药物中间体,其合成路线流程图如图:
(1)A中除羟基外还含有官能团的名称为 、 。
(2)B→C的反应类型为 。
(3)写出C→D的化学反应方程式: 。(4)满足下列条件的C的同分异构体有 种。
①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;②与氯化铁溶液反应显紫色,与
NaHCO 溶液反应有气体产生。
3
(5)写出同时满足下列条件的C的一种同分异构体的结构简式: 。
①含有苯环,且分子中有一个手性碳原子;②能发生水解反应,水解产物之一是α-氨基酸,另一水
解产物分子中只有2种不同化学环境的氢。
(6)G的分子式为C H NO,经氧化得到H,写出G的结构简式: 。
12 14 2 2
(7)已知: (R代表烃基,R'代表烃基或H)。请写出以
、 和(CH)SO 为原料制备
3 2 4
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
【答案】(除标注外,每空2分)(1)羧基(1分) 羟基(1分)
(2)还原反应(1分)
(3) +HCOOH→ +H O
2
(4)20
(5) 或
(6)(7) (3分)
【分析】A发生取代反应生成B,B和氢气发生还原反应生成C,C和甲酸发生取代反应得到D,D在碳酸
钾作用下发生取代反应得到E,E和乙酸铵和乙酸反应生成F,F反应得到
,G发生催化氧化得到H;
【解析】(1)A中除羟基外还含有官能团的名称为羧基、羟基;
(2)B→C为硝基发生加氢反应生成氨基,反应类型为还原反应;
(3)根据原子守恒,C和HCOOH反应生成D和HO,则C→D的化学反应方程式:
2
+HCOOH→ +H O;
2
(4)①含有苯环,苯环上有三个取代基,其中氨基只与苯环直接相连;②与氯化铁溶液反应显紫色说明
含有酚羟基,与NaHCO 溶液反应有气体产生说明含有羧基,满足条件的C的同分异构体有
3、 、
、其中取代基−CHCHCOOH另一种结构为 ,所以共有10×2=20种;
2 2
(5)分析C的结构特点,C分子中除苯环外,还有3个C、3个O、1个N和1个不饱和度。C的同分异构
体能发生水解,由于其中一种水解产物分子中只有2种不同的H原子,所以该水解产物一定是对苯二酚;
另一种水解产物是α−氨基酸,则该α−氨基酸一定是α−氨基丙酸,结合两种水解产物可以写出C的同分异
构体为 或 ;
(6)由F到H发生了两步反应,分析两者的结构,发现F中的酯基到G中变成了醛基,由于已知G到H
发生的是氧化反应,所以F到G发生了还原反应,结合G的分子式C H NO,可以写出G的结构简式为
12 14 2 2
;
(7)以 、 和(CH)SO 为原料制备
3 2 4
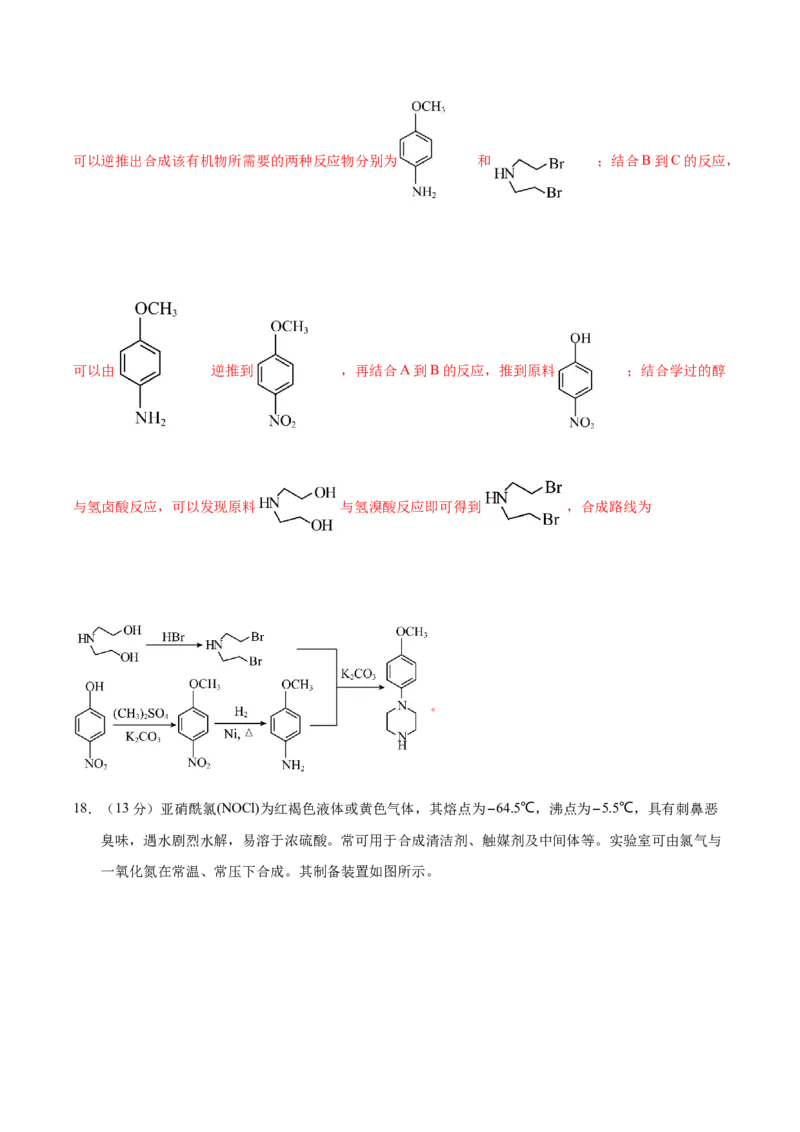
,首先分析合成对象与原料间的关系。结合上述合成路线中D到E的变化,可以逆推出合成该有机物所需要的两种反应物分别为 和 ;结合B到C的反应,
可以由 逆推到 ,再结合A到B的反应,推到原料 ;结合学过的醇
与氢卤酸反应,可以发现原料 与氢溴酸反应即可得到 ,合成路线为
。
18.(13分)亚硝酰氯(NOCl)为红褐色液体或黄色气体,其熔点为−64.5℃,沸点为−5.5℃,具有刺鼻恶
臭味,遇水剧烈水解,易溶于浓硫酸。常可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与
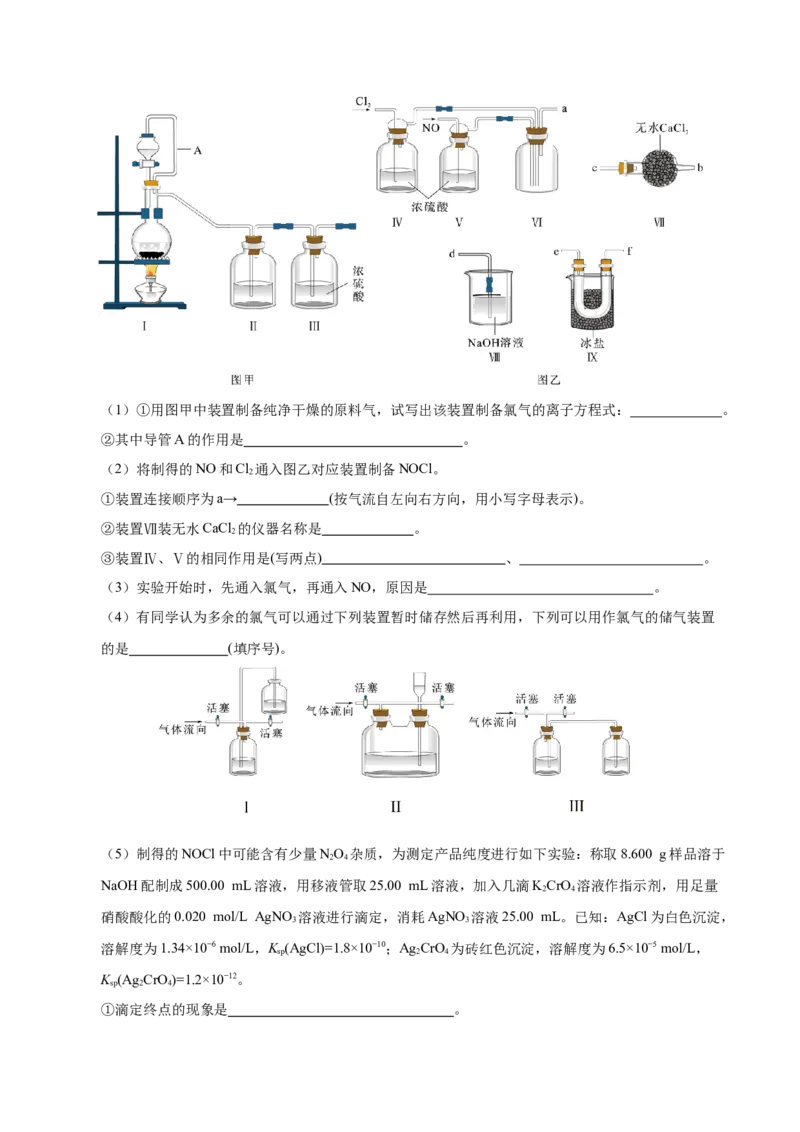
一氧化氮在常温、常压下合成。其制备装置如图所示。(1)①用图甲中装置制备纯净干燥的原料气,试写出该装置制备氯气的离子方程式: 。
②其中导管A的作用是 。
(2)将制得的NO和Cl 通入图乙对应装置制备NOCl。
2
①装置连接顺序为a→ (按气流自左向右方向,用小写字母表示)。
②装置Ⅶ装无水CaCl 的仪器名称是 。
2
③装置Ⅳ、Ⅴ的相同作用是(写两点) 、 。
(3)实验开始时,先通入氯气,再通入NO,原因是 。
(4)有同学认为多余的氯气可以通过下列装置暂时储存然后再利用,下列可以用作氯气的储气装置
的是 (填序号)。
(5)制得的NOCl中可能含有少量NO 杂质,为测定产品纯度进行如下实验:称取8.600 g样品溶于
2 4
NaOH配制成500.00 mL溶液,用移液管取25.00 mL溶液,加入几滴KCrO 溶液作指示剂,用足量
2 4
硝酸酸化的0.020 mol/L AgNO 溶液进行滴定,消耗AgNO 溶液25.00 mL。已知:AgCl为白色沉淀,
3 3
溶解度为1.34×10−6 mol/L,K (AgCl)=1.8×10−10;Ag CrO 为砖红色沉淀,溶解度为6.5×10−5 mol/L,
sp 2 4
K (Ag CrO)=1.2×10−12。
sp 2 4
①滴定终点的现象是 。②样品的纯度为 %(保留1位小数)。
【答案】(除标注外,每空2分)(1)2Cl−+MnO+4H+ Cl↑+Mn2++2H O 平衡蒸馏烧瓶和分液漏斗
2 2 2
内的压强,使浓HCl能顺利的流下(1分)
(2)e→f→c→b→d 球形干燥管(1分) 充分干燥Cl 和NO(1分) 通过观察气泡的多少
2
调节两种气体的流速(1分)
(3)用Cl 排尽装置内的空气,防止NO被O 氧化(1分)
2 2
(4)I(1分)
(5)当滴入最后半滴硝酸银标准溶液时,锥形瓶内出现红棕色沉淀﹐且半分钟内砖红色沉淀不消失,即
为滴定终点(1分) 7.6
【分析】氯气与NO在常温常压下合成亚硝酰氯;图甲装置制备氯气,实验室用浓盐酸与二氧化锰在加热
条件下制备,制得的氯气中混有氯化氢和水蒸气,先用饱和食盐水吸收除去HCl,再用浓硫酸干燥;由图
甲制备NO,用铜和稀硝酸反应制备,制得的NO中可能混有硝酸、二氧化氮,先用水净化处理,再用浓
硫酸干燥;将氯气和NO通过装置Ⅳ、Ⅴ除可进一步干燥NO、Cl 外,还可以根据气泡控制气体流速,在
2
装置Ⅵ中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶
液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置。据此回答问题。
【解析】(1)①用图甲中装置制备纯净干燥的原料气,该装置中用浓盐酸与二氧化锰制备氯气,离子方
程式为: 2Cl−+MnO+4H+ Cl↑+Mn2++2H O;②装置甲中导管A的作用是平衡蒸馏烧瓶和分液漏斗内的压
2 2 2
强,使浓HCl能顺利的流下;
(2)①由图甲制备NO,用铜和稀硝酸反应制备,制得的NO中可能混有硝酸、二氧化氮,先用水净化处
理,再用浓硫酸干燥;将氯气和NO通过装置Ⅳ、Ⅴ除可进一步干燥NO、Cl 外,还可以根据气泡控制气
2
体流速,在装置Ⅵ中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用
氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置。由分析可
知,装置连顺序为a→e→f→c→b→d;②装置Ⅶ中用球形干燥管装无水CaCl ;③装置Ⅳ、Ⅴ的相同作用除
2
可充分干燥Cl 和NO外,另一个作用是通过观察气泡的多少调节两种气体的流速;
2
(3)先通入氯气,用Cl 排尽装置内的空气,防止NO被O 氧化;
2 2
(4)氯气在饱和食盐水中溶解度不大,用排饱和食盐水法可以存贮氯气,所以装置I可以用来收集多余的
氯气,而II、Ⅲ不能形成较大压强差,在使用氯气时不能将多余的氯气排出,故选Ⅰ;(5)①用KCrO 溶液作指示剂,用足量硝酸酸化的0.020mol/LAgNO 溶液进行滴定,滴定终点的现象是:
2 4 3
当滴入最后半滴硝酸银标准溶液时,锥形瓶内出现砖红色沉淀﹐且半分钟内红棕色沉淀不消失,即为滴定
终点。
②n(AgNO)=0.025L×0.020mol/L=0.0005mol,由关系式NOCl~NaCl~AgNO 可知,n(NOCl)= 0005mol,
3 3
则样品的纯度为 ×100% 7.6%。
19.(15分)回答下列问题:
I.如图为工业合成氨的流程图:
(1)图中采取的措施可提高原料转化率的是 (填序号)。
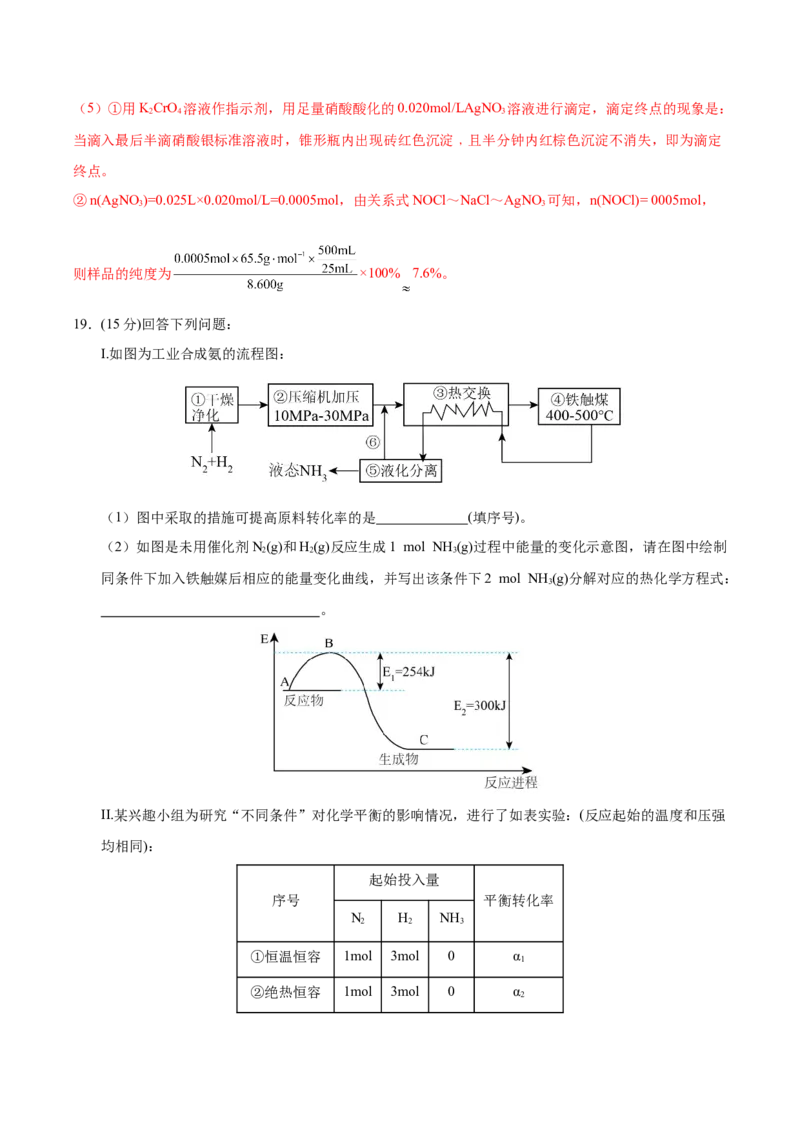
(2)如图是未用催化剂N(g)和H(g)反应生成1 mol NH (g)过程中能量的变化示意图,请在图中绘制
2 2 3
同条件下加入铁触媒后相应的能量变化曲线,并写出该条件下2 mol NH (g)分解对应的热化学方程式:
3
。
II.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如表实验:(反应起始的温度和压强
均相同):
起始投入量
序号 平衡转化率
N H NH
2 2 3
①恒温恒容 1mol 3mol 0 α
1
②绝热恒容 1mol 3mol 0 α
2③恒温恒压 2mol 6mol 0 α
3
(3)则:α α 、α α (填“>”、“=”或“<”)。
1 2 1 3
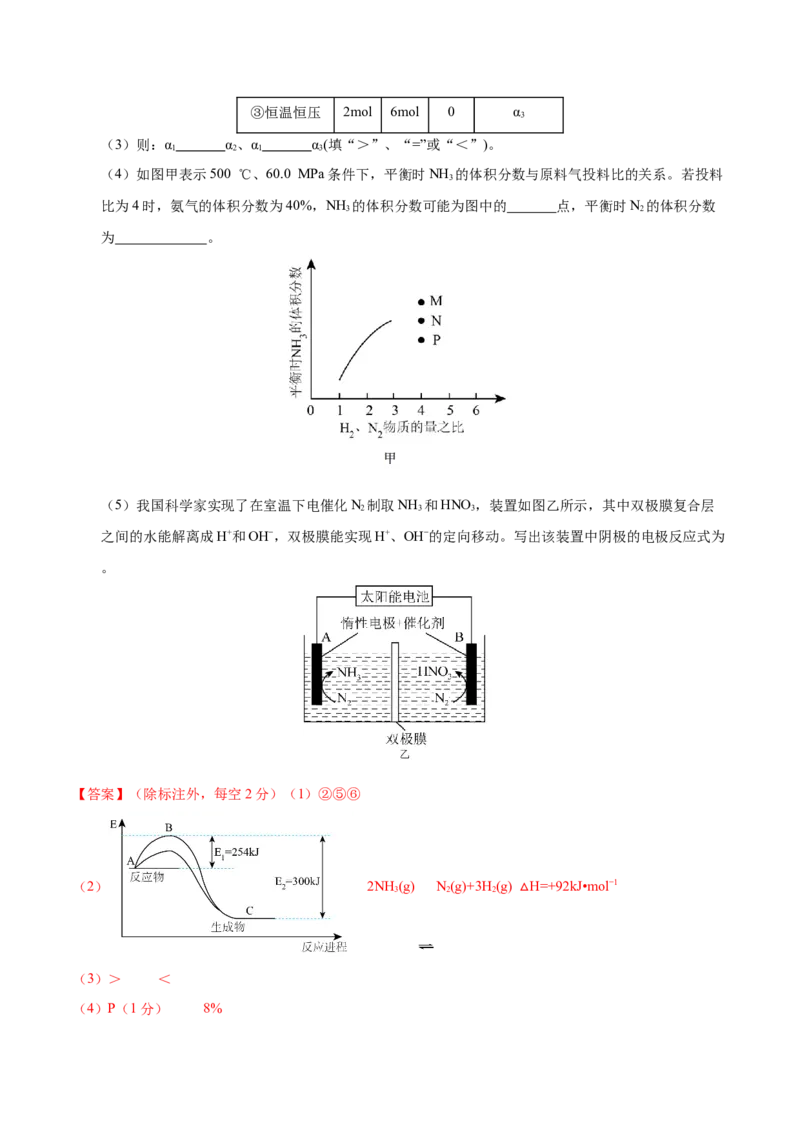
(4)如图甲表示500 ℃、60.0 MPa条件下,平衡时NH 的体积分数与原料气投料比的关系。若投料
3
比为4时,氨气的体积分数为40%,NH 的体积分数可能为图中的 点,平衡时N 的体积分数
3 2
为 。
(5)我国科学家实现了在室温下电催化N 制取NH 和HNO,装置如图乙所示,其中双极膜复合层
2 3 3
之间的水能解离成H+和OH−,双极膜能实现H+、OH−的定向移动。写出该装置中阴极的电极反应式为
。
【答案】(除标注外,每空2分)(1)②⑤⑥
(2) 2NH (g) N(g)+3H(g) H=+92kJ•mol−1
3 2 2
△
(3)> <
(4)P(1分) 8%(5)N+6e−+6H+=2NH
2 3
【解析】(1)合成氨反应是气体体积减小的放热反应,增大压强和降低温度可以提高原料转化率,增大
反应物浓度或降低生成物浓度,也可以提高原料转化率;压缩机加压、将氨液化分离并将氮气和氢气送回
合成塔中都可以提高原料的转化率,故选②⑤⑥。
(2)铁触媒作为催化剂,能降低反应的活化能,则同条件下加入铁触媒后相应的能量变化曲线为
;从图中可以看出,1mol氨分解吸收300kJ−254kJ=46kJ的热
量,则2mol氨分解吸收92kJ的热量,热化学方程式为:2NH (g) N(g)+3H(g) H=+92kJ•mol−1。
3 2 2
(3)①和②比较:该反应放热,②中绝热,则②中温度升高,温度的升高会使平衡△逆向移动,则α
1
>α
2
;
①和③比较:该反应为分子数减小的反应,恒容条件下,压强减小,会使平衡逆向移动,不利于氨气的生
成,则α <α 。
1 3
(4)合成氨反应中,当氢气和氮气的物质的量之比为方程式的系数比即3:1时,平衡时氨的体积分数最
大,所以投料比为4时,氨的体积分数减小,故为P点;设起始时投入的氢气为4mol,则氮气为1mol,设
转化的氮气为x mol,可列三段式:
,氨气的体积分数为40%,则有 ,x=
,氮气的体积分数为 =8%。
(5)在电解池中,阳离子向阴极移动,所以H+向阴极移动,在阴极,氮气得到电子生成氨气,则电极反
应式为N+6e−+6H+=2NH。
2 3