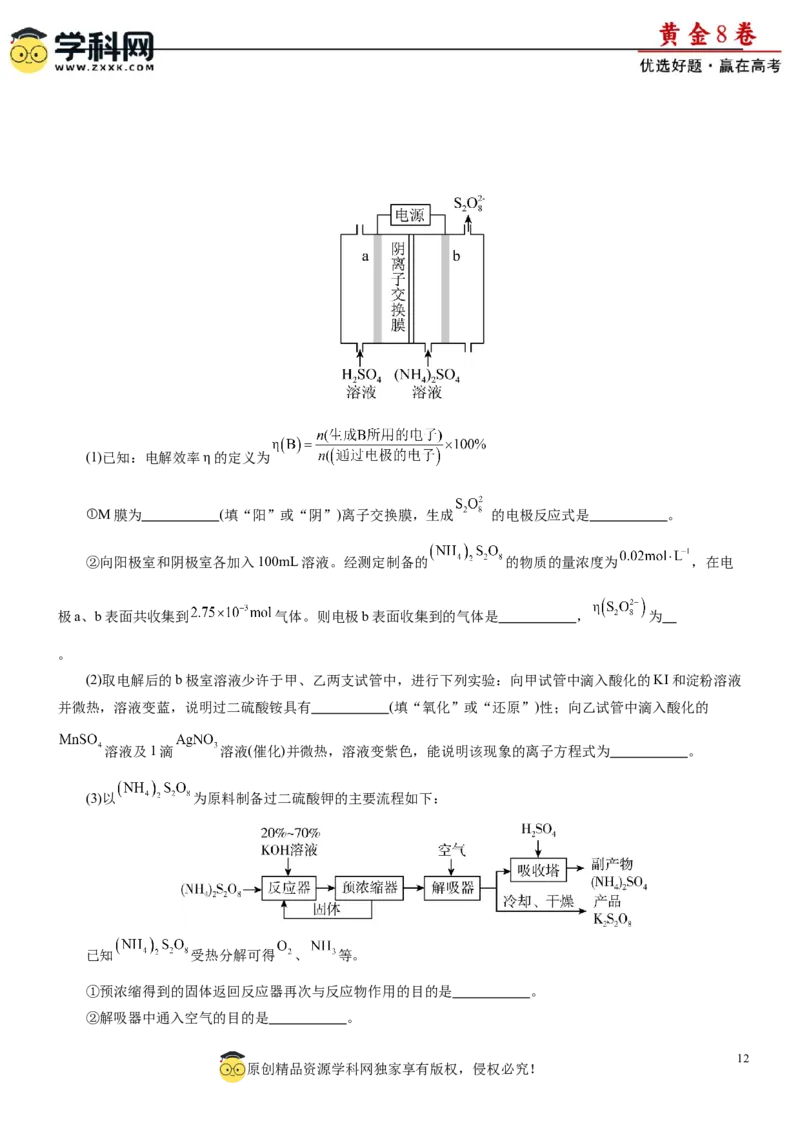
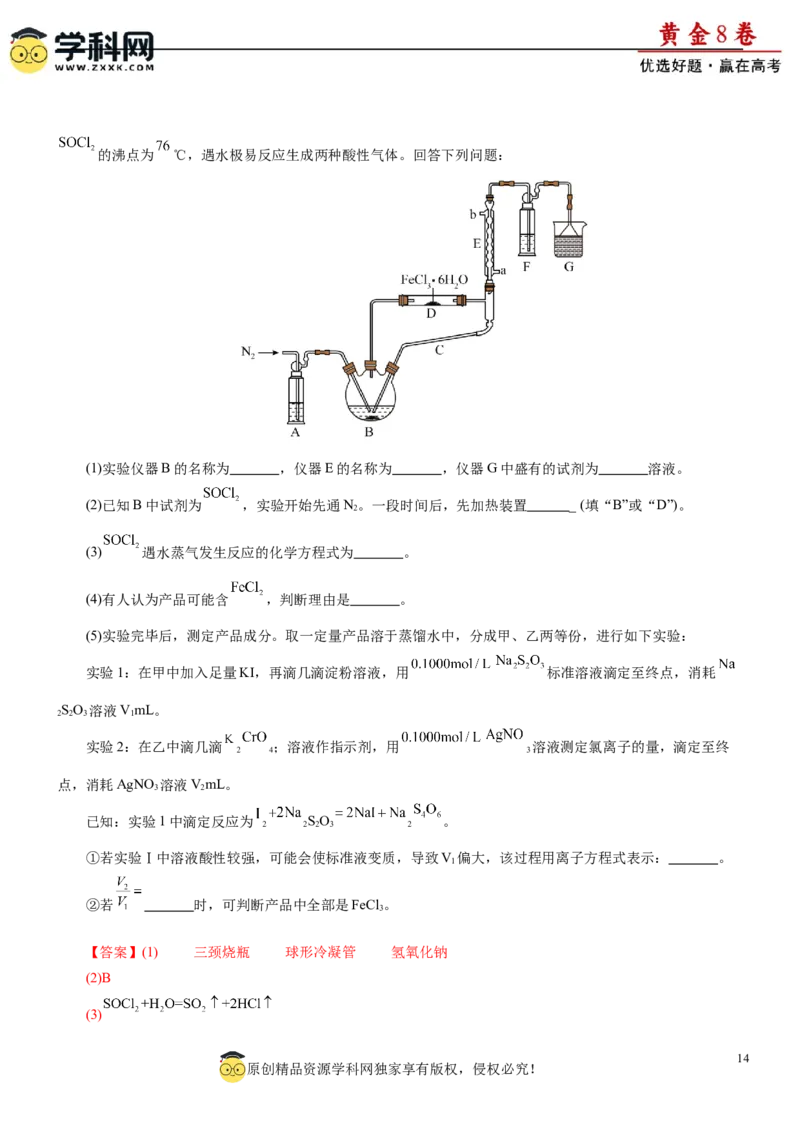
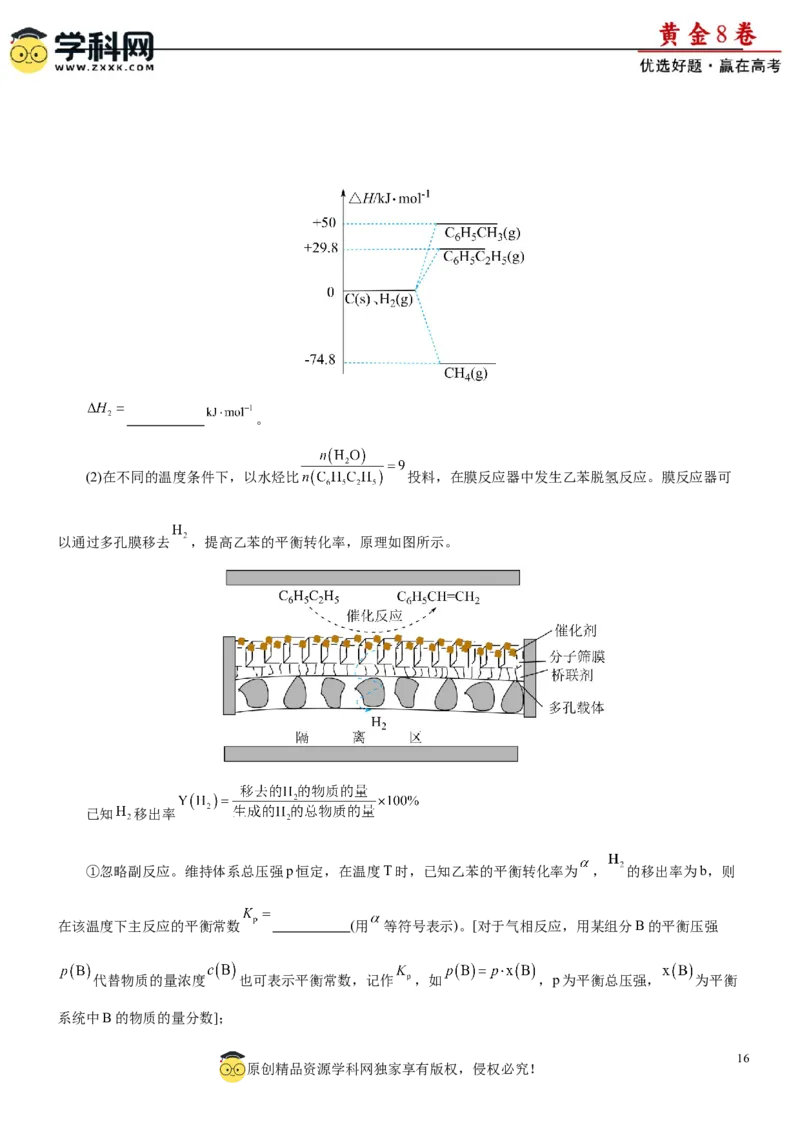
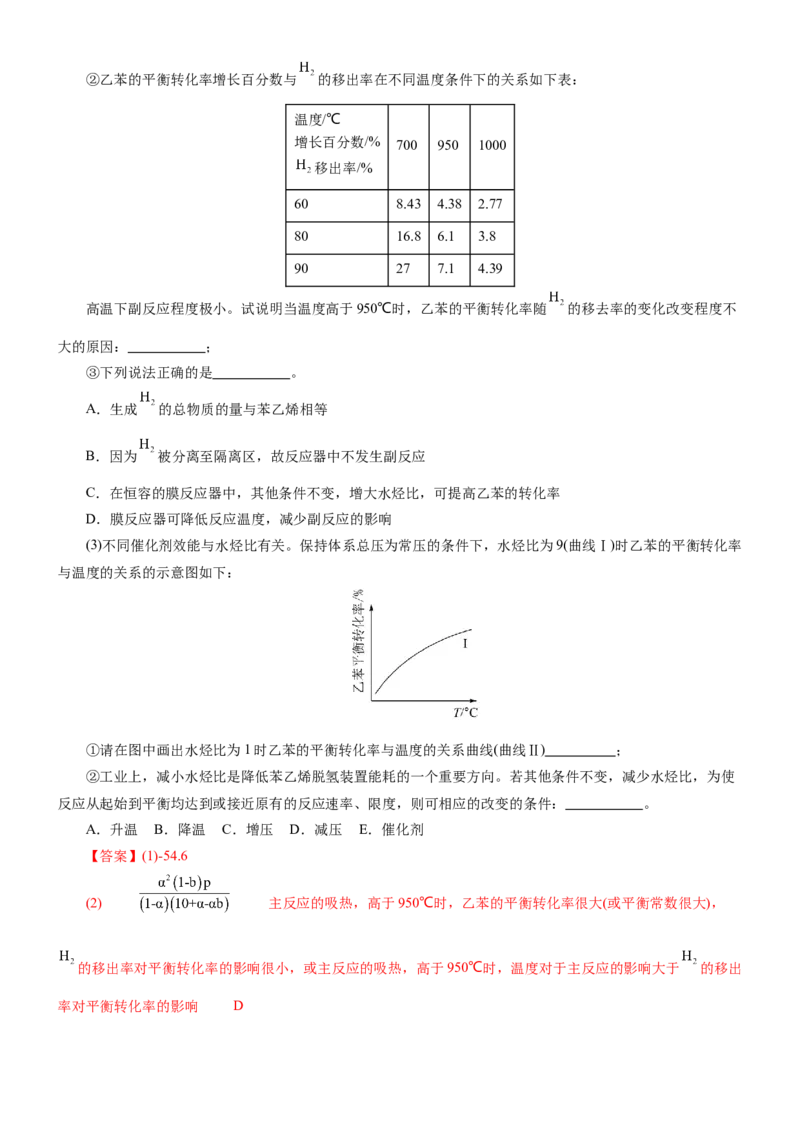
文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷01
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.近年来我国取得了很多令世界瞩目的科技成果,化学学科在“国之重器”的打造中发挥着重要作用。下
列有关说法正确的是
A.神州十五号载人飞船返回东风着陆场,返回舱逃逸系统复合材料中的酚醛树脂属于合成纤维
B.制造5G芯片的氮化铝晶圆属于传统无机非金属材料
C.“神州十六号”载人飞船使用砷化镓太阳能电池,砷化镓是一种分子晶体
D.“鲲龙”水陆两栖飞机实现海上首飞,其所用燃料航空煤油是石油分馏产品
【答案】D
【解析】A.酚醛树脂是一种合成塑料,不属于合成纤维,A错误;
B.氮化铝属于新型无机非金属材料,不是传统无机非金属材料,B错误;
C.砷化镓为原子晶体,不是分子晶体,C错误;
D.石油分馏得到煤油等物质,航空煤油通过石油分馏得到,D正确;故答案选D。
2.下列化学用语表示正确的是
A.用电子式表示HCl的形成过程:
B.基态Fe原子的价层电子轨道表示式:
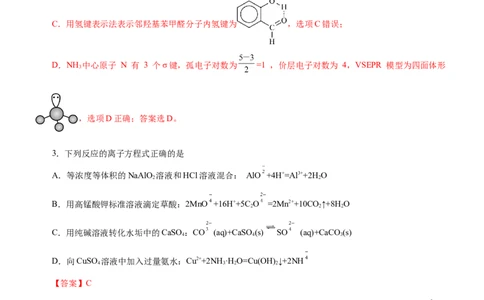
C.邻羟基苯甲醛分子内氢键示意图:
D. 的VSEPR模型:
【答案】D
【解析】A.HCl是共价化合物,H原子和Cl原子通过电子对的共用形成共价键,故用电子式表示形成过程为 ·· ·· ,选项A错误;
H · + · Cl· · H· · Cl· ·
·· ··
B.Fe是26号元素,基态Fe原子的价层电子排布式为3d64s2,价层电子轨道表示式为:
,选项B错误;
C.用氢键表示法表示邻羟基苯甲醛分子内氢键为 ,选项C错误;
D.NH 中心原子 N 有 3 个σ键,孤电子对数为 =1 ,价层电子对数为 4,VSEPR 模型为四面体形
3
,选项D正确;答案选D。
3.下列反应的离子方程式正确的是
A.等浓度等体积的NaAlO 溶液和HCl溶液混合: AlO +4H+=Al3++2H O
2 2
B.用高锰酸钾标准溶液滴定草酸:2MnO +16H++5C O =2Mn2++10CO ↑+8H O
2 2 2
C.用纯碱溶液转化水垢中的CaSO:CO (aq)+CaSO (s) SO (aq)+CaCO (s)
4 4 3
D.向CuSO 溶液中加入过量氨水:Cu2++2NH·H O=Cu(OH) ↓+2NH
4 3 2 2
【答案】C
【解析】A.等浓度等体积的NaAlO 溶液和HCl溶液混合生成Al(OH) 沉淀,故离子方程式为: AlO +H+
2 3
+H O= Al(OH) ↓,A错误;
2 3
B.草酸是弱酸,离子方程式中不能拆,故用高锰酸钾标准溶液滴定草酸的离子方程式为:2MnO +6H+
+5H C O=2Mn2++10CO ↑+8H O,B错误;
2 2 4 2 2
C.用纯碱溶液转化水垢中的CaSO 的离子方程式为:CO (aq)+CaSO (s) SO (aq)+CaCO (s),C正
4 4 3
确;
D.向CuSO 溶液中加入过量氨水生成Cu(NH )SO 溶液,故离子方程式为:Cu2++4NH·H O=[Cu(NH3) ]2+
4 3 4 4 3 2 4
2
原创精品资源学科网独家享有版权,侵权必究!+4H O,D错误;故答案为:C。
2
4.化学是以实验为基础的学科。下列实验操作、现象和结论均正确的是
选
实验操作 实验现象 结论
项
A 向某溶液滴入氯水后再滴KSCN溶液 溶液变红色 该溶液一定含
溶液中出现白色沉 原溶液中一定含有
B 向某溶液中滴入硝酸钡溶液
淀
溶液由黄色变浅绿
C 将维生素C研细加入三氯化铁溶液中 维生素C有还原性
色
将海带灰浸出液过滤,在滤液中加入氯水,再滴几滴淀粉
D 溶液呈蓝色 海带中含碘单质
溶液
【答案】C
【解析】A.原溶液可能本来就存在 ,A错误;
B.如果溶液显酸性,向溶液中加入硝酸根,在酸性环境下硝酸根具有强氧化性,可能把原溶液的 氧
化成了 ,B错误;
C. 溶液加入维C后黄色变浅绿色,说明 被还原为 ,维C有还原性,C正确;
D.碘离子被氧化为碘单质,海带中含的是 ,而不是 ,D错误;故选C。
5.在化学元素史上,氟元素的发现是参与人数最多、工作最难的研究课题之一,从发现氢氟酸到制得单质
氟,历时118年之久。设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.在标准状况下,22.4L 与足量水反应生成 的分子数为0.25 N
A
B. 氟蒸气和 氢气充分反应,转移电子数小于2 N
A
C.在标准状况下,22.4LHF所含的质子数为10 N
A
D. 的氟化钠水溶液中 与 离子数之和大于N
A
【答案】D
【解析】A.氟气与水反应生成氢氟酸和氧气,由得失电子数目守恒可知,标准状况下22.4L氟气与足量水
反应生成氧气的分子数为 × ×N mol—1=0.5N ,故A错误;
A A
B.氟气与氢气反应生成氟化氢,则1mol氟气与1mol氢气充分反应生成氟化氢时,转移电子数目为
1mol×2×N mol—1=2N ,故B错误;
A A
C.标准状况下,氟化氢为液态,则无法计算22.4L氟化氢的物质的量和含有的质子数,故C错误;D.氟化钠为强碱弱酸盐,氟离子在溶液中水解使溶液中阴离子数目增大,则1L1mol/L氟化钠溶液中氟离
子和氢氧根离子的数目之和大于1mol/L×1L×N mol—1=N ,故D正确;故选D。
A A
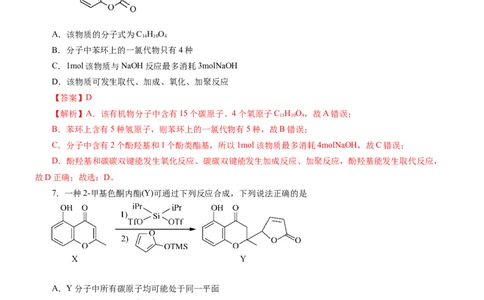
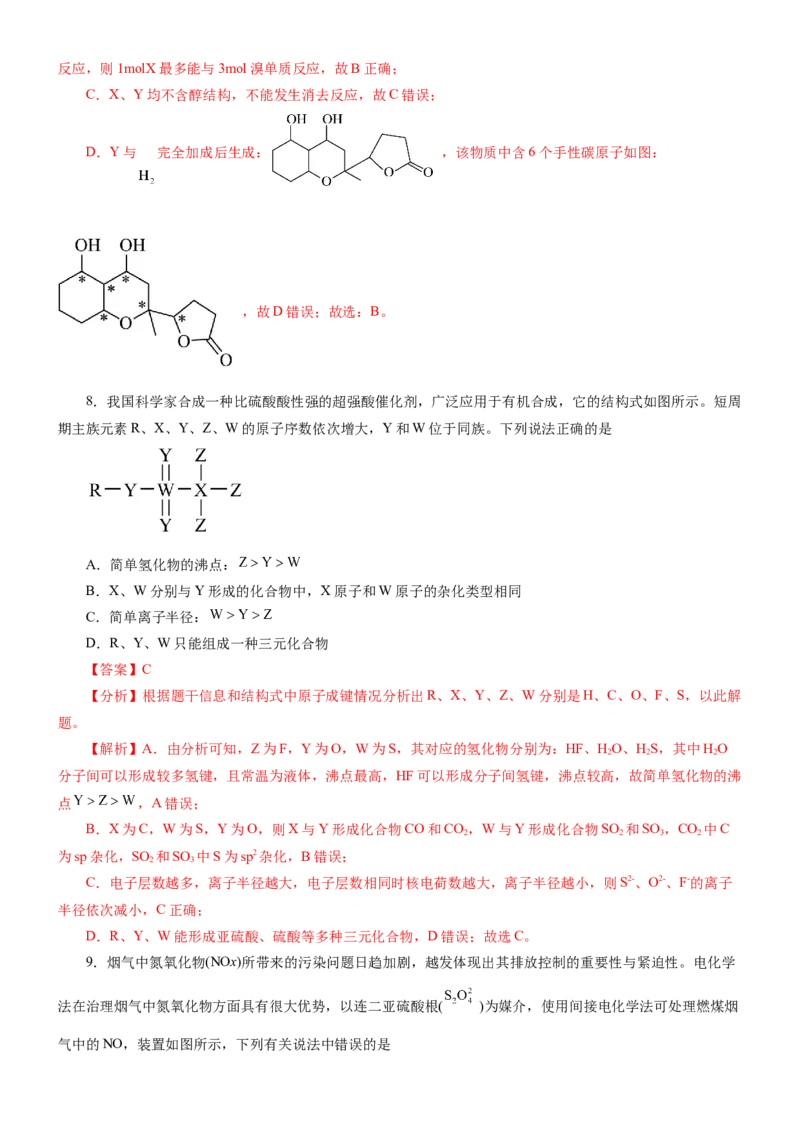
6.复旦大学科研团队发现了一种“小分子胶水”,能助力自噬细胞吞没致病蛋白,其结构如图。下列有关
该物质说法正确的是
A.该物质的分子式为C H O
14 10 4
B.分子中苯环上的一氯代物只有4种
C.1mol该物质与NaOH反应最多消耗3molNaOH
D.该物质可发生取代、加成、氧化、加聚反应
【答案】D
【解析】A.该有机物分子中含有15个碳原子、4个氧原子C H O,故A错误;
15 10 4
B.苯环上含有5种氢原子,则苯环上的一氯代物有5种,故B错误;
C.分子中含有2个酚羟基和1个酚类酯基,所以1mol该物质最多消耗4molNaOH,故C错误;
D.酚羟基和碳碳双键能发生氧化反应、碳碳双键能发生加成反应、加聚反应,酚羟基能发生取代反应,
故D正确;故选:D。
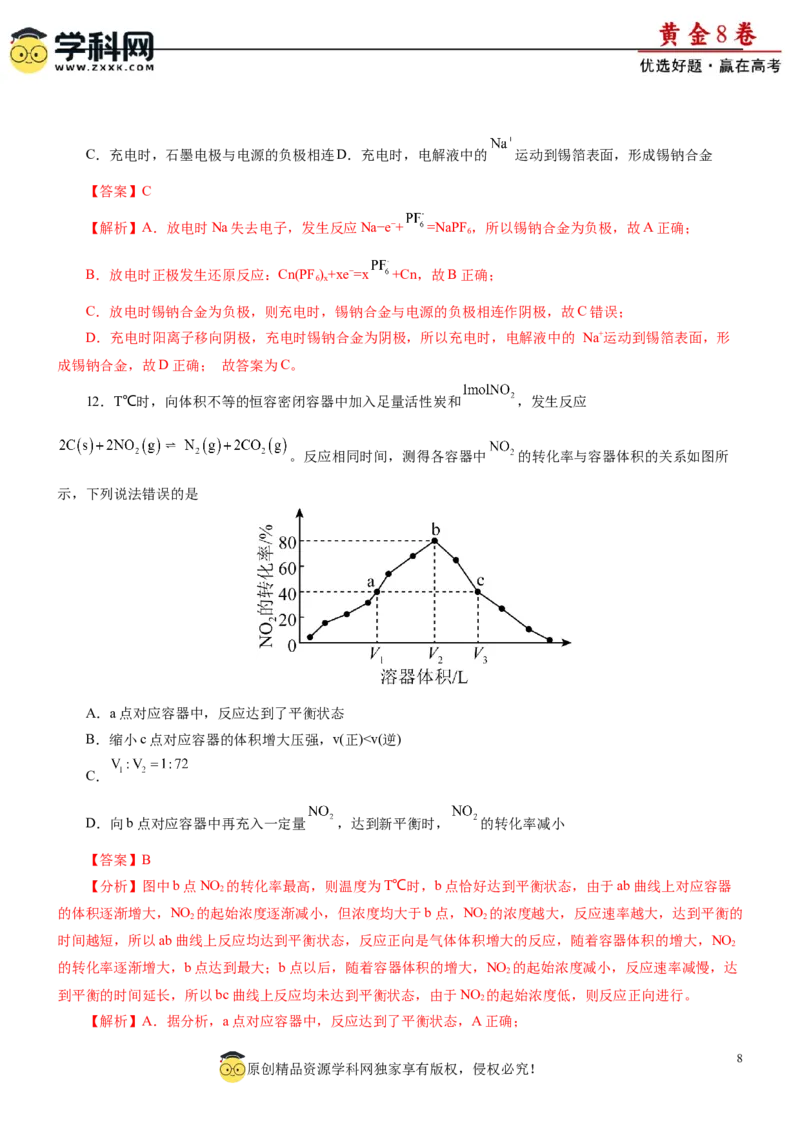
7.一种2-甲基色酮内酯(Y)可通过下列反应合成,下列说法正确的是
A.Y分子中所有碳原子均可能处于同一平面
B. 最多能与含 的浓溴水发生反应
C.X、Y在浓硫酸催化下加热可发生消去反应
D.Y与 完全加成的产物分子中含有5个手性碳原子
【答案】B
【解析】A.由结构简式可知Y中存在与三个碳原子直接相连的饱和碳原子,该碳原子呈四面体构型,所
有碳原子不可能处于同一平面上,故A错误;
B.X中含有2个酚羟基邻、对位氢原子可与溴单质发生取代反应,含有1个碳碳双键能与溴单质发生加成
4
原创精品资源学科网独家享有版权,侵权必究!反应,则1molX最多能与3mol溴单质反应,故B正确;
C.X、Y均不含醇结构,不能发生消去反应,故C错误;
D.Y与 完全加成后生成: ,该物质中含6个手性碳原子如图:
,故D错误;故选:B。
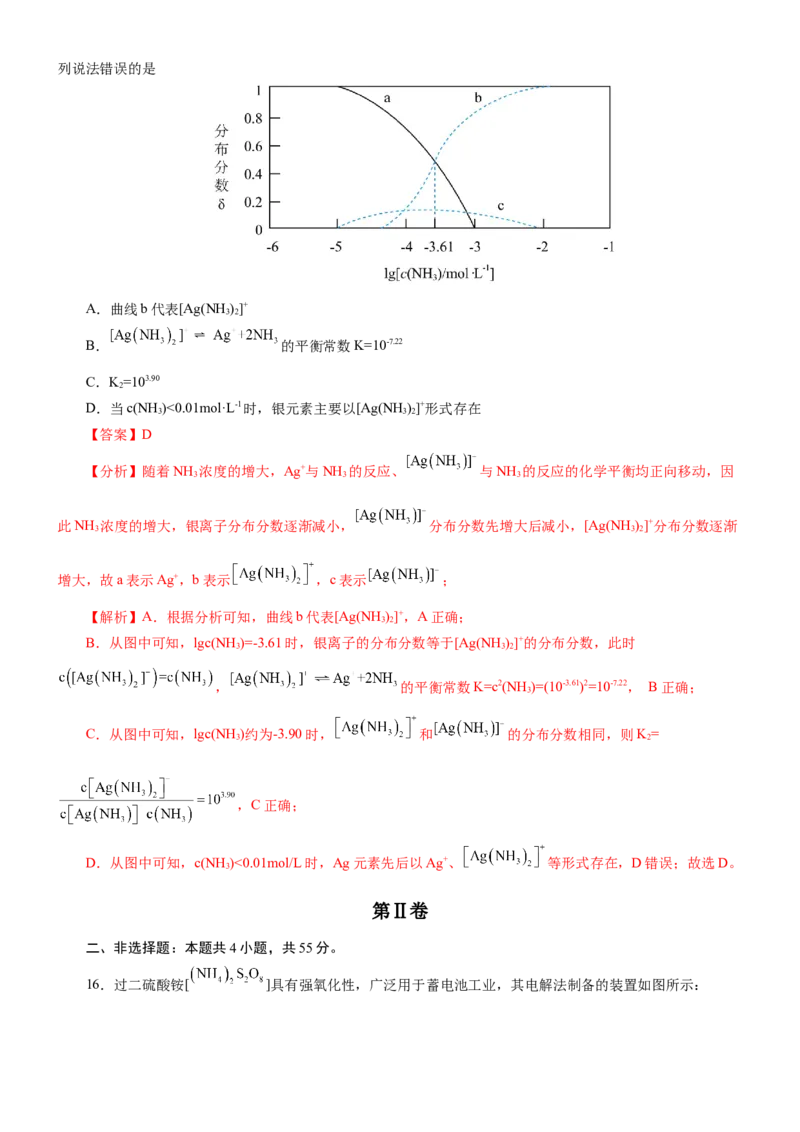
8.我国科学家合成一种比硫酸酸性强的超强酸催化剂,广泛应用于有机合成,它的结构式如图所示。短周
期主族元素R、X、Y、Z、W的原子序数依次增大,Y和W位于同族。下列说法正确的是
A.简单氢化物的沸点:
B.X、W分别与Y形成的化合物中,X原子和W原子的杂化类型相同
C.简单离子半径:
D.R、Y、W只能组成一种三元化合物
【答案】C
【分析】根据题干信息和结构式中原子成键情况分析出R、X、Y、Z、W分别是H、C、O、F、S,以此解
题。
【解析】A.由分析可知,Z为F,Y为O,W为S,其对应的氢化物分别为:HF、HO、HS,其中HO
2 2 2
分子间可以形成较多氢键,且常温为液体,沸点最高,HF可以形成分子间氢键,沸点较高,故简单氢化物的沸
点 ,A错误;
B.X为C,W为S,Y为O,则X与Y形成化合物CO和CO,W与Y形成化合物SO 和SO ,CO 中C
2 2 3 2
为sp杂化,SO 和SO 中S为sp2杂化,B错误;
2 3
C.电子层数越多,离子半径越大,电子层数相同时核电荷数越大,离子半径越小,则S2-、O2-、F-的离子
半径依次减小,C正确;
D.R、Y、W能形成亚硫酸、硫酸等多种三元化合物,D错误;故选C。
9.烟气中氮氧化物(NOx)所带来的污染问题日趋加剧,越发体现出其排放控制的重要性与紧迫性。电化学
法在治理烟气中氮氧化物方面具有很大优势,以连二亚硫酸根( )为媒介,使用间接电化学法可处理燃煤烟
气中的NO,装置如图所示,下列有关说法中错误的是A.Pt电极区电极反应式为
B.C电极区得到的产物有 和较浓的硫酸
C.离子交换膜为阴离子交换膜,电解质中的 从C电极区向Pt电极区移动
D.若电路中转移了 ,则此通电过程中理论上吸收的NO的体积为5.6L(标准状况)
【答案】C
【分析】NO与连二亚硫酸根离子发生氧化还原反应,生成氮气和亚硫酸根离子,亚硫酸根离子进入阴极
区发生还原反应,生成连二亚硫酸离子,阳极区水电离的氢氧根离子放电,发生氧化反应,生成氧气和氢离
子,水被消耗导致硫酸浓度增大;
【解析】A.Pt电极的亚硫酸根离子得到电子发生还原反应,生成连二亚硫酸离子,电极反应式为
,A正确;
B.由分析可知,C电极区得到的产物有 和较浓的硫酸,B正确;
C.离子交换膜为阳离子交换膜,阳极生成的氢离子从C电极区向Pt电极区移动,C错误;
D.反应中氮元素化合价由+2变为0: ,若电路中转移了 ,则此通电过程中理论上吸收
的0.25molNO,其体积为5.6L(标准状况),D正确;故选C。
10.实验室以浓缩盐湖水(含Na+、Li+、Cl-和少量Mg2+、Ca2+)为原料制备高纯LiCO 的实验流程如下:
2 3
6
原创精品资源学科网独家享有版权,侵权必究!LiCO 溶解度曲线如图所示
2 3
下列说法错误的是
A.“步骤Ⅰ”“步骤Ⅱ”中均需使用漏斗
B.“沉淀2”的主要成分为CaCO
3
C.“操作X”依次为蒸发浓缩、降温结晶、过滤、洗涤、干燥
D.“滤液3”经除杂后可用作氯碱工业的原料
【答案】C
【分析】浓缩盐湖水(含Na+、Li+、Cl-和少量Mg2+、Ca2+)中加入Ca(OH) ,可将Mg2+转化为沉淀,经过滤
2
得沉淀1主要为Mg(OH) ;往滤液1中加入LiCO,可将Ca2+转化为沉淀,经过滤得沉淀2主要为CaCO ,过
2 2 3 3
滤后滤液2中继续加入浓度较大的NaCO 溶液,同时升高温度,可将Li+转化为LiCO 沉淀,所得滤液3主要
2 3 2 3
为氯化钠溶液。
【解析】A. “步骤Ⅰ”“步骤Ⅱ”用于分离溶液和沉淀,为过滤操作,均需使用漏斗,A正确;
B. 据分析,“沉淀2”的主要成分为CaCO ,B正确;
3
C.题干信息显示,LiCO 在冷水中溶解度较热水中大,所以 “操作X”依次为蒸发结晶、趁热过滤、洗
2 3
涤、干燥,C不正确;
D.滤液3主要为氯化钠溶液,“滤液3”经除杂后可用作氯碱工业的原料,D正确;答案选C。
11.我国科学院深圳研究中心研究员唐永炳及其团队成功研发出一种新型高性能、低成本的锡-石墨钠型双
离子电池,其结构原理如图所示。该电池采用锡箔(不参与电极反应)作为电池电极和集流体,另一电极材料为
石墨(Cn),电解液采用溶于有机溶剂中的六氟磷酸钠。下列有关说法错误的是
A.放电时,锡钠合金为负极 B.放电时,正极反应为:C.充电时,石墨电极与电源的负极相连D.充电时,电解液中的 运动到锡箔表面,形成锡钠合金
【答案】C
【解析】A.放电时Na失去电子,发生反应Na−e−+ =NaPF,所以锡钠合金为负极,故A正确;
6
B.放电时正极发生还原反应:Cn(PF )+xe−=x +Cn,故B正确;
6 x
C.放电时锡钠合金为负极,则充电时,锡钠合金与电源的负极相连作阴极,故C错误;
D.充电时阳离子移向阴极,充电时锡钠合金为阴极,所以充电时,电解液中的 Na+运动到锡箔表面,形
成锡钠合金,故D正确; 故答案为C。
12.T℃时,向体积不等的恒容密闭容器中加入足量活性炭和 ,发生反应
。反应相同时间,测得各容器中 的转化率与容器体积的关系如图所
示,下列说法错误的是
A.a点对应容器中,反应达到了平衡状态
B.缩小c点对应容器的体积增大压强,v(正)