文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷03
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.物质的性质决定用途,下列两者关系对应不正确的是
A.铝合金质量轻、强度大,可用作制造飞机和宇宙飞船的材料
B.FeCl 溶液呈酸性,可腐蚀覆铜板制作印刷电路板
3
C.CuS、HgS极难溶,可用NaS作沉淀剂除去废水中的Cu2+和Hg2+
2
D.碳化硅硬度大,可用作砂纸、砂轮的磨料
2.下列化学用语正确的是
A.乙醛的分子式; B.2—丁烯的键线式:
C.二氧化碳的空间填充模型: D.基态氮原子的价电子排布图:
3.下列有关方程式的书写中,错误的是
A. 除去废水中的 :
B.钢铁吸氧腐蚀的正极反应:
C.Al与NaOH溶液反应:
D. 检验 :
4.几种物质在水溶液中的转化关系如图所示(依次发生反应1、2 和3)。
已知:NaBiO 微溶于水。下列叙述错误的是
3
A.反应1 中氧化剂是 NaBiO
3
B.反应2 说明氧化性:
C.反应3 中:2mol 能氧化3mol C HOH
2 5D.向乙二醇中滴加足量酸性 KMnO 溶液,最终生成乙二酸
4
5.下列有关实验的图示中,正确的是
A.实验室配制银氨溶液 B.分离 和 固体 C.测定 溶液的 D.滴定前装液排气泡
6.利用铝电解厂烟气制备冰晶石( )的流程如下图所示。下列叙述错误的是
A.冰品石常用作电解制备铝的助熔剂
B.滤液可进入吸收塔中回收利用
C.实验室模拟吸收塔中的反应不宜选用玻璃仪器
D.吸收塔中发生的反应为
7.M、W、X、Y、Z是五种原子序数依次增大的短周期主族元素,其原子序数之和为31;其中Y的最外
层电子数等于 X 的核外电子总数;五种主族元素组成的化合物Q的结构如图所示。下列说法错误的是
A.原子半径:
B.X 的氧化物属于酸性氧化物
C.Y 元素组成的最常见单质和M的单质,在加热条件下生成的化合
物中只含离子键
D.在Q 的结构中,除M外,其余原子最外层均满足8 电子稳定结构
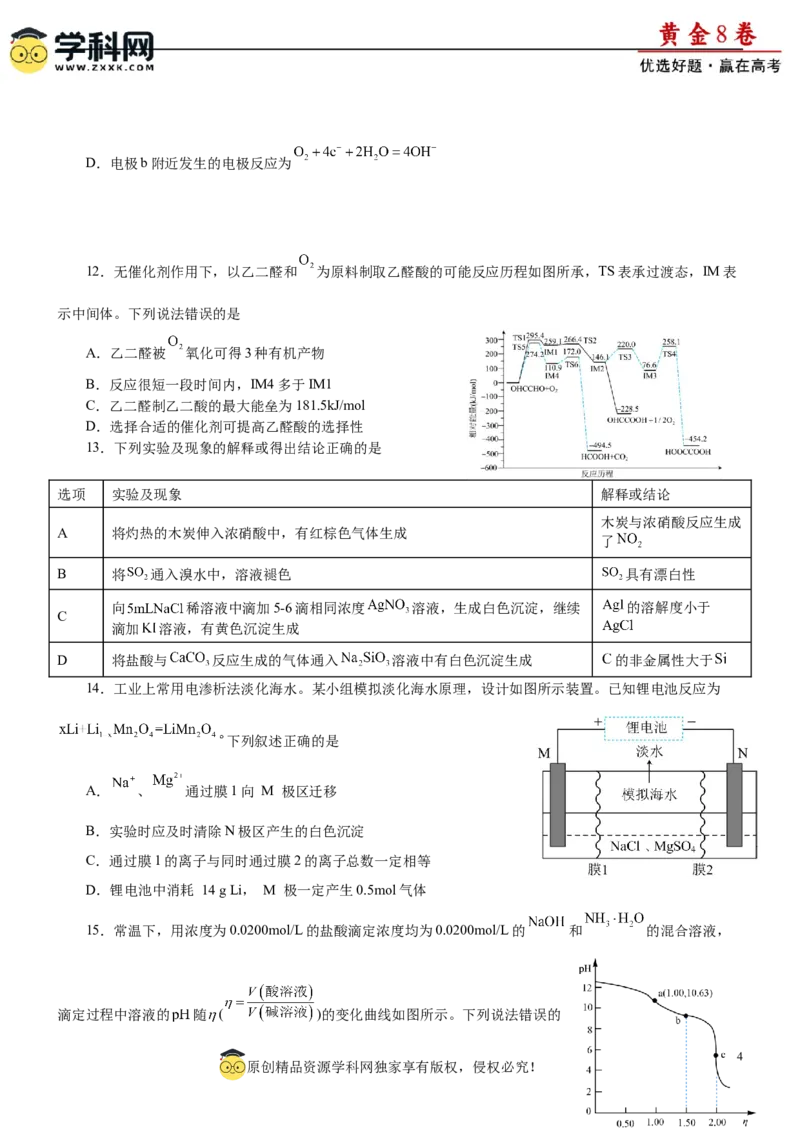
8.苯烯莫德是全球首个芳香经受体激动剂,可用于治疗多种自身免疫性疾病,其结构简式如图所示。下列
说法正确的是
A.可发生氧化反应和消去反应
B.所有碳原子可能处于同一平面
2
原创精品资源学科网独家享有版权,侵权必究!C.完全氢化后所得产物中含2个手性碳原子
D.与足量浓溴水反应最多可消耗
9.KIO 晶体具有钙钛矿型的立方结构,其一种晶胞如图所示,其中顶点为K,晶胞边长为a pm,下列说
3
法正确的是
A.碘氧键的键长为
B.距离K最近的O有12个
C.KIO 的另一种晶胞图中,若I在顶点,则O在体心
3
D.晶体密度
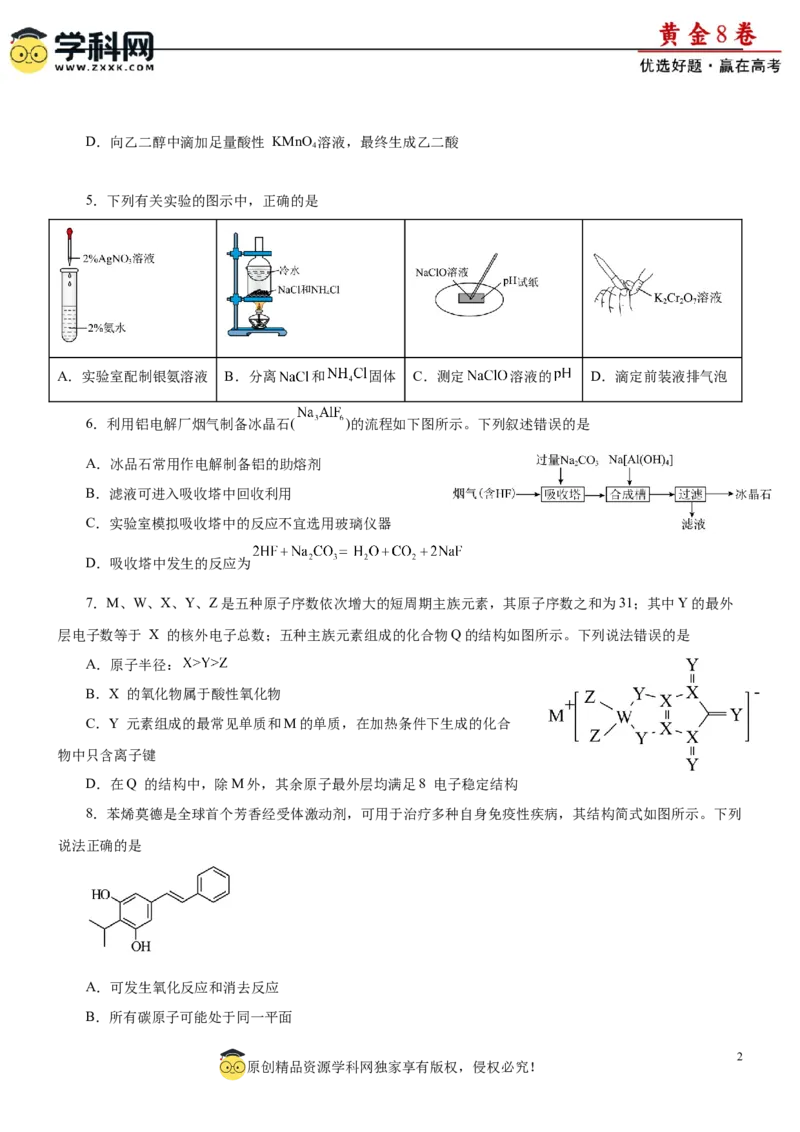
10.CO 氧化乙苯脱氢制苯乙烯的反应方程式是: (g)+CO (g)
2 2
+H O(g)+CO(g),其反应历程如图所示。下列有关说法正确的是
2
A.该反应的
B.该反应的平衡常数表达式为 ( -表示苯基)
C.催化剂表面酸性越强,苯乙烯的产率越高
D.过程③可能生成副产物
11.“打赢蓝天保卫战”,意味着对大气污染防治比过去要求更高。二氧化硫——空气质子交换膜燃料电
池实现了制硫酸、发电、环保三位一体的结合,原理如图所示。下列说法正确的是
A.该电池放电时质子从电极b移向电极a
B.相同条件下,放电过程中消耗的, 和 的体积比为2∶1
C.电极a附近发生的电极反应为D.电极b附近发生的电极反应为
12.无催化剂作用下,以乙二醛和 为原料制取乙醛酸的可能反应历程如图所承,TS表承过渡态,IM表
示中间体。下列说法错误的是
A.乙二醛被 氧化可得3种有机产物
B.反应很短一段时间内,IM4多于IM1
C.乙二醛制乙二酸的最大能垒为181.5kJ/mol
D.选择合适的催化剂可提高乙醛酸的选择性
13.下列实验及现象的解释或得出结论正确的是
选项 实验及现象 解释或结论
木炭与浓硝酸反应生成
A 将灼热的木炭伸入浓硝酸中,有红棕色气体生成
了
B 将 通入溴水中,溶液褪色 具有漂白性
向 稀溶液中滴加5-6滴相同浓度 溶液,生成白色沉淀,继续 的溶解度小于
C
滴加 溶液,有黄色沉淀生成
D 将盐酸与 反应生成的气体通入 溶液中有白色沉淀生成 的非金属性大于
14.工业上常用电渗析法淡化海水。某小组模拟淡化海水原理,设计如图所示装置。已知锂电池反应为
下列叙述正确的是
A. 、 通过膜1向 M 极区迁移
B.实验时应及时清除N极区产生的白色沉淀
C.通过膜1的离子与同时通过膜2的离子总数一定相等
D.锂电池中消耗 14 g Li, M 极一定产生0.5mol气体
15.常温下,用浓度为0.0200mol/L的盐酸滴定浓度均为0.0200mol/L的 和 的混合溶液,
滴定过程中溶液的 随 ( )的变化曲线如图所示。下列说法错误的
4
原创精品资源学科网独家享有版权,侵权必究!是
A. 约为
B.点a:
C.点b:
D.水的电离程度;
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
16.锑( )冶炼过程中产生的副产物主要成分为 、 、 和 等,因含银量很高,是重要
的银提取原料。从该副产物中提取银的工艺流程如下:
已知:①水合肼为 ,有很强的还原性;
② 在碱性条件下易转化为 ;
③常温下, 的溶解度为 , 的溶解度为0.79g。
回答下列问题:
(1) 的电子式为 。
(2)脱氯渣的主要成分有 、 、 和 。
(3)“还原脱氧”过程中会产生无色无味无毒气体,则 发生反应的化学方程式为
。
(4)“氧化分银”中,不直接用硝酸的原因是 。
(5)“氧化分银”中,银被氧化的离子方程式为 。
(6)“沉铅过滤”中主要析出 的原因是 。
(7)“沉铅过滤”中硫酸的用量系数对铅和银的沉淀率影响如图所示。硫酸的用量系数最佳选择是 ,理由是 。
17.工业上利用天然气制备合成气(CO、H)的反应原理如下:
2
①
②
回答下列问题:
(1)一定温度下,向恒容密闭容器中充入 ,充分反应,测得 CH 的转
4
化率为20%,则合成气(CO、H)的总物质的量为 。
2
(2)一定温度下,在恒容密闭容器中充入 ,仅发生反应①。下列情况能表明该反应
已达到平衡状态的是___________(填字母)。
A.混合气体的密度不随时间变化 B.混合气体的压强不随时间变化
C.CH₄的体积分数不随时间变化 D.CO、H₂的浓度之比不随时间变化
(3)已知:i.
ii.
iii.
6
原创精品资源学科网独家享有版权,侵权必究!的△H= kJ∙mol−1(用含x、y、z的代数式表示)。
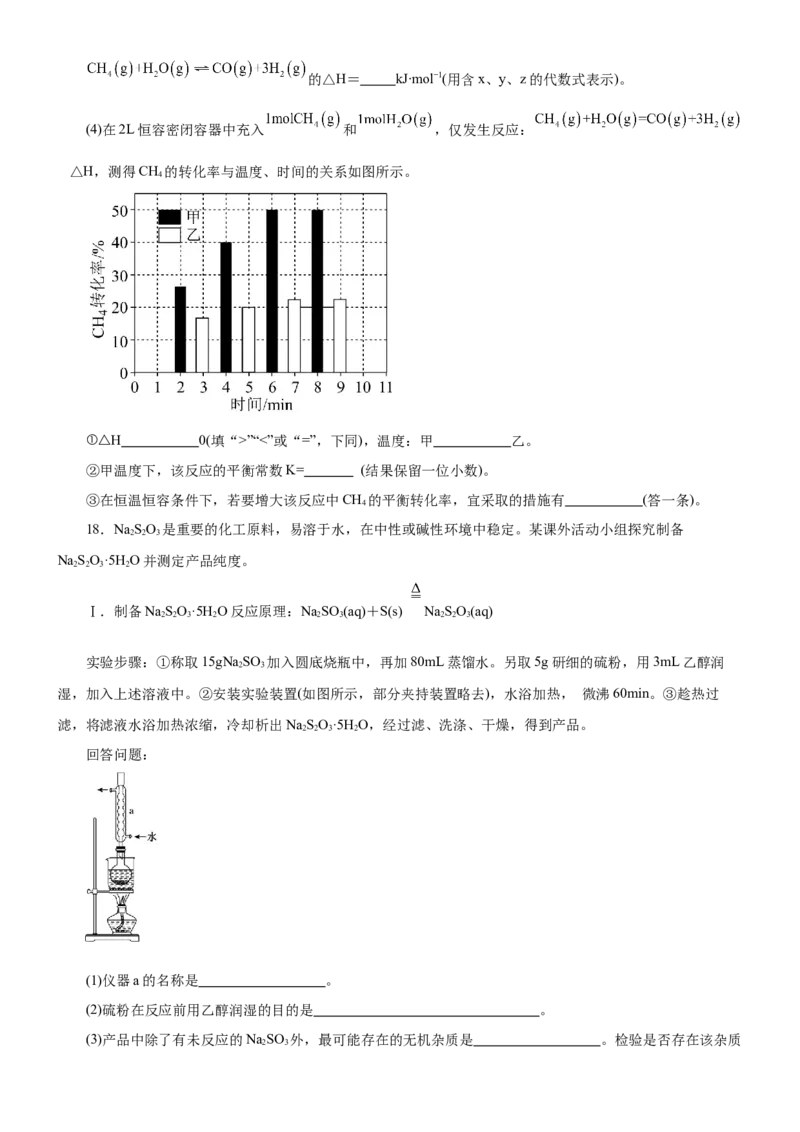
(4)在2L恒容密闭容器中充入 和 ,仅发生反应:
△H,测得CH 的转化率与温度、时间的关系如图所示。
4
①△H 0(填“>”“<”或“=”,下同),温度:甲 乙。
②甲温度下,该反应的平衡常数K= (结果保留一位小数)。
③在恒温恒容条件下,若要增大该反应中CH 的平衡转化率,宜采取的措施有 (答一条)。
4
18.NaSO 是重要的化工原料,易溶于水,在中性或碱性环境中稳定。某课外活动小组探究制备
2 2 3
NaSO·5H O并测定产品纯度。
2 2 3 2
Ⅰ.制备NaSO·5H O反应原理:NaSO (aq)+S(s) NaSO(aq)
2 2 3 2 2 3 2 2 3
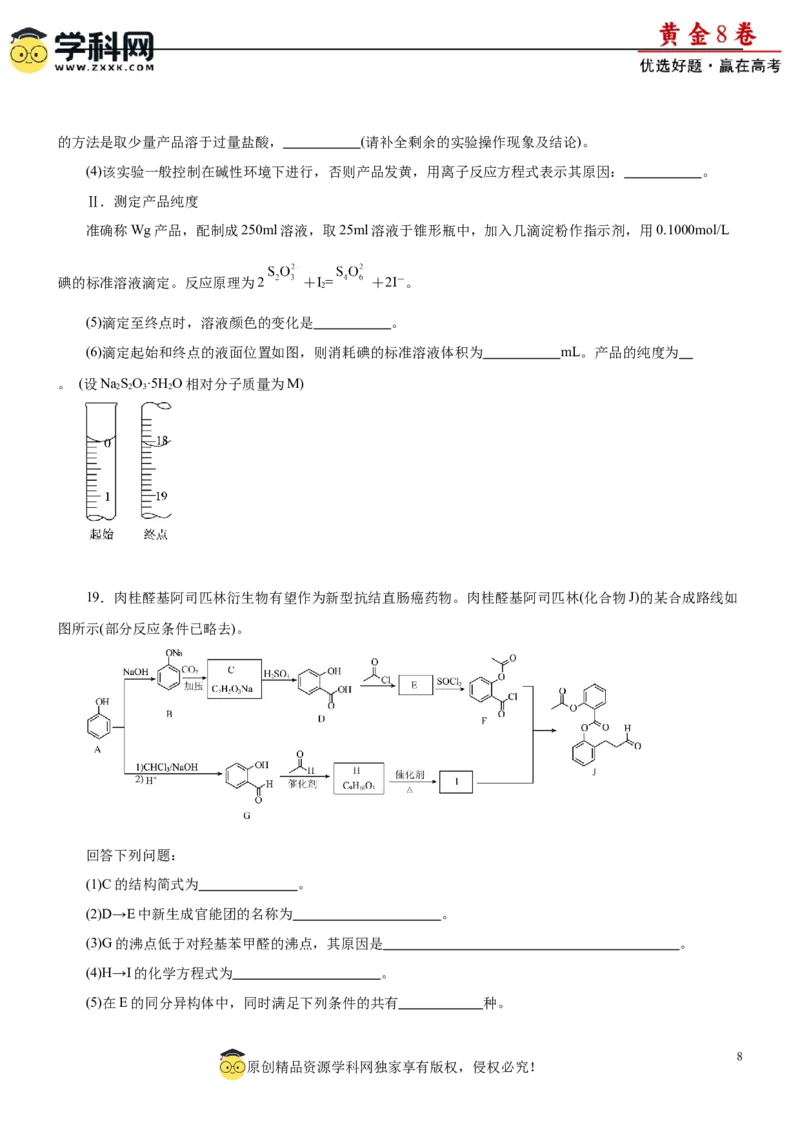
实验步骤:①称取15gNaSO 加入圆底烧瓶中,再加80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润
2 3
湿,加入上述溶液中。②安装实验装置(如图所示,部分夹持装置略去),水浴加热, 微沸60min。③趁热过
滤,将滤液水浴加热浓缩,冷却析出NaSO·5H O,经过滤、洗涤、干燥,得到产品。
2 2 3 2
回答问题:
(1)仪器a的名称是 。
(2)硫粉在反应前用乙醇润湿的目的是 。
(3)产品中除了有未反应的NaSO 外,最可能存在的无机杂质是 。检验是否存在该杂质
2 3的方法是取少量产品溶于过量盐酸, (请补全剩余的实验操作现象及结论)。
(4)该实验一般控制在碱性环境下进行,否则产品发黄,用离子反应方程式表示其原因: 。
Ⅱ.测定产品纯度
准确称Wg产品,配制成250ml溶液,取25ml溶液于锥形瓶中,加入几滴淀粉作指示剂,用0.1000mol/L
碘的标准溶液滴定。反应原理为2 +I= +2I-。
2
(5)滴定至终点时,溶液颜色的变化是 。
(6)滴定起始和终点的液面位置如图,则消耗碘的标准溶液体积为 mL。产品的纯度为
。 (设NaSO·5H O相对分子质量为M)
2 2 3 2
19.肉桂醛基阿司匹林衍生物有望作为新型抗结直肠癌药物。肉桂醛基阿司匹林(化合物J)的某合成路线如
图所示(部分反应条件已略去)。
回答下列问题:
(1)C的结构简式为 。
(2)D→E中新生成官能团的名称为 。
(3)G的沸点低于对羟基苯甲醛的沸点,其原因是 。
(4)H→I的化学方程式为 。
(5)在E的同分异构体中,同时满足下列条件的共有 种。
8
原创精品资源学科网独家享有版权,侵权必究!①含有苯环;②与E含有相同的官能团;③苯环上有两个取代基;④不含 结构
其中,核磁共振氢谱显示为4组峰,且峰面积比为3 : 2 : 2 : 1的结构简式为 (写出一种即可)。
(6)缓释阿司匹林(K)可控制阿司匹林分子在人体内的释放浓度与速度,发挥更好的药效,其合成路线如图:
则K的结构简式为 。