文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(上海专
用)
黄金卷06
(考试时间:60分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
一、钙钛矿材料的结构与性质(本题共18分)
钙钛矿型材料具有与天然钙矿(CaTiO )相同的晶体结构,其化学通式为ABX。其具
3 3
有非常优异的光电性质,是理想的 光电器件 如太阳能电池、发光二极管、 光电探测器
等的制备材料。
1. 通过元素的替换和掺杂,可以调控钙钛矿型材料的催化性能。
(1)Ti的四卤化物熔点如下表所示,TiF 熔点高于其他三种卤化物,自TiCl 至TiI 熔点依次
4 4 4
升高,原因是 。
化合物 TiF TiCl TiBr TiI
4 4 4 4
熔点/℃ 377 -2412 38.3 155
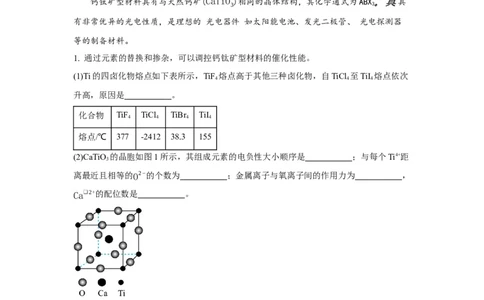
(2)CaTiO 的晶胞如图1所示,其组成元素的电负性大小顺序是 ;与每个Ti4+距
3
离最近且相等的O2−的个数为 ;金属离子与氧离子间的作用力为 ,
Ca❑2+的配位数是 。
(3)一种立方钙钛矿结构的金属卤化物光电材料的组成为 、I-和有机碱离子
Pb❑2+ CH NH+ ,
3 3
其晶胞如图2所示。有机碱 中,N原子的杂化轨道类型是 ;
CH NH+
3 3
A. p-p B. sp C.sp2 D.sp3与 是否形成配位键? 。为什么? 。若晶胞参数为
CH NH+ Pb❑2+
3 3
anm,则晶体密度为 g∙cm−3(列出计算式)。
(4)用上述金属卤化物光电材料制作的太阳能电池在使用过程中会产生单质铅和碘,降低了
器件效率和使用寿命,我国科学家巧妙地在此材料中引入稀土铕(Eu)盐,提升了太阳能电
池的效率和使用寿命,其作用原理如图3所示,用离子方程式表示该原理: 。
【答案】(1)TiF 为离子化合物,熔点高,其他三种均为共价化合物,随相对分子质量的增
4
大分子间作用力增大,熔点逐渐升高
(2) O>Ti>Ca 6 离子键 12
(3) D 不能 N原子无孤电子对
620×1021
a3×N
A
(4) 、
Pb+2Eu3+=2Eu2++Pb2+ 2Eu2++I =2Eu3++2I−
2
【解析】(1)一般不同的晶体类型的熔沸点是原子晶体>离子晶体>分子晶体,TiF 是离
4
子晶体,其余三种则为分子晶体,故TiF 的熔点高于其余三种物质;TiCl 、TiBr 、TiI 均
4 4 4 4
为分子晶体,对于结构相似的分子晶体,则其相对分子质量越大,分子间作用力依次越大,
熔点越高。
(2)CaTiO 晶体中含有Ca、Ti、O三种元素,Ca、Ti是同为第四周期的金属元素,Ca在
3
Ti的左边,根据同一周期元素的电负性从左往右依次增大,故Ti>Ca,O为非金属,故其电负性最强,故三者电负性由大到小的顺序是:O>Ti>Ca;
与每个Ti4+距离最近且相等的O2−构成以Ti4+为中心的正八面体,故有6个;
金属阳离子和氧负离子之间以离子键结合;
离子晶体晶胞中某微粒的配位数是指与之距离最近且相等的带相反电性的离子,故Ca2+的
配位数必须是与之距离最近且相等的氧离子的数目,从图(a)可知,该数目为三个相互垂直
的三个面上,每一个面上有4个,故Ca2+的配位数是12。
(3)有机碱中 N原子上无孤对电子,周围形成了4个σ键,故N原子采用sp3杂化;
CH NH+
3 3
由于N原子无孤电子对,故二者不能形成配位键;
1
从图(b)可知,一个晶胞中含有Pb2+的数目为1个,CH NH+的数目为8× =1个,I-的数目
3 3 8
1
为6× =3个,故晶胞的密度为
2
1×(207+3×127+12+14+6×1) 620×1021 。
ρ=mV= g/cm3= g/cm3
N (a×10−7 ) 3 a3×N
A ❑ A
(4)从作用原理图(c)可以推出,这里发生两个离子反应方程式,左边发生
,右边发生 。
Pb+2Eu3+=2Eu2++Pb2+ 2Eu2++I =2Eu3++2I−
2
二、甲醇的制取(本题共18分)
甲醇结构最为简单的饱和一元醇,沸点为64.7℃。甲醇有“木醇”与“木精”之名,
源自于曾经其主要的生产方式是自木醋液(为木材干馏或裂解的产物之一)萃取。现代甲
醇是直接从一氧化碳,二氧化碳和氢的一个催化作用的工业过程中制造。不同于乙醇,甲
醇毒性大,不可以饮用。通常用作溶剂、防冻剂、燃料或变性剂乙醇,亦可用于经过酯交
换反应生产生物柴油。
2.HCOOCH 是一种重要的化工产品,被公认为“万能中间体”。 (18分)
3
Ⅰ.甲醇脱氢法制HCOOCH 是工业上的一种重要方法,具有工艺流程短、原料单一、反应
3
条件温和等优点。其工艺过程涉及如下反应:
反应a:2CH OH(g)⇌ HCOOCH (g)+2H (g) ΔH
3 3 2 1
反应b:
CH OH(g)⇌ CO(g)+2H (g) ΔH =+106.0kJ⋅mol−1
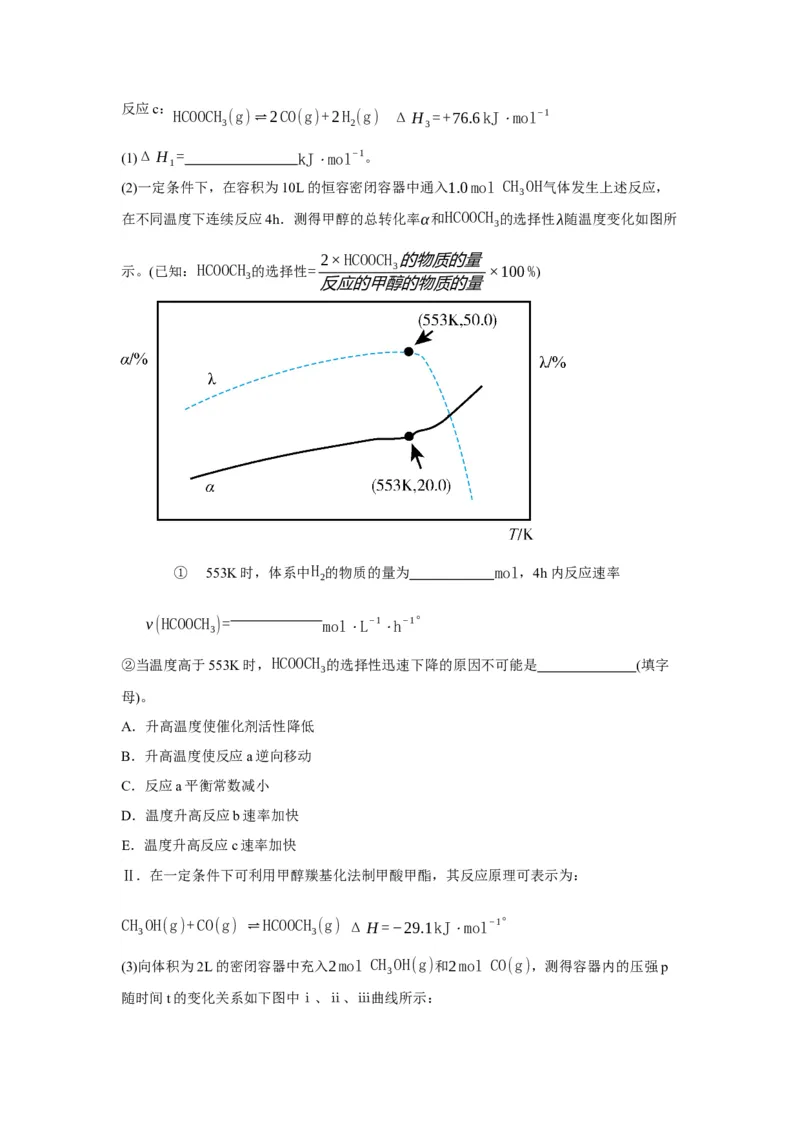
3 2 2反应c:
HCOOCH (g)⇌2CO(g)+2H (g) ΔH =+76.6kJ⋅mol−1
3 2 3
(1)ΔH = kJ⋅mol−1。
1
(2)一定条件下,在容积为10L的恒容密闭容器中通入1.0mol CH OH气体发生上述反应,
3
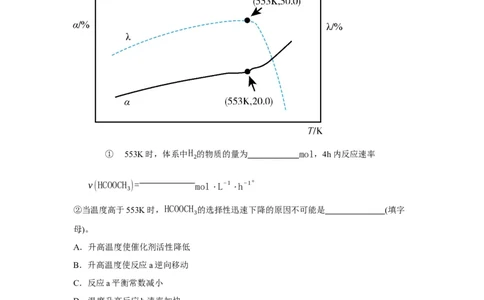
在不同温度下连续反应4h.测得甲醇的总转化率α和HCOOCH 的选择性λ随温度变化如图所
3
2×HCOOCH 的物质的量
示。(已知:HCOOCH 的选择性= 3 ×100%)
3
反应的甲醇的物质的量
① 553K时,体系中H 的物质的量为 mol,4h内反应速率
2
。
v(HCOOCH )= mol⋅L−1 ⋅h−1
3
②当温度高于553K时,HCOOCH 的选择性迅速下降的原因不可能是 (填字
3
母)。
A.升高温度使催化剂活性降低
B.升高温度使反应a逆向移动
C.反应a平衡常数减小
D.温度升高反应b速率加快
E.温度升高反应c速率加快
Ⅱ.在一定条件下可利用甲醇羰基化法制甲酸甲酯,其反应原理可表示为:
。
CH OH(g)+CO(g)
⇌
HCOOCH (g) ΔH=−29.1kJ⋅mol−1
3 3
(3)向体积为2L的密闭容器中充入2mol CH OH(g)和2mol CO(g),测得容器内的压强p
3
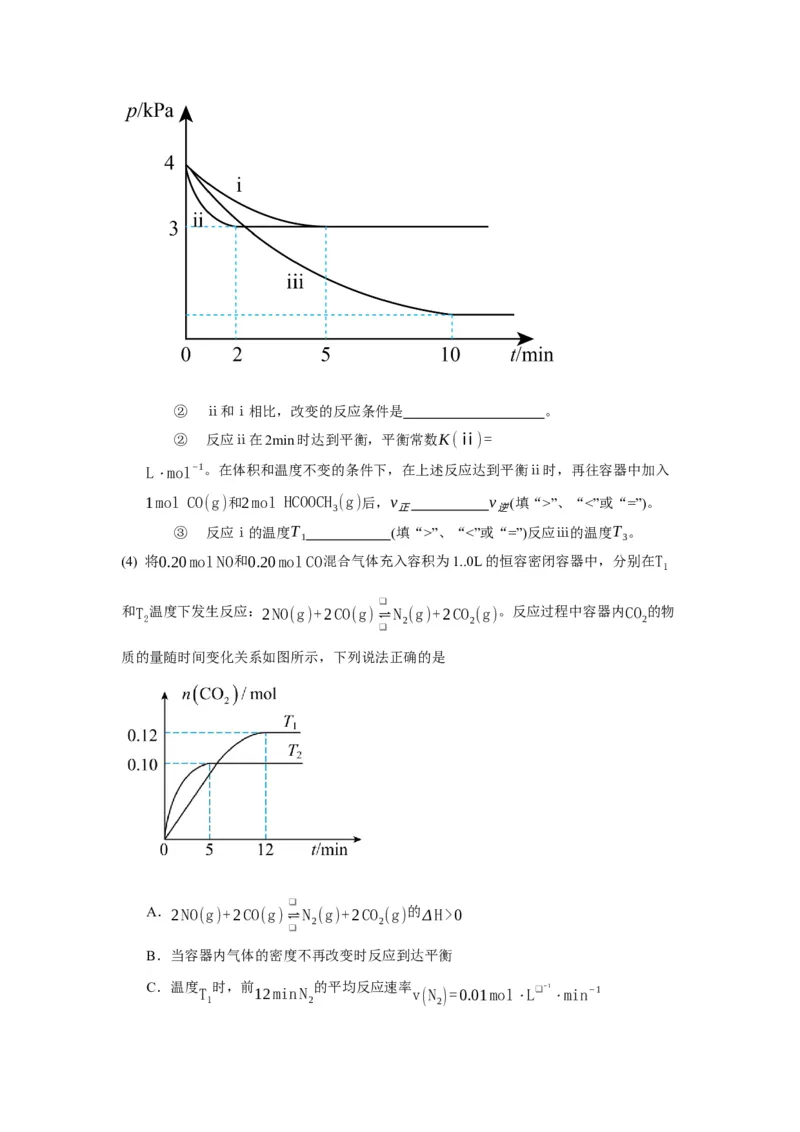
随时间t的变化关系如下图中ⅰ、ⅱ、ⅲ曲线所示:② ⅱ和ⅰ相比,改变的反应条件是 。
② 反应ⅱ在2min时达到平衡,平衡常数K(ⅱ)=
L⋅mol−1。在体积和温度不变的条件下,在上述反应达到平衡ⅱ时,再往容器中加入
1mol CO(g)和2mol HCOOCH (g)后,v v (填“>”、“<”或“=”)。
3 正 逆
③ 反应ⅰ的温度T (填“>”、“<”或“=”)反应ⅲ的温度T 。
1 3
(4) 将0.20mol NO和0.20mol CO混合气体充入容积为1..0L的恒容密闭容器中,分别在T
1
❑
和T
2
温度下发生反应:2NO(g)+2CO(g)⇌ N
2
(g)+2CO
2
(g) 。反应过程中容器内CO
2
的物
❑
质的量随时间变化关系如图所示,下列说法正确的是
❑
A.2NO(g)+2CO(g)⇌ N (g)+2CO (g) 的ΔH>0
2 2
❑
B.当容器内气体的密度不再改变时反应到达平衡
C.温度 T 时,前 12minN 的平均反应速率 v(N )=0.01mol⋅L❑−1 ⋅min−1
1 2 2D.温度T 时,若起始向容器中通入0.10mol NO、0.30mol CO、0.10molN 和
2 2
0.10molCO ,反应向正方向进行
2
【答案】
(1)+135.4
(2) 0.3 1.25×10-3 BC
(3) ⅱ使用催化剂 2 < >
(4) D
【解析】(1)利用盖斯定律求:△H1=2△H2-△H3,代入数据得△H1=+135.4kJ·mol-1,故
答案为:+135.4;
(2)①根据图中甲醇的总转化率为20.0%,可得反应的甲醇的物质的量为0.20mol,带入
HCOOCH 的选择性(50.0%)公式,可得的HCOOCH 物质的量为0.05mol,根据H元素守恒
3 3
0.05mol
可得H 的物质的量为0.3mol;根据速率公式v(HCOOCH )= =1.25×10-
2 3 10L×4h
3mol·L-1·h-1,故答案为:0.3;1.25×10-3;
②A.当温度高于535K时,HCOOCH 的选择性迅速下降,可能是催化剂活性降低,产生
3
的甲酸甲酯减少,A项正确;
B.升高温度反应I正向移动,B项错误;
C.升高温度反应I正向移动,平衡常数增大,C项错误;
D.反应Ⅱ的速率加快,单位时间内产生的CO增多,甲酸甲酯的选择性自然降低,D项正
确;
E.反应III的速率加快,产生的CO增多,甲酸甲酯的选择性自然降低,E项正确;
故答案为:BC;
(3)①ⅱ和ⅰ相比,平衡未发生移动,到达平衡的时间提前了,即反应速率加快,所以是
使用了催化剂,加快速率不影响平衡移动,故答案为ⅱ使用催化剂;
②化学平衡常数只与温度有关,可以由平衡I的数据计算K(II),平衡I体系中各组分的平
衡浓度均为0.5mol/L。在相同温度下,反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ) = K(I)=
0.5mol/L
=2 L·mol-1。
(0.5mol/L) 2
③在体积和温度不变的条件下,在上述反应达到平衡Ⅱ时,再往容器中加入1mol CO和
2mol HCOOCH 后v ﹤v ,原因是:由浓度商Qc=1.5/(0.5×1)=3﹥2=K 可知,反应向
3 (正) (逆)
逆方向进行,故v ﹤v 。
(正) (逆)④反应Ⅰ的温度(T )和反应Ⅲ的温度(T )相比,T﹥T,判断的理由是:此反应为放热反应,
1 3 1 3
降温可以使平衡向正反应方向移动,容器内气体的压强减小(或反应Ⅰ达平衡时所需的时
间比反应Ⅲ达平衡时所需的时间短,反应速率快,故T 温度更高)。
1
(4)A.由图可知,T 先达到平衡状态,即温度T >T ,温度升高,二氧化碳的物质的量
2 2 1
减小,说明升高温度,反应逆向进行,该反应是放热反应,
2NO(g)+2CO(g)
⇌
N (g)+2CO (g)的ΔH<0,A项错误;
2 2
B.气体的质量不变,体积不变,容器内气体的密度不再改变时,不能判断反应是否达到
平衡,B项错误;
0.06mol
C.T 温度时,前12min的平均反应速率 1L ,C项错误;
1 v(N )= =0.005mol/Lmin
2 12min
D.列三段式:
2NO(g) + 2CO(g) ⇌ N (g) +2CO (g) ¿起始(mol) 0.2 ¿0.2 ¿0 0 ¿变化(mol) 0.1 ¿0.1 ¿0.05 0.1 ¿平衡(mol) 0.1 ¿0.1 ¿0.05 0.1 ¿
2 2
0.1 2 0.05
( ) ( )
c2(CO )⋅c(N ) 1 1
温度为T 时,平衡常数K= 2 2 = =5,
2 c2(NO)⋅c2(CO) 0.1 2 0.1 2
( ) ( )
1 1
0.1 20.1
( )
1 1
Q = ≈1.1<5=K,则该反应正反应方向进行;
c 0.1 2 0.3 2
( ) ( )
1 1
答案选D。
三、金属铋的制取(本题共21分)
铋(Bi)的化合物广泛应用于电子、医药等领域。硫化铋具有环境友好、光电导和非线
性光学响应等优点,广泛应用于太阳能电池、光电二级管阵列以及红外光谱学等,也可以
应用于制其它铋合物、易切削钢添加剂、微电子工业。
3. 由辉铋矿(主要成分为Bi S ,含FeS、CuO、SiO 等杂质)制备NaBiO 的工艺流程如下:
2 3 2 3
(21分)已知:
ⅰ.NaBiO 难溶于冷水;
3
ⅱ.“氧化浸取”时,铋元素转化为Bi3+,硫元素转化为硫单质;
ⅲ. Cu(OH) +4NH =[Cu(NH ) ] 2+ +2OH− 。
2 3 3 4
回答下列问题。
(1)“氧化浸取”步骤中温度升高可以增大速率,但高于50℃时浸取速率会下降,其可能的
原因是 。滤渣1经过除硫后的另一种成分在工业上用途广泛,写出一种用途:
。
(2)“氧化浸取”时,FeS发生反应的离子方程式为 。
(3)“除铁”步骤中调节pH最好选用的试剂为___________(填字母)。
A.稀硫酸 B.碳酸钠 C.三氧化二铋 D.氨水
(4)“转化”时,生成NaBiO 的反应中氧化剂与氧化产物的物质的量之比为 。
3
(5) 产品纯度的测定。取 产品wg,加入足量稀硫酸和 稀溶
NaBiO NaBiO amol⋅L−1FeSO
3 3 4
液10mL使其完全反应(Bi被还原为+3价),再用 标准溶液滴定溶液中剩
bmol⋅L−1K Cr O
2 2 7
余的Fe2+(Cr被还原为+3价),恰好消耗10mLK Cr O 标准溶液。该产品的纯度为
2 2 7
(用含w、a、b的代数式表示)。
(6)组装为下图装置后发现导线中电流方向为石墨1→石墨2,则该装置的负极为
,石墨2电极上的电极反应式为 。
【答案】(1) 盐酸挥发、双氧水分解 制取玻璃等
(2)
2FeS+3H O +6H+=2Fe3++2S+6H O
2 2 2
(3)C
(4)1:1
140(a−6b)
(5) %
w(6) 石墨2
Mn2+-5e-+4H O=MnO-+8H+
2 4
【解析】(1)盐酸易挥发、过氧化氢不稳定,高于40℃时浸取率快速下降,其可能的原
因是高于40℃时,盐酸挥发、双氧水分解;由分析可知,滤渣1经过除硫后的另一种成分
为二氧化硅,可以用于工业制取玻璃等;
(2)由分析可知,“氧化浸取”时,FeS发生反应的离子方程式为
;
2FeS+3H O +6H+=2Fe3++2S+6H O
2 2 2
(3)“除铁”步骤中调节pH为降低溶液的酸性使得铁离子沉淀,且不引入新杂质,故最
好选用的试剂为三氧化二铋,故选C;
(4)“转化”时,次氯酸钠将溶液中的氯化铋转化为铋酸钠沉淀,氯元素化合价由+1变
为-1为氧化剂,铋元素化合价由+3变为+5发生氧化反应生成氧化产物NaBiO ,结合电子
3
守恒可知
NaBiO ∼2e− ∼ClO-
,故氧化剂与氧化产物的物质的量之比为1:1;
3
(5)酸性环境下,NaBiO 将Fe2+氧化成Fe3+ (NaBiO 被还原成Bi3+),根据电子守恒可知
3 3
;剩余剩余的 恰好消耗 (Cr被还原为+3价)标准溶液氧化,
NaBiO ∼2Fe2+ Fe2+ 10mLK Cr O
3 2 2 7
根据得失电子守恒可知 ,被 氧化的亚铁离子为
K Cr O ∼6e− ∼6Fe2+ bmol⋅L−1K Cr O
2 2 7 2 2 7
,被 氧化的亚铁离子为
6×b×10×10−3mol NaBiO
3
,则 为
a×10×10−3mol−6×b×10×10−3mol NaBiO
3
1
(a×10×10−3mol−6×b×10×10−3mol),该产品的纯度为
2
1
(a×10×10−3mol−6×b×10×10−3mol)×280g/mol 140(a−6b)
2 = %;
×100% w
wg
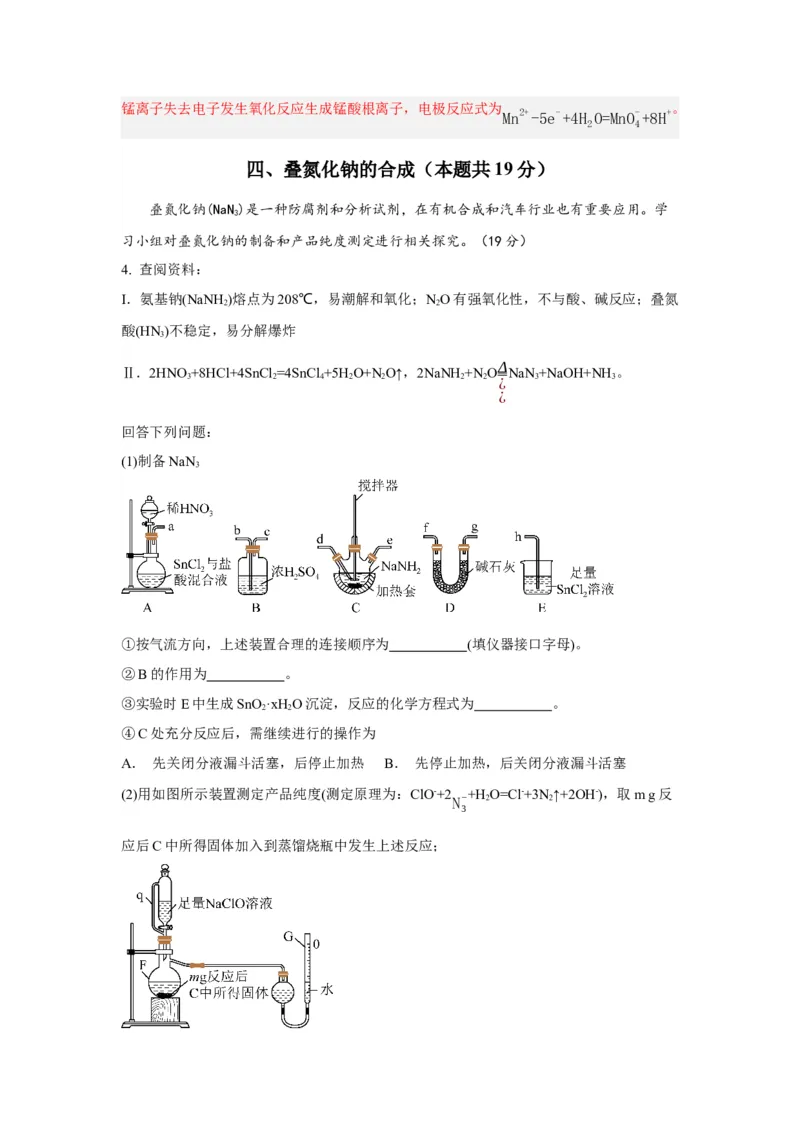
(6)导线中电流方向为石墨1→石墨2,则石墨1为正极、石墨2为负极,石墨2电极上锰离子失去电子发生氧化反应生成锰酸根离子,电极反应式为 。
Mn2+-5e-+4H O=MnO-+8H+
2 4
四、叠氮化钠的合成(本题共19分)
叠氮化钠(NaN)是一种防腐剂和分析试剂,在有机合成和汽车行业也有重要应用。学
3
习小组对叠氮化钠的制备和产品纯度测定进行相关探究。(19分)
4. 查阅资料:
I.氨基钠(NaNH )熔点为208℃,易潮解和氧化;NO有强氧化性,不与酸、碱反应;叠氮
2 2
酸(HN )不稳定,易分解爆炸
3
Δ
Ⅱ.2HNO+8HCl+4SnCl =4SnCl +5H O+NO↑,2NaNH +N O NaN +NaOH+NH 。
3 2 4 2 2 2 2 3 3
¿
¿
回答下列问题:
(1)制备NaN
3
①按气流方向,上述装置合理的连接顺序为 (填仪器接口字母)。
②B的作用为 。
③实验时E中生成SnO ·xH O沉淀,反应的化学方程式为 。
2 2
④C处充分反应后,需继续进行的操作为
A. 先关闭分液漏斗活塞,后停止加热 B. 先停止加热,后关闭分液漏斗活塞
(2)用如图所示装置测定产品纯度(测定原理为:ClO-+2 +H O=Cl-+3N ↑+2OH-),取m g反
N− 2 2
3
应后C中所得固体加入到蒸馏烧瓶中发生上述反应;①管q的作用为 。
②若G的初始读数为V mL、末读数为V mL,本实验条件下气体摩尔体积为V L·mol-1,
1 2 m
则产品中NaN 的质量分数为
3
③反应结束读数时,若G中液面高于球形干燥管液面,则测定结果 (填“偏
高”、“偏低”或不影响)
【答案】(1) afg(或gf)debch 防止水蒸气进入C装置 SnCl +N O+
2 2
(x+1)HO=SnO ·xH O↓+N+2HCl B
2 2 2 2
0.13(V -V )
(2) 平衡压强、使液体容易流下,使测量气体体积数据更准确 1 2
3mV
m
×100% 偏低
【解析】(1)①由上述分析可知,按气流方向,装置的连接顺序为
a→f(g)→g(f)→d→e→b→c→h,
故答案为:a→f(g)→g(f)→d→e→b→c→h,故答案为:afg(或gf)debch;
②由分析可知,B用于防止E中水蒸气进入C中干扰实验,故答案为:防止水蒸气进入C
装置;
③由信息,NO有强氧化性,故E中生成SnO •xH O沉淀的化学方程式为SnCl +N O+
2 2 2 2 2
(x+1)HO=SnO •xH O↓+N+2HCl,故答案为:SnCl +N O+(x+1)H O=SnO •xH O↓+N+2HCl;
2 2 2 2 2 2 2 2 2 2
④C处充分反应后,停止加热,为防止倒吸,需继续进行的操作为继续通入NO至三颈瓶
2
冷却后,关闭分液漏斗活塞,故答案为:B;
(2)①管q可以平衡压强、使液体容易流下和减小测定气体体积时误差的作用,故答案为:
平衡压强、使液体容易流下和减小测定气体体积时误差的作用;
②若G的初始读数为V mL、末读数为V mL,本实验条件下气体摩尔体积为V L·mol-1,
1 2 m
由题给信息可知,N 的体积为(V -V )mL,由关系式2NaN ~3N 可得,产品中NaN 的质量
2 1 2 2 2 3
(V −V )×10−3L 2
分数为
V
1
L⋅
2
mol−1
×
3
×65g/mol ×100%= 0.13(V
1
−V
2
) ×100%,故答案为:
m 3mV
m
mg
0.13(V −V )×100%;
1 2
3mV
m
③反应结束读数时,若G中液面高于球形干燥管液面,导致量气管中气体压强大于外面大气压,使得气体体积偏小,故则测定结果偏低,故答案为:偏低。
五、细菌治疗药物氧氟沙星的有机合成(本题共24分)
氧氟沙星是一种人工合成、广谱抗菌的氟喹诺酮类药物,主要用于革兰阴性菌所致的
呼吸道、咽喉、扁桃体、泌尿道(包括前列腺)、皮肤及软组织、胆囊及胆管、中耳、鼻
窦、泪囊、肠道等部位的急、慢性感染。
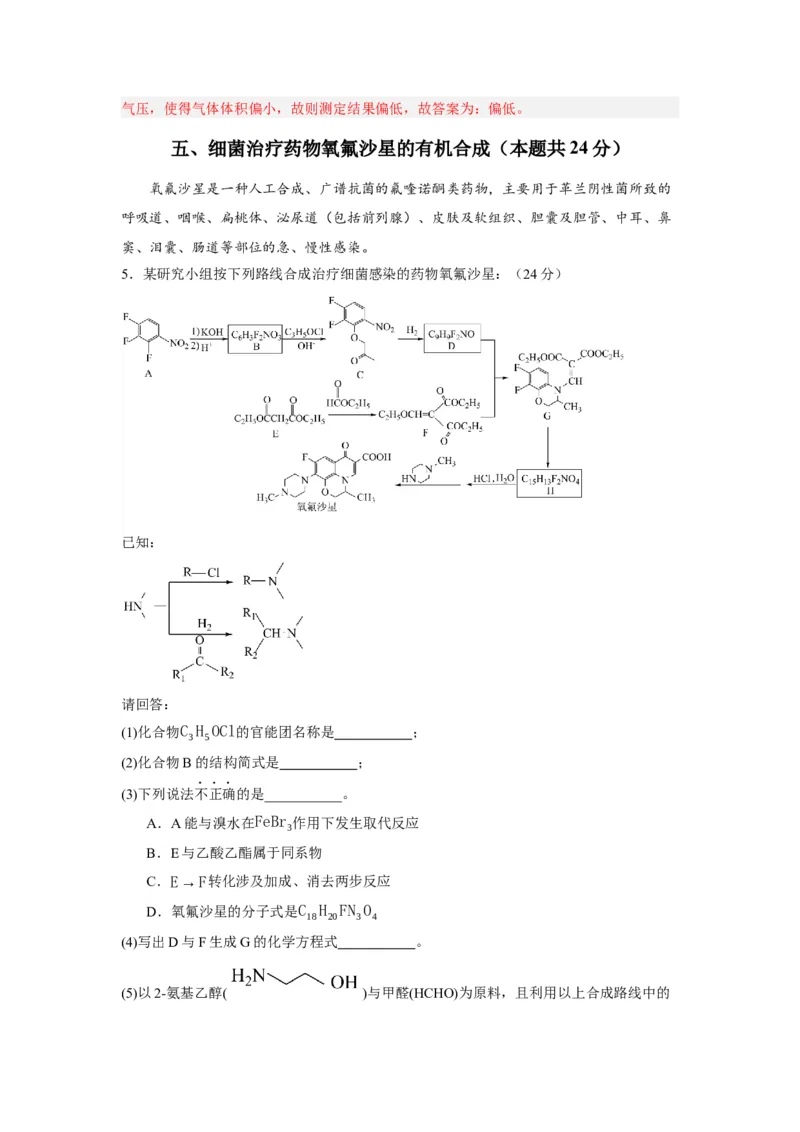
5.某研究小组按下列路线合成治疗细菌感染的药物氧氟沙星:(24分)
已知:
请回答:
(1)化合物C H OCl的官能团名称是 ;
3 5
(2)化合物B的结构简式是 ;
(3)下列说法不正确的是___________。
A.A能与溴水在FeBr 作用下发生取代反应
3
B.E与乙酸乙酯属于同系物
C.E→F转化涉及加成、消去两步反应
D.氧氟沙星的分子式是C H FN O
18 20 3 4
(4)写出D与F生成G的化学方程式 。
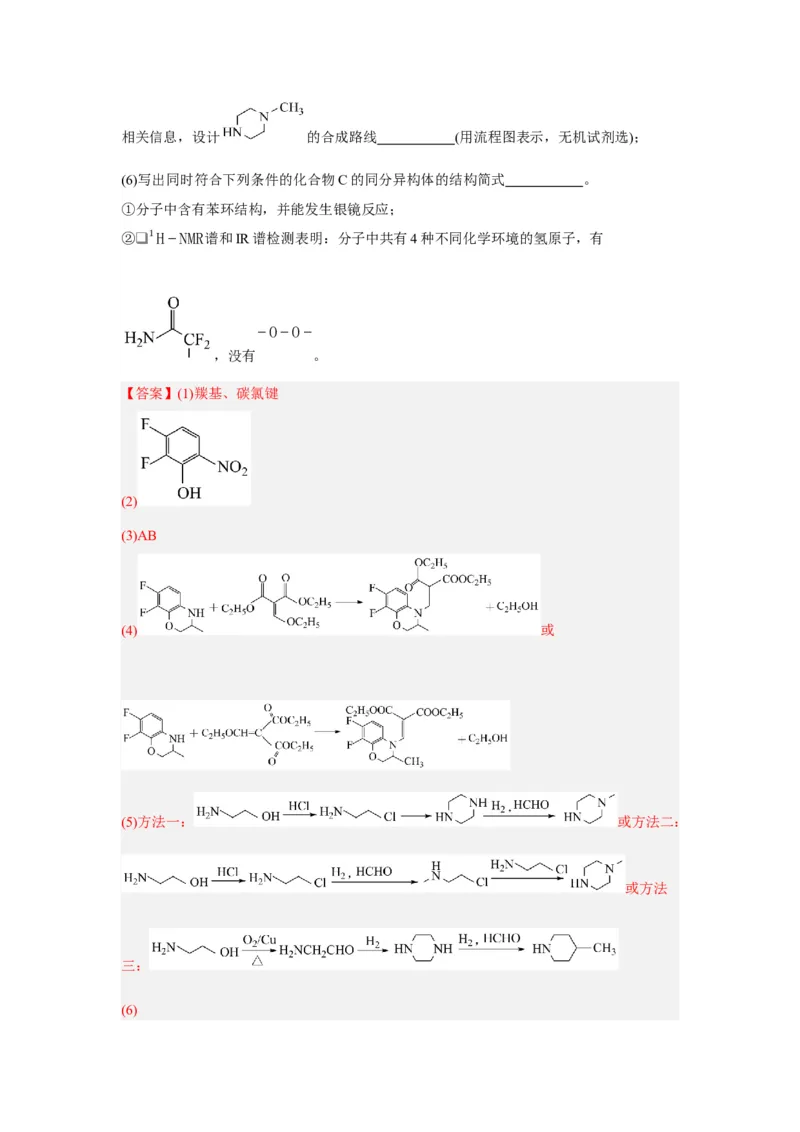
(5)以2-氨基乙醇( )与甲醛(HCHO)为原料,且利用以上合成路线中的相关信息,设计 的合成路线 (用流程图表示,无机试剂选);
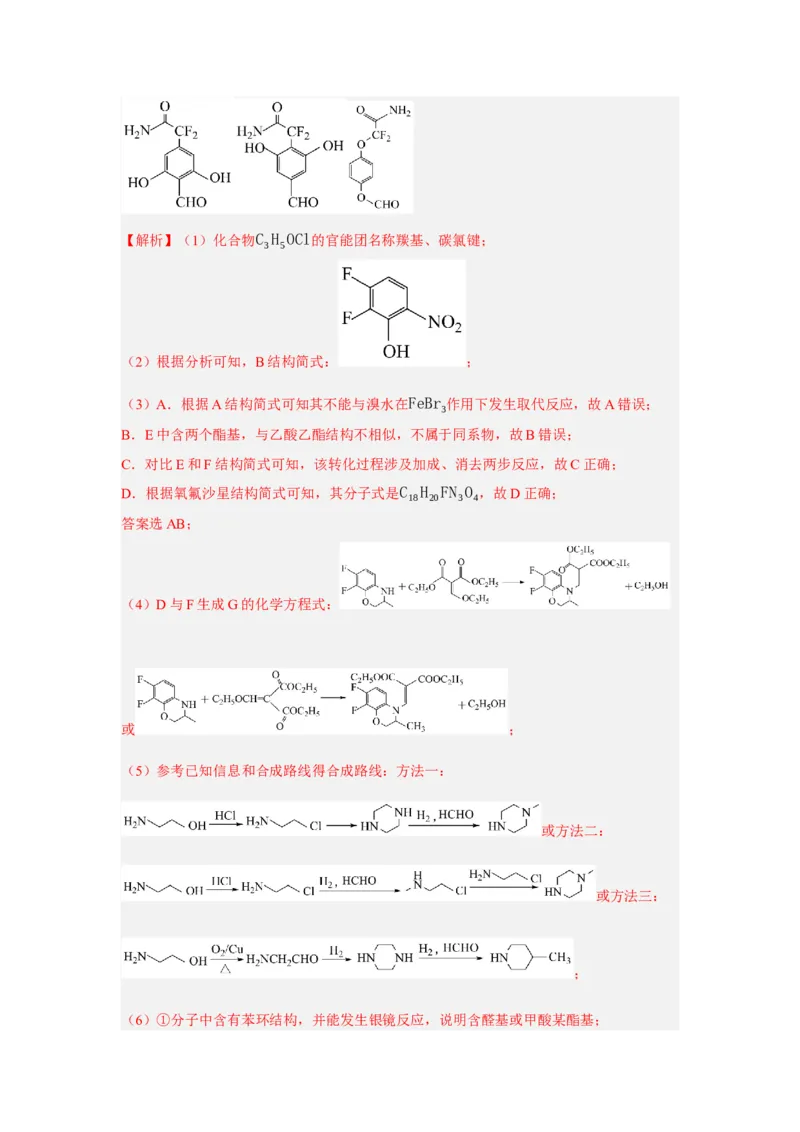
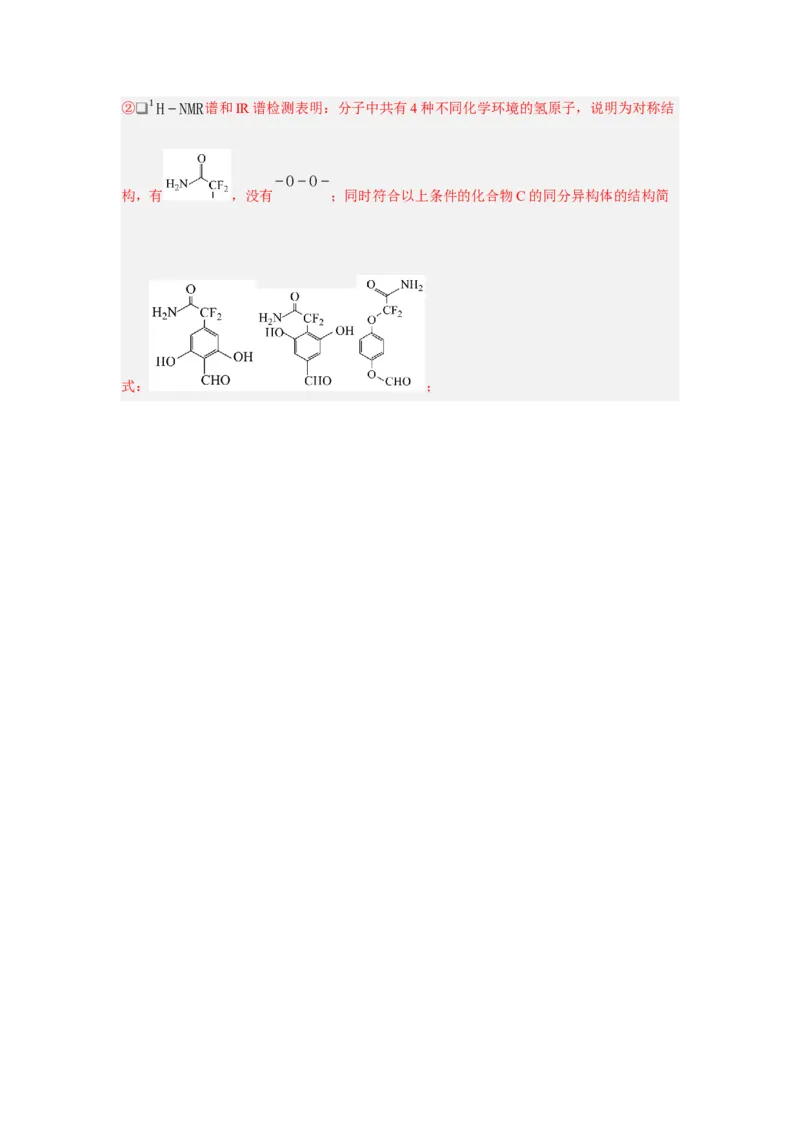
(6)写出同时符合下列条件的化合物C的同分异构体的结构简式 。
①分子中含有苯环结构,并能发生银镜反应;
②❑ 1H−NMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,有
−O−O−
,没有 。
【答案】(1)羰基、碳氯键
(2)
(3)AB
(4) 或
(5)方法一: 或方法二:
或方法
三:
(6)【解析】(1)化合物C H OCl的官能团名称羰基、碳氯键;
3 5
(2)根据分析可知,B结构简式: ;
(3)A.根据A结构简式可知其不能与溴水在FeBr 作用下发生取代反应,故A错误;
3
B.E中含两个酯基,与乙酸乙酯结构不相似,不属于同系物,故B错误;
C.对比E和F结构简式可知,该转化过程涉及加成、消去两步反应,故C正确;
D.根据氧氟沙星结构简式可知,其分子式是C H FN O ,故D正确;
18 20 3 4
答案选AB;
(4)D与F生成G的化学方程式:
或 ;
(5)参考已知信息和合成路线得合成路线:方法一:
或方法二:
或方法三:
;
(6)①分子中含有苯环结构,并能发生银镜反应,说明含醛基或甲酸某酯基;②❑ 1H−NMR谱和IR谱检测表明:分子中共有4种不同化学环境的氢原子,说明为对称结
−O−O−
构,有 ,没有 ;同时符合以上条件的化合物C的同分异构体的结构简
式: ;