文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(浙江专用)
黄金卷08
(考试时间:90分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28 P 31 S 32 Cl
35.5 K 39 Ca 40 Cr 52 Mn 55 Fe 56 Cu 64 Zn 65 Ga 70 As 75 Br 80 Pd 106 Ag 108
Ba 137
第Ⅰ卷
一、单项选择题:共16题,每题3分,共48分。每题只有一个选项最符合题意。
1.材料是人类赖以生存和发展的物质基础,下列属于新型无机非金属材料的是( )
A.水泥 B.碳化硅 C.橡胶 D.塑料
【答案】B
【解析】A项,水泥为传统无机硅酸盐材料,A错误;B项,碳化硅为新型无机非金属材料,B正
确;C项,橡胶为有机高分子材料,C错误;D项,塑料为有机高分子材料,D错误;故选B。
2.下列化学用语表示正确的是( )
A.溴的简化电子排布式:
B.1-丁醇的键线式:
C.Cl-Cl形成的 键模型:
D.水的VSEPR模型:
【答案】D
【解析】A项,溴位于周期表中第4周期第ⅤⅡA族,核外电子数35,电子排布式为
,A错误;B项,1-丁醇的键线式为 ,而 为1-丙醇,选项B错误;C项,Cl-Cl形成的 键模型: ,选项C错误;D项,HO中价层电子对个数=2+ =4,
2
且含有2个孤电子对,所以HO的VSEPR模型为四面体 ,选项D正确;故选D。
2
3.NaCO 是一种重要的盐,下列说法不正确的是( )
2 3
A.NaCO 属于强电解质
2 3
B.厨房油烟污渍可用热的NaCO 溶液清洗
2 3
C.NaCO 又称食用碱
2 3
D.NaCO 是泡沫灭火器的主要成分
2 3
【答案】D
【解析】A项,NaCO 在水溶液中完全电离,属于强电解质,故A正确;B项,NaCO 水解溶液呈碱
2 3 2 3
性,加热促进水解平衡正向移动,溶液碱性增强,所以厨房油烟污渍可用热的NaCO 溶液清洗,故B正
2 3
确;C项,NaCO 又称食用碱,故C正确;D项,NaHCO 是泡沫灭火器的主要成分之一,故D错误;故
2 3 3
选D。
4.规范的实验操作是实验成功的必要保证,下列有关实验操作描述正确的是( )
A.电解精炼铜时,粗铜作阴极
B.容量瓶和分液漏斗使用前均需查漏
C.滴定实验前,需用所盛装溶液分别润洗滴定管和锥形瓶
D.试管和烧杯均可用酒精灯直接加热
【答案】B
【关键能力】科学探究与创新意识
【解析】A项,根据电解析理,电解精炼铜时,粗铜作阳极,纯铜作阴极,A错误;B项,容量瓶和
分液漏斗使用前均需查漏,B正确;C项,滴定实验前,滴定管应要用所盛装溶液润洗,但锥形瓶不需要
润洗,C错误;D项,试管可用酒精灯直接加热,烧杯应垫上石棉网加热,而不能用酒精灯直接加热,D
错误;故选B。
5.下列说法不正确的是( )A.图①:进行化学实验时,需要佩戴护目镜,以保护眼睛
B.图②:可用于分离植物油和水的混合液
C.图③:可用于硫酸钠的焰色试验
D.图④:牺牲阳极法保护钢铁设备的示意图
【答案】D
【解析】A项, 是护目镜,进行化学实验时,需要佩戴护目镜,以保护眼睛,故A正确;B
项,植物油和水不互溶,可以利用分液分离。故B正确;C项,光洁的无锈铁丝焰色无色,可以用于硫酸
钠的焰色试验,故C正确;D项,将闸门与电源的负极相连,属于外加电源阴极保护法,故D错误;故选
D。
6.一种用氢气制备双氧水的反应原理如图所示,已知在化合物中钯(Pd)均以+2价形式存在,下列有
关说法正确的是( )
A.反应①②③均为氧化还原反应
B.反应①中HCl为还原产物
C.反应②中每产生1mol [PdCl O]2-,转移2mol电子
2 2
D.[PdCl ]2-和HCl均为该反应的催化剂
4
【答案】C
【解析】A项,由图可知,反应③中没有元素发生化合价变化,属于非氧化还原反应,故A错误;B
项,由图可知,反应①中氢元素的化合价升高被氧化,氢气是反应的还原剂,氯化氢是氧化产物,故B错
误;C项,由图可知,反应②中钯生成1mol二过氧根二氯合钯离子时,反应转移2mol电子,故C正确;D项,由图可知,四氯合钯离子是反应的催化剂,氯化氢是反应的中间产物,故D错误;故选C。
7.设N 为阿伏加德罗常数的值,下列叙述正确的是( )
A
A.4.6gN 完全燃烧,一定有0.5N 个C-H键断裂
A A
B.0.1mol丙烯酸(CH=CHCOOH)中含有0.8N 个σ键
2 A
C.含0.5mol Cr O2-的酸性溶液与足量HO 反应生成 ,转移电子数4N
2 7 2 2 A
D.0.2mol FeCl 完全水解形成的Fe(OH) 胶体粒子数等于0.2N
3 3 A
【答案】B
【解析】A项,C HO存在同分异构体,可能为CHCHOH,也可能为CHOCH ,题目所给条件无法
2 6 3 2 3 3
判断物质结构,故无法确定C-H键断裂数目,故A错误;B项,每个CH=CHCOOH分子中有3个C-H
2
键,2个C-C键,2个C-O键,1个O-H键,0.1mol丙烯酸(CH=CHCOOH)中含有0.8N 个σ键,故B正
2 A
确;C项, 中存在的氧元素化合价为-2价和四个-1价,Cr元素化合价+6价,Cr O2-中铬元素化
2 7
合价+6价,元素化合价不变,不是氧化还原反应,故C错误;D项,胶体粒子是由多个分子或离子的聚集
体,0.2mol FeCl 完全水解形成的 Fe(OH) 胶体粒子数少于0.2N ,故D错误;故选B。
3 3 A
8.下列说法不正确的是( )
A.天然氨基酸均为无色晶体,熔点较高,难溶于乙醚
B.在碱催化下,苯酚和甲醛可缩聚成网状结构的热固性酚醛树脂
C.大豆蛋白纤维是一种可降解材料
D.聚氯乙烯通过加聚反应制得,可用作不粘锅的耐热涂层
【答案】D
【解析】A项,天然氨基酸均为无色晶体,熔点较高,一般能溶于水,难溶于乙醚等有机溶剂,A正
确;B项,碱性条件下,苯酚邻对位上的活泼氢先与甲醛加成,后在发生缩聚,生成网状结构的热固性酚
醛树脂,B正确;C项,蛋白质在酸性或者碱性条件下都能水解生成氨基酸,故大豆蛋白纤维是一种可降
解材料,C正确;D项,聚氯乙烯有毒,不能用来制作不粘锅的耐热涂层,D错误;故选D。
9.下列反应的离子方程式正确的是( )
A.用酸性KMnO 标准溶液滴定草酸:2MnO -+5C O2-+16H+=2Mn2++10CO ↑+8H O
4 4 2 4 2 2
B.Mg(HCO ) 溶液与过量NaOH溶液反应:Mg2++2HCO-+2OH-=MgCO↓+2H O
3 2 3 3 2C.用石墨电极电解CuCl 溶液:Cu2++2Cl-+2H O Cu(OH) ↓+H ↑+ Cl ↑
2 2 2 2 2
D.酸化的FeSO 溶液暴露在空气中:4Fe2++O +4H+═4Fe3++2H O
4 2 2
【答案】D
【解析】A项,草酸是弱酸,在离子反应中保留化学式,酸性KMnO 标准溶液滴定草酸:2MnO -
4 4
+5H C O+6H+=2Mn2++10CO ↑+8H O,故A错误;B项,向Mg(HCO ) 溶液中加入过量 的NaOH溶液,
2 2 4 2 2 3 2
反应的离子方程式为:Mg2++2HCO-+4OH-=Mg(OH) ↓+2CO 2-+2H O,故B错误;C项,用惰性石墨电极电
3 2 3 2
解CuCl 溶液,阳极的电极材料不参与反应,反应的离子方程式为:Cu2++2Cl- Cu+ Cl ↑,故C错误;D
2 2
项,酸化的FeSO 溶液暴露在空气中,离子方程式为:4Fe2++O +4H+═4Fe3++2H O,故D正确;故选D。
4 2 2
10.磷酸奥司他韦可以用于治疗流行性感冒,其结构如图所示。
下列关于磷酸奥司他韦的说法正确的是( )
A.分子中至少有7个碳原子共平面
B.该物质的分子式为C H ONP
16 31 8 2
C.1mol该物质最多能与2molNaOH发生反应
D.1mol该物质最多能与3molH 发生加成反应
2
【答案】B
【解析】A项,乙烯、-COO-中所有原子共平面,碳碳双键及直接连接碳碳双键的碳原子共平面,单
键可以旋转,该分子中至少有5个碳原子共平面,故A错误;B项,分子中C、H、O、N、P原子个数依
次是16、31、8、2、1,分子式为C H ONP,故B正确;C项,酰胺基、酯基水解生成的羧基及磷酸都
16 31 8 2
能和NaOH溶液反应,1mol该物质最多能消耗5molNaOH,故C错误;D项,碳碳双键和氢气以1:1发
生加成反应,酯基、酰胺基中碳氧双键和氢气不反应,1mol该物质最多消耗1mol氢气,故D错误;故选
B。
11.X、Y、Z、W四种元素,原子序数依次增大。Y与X、Z均相邻,元素Y的原子最外层电子数是
其内层电子数的3倍,元素Z基态原子的3p轨道上有4个电子。元素W基态原子的内层轨道全部排满电
子,且最外层电子数为1。下列说法不正确的是( )
A.第一电离能:X>Y>Z>W
B.电负性:Y>X>ZC.元素Y和Z能形成含有极性键的非极性分子
D.元素Z和W的单质加热反应后产物的化学式为WZ
【答案】D
【解析】X、Y、Z、W四种元素,原子序数依次增大,Y与X、Z均相邻,元素Y的原子最外层电子
数是其内层电子数的3倍,则Y为O,元素Z基态原子的3p轨道上有4个电子,则X为N,Z为S,元素
W基态原子的内层轨道全部排满电子,且最外层电子数为1,则W为Cu。A项,第一电离能:N>O>S
>Cu,A正确;B项,根据分析可知电负性:N>O>S,B正确;C项,元素Y和Z能形成含有极性键的
非极性分子SO ,C正确;D项,元素Z和W的单质加热反应后产物的化学式为Cu S,D错误; 故选
3 2
D。
12.实验室合成并提纯山梨酸乙酯(密度 ,沸点195.5℃)的过程如下图所示。下列说法正
确的是( )
A.操作①控温110℃,目的是除去生成的水
B.操作③可以通过观察气泡现象控制试剂a的用量
C.操作③④均应收集下层液体
D.操作②⑤可用玻璃棒轻轻拨散固体,以加快过滤速率
【答案】B
【解析】山梨酸和乙醇在浓硫酸、110℃条件下发生酯化反应生成山梨酸乙酯,产物混合物过滤后滤
液中加入试剂a为碳酸氢钠,用于中和多余的山梨酸,再用水洗涤分液,在有机层中加入少量无水硫酸镁
吸收多余的水分,再进行过滤得到滤液,滤液进行蒸馏得到山梨酸乙酯。A项,操作①控制温度为
110℃,加热可以加快反应的进行,同时温度又不至于过高导致乙醇大量挥发,且山梨酸乙酯的沸点高于
110℃可减少山梨酸乙酯的挥发,A错误;B项,操作③加入的是碳酸氢钠溶液,用于除去多余的山梨酸,
碳酸氢钠与山梨酸反应生成二氧化碳气体,可观察气泡现象控制碳酸氢钠溶液的用量,B正确;C项,操
作③④最后得到含有山梨酸乙酯的有机层,山梨酸乙酯密度小于水,因此应该收集上层的液体,C错误;
D项,过滤时玻璃棒的作用为引流,不能用其拨散固体,防止捣破滤纸,D错误;故选B。
13.一种用于发动机SCR系统的电解尿素(H NCONH)混合装置(X、Y为石墨电极,隔膜仅阻止气体
2 2
通过)如图,下列说法不正确的是( )A.装置工作时,电子由Y极流入,X极流出
B.Y极发生还原反应
C.X极的电极反应式为HNCONH+8OH--6e- = N ↑+CO 2-+6H O
2 2 2 3 2
D.若用铅酸蓄电池为电源,理论上消耗49 g HSO 时,此装置中有0.5mol H 生成
2 4 2
【答案】D
【解析】该电池反应时中,氮元素化合价由-3价变为0价,H元素化合价由+1价变为0价,所以生成
氮气的电极X是阳极,生成氢气的电极Y是阴极,阳极反应式为HNCONH+8OH--6e- = N ↑+CO 2-+6H O,
2 2 2 3 2
阴极反应式为2HO+2e-═H ↑+2OH-。A项,该装置为电解池,由分析可知电极X是阳极,Y是阴极,阳极
2 2
与原电池中正极相连,阴极与负极相连,由电子由负极流向正极,则电子由Y极流入,X极流出,故A正
确;B项,Y为阴极得电子发生还原反应,阴极反应式为2HO+2e-═H ↑+2OH-,故B正确;C项,该电池
2 2
反应时中,氮元素化合价由-3价变为0价,H元素化合价由+1价变为0价,X是阳极,阳极反应式为
HNCONH+8OH--6e- = N ↑+CO 2-+6H O,故C正确;D项,铅酸蓄电池的总反应为
2 2 2 3 2
Pb+PbO+2H SO =2PbSO+2H O,每消耗2mol HSO 转移2mol电子,理论上消耗49 g HSO 即物质的量为
2 2 4 4 2 2 4 2 4
,转移0.5mol电子,由2HO+2e-═H ↑+2OH-,可知有0.25mol H 生成,故D错
2 2 2
误;故选D。
14.2-溴-2-甲基丙烷发生水解反应[(CH )C Br +H O (CH)C +HBr]的能量变化与反应过程的关
3 3 2 3 3
系如下图所示。下列说法不正确的是( )A.溶液碱性增强,2-溴-2-甲基丙烷的水解百分率增大
B.该反应在低温下自发进行
C.分子中碳溴键断裂的速率比(CH)C +与HO结合速率快
3 3 2
D.碘原子半径比氯大,因此(CH)C-I水解生成(CH)C-OH的速率比(CH)C -Cl快
3 3 3 3 3 3
【答案】C
【解析】A项,溶液碱性增强,(CH)C Br +H O (CH)C +HBr平衡正向移动,2-溴-2-甲基丙烷
3 3 2 3 3
的水解百分率增大,故A正确;B项,正反应放热,△H<0,生成物微粒增多,△S>0,所以该反应在任意
温度下都能自发进行,故B正确;C项,分子中碳溴键断裂的活化能大,所以碳溴键断裂的速率比(CH)C
3 3
+与HO结合速率慢,故C错误;D项,碘原子半径比氯大,C-Cl键能大于C-I键能大,因此(CH)C-I水
2 3 3
解生成(CH)C-OH的速率比(CH)C -Cl快,故D正确;故选C。
3 3 3 3
15.可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。已知:K (BaCO)=5.0×10-9;
sp 3
K (BaSO)=1.0×10-10。下列推断正确的是( )
sp 4
A.饱和BaCO 溶液中存在:c(Ba2+)=c(HCO -)+c(CO2-)
3 3 3
B.向BaCO 、BaSO 的饱和混合溶液中加入少量BaCl ,溶液中 减小
3 4 2
C.不用碳酸钡作为内服造影剂,是因为K (BaCO)>K (BaSO)
sp 3 sp 4
D.若每次加入1 L2mol·L-1的NaCO 溶液,至少需要6次可将0.2mol BaSO 转化为BaCO
2 3 4 3
【答案】D
【解析】A项,BaCO 是难溶性盐,饱和BaCO 溶液中存在:BaCO (s) Ba2+ (aq)+ CO 2- (aq),
3 3 3 3
根据物料守恒:c(Ba2+)=c(HCO -)+c(CO2-)+c(H CO),故A错误;B项,BaCO 、BaSO 的饱和混合溶液中
3 3 2 3 3 4存在平衡:BaCO (s)+SO 2-(aq) BaSO (s)+ CO 2- (aq),溶液中 ,少量
3 4 4 3
BaCl ,度不变,K (BaCO)和K (BaSO)不变, 不变,故B错误;C项,胃液中含有盐酸,不用
2 sp 3 sp 4
碳酸钡作为内服造影剂的原因是:碳酸钡能和盐酸反应而溶解,和溶度积常数无关,故C错误;D项,向
BaSO 中加入NaCO 溶液,发生反应BaSO (s)+CO 2-(aq) BaCO (s)+ SO 2- (aq),该反应的平衡常
4 2 3 4 3 3 4
数K= ,若每次加入1 L2mol·L-1的NaCO 溶液,能处理BaSO 物质的
2 3 4
量xmol,则K= ,x= , ,所以至少6次可以将0.2mol BaSO 转化为
4
BaCO ,故D正确;故选D。
3
16.探究钠及其化合物的性质,下列方案设计、现象和结论都正确的是( )
实验方案 现象 结论
分别测定NaHCO 和NaCO 两者都大于7,且
A 3 2 3 CO2-的水解能力强于HCO -
溶液的pH NaCO 溶液的pH大 3 3
2 3
B 对某未知溶液进行焰色试验 火焰呈黄色 该溶液中含有钠盐
用形状和质量相同的钠,分
钠与乙醇反应比与 乙醇中羟基的活性强于苯酚中羟
C 别和等物质的量的苯酚和乙
苯酚反应剧烈 基的活性
醇反应
向饱和NaHCO 溶液中滴加 溶液变浑浊同时产 发 生 的 反 应 : Ba2++2HCO-
D 3 3
一定量的浓BaCl 溶液 生气泡 =BaCO↓+CO ↑+H O
2 3 2 2
【答案】D
【解析】A项,两溶液的浓度不确定,不能根据溶液的pH值判断水解程度的大小,故A错误;B
项,焰色呈黄色说明溶液中存在钠离子,不一定是钠盐,故B错误;C项,钠与苯酚反应比钠与乙醇反应
剧烈,苯酚中的羟基活性强于乙醇中羟基,故C错误;D项,通过现象可知反应生成碳酸钡和二氧化碳气
体,则反应离子方程式为:Ba2++2HCO-=BaCO ↓+CO ↑+H O,故D正确;故选D。
3 3 2 2
第Ⅱ卷二、非选择题:共5题,共52分。
17.(10分)第ⅢA和第ⅤA元素可形成多种化合物。请回答:
(1)基态B原子核外电子占据的最高能级符号是 ,基态As原子的价层电子排布式是
。
(2)① 固体储氢材料氨硼烷BH·NH ,其结构和乙烷相似,下列有关说法正确的是 。
3 3
A.氨硼烷中B原子的杂化方式为sp2
B.相同条件下在水中的溶解度:氨硼烷>乙烷
C.元素B、N的第一电离能均高于相邻元素
D. 是硼原子能量最低的激发态
②BF 形成的化合物中配位键的强度:BF·N(CH )Cl BF·N(CH )Cl (填“>”、“<”或“=”),
3 3 3 2 3 3 2
理由是 。
(3)一种含Ga化合物晶胞如图甲,三个晶胞围成一个六棱柱,如图乙,该化合物的化学式为
,每个N原子周围距离最近的N原子数目为 。
【答案】(1) 2p(1分) 4s24p3(1分)
(2) B(1分) >(1分) Cl电负性大,N(CH )Cl中Cl原子多,使N电子云密度降低,N的孤电子
3 2
对不易给出与BF 形成配位键,即形成的配位键稳定性低(2分)
3
(3) GaN(2分) 12(2分)
【解析】(1)基态B原子核外电子排布:1s22s22p1,占据的最高能级符号2p;As原子序数33,基态As
原子与的价层电子排布式4s24p3;(2)①A项,氨硼烷BH·NH ,其结构和乙烷相似,则氨硼烷中B原子的
3 3
杂化方式为sp3,A错误;B项,氨硼烷分子与水分子间可形成氢键,所以相同条件下在水中的溶解度:氨
硼烷>乙烷,B正确;C项,N原子核外电子排布处于半充满稳定结构,第一电离能高于相邻元素;B核外
电子排布:1s22s22p1,第一电离能不高于相邻元素,C错误;D项, 2s能级未排满电子,不是硼原子能量最低的激发态,D错误;故选B;②Cl电负性大,N(CH )Cl 中Cl原子多,使N
3 2
电子云密度降低,N的孤电子对不易给出与BF 形成配位键,即形成的配位键稳定性低;(3)均摊法计算可
3
知Ga原子与N原子个数比为1:1,则其化学式:GaN;距离每个N原子距离最近的N原子数目为12。
18.(10分)工业上按如下流程制备硝酸和肼(N H)。
2 4
(1)途径Ⅰ是工业制硝酸的第一步,写出化学方程式 。
(2) N H 的制法可通过途径Ⅱ:用过量NH 和CHCHO的混合物与氯气进行气相反应合成异肼
2 4 3 3
,然后使其水解得到肼。
①下列说法不正确的是 。
A.NH 属于电解质 B.途径Ⅱ中氯气作还原剂
3
C.N、H、NH 均为非极性分子 D.异肼中氮的化合价呈负价
2 2 2 4
②相同条件下,氨的沸点低于肼的主要原因是 。
(3)Zn元素的化学性质与Al相似。Zn与很稀的硝酸反应,氮元素被还原到最低价,写出该反应的离子
方程式 ;检验反应后溶液中除H+外的阳离子的方法是 。
【答案】(1)4NH +5O 4NO+6H O(2分)
3 2 2
(2) ABC(2分) 肼分子间形成的氢键数目多于氨(2分)
(3) 4Zn+10H++NO-=4Zn2++NH++3H O(2分) 取反应后的少量溶液分成两份,一份滴加足量NaOH
3 4 2
溶液并加热,产生能使湿润红色试纸变蓝的气体,则含有NH +,另一份滴加NaOH溶液至过量,先产生白
4
色沉淀后沉淀完全溶解,则含有Zn2+(2分)
【解析】N、H 在催化剂作用下合成NH ,NH 催化氧化可生成NO等,NO再被O 氧化为NO ,NO
2 2 3 3 2 2 2
用水吸收可制得HNO;NH 、CHCHO、Cl 发生氧化还原反应,可生成异肼 等,异肼
3 3 3 2与HO反应可生成NH。(1)途径Ⅰ是工业制硝酸的第一步,NH 催化氧化可生成NO等,化
2 2 4 3
学方程式为4NH +5O NO+6H O。(2)①A项,氨水能导电,但导电离子来自一水合氨的电离,所以
3 2 4 2
NH 属于非电解质,A不正确;B项,途径Ⅱ中,NH 中N元素显-3价,异肼 中N元素显-2
3 3
价,N元素的化合价升高,做还原剂,则氯气作氧化剂,B不正确;C项,N、H 为非极性分子,NH
2 2 2 4
中,N原子的最外层有1个孤电子对,对成键电子有排斥作用,使分子结构不对称,为极性分子,C不正
确;D项,N的非金属性大于C,则异肼中氮的化合价呈-2价,D正确;故选ABC。②相同条件下,氨和
肼都能形成分子间的氢键,但肼形成氢键的数目比氨更多,所以氨的沸点低于肼的主要原因是:肼分子间
形成的氢键数目多于氨。(3)Zn与很稀的硝酸反应,氮元素被还原到最低价(-3价),即生成NH +,该反应
4
的离子方程式为4Zn+10H++NO-=4Zn2++NH++3H O;溶液中除H+外的阳离子还有NH +和Zn2+,检验
3 4 2 4
NH +时,可加入碱,再检验产生的气体,检验Zn2+时,可利用Zn(OH) 的两性,方法是:取反应后的少量
4 2
溶液分成两份,一份滴加足量NaOH溶液并加热,产生能使湿润红色试纸变蓝的气体,则含有NH +,另一
4
份滴加NaOH溶液至过量,先产生白色沉淀后沉淀完全溶解,则含有Zn2+。
19.(10分)CO 过度排放会引起气候、环境等问题。在Cu/ZnO催化剂下,CO 和H 可发生反应生成
2 2 2
CHOH和CO,热化学方程式如下:
3
Ⅰ.CO(g)+3H(g) CHOH(g)+HO(g) ΔH=-50kJ·mol−1
2 3 2
Ⅱ.CO(g)+H(g) CO(g)+HO(g) ΔH=+41.2kJ·mol−1
2 2 2
(1)已知:2CO(g)+O(g)=2CO (g) ΔH =-566kJ·mol−1
2 2 1
HO(g)=H O(l) ΔH=-44kJ·mol−1
2 2
写出表示氢气燃烧热的热化学方程式 。
(2)在一定温度下,向体积固定的密闭容器中通入1mol CO 和2.31molH,起始压强为0.33MPa,发生
2 2
反应Ⅰ和Ⅱ。平衡时,总压为0.25MPa,CO 的转化率为50%,则反应Ⅰ的平衡常数K =
2 P
(以分压表示,分压=总压×物质的量分数)
(3)不同压强下,维持投料比相同,实验测定CO 的平衡转化率随温度的变化关系如图1所示。在恒压
2
密闭容器中,维持投料比相同,将CO 和H 按一定的流速通过反应器,二氧化碳的转化率 和甲
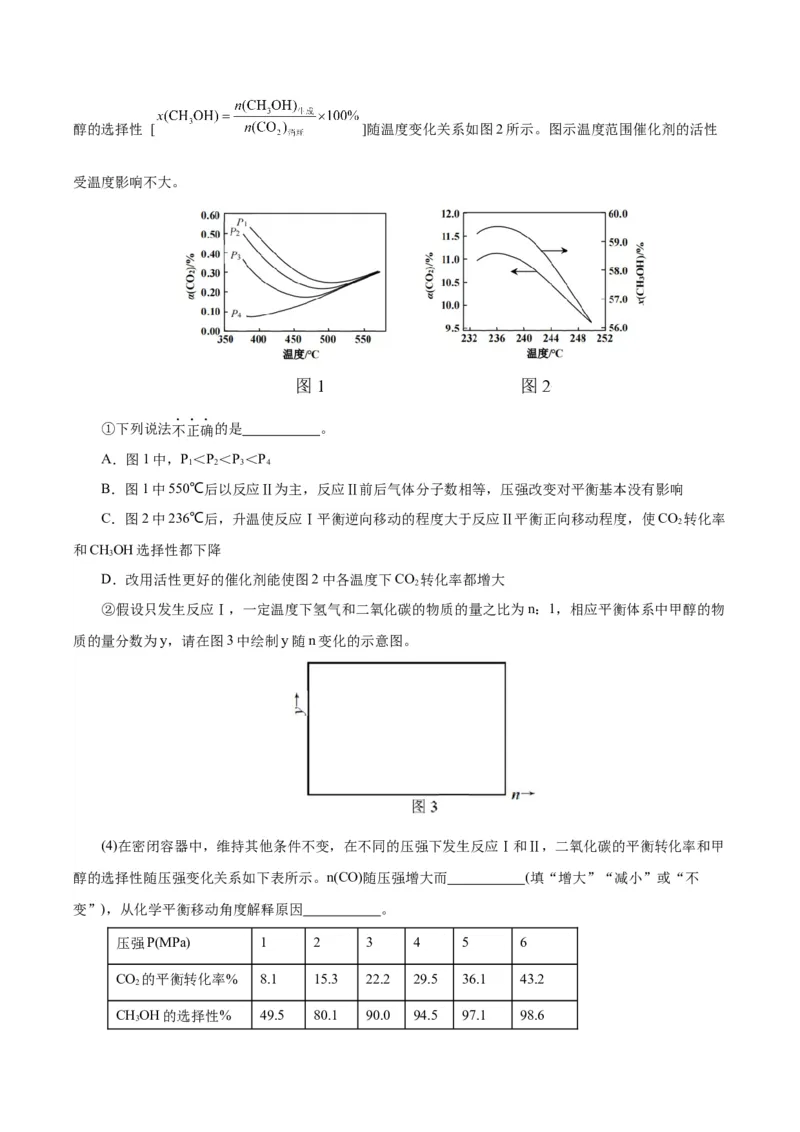
2 2醇的选择性 [ ]随温度变化关系如图2所示。图示温度范围催化剂的活性
受温度影响不大。
①下列说法不正确的是 。
A.图1中,P<P<P<P
1 2 3 4
B.图1中550℃后以反应Ⅱ为主,反应Ⅱ前后气体分子数相等,压强改变对平衡基本没有影响
C.图2中236℃后,升温使反应Ⅰ平衡逆向移动的程度大于反应Ⅱ平衡正向移动程度,使CO 转化率
2
和CHOH选择性都下降
3
D.改用活性更好的催化剂能使图2中各温度下CO 转化率都增大
2
②假设只发生反应Ⅰ,一定温度下氢气和二氧化碳的物质的量之比为n:1,相应平衡体系中甲醇的物
质的量分数为y,请在图3中绘制y随n变化的示意图。
(4)在密闭容器中,维持其他条件不变,在不同的压强下发生反应Ⅰ和Ⅱ,二氧化碳的平衡转化率和甲
醇的选择性随压强变化关系如下表所示。n(CO)随压强增大而 (填“增大”“减小”或“不
变”),从化学平衡移动角度解释原因 。
压强P(MPa) 1 2 3 4 5 6
CO 的平衡转化率% 8.1 15.3 22.2 29.5 36.1 43.2
2
CHOH的选择性% 49.5 80.1 90.0 94.5 97.1 98.6
3【答案】(1) (1分)
(2)40(2分) (3) AD(2分) (2分)
(4)减小(1分) 增大压强使反应Ⅰ平衡正向移动,水蒸气浓度变大,CO 和H 浓度下降,使反应Ⅱ
2 2
平衡逆向移动(2分)
【解析】(1)氢气燃烧热的热化学方程式 ,已知①2CO(g)+O(g)=2CO (g)、
2 2
②HO(g)=H O(l),根据盖斯定律,反应II+ 反应①+反应②可得,
2 2
,则表示氢气燃烧热的热化学方程式
;(2)一定温度体积不变的情况下,气体的物质的量与压强成正比,起始压强为
0.33MPa,平衡时总压为0.25MPa,则平衡时总物质的量为 ,CO 的转化率为
2
50%,则消耗n(CO)=0.5mol,设反应I和II分别消耗CO x mol、y mol,列三段式:
2 2
则有x+y=0.5、(1-x-y)+(2.3-3x-y)+(x+y)+(x+y)=2.5,解得x=0.4,y=0.1,平衡时n(CO)=0.5mol,
2n(H )=1mol,n(CHOH)=0.4mol,n(H O)=0.5mol,反应Ⅰ的平衡常数
2 3 2
;(3)①A项,相同温度下,增大压
强平衡正向移动,二氧化碳的转化率 增大,则图1中,P>P>P>P,故A错误;B项,图1
1 2 3 4
中550℃后以反应Ⅱ为主,反应Ⅱ前后气体分子数相等,压强改变对平衡基本没有影响,因此二氧化碳的
转化率 几乎相等,故B正确;C项,反应I为放热反应,升高温度,平衡逆向移动,二氧化碳的
转化率降低,反应II为吸热反应,升高温度,平衡正向移动,所以甲醇的选择性随温度升高而下降,则图
2中236℃后,升温使反应Ⅰ平衡逆向移动的程度大于反应Ⅱ平衡正向移动程度,使CO 转化率和CHOH
2 3
选择性都下降,故C正确;D项,催化剂只改变反应速率,不影响平衡移动,改用活性更好的催化剂能使
图2中各温度下CO 转化率都不变,故D错误;故选AD;②若只发生反应Ⅰ,当氢气和二氧化碳的物质
2
的量之比为3:1时,甲醇的物质的量分数最大,此时n=3,最后随着n的增大,甲醇的物质的量分数开始
逐渐减小,示意图为 ;(4)根据表格可知随着压强增大,CO 的平衡转化率变
2
大,说明消耗CO 增多,剩余的n(CO)随压强增大而减小,从化学平衡移动角度解释原因为:增大压强使
2
反应Ⅰ平衡正向移动,水蒸气浓度变大,CO 和H 浓度下降,使反应Ⅱ平衡逆向移动。
2 2
20.(10分)我国是稀土储量大国,氧化铈(CeO)是一种应用广泛的稀土氧化物。一种用氟碳铈矿
2
(CeFCO,含BaO、SiO 等杂质)为原料制备CeO 的工艺如下图。
3 2 2已知:①Ce3+可形成难溶于水的复盐[(Ce (SO )·Na SO ·nH O],其氢氧化物也难溶于水。
2 4 3 2 4 2
②硫脲的结构简式为CS(NH ),在酸条件下易被氧化为(CSN H)。
2 2 2 3 2
请回答:
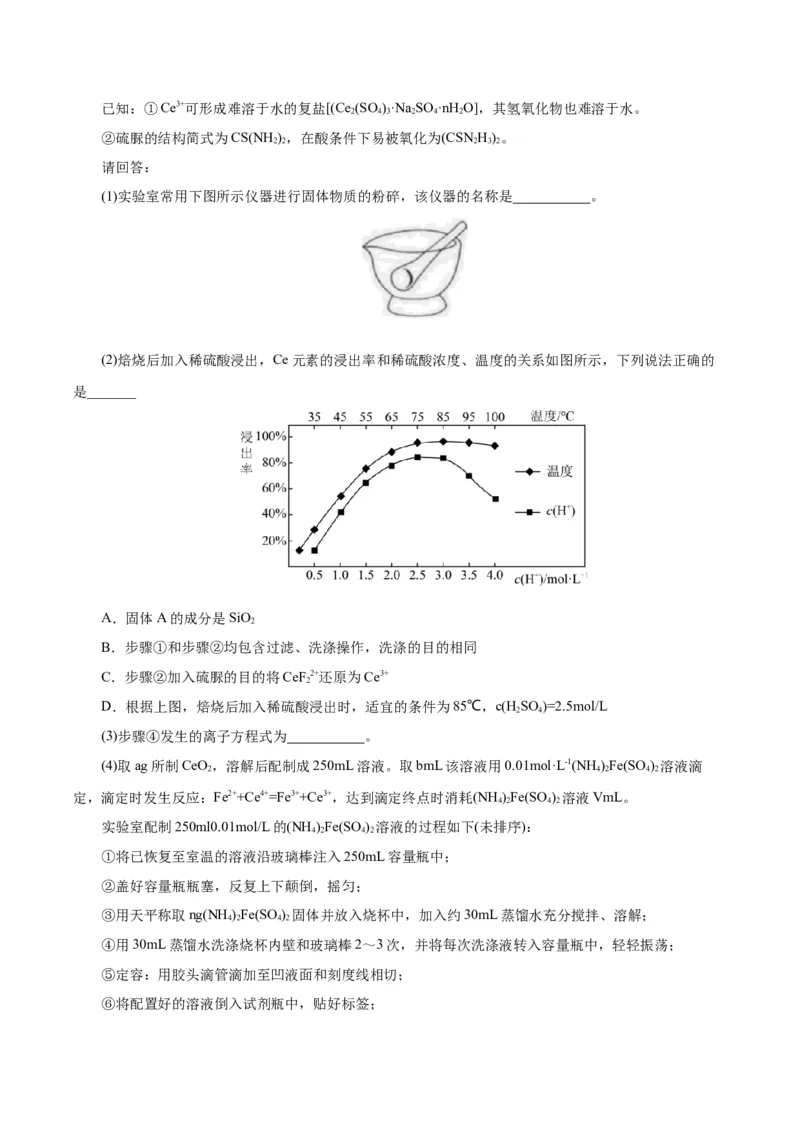
(1)实验室常用下图所示仪器进行固体物质的粉碎,该仪器的名称是 。
(2)焙烧后加入稀硫酸浸出,Ce元素的浸出率和稀硫酸浓度、温度的关系如图所示,下列说法正确的
是_______
A.固体A的成分是SiO
2
B.步骤①和步骤②均包含过滤、洗涤操作,洗涤的目的相同
C.步骤②加入硫脲的目的将CeF 2+还原为Ce3+
2
D.根据上图,焙烧后加入稀硫酸浸出时,适宜的条件为85℃,c(HSO )=2.5mol/L
2 4
(3)步骤④发生的离子方程式为 。
(4)取ag所制CeO,溶解后配制成250mL溶液。取bmL该溶液用0.01mol·L-1(NH )Fe(SO ) 溶液滴
2 4 2 4 2
定,滴定时发生反应:Fe2++Ce4+=Fe3++Ce3+,达到滴定终点时消耗(NH )Fe(SO ) 溶液VmL。
4 2 4 2
实验室配制250ml0.01mol/L的(NH )Fe(SO ) 溶液的过程如下(未排序):
4 2 4 2
①将已恢复至室温的溶液沿玻璃棒注入250mL容量瓶中;
②盖好容量瓶瓶塞,反复上下颠倒,摇匀;
③用天平称取ng(NH )Fe(SO ) 固体并放入烧杯中,加入约30mL蒸馏水充分搅拌、溶解;
4 2 4 2
④用30mL蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤液转入容量瓶中,轻轻振荡;
⑤定容:用胶头滴管滴加至凹液面和刻度线相切;
⑥将配置好的溶液倒入试剂瓶中,贴好标签;实验操作顺序依次为 (填序号)。滴定过程中,接近终点时需采用半滴操作,具体操作是
。
(5)该产品的质量分数为 (列出表达式)
【答案】(1)研钵(1分) (2)C(2分) (3)2Ce3++6HCO-=Ce (CO) ↓+3H O+3CO↑(1分)
3 2 3 2 2
(4)③①④⑤②⑥(2分) 慢慢旋转滴定管旋塞,使滴定管口悬挂液滴而不滴落,用锥形瓶内壁靠落
液滴,并用蒸馏水将液滴冲入溶液中,振荡锥形瓶使溶液充分混合(2分)
(5) (2分)
【解析】氟碳铈矿在空气中焙烧,Ce3+在空气中氧化为四价Ce,用硫酸浸取,四价Ce进入溶液得到
含CeF 2+溶液,SiO 不反应,BaO与硫酸反应生成BaSO 沉淀,过滤分离,滤渣A为SiO、BaSO,含
2 2 4 2 4
CeF 2+溶液中加入硫脲将四价Ce还原为Ce3+,Ce (SO ) 与NaSO 形成复盐沉淀Ce (SO )· Na SO ·nH O,
2 2 4 3 2 4 2 4 3 2 4 2
过滤分离,复盐沉淀加入碱,再加入酸,Ce3+被转移到溶液中,再加入碳酸氢铵使Ce3+沉淀为Ce (CO),
2 3 3
最后灼烧分解生成CeO。(1)该仪器的名称是研钵;(2)A项,由分析可知,固体A的成分是SiO、BaSO,
2 2 4
错误;B项,步骤①和步骤②均为分离固液的操作,包含过滤,但是步骤①洗涤沉淀的目的是回收残留的
Ce4+,而步骤②洗涤的目的是去除残留在沉淀B表面的杂质残液,错误;C项,步骤②加入硫脲的目的将
CeF 2+还原为Ce3+,正确;D项,根据上图,焙烧后加入稀硫酸浸出时,适宜的条件为85℃,氢离子浓度
2
约为2.5mol/L,则c(HSO )=1.25mol/L,错误;故选C;(3)步骤④反应为Ce3+溶液中加入碳酸氢铵使Ce3+沉
2 4
淀为Ce (CO),根据质量守恒可知,还会生成水和二氧化碳气体,发生的离子方程式为2Ce3++6HCO-
2 3 3 3
=Ce (CO) ↓+3H O+3CO↑;(4)配制一定物质的量浓度的溶液,所需的步骤有计算、称量、溶解(冷却)、转
2 3 2 2
移、洗涤、定容、摇匀、装瓶贴签;因此顺序为③①④⑤②⑥;滴定过程中,接近终点时需采用半滴操
作,具体操作是:慢慢旋转滴定管旋塞,使滴定管口悬挂液滴而不滴落,用锥形瓶内壁靠落液滴,并用蒸
馏水将液滴冲入溶液中,振荡锥形瓶使溶液充分混合;(5)滴定时发生反应:Fe2++Ce4+=Fe3++Ce3+,则该产
品中CeO 物质的量为: ,该产品的质量分数为
2
。
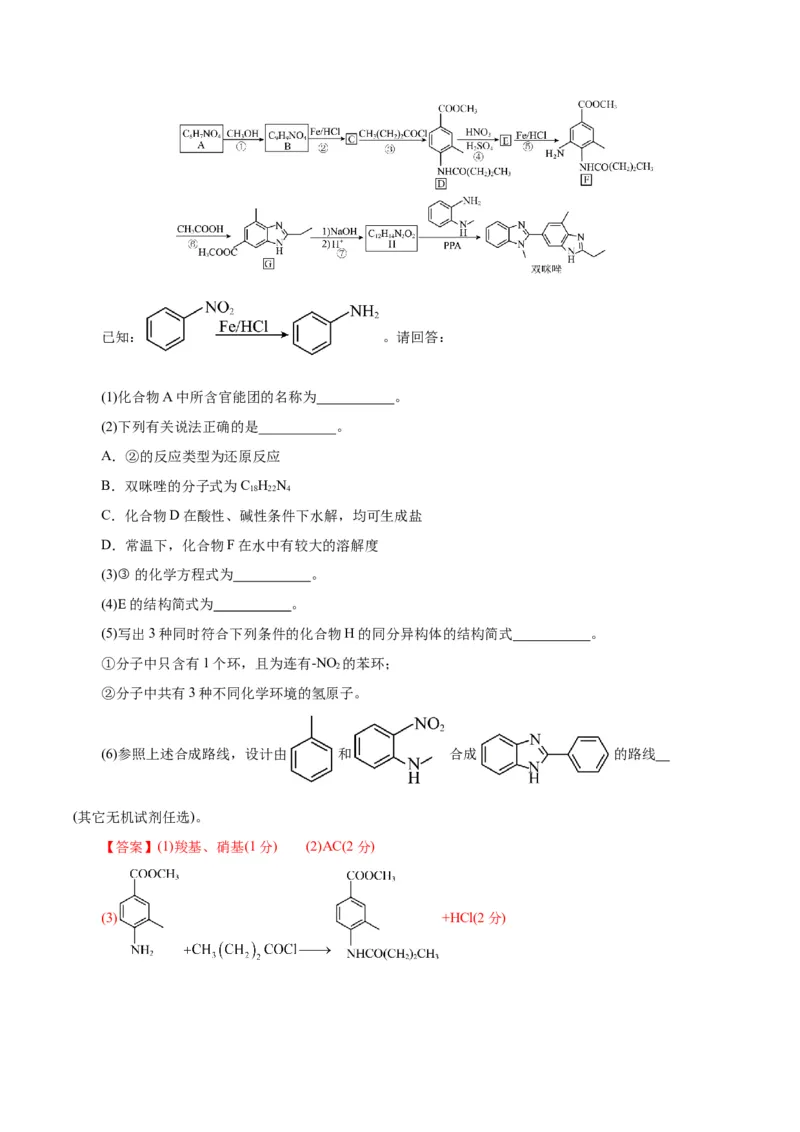
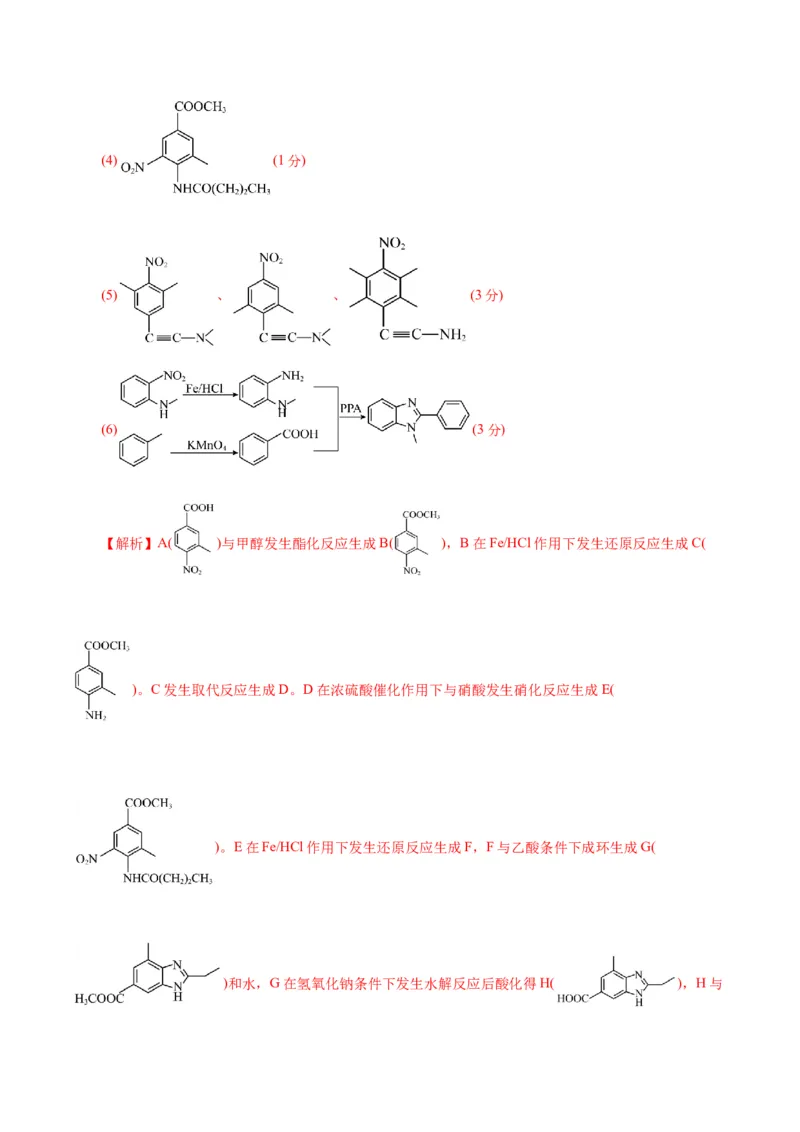
21.(12分)双咪唑是合成治疗高血压药物替米沙坦的一种中间体,其合成路线如下:已知: 。请回答:
(1)化合物A中所含官能团的名称为 。
(2)下列有关说法正确的是___________。
A.②的反应类型为还原反应
B.双咪唑的分子式为C H N
18 22 4
C.化合物D在酸性、碱性条件下水解,均可生成盐
D.常温下,化合物F在水中有较大的溶解度
(3)③ 的化学方程式为 。
(4)E的结构简式为 。
(5)写出3种同时符合下列条件的化合物H的同分异构体的结构简式 。
①分子中只含有1个环,且为连有-NO 的苯环;
2
②分子中共有3种不同化学环境的氢原子。
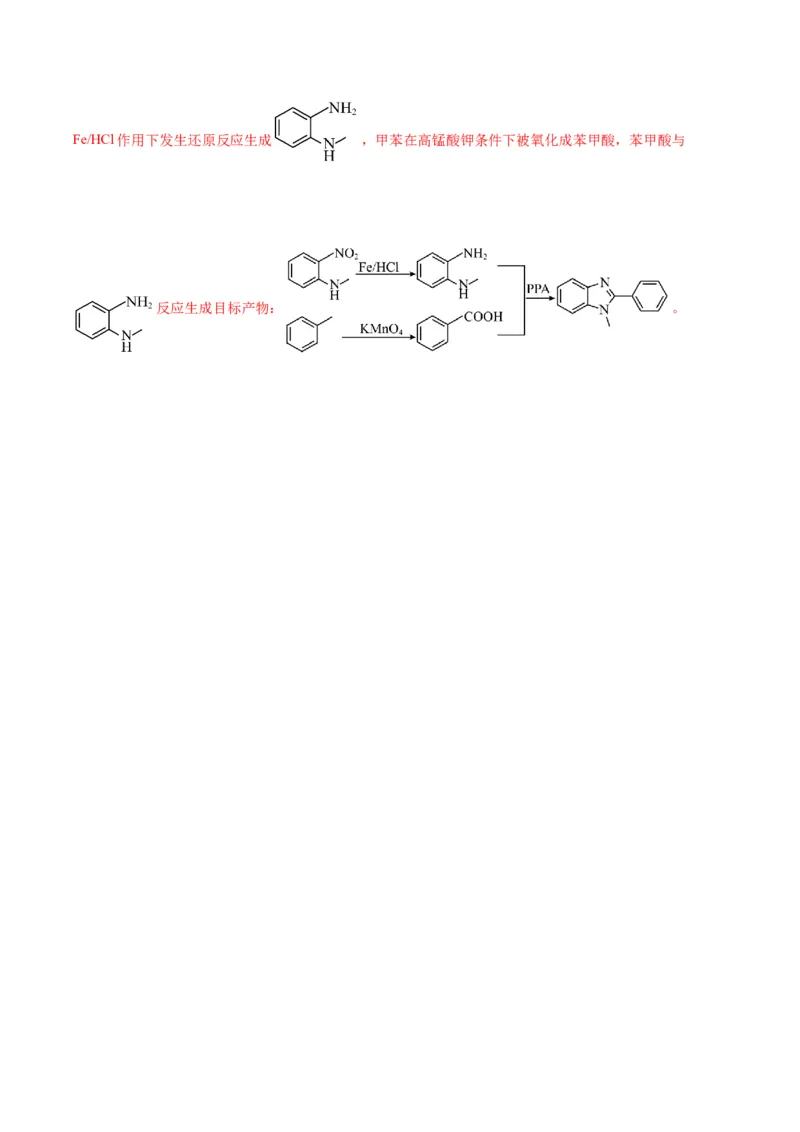
(6)参照上述合成路线,设计由 和 合成 的路线
(其它无机试剂任选)。
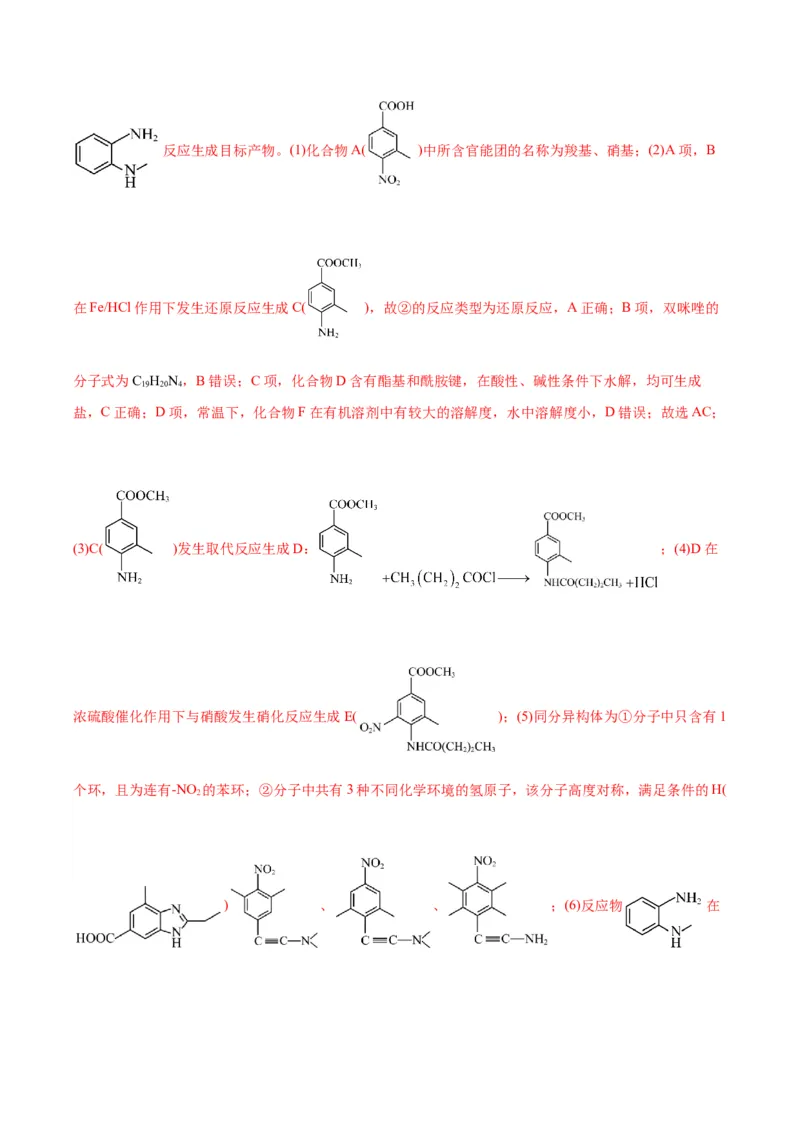
【答案】(1)羧基、硝基(1分) (2)AC(2分)
(3) +HCl(2分)(4) (1分)
(5) 、 、 (3分)
(6) (3分)
【解析】A( )与甲醇发生酯化反应生成B( ),B在Fe/HCl作用下发生还原反应生成C(
)。C发生取代反应生成D。D在浓硫酸催化作用下与硝酸发生硝化反应生成E(
)。E在Fe/HCl作用下发生还原反应生成F,F与乙酸条件下成环生成G(
)和水,G在氢氧化钠条件下发生水解反应后酸化得H( ),H与反应生成目标产物。(1)化合物A( )中所含官能团的名称为羧基、硝基;(2)A项,B
在Fe/HCl作用下发生还原反应生成C( ),故②的反应类型为还原反应,A正确;B项,双咪唑的
分子式为C H N,B错误;C项,化合物D含有酯基和酰胺键,在酸性、碱性条件下水解,均可生成
19 20 4
盐,C正确;D项,常温下,化合物F在有机溶剂中有较大的溶解度,水中溶解度小,D错误;故选AC;
(3)C( )发生取代反应生成D: ;(4)D在
浓硫酸催化作用下与硝酸发生硝化反应生成E( );(5)同分异构体为①分子中只含有1
个环,且为连有-NO 的苯环;②分子中共有3种不同化学环境的氢原子,该分子高度对称,满足条件的H(
2
) 、 、 ;(6)反应物 在Fe/HCl作用下发生还原反应生成 ,甲苯在高锰酸钾条件下被氧化成苯甲酸,苯甲酸与
反应生成目标产物: 。