文档内容
【赢在高考·黄金8卷】备战2024年高考化学模拟卷(辽宁专用)
黄金卷08
(考试时间:75分钟 试卷满分:100分)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cl 35.5 Cr 52 Fe 56 Cu 64
第Ⅰ卷
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项符合题目要
求。
1.化学渗透在社会生活的各个方面。下列叙述正确的是
A.合成氨的反应塔与外加电源的正极相连,并维持一定的电压可以钝化防腐
B.纳米铁粉主要通过物理吸附作用除去污水中的Cu2+、Ag+、Hg2+
C.开发利用新能源,减少化石燃料的使用是实现“碳中和”目标的有效途径
D.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
【答案】C
【解析】A.合成氨的反应塔为钢铁材质,在电解池中,金属做阳极是先被腐蚀,应该与负极相连作阴极
才能被保护,不被腐蚀,A错误;
B.纳米铁粉主具有吸附性及还原性,主要通过还原性除去污水中的Cu2+、Ag+、Hg2+,B错误;
C.开发利用新能源,减少化石燃料的燃烧,进一步减少CO 的排放,有利于实现“碳达峰、碳中和”,C
2
正确;
D.晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料,常用于制造芯片、半导体材料和太阳
能电池板,而光导纤维的主要成分是SiO,D错误;
2
故答案为:C。
2.化学用语是化学专业术语.下列术语错误的是
A.基态砷原子的价层电子轨道表示式:
B. 分子的VSEPR模型:
C. 的电子式:D.4―氯丁酸的结构简式:
【答案】B
【解析】A.基态砷原子的价层电子排布式为 ,价层电子轨道表示式: ,
A正确;
B. 分子的中心原子氮原子的价层电子对数 ,VSEPR模型为四面体形,B错误;
C. 的电子式: ,C正确;
D.4―氯丁酸的结构简式: ,D正确;
故选B。
3.设 为阿伏加德罗常数,下列说法中正确的是
A. 硅酸钠溶液中滴入盐酸制硅酸胶体,所得胶粒数目为
B.将标准状况下 与 混合后的体积约为
C. 与足量铁粉反应转移的电子数为
D. 二氧化硅晶体中含有 键数为
【答案】C
【解析】A.胶体粒子是多个微粒的聚集体,不能算数目,A错误;
B.NO与O 混合后生成NO ,常温下2NO NO,无法计算混合后体积,B错误;
2 2 2 2 4
C.n(Cl )= mol=0.1mol,1mol Cl 转移2mole-,0.1mol Cl 转移0.2N e-,C正确;
2 2 2 A
2
原创精品资源学科网独家享有版权,侵权必究!D.60g二氧化硅的物质的量为 =1mol,1mol二氧化硅晶体中含有Si−O键数为4NA,D错误;
故选C。
4.能正确表示下列反应的离子方程式或电极反应式的是
A.少量 通入 溶液中:
B.电解液为 溶液的 燃料电池的负极反应式:
C.向四羟基合铝酸钠溶液中加入小苏打溶液:
D.食醋和84消毒液混合:
【答案】C
【解析】A. 次氯酸根离子具有强氧化性,二氧化硫具有还原性,少量二氧化硫与次氯酸钙反应生成硫酸钙
沉淀和次氯酸,离子反应为 ,A错误;
B. 燃料电池的负极反应式为 ,B错误;
C. 向四羟基合铝酸钠溶液中加入小苏打溶液,反应生成氢氧化铝沉淀和碳酸钠,离子反应式为
,C正确;
D. 食醋与84消毒液反应产生氯气,醋酸为弱酸,离子方程式为
,D错误;
答案选C。
5.乙醛是一种重要的二碳试剂,其某种合成机理如图所示。下列说法错误的是
A.Fe+是该反应的催化剂B.C HOH是合成过程中的副产物
2 5
C.该合成乙醛的反应为
D.及时分离出C HOH,有利于提高CHCHO的产率
2 5 3
【答案】D
【解析】A.根据合成机理可知Fe+在第一步消耗,最后一步生成,是该反应的催化剂,A正确;
B.由合成机理可知C HOH为生成物,所以C HOH是合成过程中的副产物,B正确;
2 5 2 5
C.根据合成机理的箭头指入情况和指出情况可知该合成乙醛的反应为
,C正确;
D.及时分离出C HOH会增加副产物的生成,不利于提高CHCHO的产率,D错误;
2 5 3
故选D。
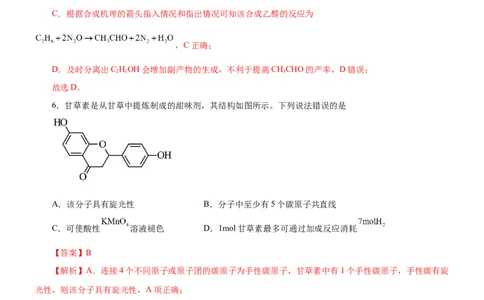
6.甘草素是从甘草中提炼制成的甜味剂,其结构如图所示。下列说法错误的是
A.该分子具有旋光性 B.分子中至少有5个碳原子共直线
C.可使酸性 溶液褪色 D.1mol甘草素最多可通过加成反应消耗
【答案】B
【解析】A.连接4个不同原子或原子团的碳原子为手性碳原子,甘草素中有1个手性碳原子,手性碳有旋
光性,则该分子具有旋光性,A项正确;
B.甘草素分子结构中含有苯环结构,对角线上的四个原子共线,若碳原子共线,则至少有3个碳原子共直
线,B项错误;
C.甘草素含有酚羟基,能使酸性高锰酸钾褪色,C项正确;
D.甘草素含有两个苯环,一个羰基,1mol甘草素,最多可以通过加成反应消耗7mol氢气,D项正确;
答案选B。
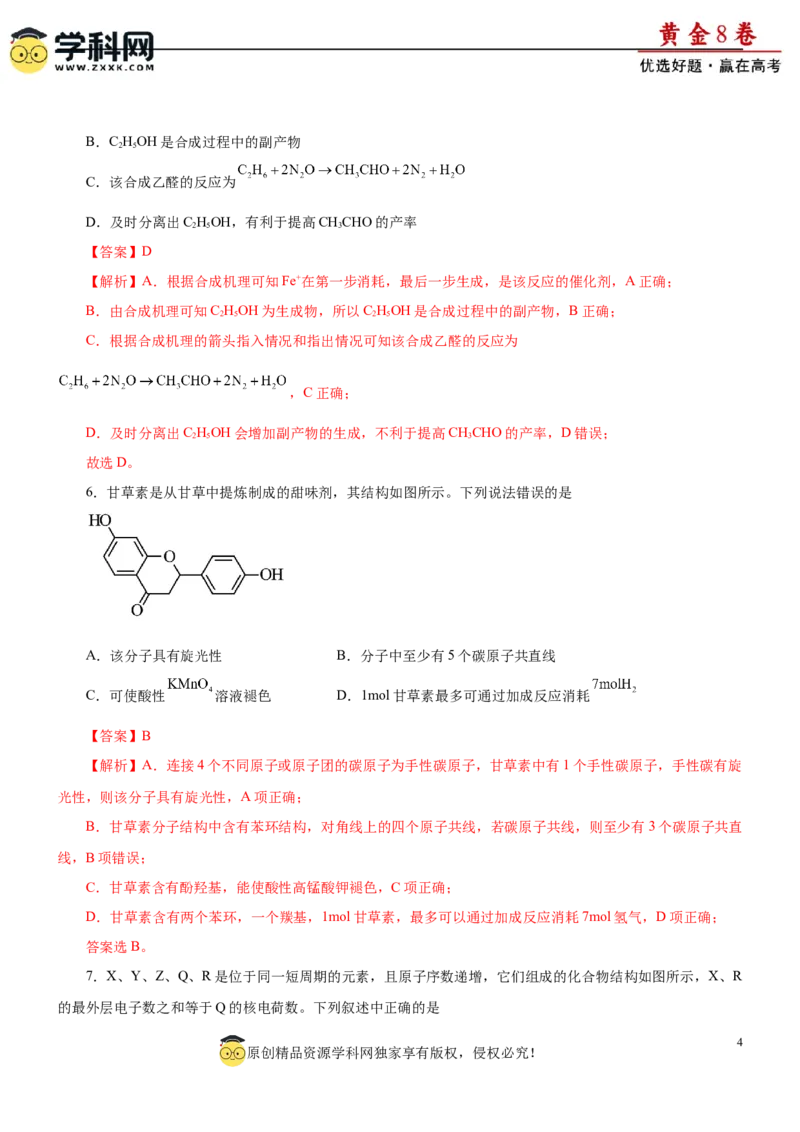
7.X、Y、Z、Q、R是位于同一短周期的元素,且原子序数递增,它们组成的化合物结构如图所示,X、R
的最外层电子数之和等于Q的核电荷数。下列叙述中正确的是
4
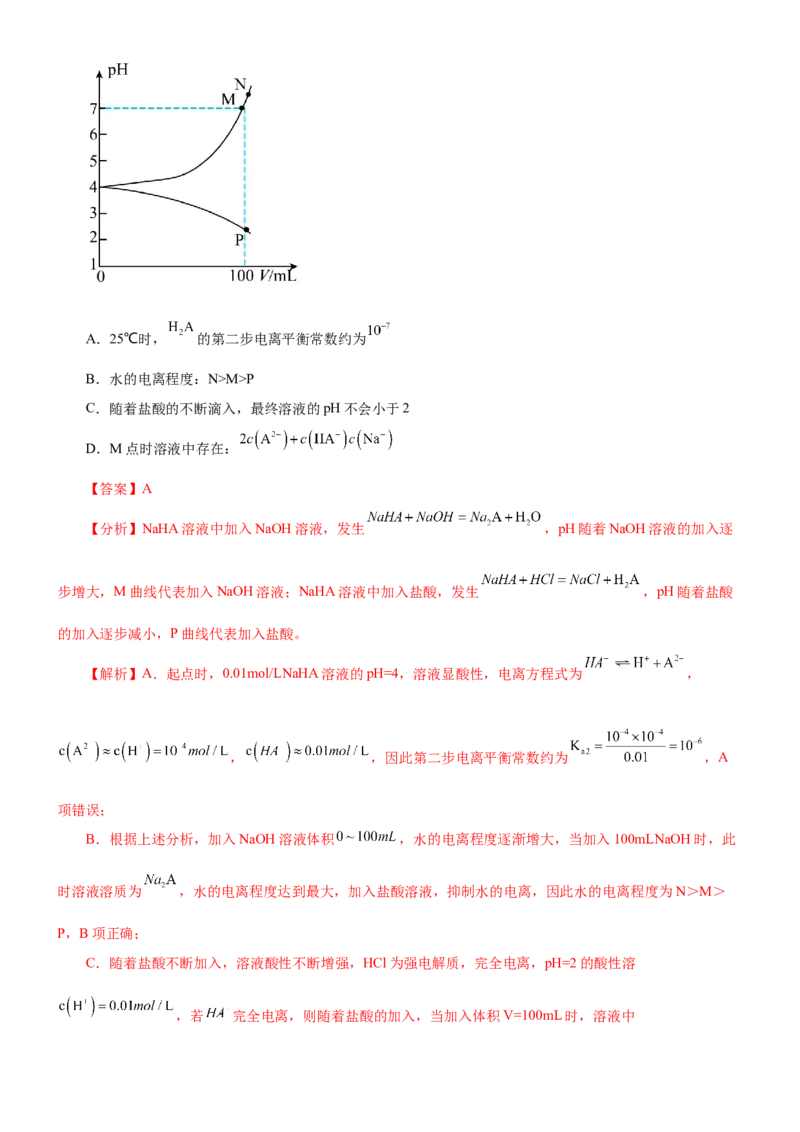
原创精品资源学科网独家享有版权,侵权必究!A.简单离子半径:XM>P
C.随着盐酸的不断滴入,最终溶液的pH不会小于2
D.M点时溶液中存在:
【答案】A
【分析】NaHA溶液中加入NaOH溶液,发生 ,pH随着NaOH溶液的加入逐
步增大,M曲线代表加入NaOH溶液;NaHA溶液中加入盐酸,发生 ,pH随着盐酸
的加入逐步减小,P曲线代表加入盐酸。
【解析】A.起点时,0.01mol/LNaHA溶液的pH=4,溶液显酸性,电离方程式为 ,
, ,因此第二步电离平衡常数约为 ,A
项错误;
B.根据上述分析,加入NaOH溶液体积 ,水的电离程度逐渐增大,当加入100mLNaOH时,此
时溶液溶质为 ,水的电离程度达到最大,加入盐酸溶液,抑制水的电离,因此水的电离程度为N>M>
P,B项正确;
C.随着盐酸不断加入,溶液酸性不断增强,HCl为强电解质,完全电离,pH=2的酸性溶
,若 完全电离,则随着盐酸的加入,当加入体积V=100mL时,溶液中,但 并不完全解离,因此溶液中
,最终溶液pH不会小于2,C项正确;
D.根据电荷守恒有 ,M点溶液的pH=7, ,
即有 ,D项正确;
故选A。
第Ⅱ卷
二、非选择题:本题共4小题,共55分。
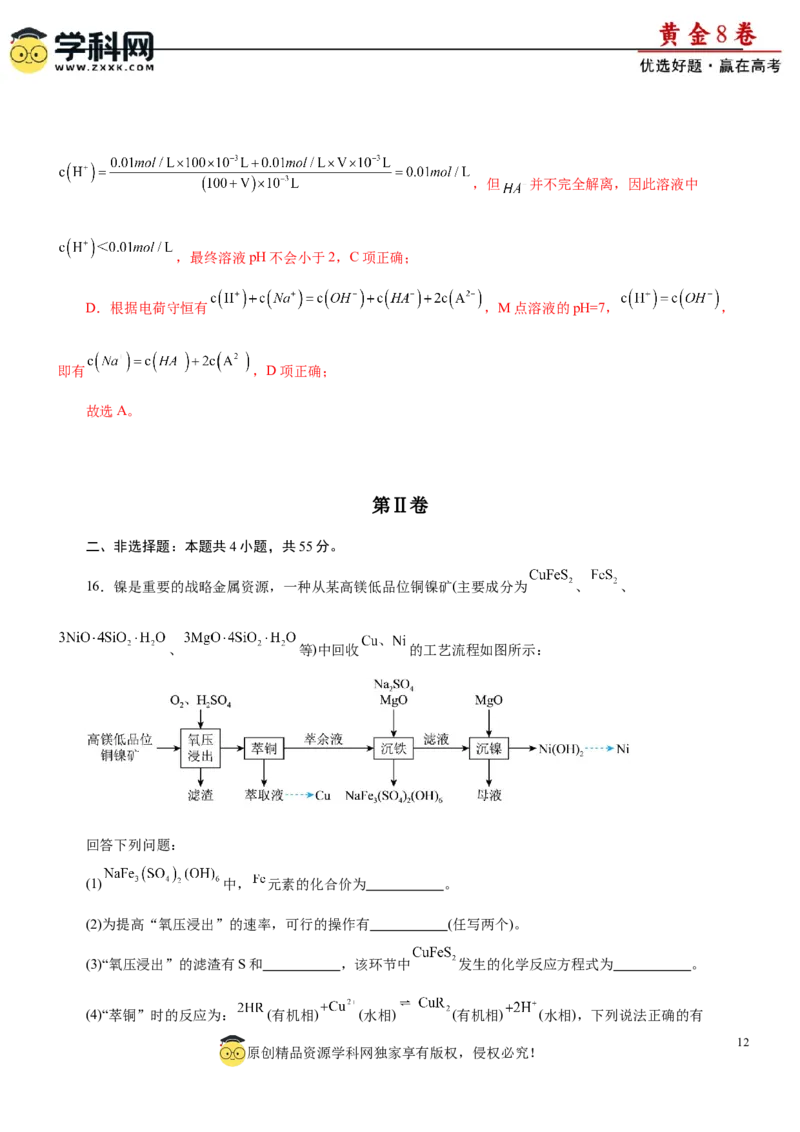
16.镍是重要的战略金属资源,一种从某高镁低品位铜镍矿(主要成分为 、 、
、 等)中回收 的工艺流程如图所示:
回答下列问题:
(1) 中, 元素的化合价为 。
(2)为提高“氧压浸出”的速率,可行的操作有 (任写两个)。
(3)“氧压浸出”的滤渣有S和 ,该环节中 发生的化学反应方程式为 。
(4)“萃铜”时的反应为: (有机相) (水相) (有机相) (水相),下列说法正确的有
12
原创精品资源学科网独家享有版权,侵权必究!___________。
A.萃余液中的阳离子为:
B.为提高 的萃取率,可适当提高溶液
C.一定条件下,萃取平衡时, ,则 的萃取率为
D.向萃取液中加入稀硫酸进行“反萃取”,可得到单质
(5)已知 ,“滤液”中 ,“沉镍”时,控制 为7.50,此时
的沉淀率为 ,“沉镍”后的母液,含有的主要溶质为 (填化学式)。
【答案】(1)+3
(2)适当升高温度、适当增压、将高镁低品位铜镍矿粉碎以增大固液接触面积或适当增大硫酸的浓度
(3) (或难溶性硅酸盐)
(4)BC
(5) 90%
【分析】由题干工艺流程图可知,向高镁低品位铜镍矿(主要成分为CuFeS、FeS、3NiO·4SiO ·H O、
2 2 2 2
3MgO·4SiO ·H O等)中加入O、HSO 进行氧压浸出,将铁元素转化为Fe (SO ),镍元素转化为NiSO 、铜元素
2 2 2 2 4 2 4 3 4
转化为CuSO 、镁元素转化为MgSO ,硫元素转化为S单质,过滤得到滤渣主要成分为SiO 和S,用铜离子萃
4 4 2
取剂萃取出Cu2+,分液得到萃取液,萃余液中主要含有Fe3+、Mg2+、Ni2+,向萃余液中加入NaSO 和MgO进行
2 4
沉铁将Fe3+转化为NaFe (SO )(OH) 、过滤出沉淀,向滤液中加入MgO将Ni2+以Ni(OH) 的形成沉淀,最后对
3 4 2 6 2
Ni(OH) 进行处理制得Ni,母液中主要溶质为MgSO ,据此分析解题。
2 4
【解析】(1)已知钠离子带一个正电荷,硫酸根带2个负电荷,氢氧根带一个负电荷,根据化合价代数和
为0可知NaFe (SO )(OH) 中,Fe元素的化合价为+3价,故答案为:+3;
3 4 2 6
(2)将高镁低品位铜镍矿粉碎以增大固液接触面积、适当升高反应温度、充分搅拌和适当增大硫酸的浓度
等措施均能提高“氧压浸出”的速率,故答案为:将高镁低品位铜镍矿粉碎以增大固液接触面积或适当升高反
应温度或充分搅拌或适当增大硫酸的浓度;
(3)由分析可知,“氧压浸出”的滤渣有S和SiO,该环节中CuFeS 与HSO 、O 反应生成CuSO 、
2 2 2 4 2 4
Fe (SO )、S和HO,根据氧化还原反应配平可得该反应的化学反应方程式为:
2 4 3 24CuFeS+10H SO +5O =4CuSO+2Fe (SO )+8S↓+10H O,故答案为:SiO;
2 2 4 2 4 2 4 3 2 2
4CuFeS+10H SO +5O =4CuSO+2Fe (SO )+8S↓+10H O;
2 2 4 2 4 2 4 3 2
(4)A.由题干分析结合小问1分析可知,萃余液中主要含有Fe3+、Mg2+、Ni2+,A错误;
B.适当提高溶液则H+浓度减小,平衡正向移动,故可提高的萃取率,B正确;
C.一定条件下,萃取平衡时, ,即被萃取的Cu2+也就是形成CuR 的Cu2+是残留在溶液中的
2
Cu2+的4倍,则Cu2+的萃取率为 =80%,C正确;
D.向萃取液中加入稀硫酸进行“反萃取”,萃取平衡逆向移动,故可得到Cu2+,得不到单质Cu,D错
误;
故答案为:BC;
(5)已知 ,“滤液”中c(Ni2+)=0.2mol/L,“沉镍”时,控制为7.50,此时溶液中
c(OH-)=10-6.5mol/L,溶液中残留的Ni2+浓度为:c(Ni2+)= = 0.02mol/L,则此时的沉淀率
为 ×100%=90%,由分析可知,“沉镍”后的母液,含有的主要溶质为MgSO ,故答案
4
为:90%;MgSO 。
4
17.氧化石墨烯在能源、材料等领域有重要的应用前景。研究人员采用无NaNO 的方法氧化剥离石墨制备
3
氧化石墨烯,实现了废气减排,废液无害化处理,使制备过程更加环境友好。其方法如下,装置如图所示:
14
原创精品资源学科网独家享有版权,侵权必究!Ⅰ.将浓HSO 、石墨粉末在c中混合,置于冰水浴中,剧烈搅拌下,分批缓慢加入KMnO 粉末,塞好瓶
2 4 4
口。
Ⅱ.转至油浴中,40℃下搅拌0.5h,缓慢滴加一定量的蒸馏水。升温至95℃并保持15min。
Ⅲ.转移至大烧杯中,静置冷却至室温。加入大量蒸馏水,而后滴加HO 至悬浊液由紫色变为土黄色。
2 2
Ⅳ.过滤分离,用稀盐酸洗涤沉淀。
Ⅴ.空气中干燥,用蒸馏水溶解并搅拌过夜,将得到的氧化石墨烯水体系分散液透析净化。
Ⅵ.收集制备时产生的废水,对废水进行处理。
回答下列问题:
(1)装置图中,仪器 的作用是
(2)若原料中有NaNO ,则产生的有毒有害气体造成的环境问题有 。(写两条)
3
(3)从氧化还原角度分析,步骤Ⅲ中体现了HO 的 。
2 2
(4)步骤Ⅳ中,检验洗涤液中是否含有 的操作及现象为 。
(5)透析法分离提纯物质的原理与渗析法相似。下列物质(括号中为杂质)的分离提纯可采用渗析法的是
(填标号)。
a.NaCl溶液(NH Cl) b.淀粉溶液(NaCl)
4
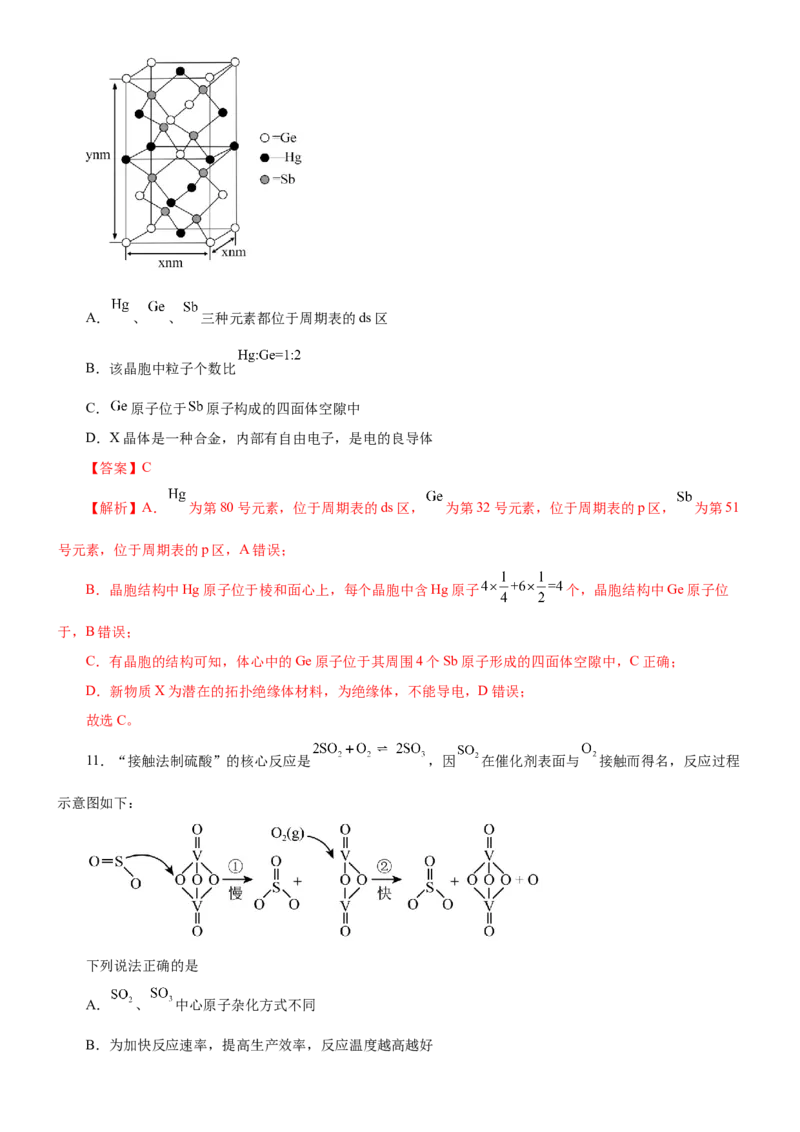
(6)废水中Mn2+的含量可用KSO 溶液测定,滴定终点现象为溶液由无色变为紫色。某实验小组收集了
2 2 8
20.00mL废水样品,用cmol∙L-1的KSO 标准溶液滴定,共消耗标准溶液10.00mL。
2 2 8
①写出滴定反应的离子方程式: (已知 的结构为 )。
②废水中Mn2+的浓度为 mg∙mL-1。
【答案】(1)冷凝回流
(2)光化学烟雾、酸雨
(3)还原性
(4)取最后一次洗涤液少量,用稀盐酸酸化,再滴加BaCl 溶液,若无白色沉淀生成,说明洗涤液中不含有
2
,反之洗涤液中含有
(5)b
(6) 5 +2Mn2++8H O=10 +16H++2 11c
2
【分析】制取氧化石墨烯时,将浓HSO 、石墨粉末混合后置于冰水浴中,剧烈搅拌下,分批缓慢加入
2 4
KMnO 粉末,油浴加热至95℃并保持15min,静置冷却至室温;加入大量蒸馏水,滴加HO 将多余KMnO 还
4 2 2 4
原;过滤分离后,用稀盐酸洗去表面吸附的杂质,再用蒸馏水洗涤,最后将氧化石墨烯水体系分散液透析净化,从而得到纯净的氧化石墨烯。
【解析】(1)装置图中,仪器 的作用是冷凝回流。
(2)若原料中有NaNO ,则产生的有毒有害气体为NO 等,造成的环境问题有:光化学烟雾、酸雨。
3 2
(3)从氧化还原角度分析,步骤Ⅲ中滴加HO 至悬浊液由紫色变为土黄色,表明 转化为Mn2+,则
2 2
HO 表现的性质是还原性。
2 2
(4)步骤Ⅳ中,检验洗涤液中是否含有 ,常加入BaCl 溶液,看是否有白色沉淀产生,具体操作及现
2
象为:取最后一次洗涤液少量,用稀盐酸酸化,再滴加BaCl 溶液,若无白色沉淀生成,说明洗涤液中不含有
2
,反之洗涤液中含有 。
(5)渗析法是精制胶体常用的方法,则淀粉溶液中混有NaCl时,可采用渗析法,故选b。
(6)①滴定反应时,Mn2+与 在酸性溶液中发生氧化还原反应,生成 和 ,离子方程式:5
+2Mn2++8H O=10 +16H++2 。
2
②废水中Mn2+的浓度为 =11c mg∙mL-1。
【点睛】胶粒不能透过半透膜孔隙,而溶液中的离子和小分子可透过半透膜孔隙。
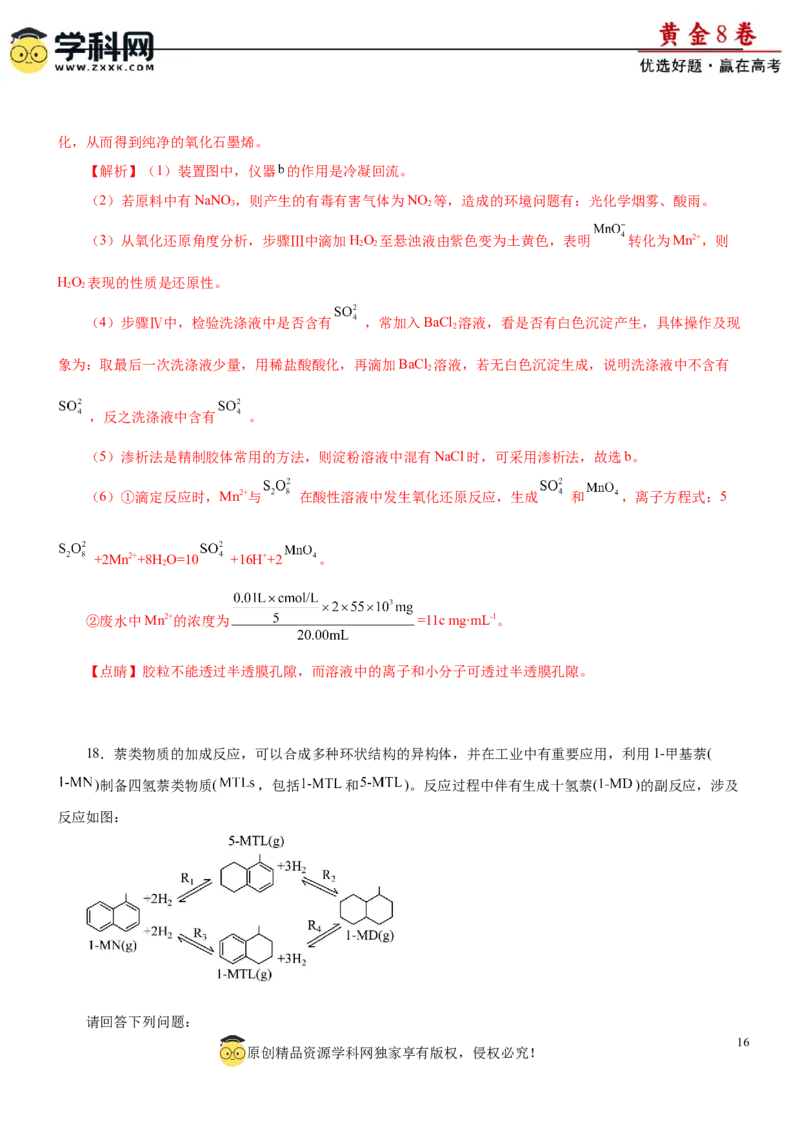
18.萘类物质的加成反应,可以合成多种环状结构的异构体,并在工业中有重要应用,利用1-甲基萘(
)制备四氢萘类物质( ,包括 和 )。反应过程中伴有生成十氢萘( )的副反应,涉及
反应如图:
请回答下列问题:
16
原创精品资源学科网独家享有版权,侵权必究!(1)已知一定条件下反应 的焓变分别为 ,则反应 的焓变 (用含
的代数式表示)。
(2)根据 和 的结构及命名方式, 和 的一种同分异构体 的名称
为 。
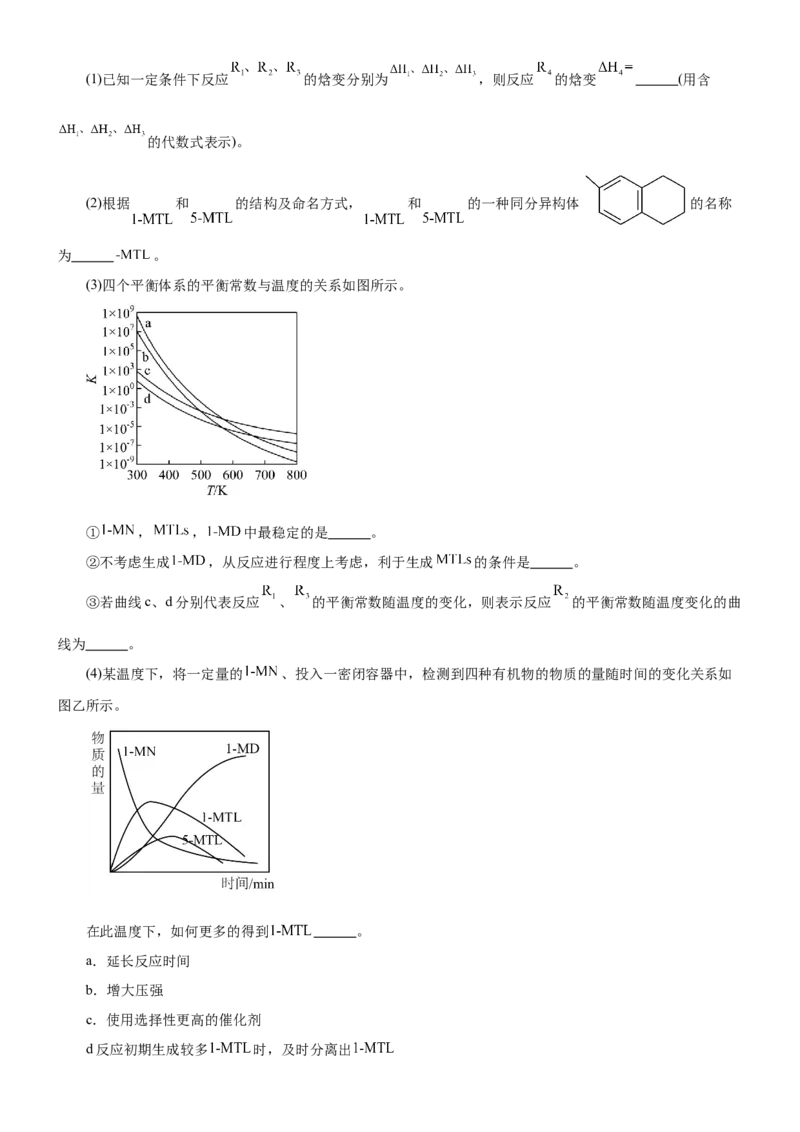
(3)四个平衡体系的平衡常数与温度的关系如图所示。
① , , 中最稳定的是 。
②不考虑生成 ,从反应进行程度上考虑,利于生成 的条件是 。
③若曲线c、d分别代表反应 、 的平衡常数随温度的变化,则表示反应 的平衡常数随温度变化的曲
线为 。
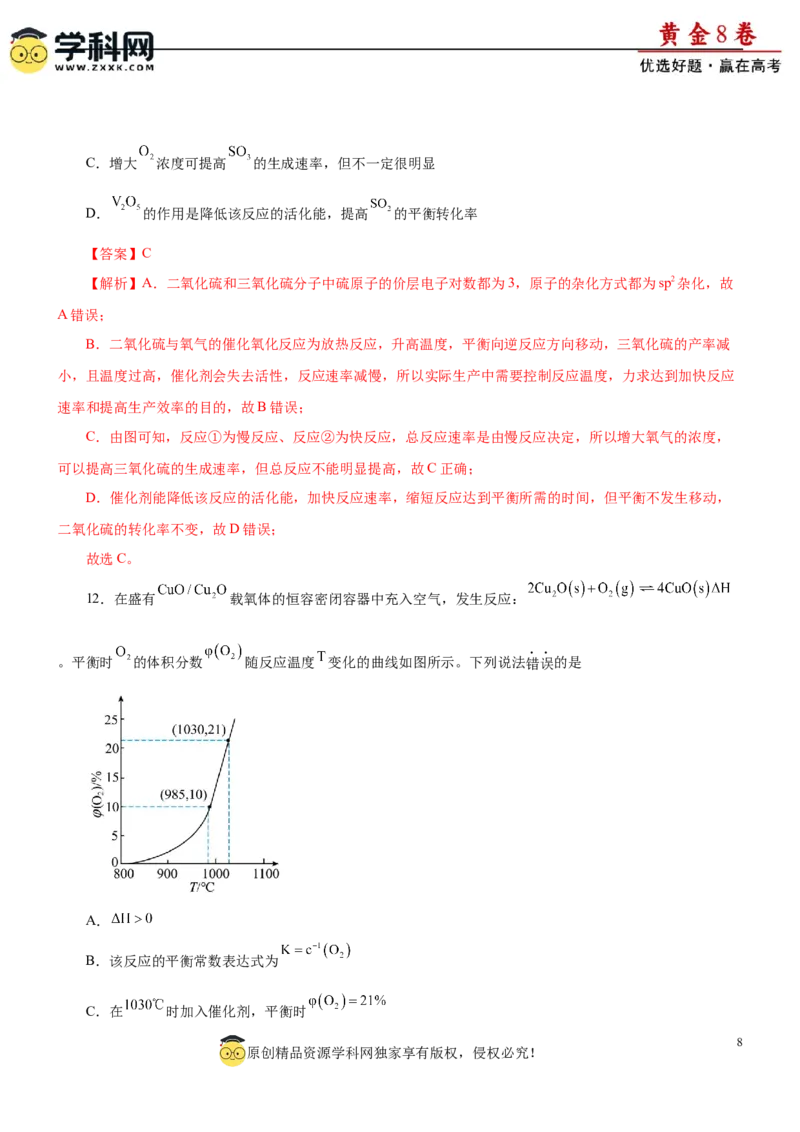
(4)某温度下,将一定量的 、投入一密闭容器中,检测到四种有机物的物质的量随时间的变化关系如
图乙所示。
在此温度下,如何更多的得到 。
a.延长反应时间
b.增大压强
c.使用选择性更高的催化剂
d反应初期生成较多 时,及时分离出(5) 时,在体积恒定的密闭容器中投入一定量的 ,假定只发生 过程, 足量,且反应过程中
氢气的浓度恒定为 ,当 的转化率为a时,反应的平衡常数为 。
【答案】(1)
(2)6
(3) 1-MD 低温高压 b
(4)cd
(5)
【解析】(1)由盖斯定律可知, ,则 ,故反应 的焓变
。
(2)根据1-MTL和5-MTL的结构及命名规律,可知, 的编号顺序为, ,
因此, 的名称为6-MTL
(3)①由图可知,温度升高,4个反应的平衡常数均减小,则所有的反应均为放热反应,根据能量越低越
稳定,1-MD的能量最低,则反应体系中1-MD最稳定
②反应为放热反应,且正向反应的气体分子数目减小,因此,利于生成MTLs的条件是低温高压
③由(1)可知 ,则 ,若c、d分别代表反应 、 的平衡常数随温度的变化,由
图可知 ,则 ,故表示反应R 的平衡常数随温度变化的曲线为b。
2
(4)a.由图可知,超过一定的时间后, 的量反而减小,错误;
18
原创精品资源学科网独家享有版权,侵权必究!b.生成 和 的反应均为气体分子数减小的反应,增大压强,副产物也会增加,错误;
c.使用选择性更高的催化剂,可以选择性的增加生成 的速率,利于 的生成,正确;
d反应初期生成较多 时,及时分离出 ,促使反应向生成 的方向进行,正确;
故选cd;
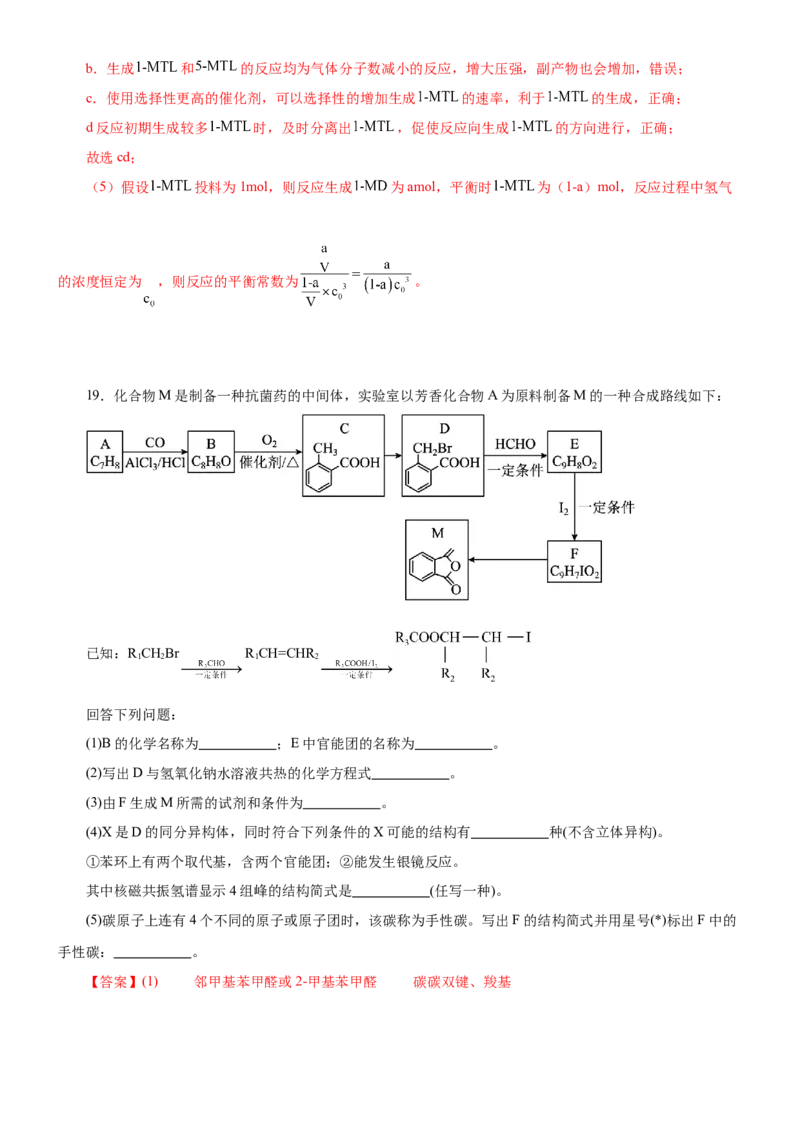
(5)假设 投料为1mol,则反应生成 为amol,平衡时 为(1-a)mol,反应过程中氢气
的浓度恒定为 ,则反应的平衡常数为 。
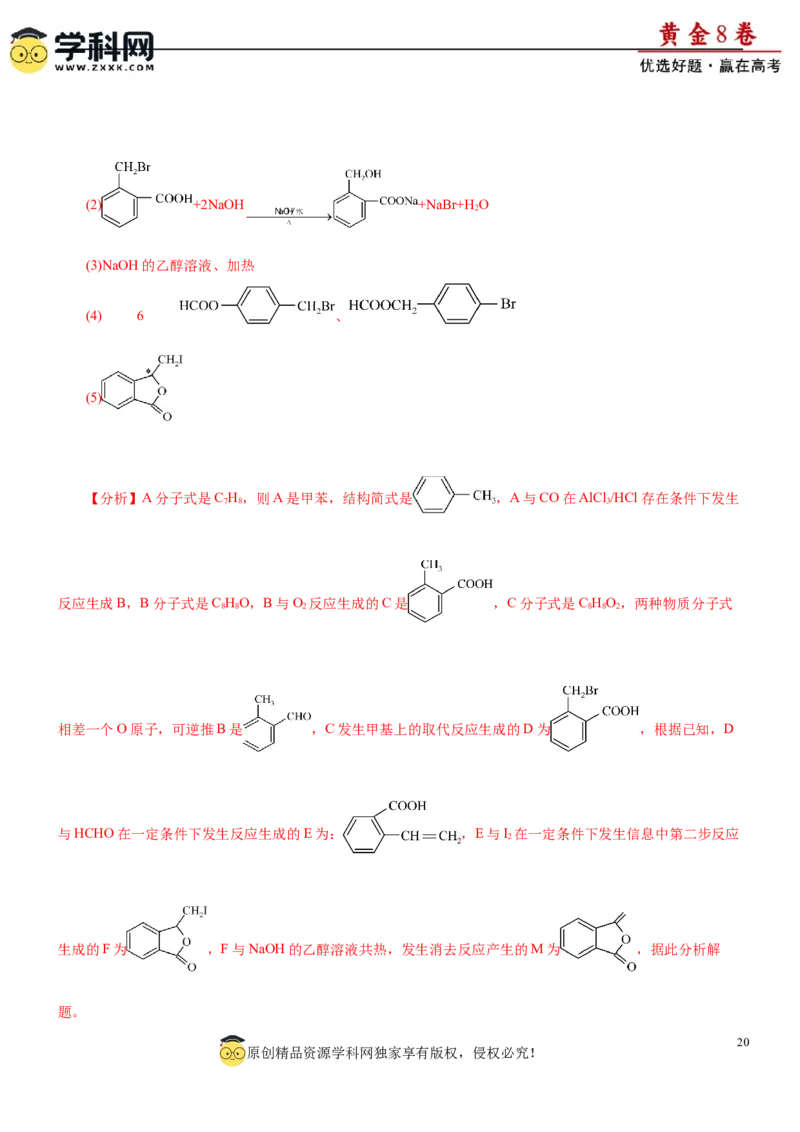
19.化合物M是制备一种抗菌药的中间体,实验室以芳香化合物A为原料制备M的一种合成路线如下:
已知:R CHBr R CH=CHR
1 2 1 2
回答下列问题:
(1)B的化学名称为 ;E中官能团的名称为 。
(2)写出D与氢氧化钠水溶液共热的化学方程式 。
(3)由F生成M所需的试剂和条件为 。
(4)X是D的同分异构体,同时符合下列条件的X可能的结构有 种(不含立体异构)。
①苯环上有两个取代基,含两个官能团;②能发生银镜反应。
其中核磁共振氢谱显示4组峰的结构简式是 (任写一种)。
(5)碳原子上连有4个不同的原子或原子团时,该碳称为手性碳。写出F的结构简式并用星号(*)标出F中的
手性碳: 。
【答案】(1) 邻甲基苯甲醛或2-甲基苯甲醛 碳碳双键、羧基(2) +2NaOH +NaBr+H O
2
(3)NaOH的乙醇溶液、加热
(4) 6 、
(5)
【分析】A分子式是C H,则A是甲苯,结构简式是 ,A与CO在AlCl /HCl存在条件下发生
7 8 3
反应生成B,B分子式是C HO,B与O 反应生成的C是 ,C分子式是C HO,两种物质分子式
8 8 2 8 8 2
相差一个O原子,可逆推B是 ,C发生甲基上的取代反应生成的D为 ,根据已知,D
与HCHO在一定条件下发生反应生成的E为: ,E与I 在一定条件下发生信息中第二步反应
2
生成的F为 ,F与NaOH的乙醇溶液共热,发生消去反应产生的M为 ,据此分析解
题。
20
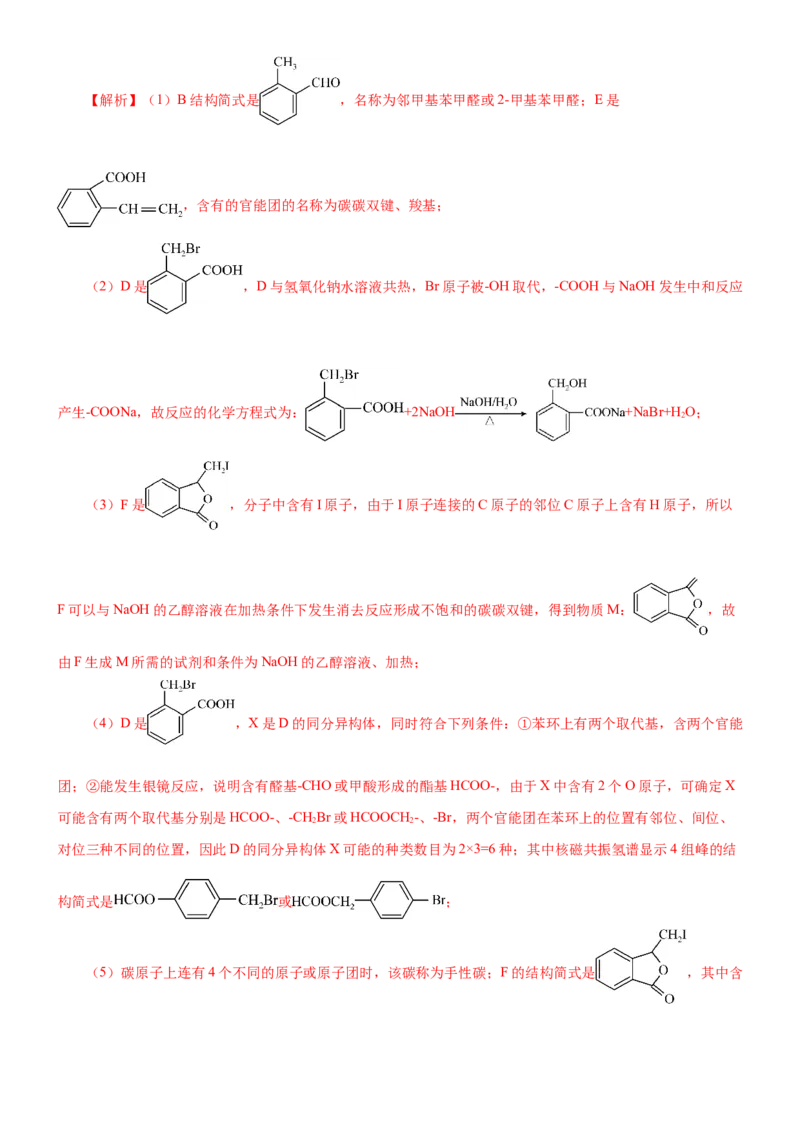
原创精品资源学科网独家享有版权,侵权必究!【解析】(1)B结构简式是 ,名称为邻甲基苯甲醛或2-甲基苯甲醛;E是
,含有的官能团的名称为碳碳双键、羧基;
(2)D是 ,D与氢氧化钠水溶液共热,Br原子被-OH取代,-COOH与NaOH发生中和反应
产生-COONa,故反应的化学方程式为: +2NaOH +NaBr+H O;
2
(3)F是 ,分子中含有I原子,由于I原子连接的C原子的邻位C原子上含有H原子,所以
F可以与NaOH的乙醇溶液在加热条件下发生消去反应形成不饱和的碳碳双键,得到物质M: ,故
由F生成M所需的试剂和条件为NaOH的乙醇溶液、加热;
(4)D是 ,X是D的同分异构体,同时符合下列条件:①苯环上有两个取代基,含两个官能
团;②能发生银镜反应,说明含有醛基-CHO或甲酸形成的酯基HCOO-,由于X中含有2个O原子,可确定X
可能含有两个取代基分别是HCOO-、-CHBr或HCOOCH -、-Br,两个官能团在苯环上的位置有邻位、间位、
2 2
对位三种不同的位置,因此D的同分异构体X可能的种类数目为2×3=6种;其中核磁共振氢谱显示4组峰的结
构简式是 或 ;
(5)碳原子上连有4个不同的原子或原子团时,该碳称为手性碳;F的结构简式是 ,其中含有的手性碳原子用星号(*)标出为: ;
22
原创精品资源学科网独家享有版权,侵权必究!