文档内容
牡丹江二中 2022-2023 学年度高三第二次阶段性测试
化 学
考生注意:
1. 本试卷分第 I 卷 (选择题)和第 II 卷(非选择题) 两部分。满分 100 分, 考试时间 90
分钟。
2. 答题前, 考生务必将密封线内项目填写清楚。考生作答时, 请将答案答在答题卡上。必
须在题号所指示的答题区域作答, 超出答题区域书写的答案无效,在试题卷、草稿 纸上作答无
效。
3. 本试卷主要命题范围: 必修第一册; 必修第二册第五章; 选择性必修 2 ; 选择性必修
3。
4.可能用到的相对原子质量:H1 C12 N14 O16 Na23 S32 C135.5
第 I 卷(选择题 共 42 分)
一、选择题(本题包括 14 小题,每小题 3 分,共 42 分。每小题只有一个选项符合题意)
1. 中国古文化源远流长, 留下不少脍多人口的古诗词, 不少古诗词清晰的描绘了我国古代
人民 的生活、生产场景, 下面的“诗”情“化”意, 分析不正确的是
A. “粉身碎骨浑不怕, 要留清白在人间”中涉及化学变化
B. “日照澄州江雾开”, 雾是一种气溶胶, 受阳光照射时会产生丁达尔现象
C. “美人首饰侯王印, 尽是沙中浪底来”, 说明金以单质的形式存在于自然界
D. “绿蚁新醅酒”, “新醅酒”即新酿的酒, 葡萄糖发生水解反应生成乙醇
2. 设 N 为阿伏加德罗常数的值。下列叙述不正确的是
A
A. 0.1mol 乙烯和乙醇的混合物完全燃烧所消耗 O 的分子数为 0.3N
2 A
B. 常温常压下, 46gNO 和 N O 的混合气体中含有的 N 原子数为 N
2 2 4 A
C. 1molHClO 中含有 H−Cl 键数为 N
AD. 46g 钠与氧气反应, 生成 Na O 和 Na O 的混合物, 转移电子数为 2N
2 2 2 A
3. 下列反应的离子方程式的书写正确的是
A. 稀硫酸和氢氧化钡溶液反应: Ba2++OH−+H++SO2−=BaSO ↓+H O
4 4 2
B. 铜和稀硝酸反应: Cu+4H++2NO−=Cu2++2H O+2NO ↑
3 2 2
C. 1L0.1mol⋅L−1FeI 溶液中通入标准状况下 2.24LCl :2Fe2++2I−+2Cl =I +
2 2 2 2
4Cl−+2Fe3+
D. 等体积、等浓度的 NaOH 稀溶液与 NH HCO 稀溶液混合: OH−+HCO−=CO2−+H O
4 3 3 3 2
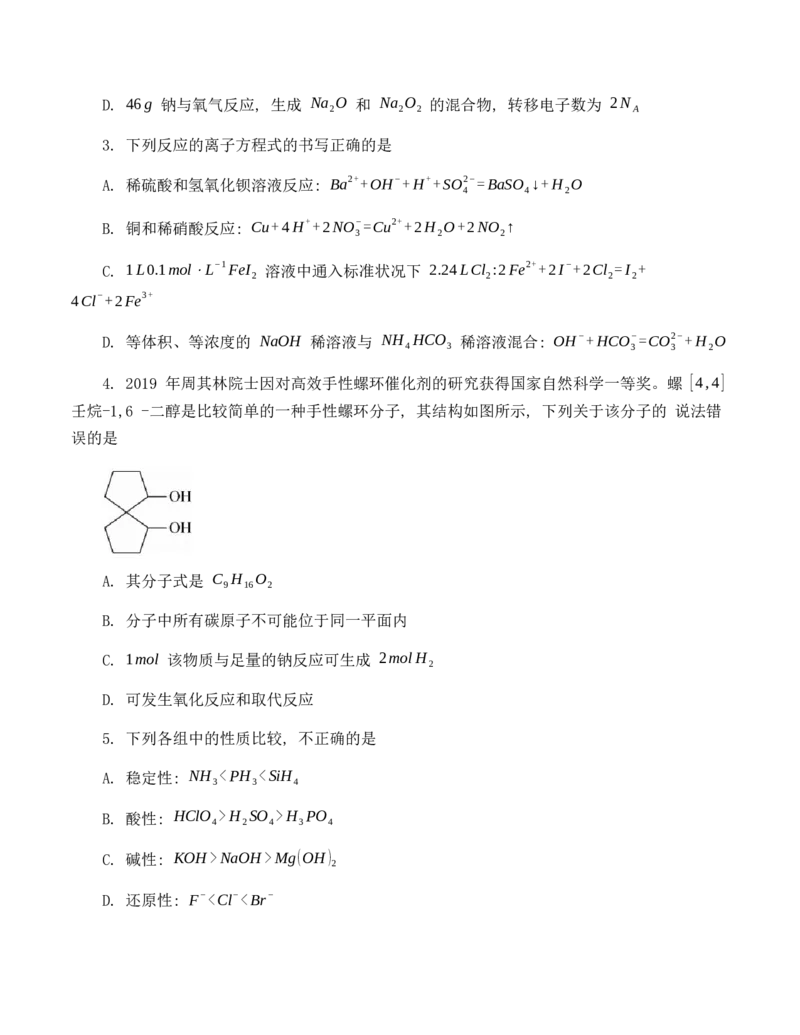
4. 2019 年周其林院士因对高效手性螺环催化剂的研究获得国家自然科学一等奖。螺 [4,4]
壬烷-1,6 -二醇是比较简单的一种手性螺环分子, 其结构如图所示, 下列关于该分子的 说法错
误的是
A. 其分子式是 C H O
9 16 2
B. 分子中所有碳原子不可能位于同一平面内
C. 1mol 该物质与足量的钠反应可生成 2molH
2
D. 可发生氧化反应和取代反应
5. 下列各组中的性质比较, 不正确的是
A. 稳定性: NH H SO >H PO
4 2 4 3 4
C. 碱性: KOH>NaOH>Mg(OH)
2
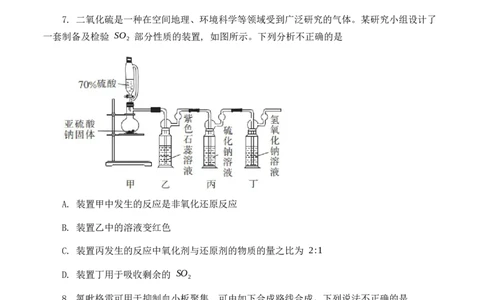
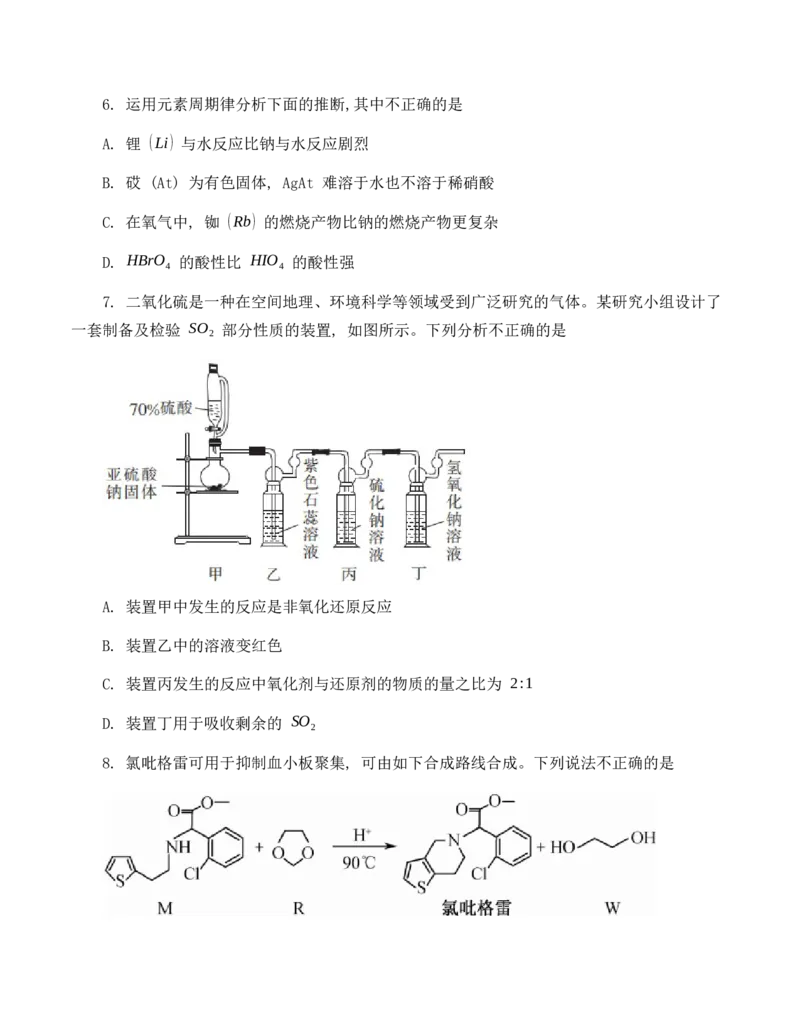
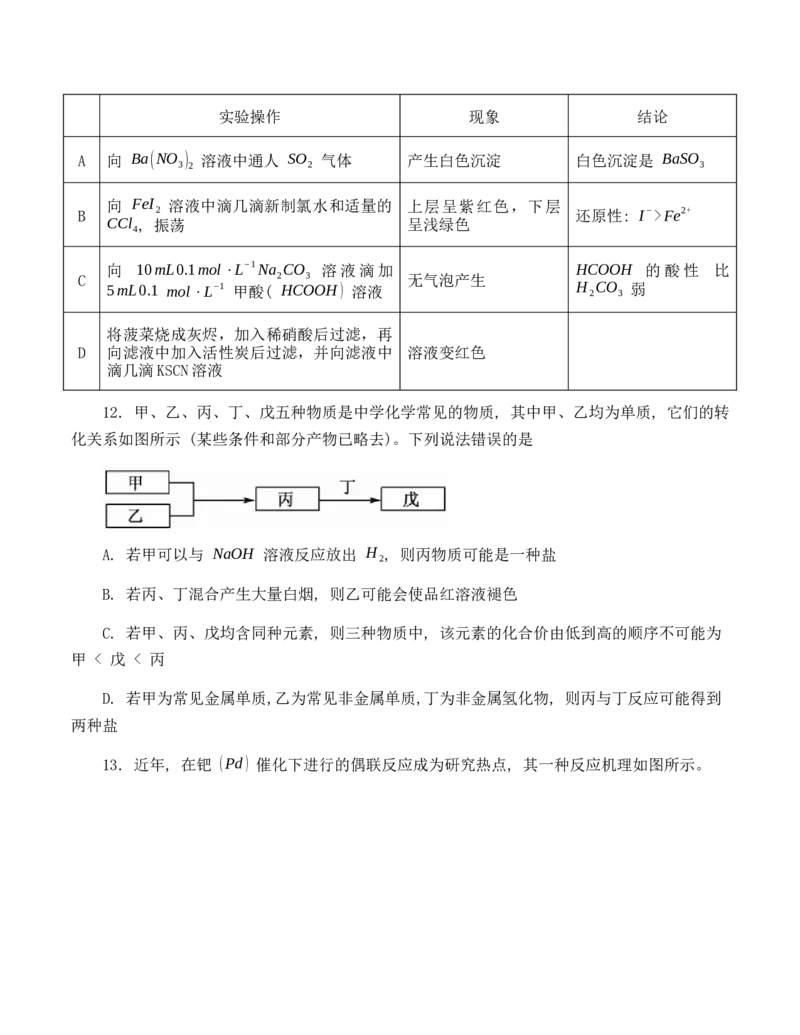
D. 还原性: F−X>W>Z
D. 该离子中 W、X、Y 都满足最外层 8 电子稳定结构
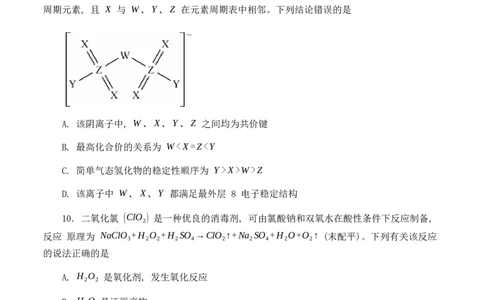
10. 二氧化氯 (ClO ) 是一种优良的消毒剂, 可由氯酸钠和双氧水在酸性条件下反应制备,
2
反应 原理为 NaClO +H O +H SO →ClO ↑+Na SO +H O+O ↑ (末配平)。下列有关该反应
3 2 2 2 4 2 2 4 2 2
的说法正确的是
A. H O 是氧化剂, 发生氧化反应
2 2
B. H O 是还原产物
2
C. 产物中 ClO 与 O 的物质的量之比为 1:2
2 2
D. 每转移 1mol 电子, 生成标准状况下 11.2LO
2
11. 下列实验操作, 现象和结论都正确且有相关性的是实验操作 现象 结论
A 向 Ba(NO ) 溶液中通人 SO 气体 产生白色沉淀 白色沉淀是 BaSO
3 2 2 3
向 FeI 溶液中滴几滴新制氯水和适量的 上层呈紫红色,下层
B 2 还原性: I−>Fe2+
CCl , 振荡 呈浅绿色
4
向 10mL0.1mol⋅L−1Na CO 溶液滴加 HCOOH 的酸性 比
C 2 3 无气泡产生
5mL0.1 mol⋅L−1 甲酸( HCOOH) 溶液 H
2
CO
3
弱
将菠菜烧成灰烬,加入稀硝酸后过滤,再
D 向滤液中加入活性炭后过滤,并向滤液中 溶液变红色
滴几滴KSCN溶液
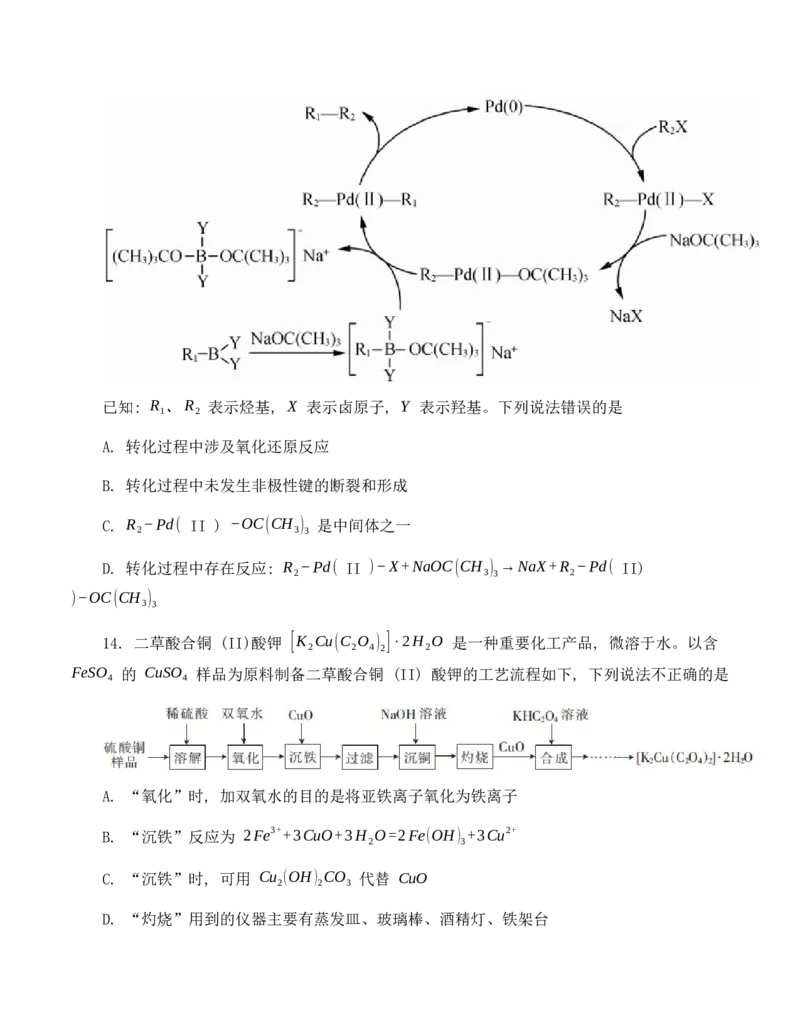
12. 甲、乙、丙、丁、戊五种物质是中学化学常见的物质, 其中甲、乙均为单质, 它们的转
化关系如图所示 (某些条件和部分产物已略去)。下列说法错误的是
A. 若甲可以与 NaOH 溶液反应放出 H , 则丙物质可能是一种盐
2
B. 若丙、丁混合产生大量白烟, 则乙可能会使品红溶液褪色
C. 若甲、丙、戊均含同种元素, 则三种物质中, 该元素的化合价由低到高的顺序不可能为
甲 < 戊 < 丙
D. 若甲为常见金属单质,乙为常见非金属单质,丁为非金属氢化物, 则丙与丁反应可能得到
两种盐
13. 近年, 在钯 (Pd) 催化下进行的偶联反应成为研究热点, 其一种反应机理如图所示。已知: R 、R 表示烃基, X 表示卤原子, Y 表示羟基。下列说法错误的是
1 2
A. 转化过程中涉及氧化还原反应
B. 转化过程中未发生非极性键的断裂和形成
C. R −Pd( II ) −OC(CH ) 是中间体之一
2 3 3
D. 转化过程中存在反应: R −Pd( II )−X+NaOC(CH ) →NaX+R −Pd( II)
2 3 3 2
)−OC(CH )
3 3
14. 二草酸合铜 (II)酸钾 [K Cu(C O ) ]⋅2H O 是一种重要化工产品, 微溶于水。以含
2 2 4 2 2
FeSO 的 CuSO 样品为原料制备二草酸合铜 (II) 酸钾的工艺流程如下, 下列说法不正确的是
4 4
A. “氧化”时, 加双氧水的目的是将亚铁离子氧化为铁离子
B. “沉铁”反应为 2Fe3++3CuO+3H O=2Fe(OH) +3Cu2+
2 3
C. “沉铁”时, 可用 Cu (OH) CO 代替 CuO
2 2 3
D. “灼烧”用到的仪器主要有蒸发皿、玻璃棒、酒精灯、铁架台第 II 卷(非选择题 共 58 分)
二、非选择题(本题包括 5 小题,共 58 分)
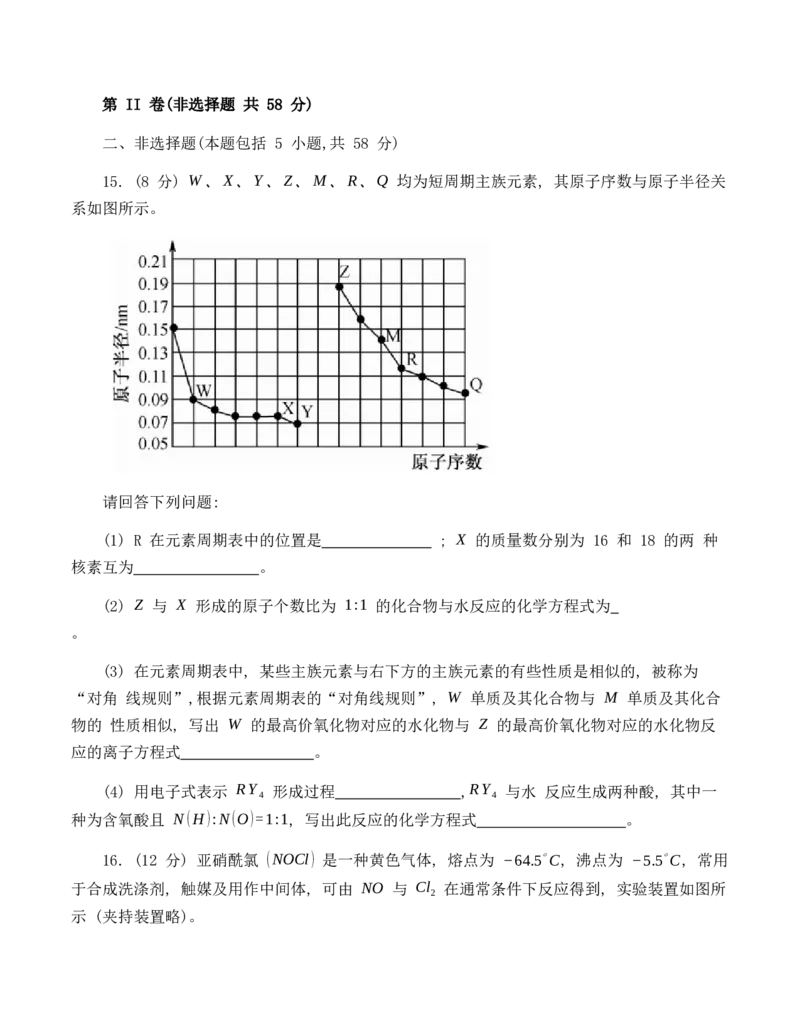
15. (8 分) W、X、Y、Z、M、R、Q 均为短周期主族元素, 其原子序数与原子半径关
系如图所示。
请回答下列问题:
(1) R 在元素周期表中的位置是 ; X 的质量数分别为 16 和 18 的两 种
核素互为 。
(2) Z 与 X 形成的原子个数比为 1:1 的化合物与水反应的化学方程式为
。
(3) 在元素周期表中, 某些主族元素与右下方的主族元素的有些性质是相似的, 被称为
“对角 线规则”,根据元素周期表的“对角线规则”, W 单质及其化合物与 M 单质及其化合
物的 性质相似, 写出 W 的最高价氧化物对应的水化物与 Z 的最高价氧化物对应的水化物反
应的离子方程式 。
(4) 用电子式表示 RY 形成过程 ,RY 与水 反应生成两种酸, 其中一
4 4
种为含氧酸且 N(H):N(O)=1:1, 写出此反应的化学方程式 。
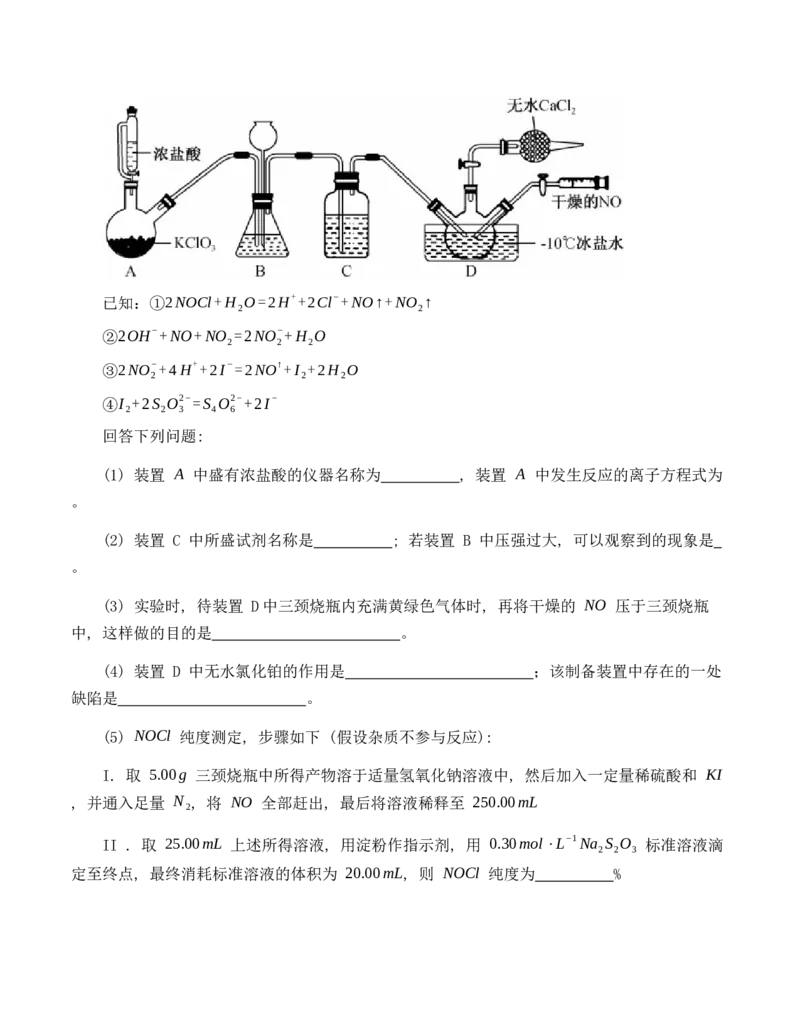
16. (12 分) 亚硝酰氯 (NOCl) 是一种黄色气体, 熔点为 −64.5∘C, 沸点为 −5.5∘C, 常用
于合成洗涤剂, 触媒及用作中间体, 可由 NO 与 Cl 在通常条件下反应得到, 实验装置如图所
2
示 (夹持装置略)。已知:①2NOCl+H O=2H++2Cl−+NO↑+NO ↑
2 2
②2OH−+NO+NO =2NO−+H O
2 2 2
③2NO−+4H++2I−=2NO↑+I +2H O
2 2 2
④I +2S O2−=S O2−+2I−
2 2 3 4 6
回答下列问题:
(1) 装置 A 中盛有浓盐酸的仪器名称为 , 装置 A 中发生反应的离子方程式为
。
(2) 装置 C 中所盛试剂名称是 ; 若装置 B 中压强过大, 可以观察到的现象是
。
(3) 实验时, 待装置 D中三颈烧瓶内充满黄绿色气体时, 再将干燥的 NO 压于三颈烧瓶
中, 这样做的目的是 。
(4) 装置 D 中无水氯化铂的作用是 ;该制备装置中存在的一处
缺陷是 。
(5) NOCl 纯度测定, 步骤如下 (假设杂质不参与反应):
I. 取 5.00g 三颈烧瓶中所得产物溶于适量氢氧化钠溶液中, 然后加入一定量稀硫酸和 KI
, 并通入足量 N , 将 NO 全部赶出, 最后将溶液稀释至 250.00mL
2
II . 取 25.00mL 上述所得溶液, 用淀粉作指示剂, 用 0.30mol⋅L−1Na S O 标准溶液滴
2 2 3
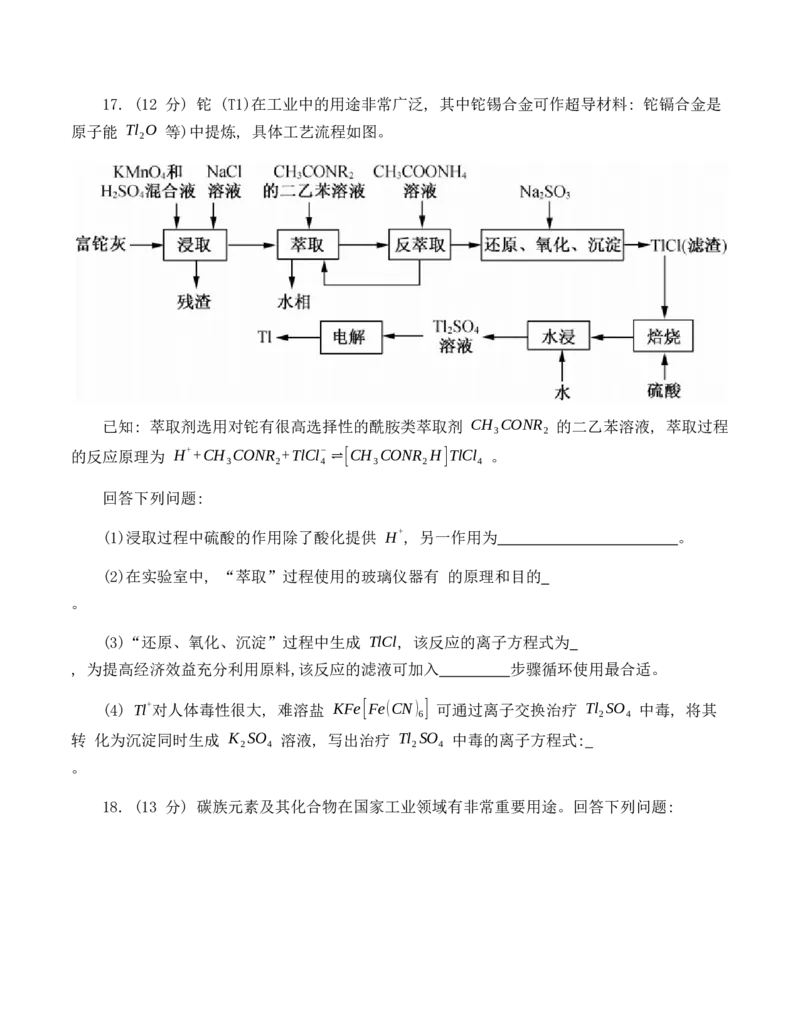
定至终点, 最终消耗标准溶液的体积为 20.00mL, 则 NOCl 纯度为 %17. (12 分) 铊 (T1)在工业中的用途非常广泛, 其中铊锡合金可作超导材料: 铊镉合金是
原子能 Tl O 等)中提炼, 具体工艺流程如图。
2
已知: 萃取剂选用对铊有很高选择性的酰胺类萃取剂 CH CONR 的二乙苯溶液, 萃取过程
3 2
的反应原理为 H++CH CONR +TlCl− ⇌[CH CONR H]TlCl 。
3 2 4 3 2 4
回答下列问题:
(1)浸取过程中硫酸的作用除了酸化提供 H+, 另一作用为 。
(2)在实验室中, “萃取”过程使用的玻璃仪器有 的原理和目的
。
(3)“还原、氧化、沉淀”过程中生成 TlCl, 该反应的离子方程式为
, 为提高经济效益充分利用原料,该反应的滤液可加入 步骤循环使用最合适。
(4) Tl+对人体毒性很大, 难溶盐 KFe[Fe(CN) ] 可通过离子交换治疗 Tl SO 中毒, 将其
6 2 4
转 化为沉淀同时生成 K SO 溶液, 写出治疗 Tl SO 中毒的离子方程式:
2 4 2 4
。
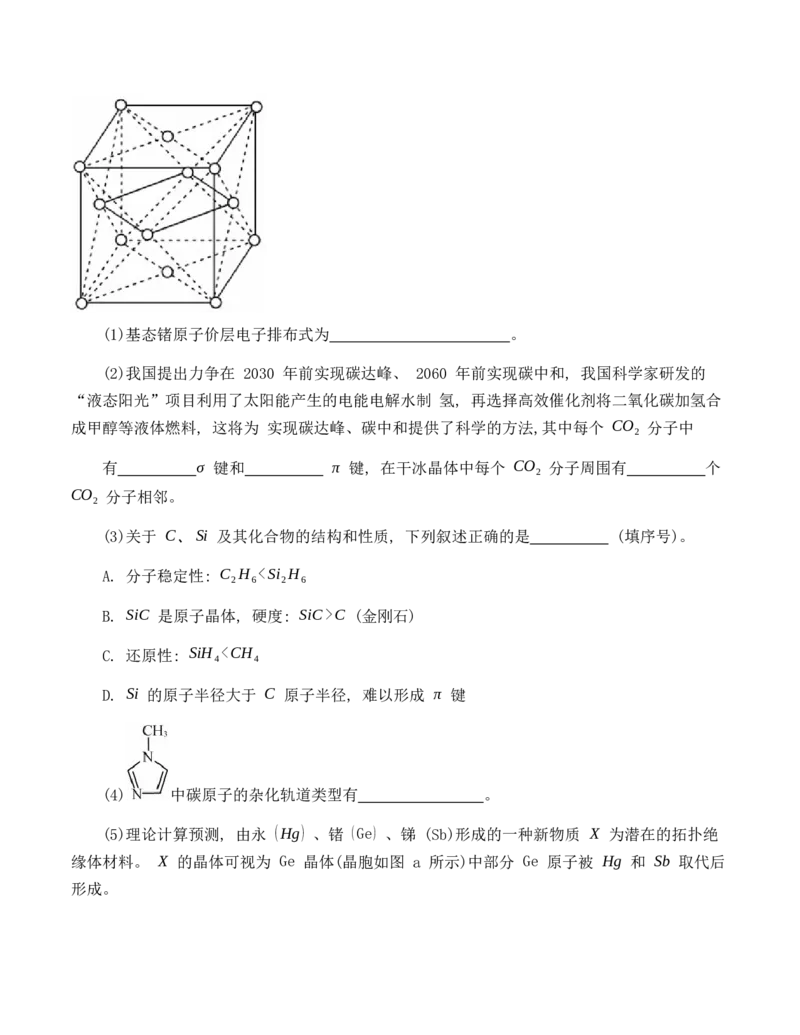
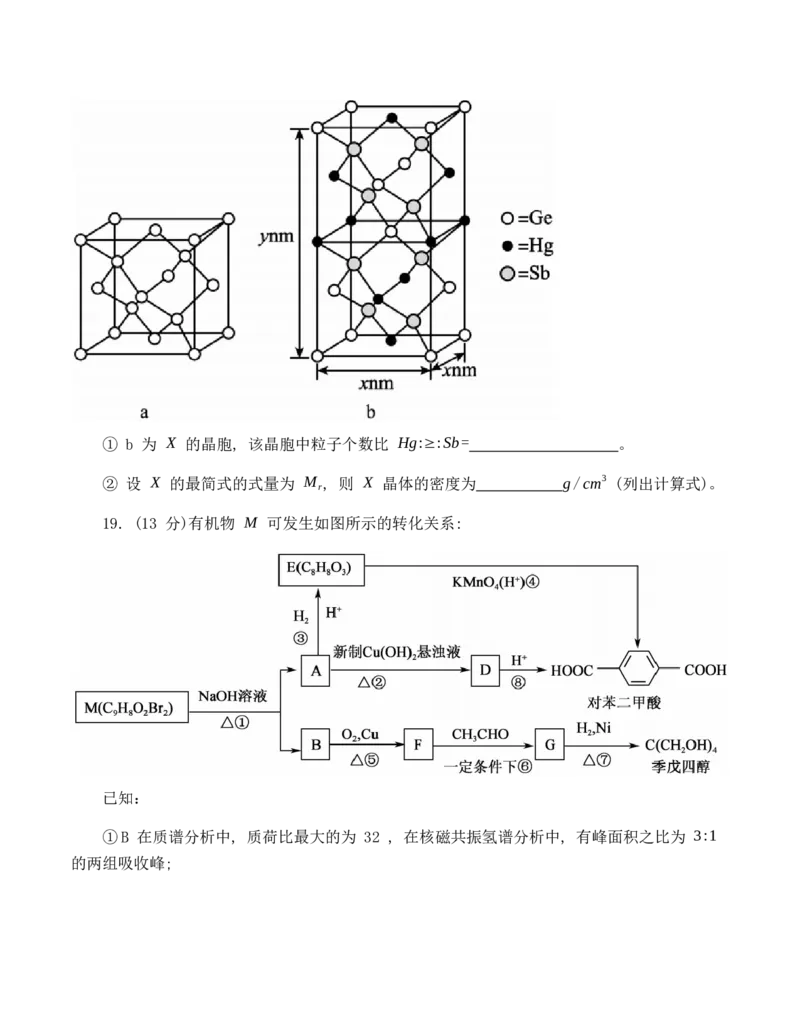
18. (13 分) 碳族元素及其化合物在国家工业领域有非常重要用途。回答下列问题:(1)基态锗原子价层电子排布式为 。
(2)我国提出力争在 2030 年前实现碳达峰、 2060 年前实现碳中和, 我国科学家研发的
“液态阳光”项目利用了太阳能产生的电能电解水制 氢, 再选择高效催化剂将二氧化碳加氢合
成甲醇等液体燃料, 这将为 实现碳达峰、碳中和提供了科学的方法,其中每个 CO 分子中
2
有 σ 键和 π 键, 在干冰晶体中每个 CO 分子周围有 个
2
CO 分子相邻。
2
(3)关于 C、Si 及其化合物的结构和性质, 下列叙述正确的是 (填序号)。
A. 分子稳定性: C H C (金刚石)
C. 还原性: SiH