文档内容
高三年级化学测试题
第Ⅰ卷(选择题,共42分)
可能用到的相对原子质量:(N:14;Al:27;Mn:55;O:16;Ge:70;
As:75)
本卷共14小题,每小题3分,每小题只有一项是最符合题目要求的。
1. 化学与生产、生活、社会发展息息相关,下列有关说法正确的是
A. 侯氏制碱法的工艺流程中应用了物质溶解度的差异
B. 5G技术中使用的光导纤维不与任何酸碱反应
C. 香云纱染整技艺中去除丝胶所用的纯碱水溶液属于纯净物
D. 我国古代“灌钢法”的原料之一赤铁矿的主要成分为FeO
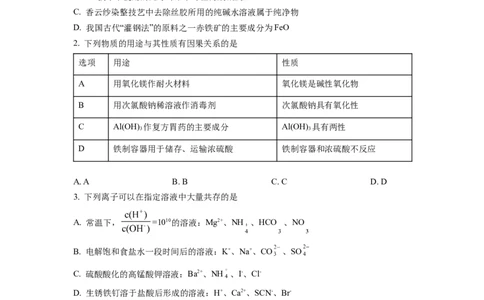
2. 下列物质的用途与其性质有因果关系的是
选项 用途 性质
A 用氧化镁作耐火材料 氧化镁是碱性氧化物
B 用次氯酸钠稀溶液作消毒剂 次氯酸钠具有氧化性
C Al(OH) 作复方胃药的主要成分 Al(OH) 具有两性
3 3
D 铁制容器用于储存、运输浓硫酸 铁制容器和浓硫酸不反应
A. A B. B C. C D. D
3. 下列离子可以在指定溶液中大量共存的是
A. 常温下, =1010的溶液:Mg2+、NH 、HCO 、NO
B. 电解饱和食盐水一段时间后的溶液:K+、Na+、CO 、SO
C. 硫酸酸化的高锰酸钾溶液:Ba2+、NH 、I-、Cl-
D. 生锈铁钉溶于盐酸后形成的溶液:H+、Ca2+、SCN-、Br-
4. 下列有关说法正确的是
①氟氯代烷化学性质稳定,排放到大气中不会对环境造成危害
②体积分数为75%的酒精可用来消毒
③苯酚有毒,所以日常所用的药皂中不可能掺入苯酚
④各种水果之所以有水果香味,是因为水果中含有酯类物质
⑤2,4,6-三硝基苯酚又叫TNT,是一种烈性炸药,可用于开矿
⑥乙醇结构中有-OH,所以乙醇溶解于水,可以电离OH-
⑦甲醛通常条件下是一种无色、有刺激性气味的气体,不溶于水⑧葡萄糖可用作热水瓶胆镀银的还原剂
⑨食醋中一般含有3%~5%的醋酸,可用去除水壶内的水垢
⑩乙醇可发生还原反应使橙红色的重铬酸钾溶液褪色
A. ①②④⑨ B. ②④⑧⑨ C. ②③⑦⑨ D.
⑤⑥⑨⑩
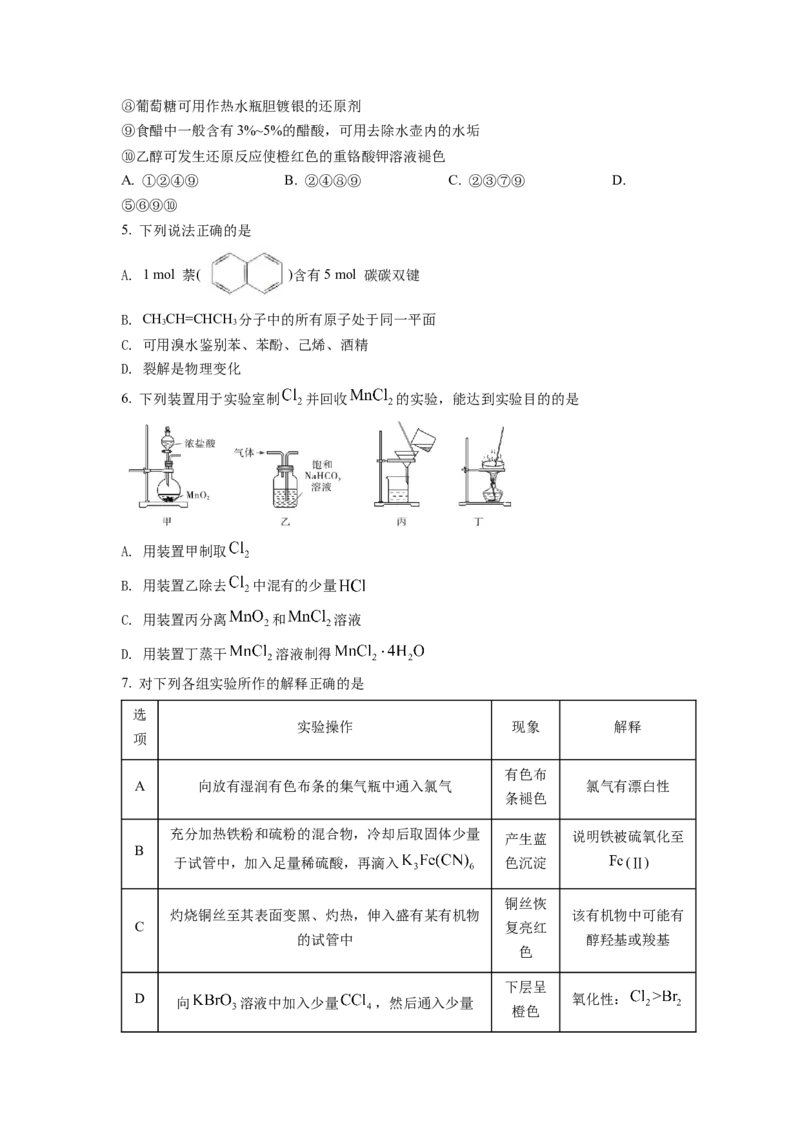
5. 下列说法正确的是
A. 1 mol 萘( )含有5 mol 碳碳双键
B. CHCH=CHCH 分子中的所有原子处于同一平面
3 3
C. 可用溴水鉴别苯、苯酚、己烯、酒精
D. 裂解是物理变化
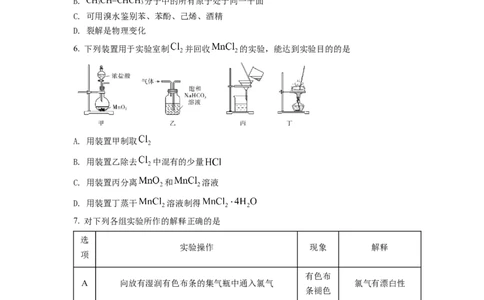
6. 下列装置用于实验室制 并回收 的实验,能达到实验目的的是
A. 用装置甲制取
B. 用装置乙除去 中混有的少量
C. 用装置丙分离 和 溶液
D. 用装置丁蒸干 溶液制得
7. 对下列各组实验所作的解释正确的是
选
实验操作 现象 解释
项
有色布
A 向放有湿润有色布条的集气瓶中通入氯气 氯气有漂白性
条褪色
充分加热铁粉和硫粉的混合物,冷却后取固体少量 产生蓝 说明铁被硫氧化至
B
于试管中,加入足量稀硫酸,再滴入 色沉淀 (Ⅱ)
铜丝恢
灼烧铜丝至其表面变黑、灼热,伸入盛有某有机物 该有机物中可能有
C 复亮红
的试管中 醇羟基或羧基
色
下层呈
D 向 溶液中加入少量 ,然后通入少量 氧化性:
橙色,充分振荡,静置
A. A B. B C. C D. D
8. 在给定条件下,下列所示物质间转化合理的是
A. Mg(OH) MgCl (aq) Mg
2 2
B. Cu CuSO Cu(NO )
4 3 2
C. 浓盐酸 Cl 漂白粉
2
D. FeO FeCl (aq) 无水FeCl
3 3
9. 下列说法不正确的是
A. 等体积等浓度的 与 溶液中的 数相等
B. 标准状况下,5.6L 中所含 键的数目为
C. 等质量的 与足量 在加热、常温下充分反应时转移的电子数相等
D. 等物质的量 和 (重水)所含的质子数相同
10. 下列说法不正确的是
A. 钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
B. 油脂、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应
C. 除去干燥 中混有的少量 ,可将混合气体依次通过盛有酸性 溶液、浓
硫酸的洗气瓶
D. “中和滴定”实验中,锥形瓶用蒸馏水洗涤后即可使用,滴定管用蒸馏水洗涤后,需经润
洗方可使用
11. 工业上用某种氧化铝矿石(含Fe O 杂质)为原料冶炼铝的工艺流程如下:
2 3
对上述流程的判断正确的是
A. 试剂X可以为氨水,沉淀中含有铁的化合物
B. CO 可以用HSO 溶液或稀盐酸代替
2 2 4
C. 反应Ⅱ中的离子方程式为CO+ +2HO=Al(OH) ↓+
2 2 3
D. 工业上还可采用Fe还原Al O 的方法制Al,成本更低
2 3
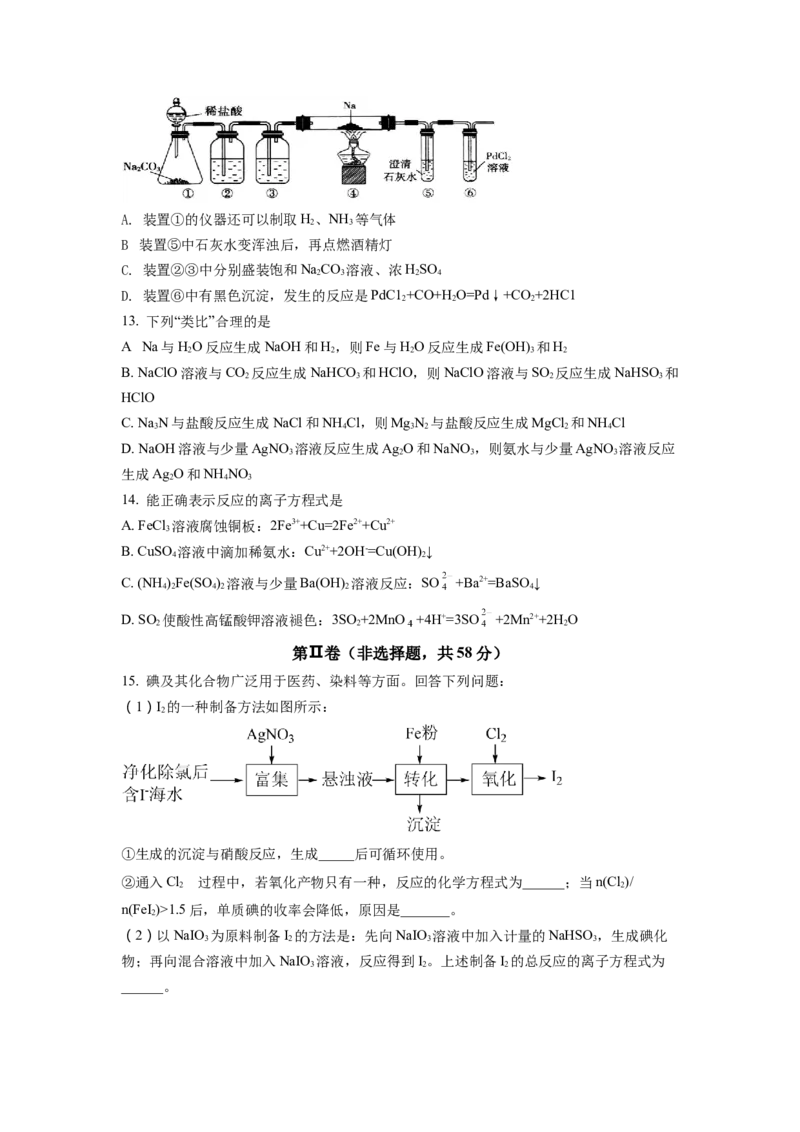
12. 实验室验证钠能与二氧化碳发生反应,并确定其产物的装置如图所示(已知:PdC1 溶
2
液遇CO能产生黑色的Pd),下列说法错误的是A. 装置①的仪器还可以制取H、NH 等气体
. 2 3
B 装置⑤中石灰水变浑浊后,再点燃酒精灯
C. 装置②③中分别盛装饱和NaCO 溶液、浓HSO
2 3 2 4
D. 装置⑥中有黑色沉淀,发生的反应是PdC1 +CO+H O=Pd↓+CO +2HC1
2 2 2
13. 下列“类比”合理的是
.
A Na与HO反应生成NaOH和H,则Fe与HO反应生成Fe(OH) 和H
2 2 2 3 2
B. NaClO溶液与CO 反应生成NaHCO 和HClO,则NaClO溶液与SO 反应生成NaHSO 和
2 3 2 3
HClO
C. Na N与盐酸反应生成NaCl和NH Cl,则MgN 与盐酸反应生成MgCl 和NH Cl
3 4 3 2 2 4
D. NaOH溶液与少量AgNO 溶液反应生成Ag O和NaNO ,则氨水与少量AgNO 溶液反应
3 2 3 3
生成Ag O和NH NO
2 4 3
14. 能正确表示反应的离子方程式是
A. FeCl 溶液腐蚀铜板:2Fe3++Cu=2Fe2++Cu2+
3
B. CuSO 溶液中滴加稀氨水:Cu2++2OH-=Cu(OH) ↓
4 2
C. (NH )Fe(SO ) 溶液与少量Ba(OH) 溶液反应:SO +Ba2+=BaSO ↓
4 2 4 2 2 4
D. SO 使酸性高锰酸钾溶液褪色:3SO +2MnO +4H+=3SO +2Mn2++2H O
2 2 2
第Ⅱ卷(非选择题,共58分)
15. 碘及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I 的一种制备方法如图所示:
2
①生成的沉淀与硝酸反应,生成_____后可循环使用。
②通入Cl 的过程中,若氧化产物只有一种,反应的化学方程式为______;当n(Cl )/
2 2
n(FeI )>1.5后,单质碘的收率会降低,原因是_______。
2
(2)以NaIO 为原料制备I 的方法是:先向NaIO 溶液中加入计量的NaHSO,生成碘化
3 2 3 3
物;再向混合溶液中加入NaIO 溶液,反应得到I。上述制备I 的总反应的离子方程式为
3 2 2
______。(3)I 在KI溶液中可发生反应: 。实验室中使用过量的KI与CuSO 溶液
2 4
反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是_______。
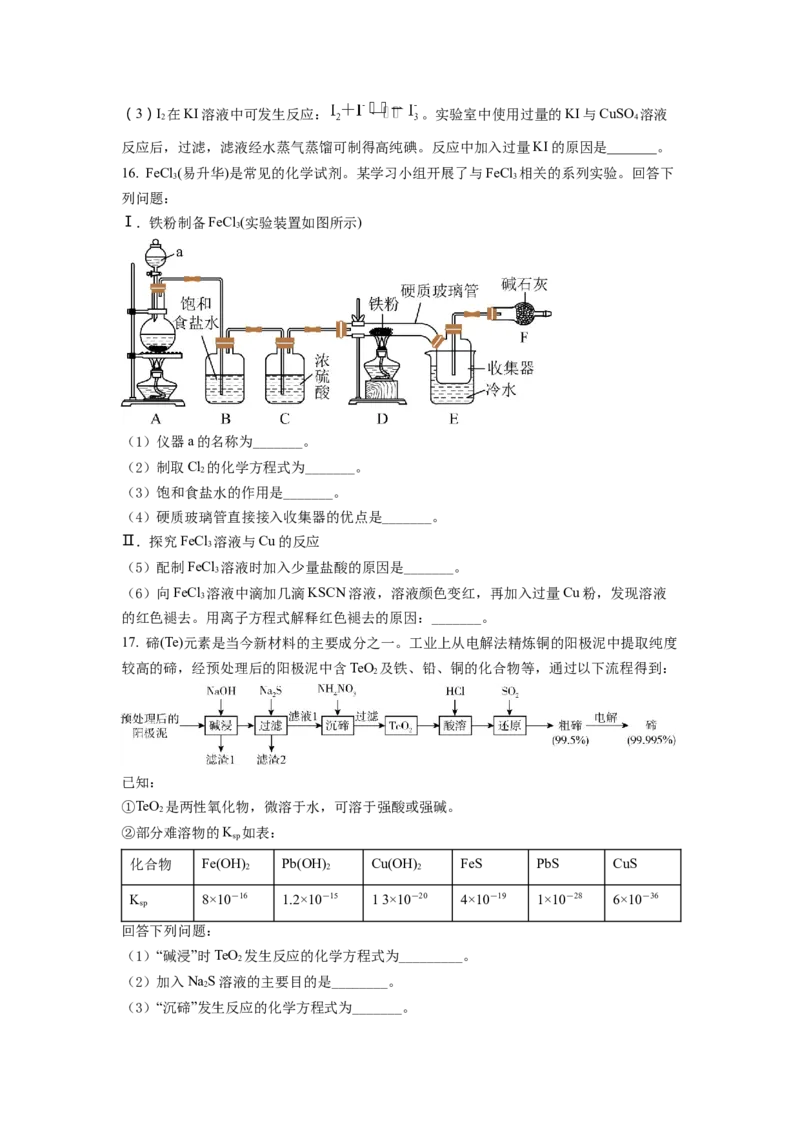
16. FeCl (易升华)是常见的化学试剂。某学习小组开展了与FeCl 相关的系列实验。回答下
3 3
列问题:
Ⅰ.铁粉制备FeCl (实验装置如图所示)
3
(1)仪器a的名称为_______。
(2)制取Cl 的化学方程式为_______。
2
(3)饱和食盐水的作用是_______。
(4)硬质玻璃管直接接入收集器的优点是_______。
Ⅱ.探究FeCl 溶液与Cu的反应
3
(5)配制FeCl 溶液时加入少量盐酸的原因是_______。
3
(6)向FeCl 溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液
3
的红色褪去。用离子方程式解释红色褪去的原因:_______。
17. 碲(Te)元素是当今新材料的主要成分之一。工业上从电解法精炼铜的阳极泥中提取纯度
较高的碲,经预处理后的阳极泥中含TeO 及铁、铅、铜的化合物等,通过以下流程得到:
2
已知:
①TeO 是两性氧化物,微溶于水,可溶于强酸或强碱。
2
②部分难溶物的K 如表:
sp
化合物 Fe(OH) Pb(OH) Cu(OH) FeS PbS CuS
2 2 2
.
K 8×10-16 1.2×10-15 13×10-20 4×10-19 1×10-28 6×10-36
sp
回答下列问题:
(1)“碱浸”时TeO 发生反应的化学方程式为_________。
2
(2)加入NaS溶液的主要目的是________。
2
(3)“沉碲”发生反应的化学方程式为_______。(4)电解法提纯粗碲时,以NaTeO 溶液为电解质溶液,阳极材料为_______。
2 3
(5)常温下,向0.lmol/LNa TeO 溶液中滴加盐酸,当溶液pH=5时,溶液中 :
2 3
c(HTeO ) =________。(已知:HTeO 的K =1.0×10-3K =2.0×10-8)
2 3 2 3 a1 a2
18. 按要求填空。
(1) 的化学名称是________。
(2)写出肉桂醛( )与银氨溶液反应的化学方程式________。
(3)1mol有机物 最多与______molNaOH反应;要把它转化为
,可加入_______(填化学式)。
(4)利用乙醇经过下列步骤可制得常见的溶剂1,4—二氧六环 。
①步骤Ⅰ的反应条件为______。
②步骤Ⅲ的化学方程式_____。
(5)已知: +ROH ,则 与乙二醇
在该条件下发生反应生成的有机物的结构简式为_______(键线式表示)。
19. GaN是研制微电子器件、光电子器件 的第三代半导体材料。
(1)基态Ga的核外电子排布为 ,转化为下列激发态时所需能量最少的是
_______(填标号)。
A. B.C. D.
(2)与家同主族的B具有缺电子性,硼氢化钠( )是有机合成中重要的还原剂,其
阴离子 的立体构型为_______。另一种含硼的阴离子 的结构如图所
示,其中B原子的杂化方式为_______。
(3)GaN、GaP、GaAs熔融状态均不导电,据此判断它们是_______(填“共价”或“离子”)化
合物,它们的晶体结构与金刚石相似,其熔点如下表所示,试分析GaN、CaP、GaAs熔点
依次降低的原因:_______。
物质 GaN CaP GaAs
熔点/℃ 1700 1480 1238
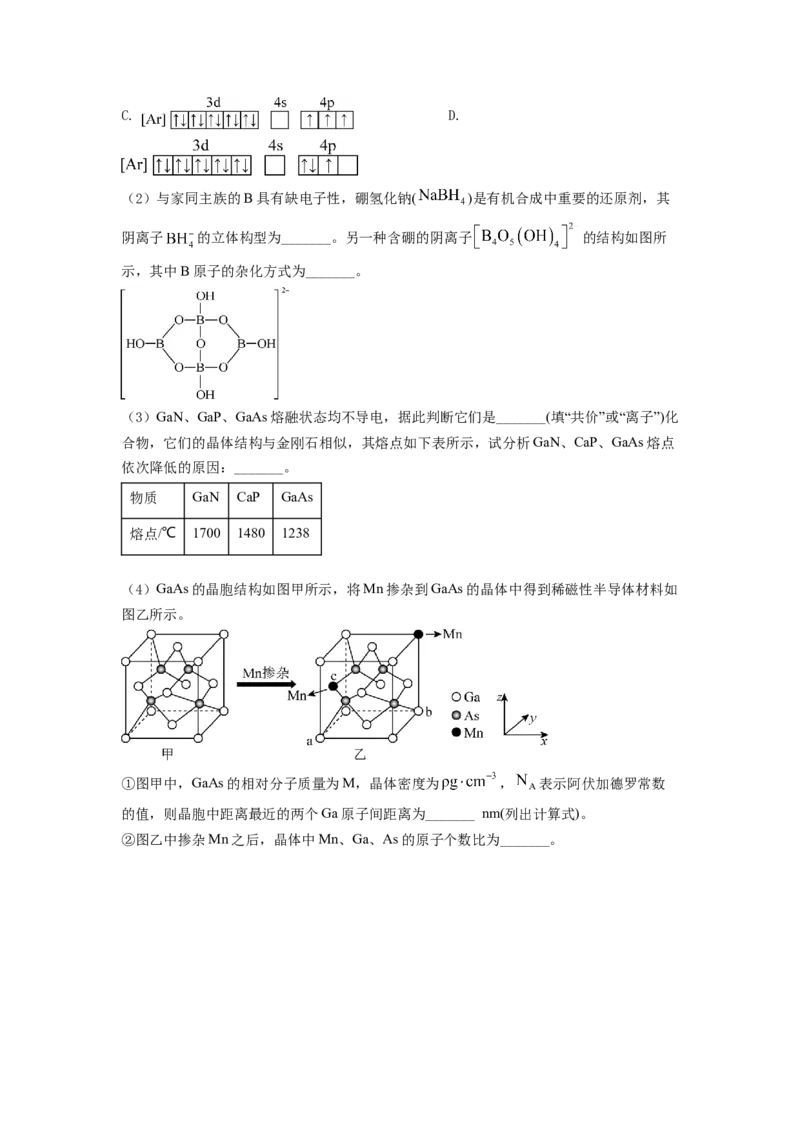
(4)GaAs的晶胞结构如图甲所示,将Mn掺杂到GaAs的晶体中得到稀磁性半导体材料如
图乙所示。
①图甲中,GaAs的相对分子质量为M,晶体密度为 , 表示阿伏加德罗常数
的值,则晶胞中距离最近的两个Ga原子间距离为_______ nm(列出计算式)。
②图乙中掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为_______。