文档内容
原子结构与元素周期表
【学习目标与素养】
1.微观探析:认识原子结构。了解原子核外电子的排布。
2.宏观辨识与微观探析:能够正确书写 1~20号元素的原子结构示意图。知道元素、核
素的含义。认识原子结构以及元素在元素周期表中位置的关系。知道元素周期表的结构。体
会元素周期表在学习元素及其化合物知识及科学研究中的重要作用。通过碱金属、卤素原子
的结构特点,认识原子结构与元素性质的关系。
3.变化观念:能初步运用原子结构理论解释碱金属、卤素性质的相似性和递变性。
【学习重难点】
了解原子核外的电子排布;知道元素周期表的结构;知道元素、核素、同位素的含义。
认识碱金属元素、卤族元素的性质与其在元素周期表中位置的关系;以碱金属元素和卤
族元素为例,了解同主族元素性质的递变规律。
【学习过程】
【第一课时】
(一)基础知识填充
一、原子的构成
1.构成
(1)原子
(2)关系:原子序数=核电荷数=质子数=核外电子数(电中性原子中)。
2.质量数
(1)概念:质子和中子的相对质量都近似为1,忽略电子的质量,将原子核内所有质子
和中子的相对质量取近似整数值相加,所得的数值叫作质量数。
(2)关系:质量数(A)= 质子数( Z ) + 中子数( N ) 。
二、核外电子排布
1.电子层
(1)概念:在多电子原子里,把电子运动的能量不同的区域简化为不连续的壳层,称作
电子层。
(2)不同电子层的表示及能量关系
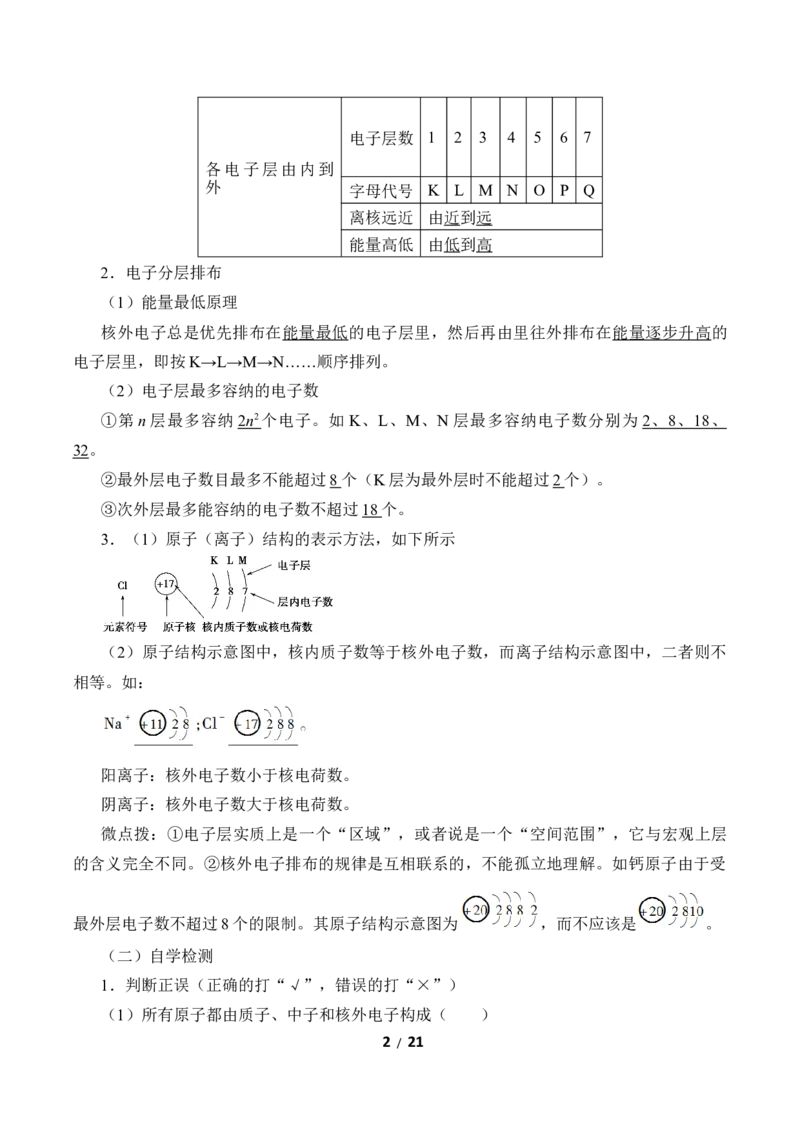
1 / 21电子层数 1 2 3 4 5 6 7
各电子层由内到
外 字母代号 K L M N O P Q
离核远近 由近到远
能量高低 由低到高
2.电子分层排布
(1)能量最低原理
核外电子总是优先排布在能量最低的电子层里,然后再由里往外排布在能量逐步升高的
电子层里,即按K→L→M→N……顺序排列。
(2)电子层最多容纳的电子数
①第n层最多容纳 2 n 2 个电子。如 K、L、M、N层最多容纳电子数分别为 2 、 8 、 18 、
32。
②最外层电子数目最多不能超过8 个(K层为最外层时不能超过2 个)。
③次外层最多能容纳的电子数不超过18 个。
3.(1)原子(离子)结构的表示方法,如下所示
(2)原子结构示意图中,核内质子数等于核外电子数,而离子结构示意图中,二者则不
相等。如:
阳离子:核外电子数小于核电荷数。
阴离子:核外电子数大于核电荷数。
微点拨:①电子层实质上是一个“区域”,或者说是一个“空间范围”,它与宏观上层
的含义完全不同。②核外电子排布的规律是互相联系的,不能孤立地理解。如钙原子由于受
最外层电子数不超过8个的限制。其原子结构示意图为 ,而不应该是 。
(二)自学检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)所有原子都由质子、中子和核外电子构成( )
2 / 21(2)某种氯原子的中子数是18,则其质量数是35,核外电子数是17。( )
(3)锂的原子结构示意图是 。( )
(4)某原子M层电子数为L层电子数的4倍。( )
答案:(1)×(2)√(3)×(4)×
2.下列各原子结构示意图中所表示的核外电子排布正确的是( )
答案:C
解析:A项不符合能量最低原理,应该先排满 K层再排L层;B项不符合各层最多排 2n2
个电子,K层最多排2个电子;D项不符合最外层最多只能排8个电子。
3.(1)A元素原子的核电荷数为8,其原子核内的质子数为______,该元素原子的二价
阴离子中,核外电子数为______。
(2)B元素原子的一价阳离子的核外有 18个电子,质量数为 40,该元素原子的原子核
内中子数为________。
解析:(1)核电荷数=质子数,阴离子的核外电子数=质子数+所带电荷数=10。
(2)B元素质子数是18+1=19,质量数为40,该元素原子的中子数为40-19=21。
答案:(1)8;10
(2)21
(三)重难点突破
重难点1:原子核外电子排布规律的应用
1.确定元素的种类
根据原子核外电子排布的某些特点可以确定元素的种类,注意1~20号元素原子结构的
特殊关系。
特殊关系 元素
最外层电子数等于次外层电子数的一半 Li、Si
最外层电子数等于次外层电子数 Be、Ar
最外层电子数等于次外层电子数的2倍 C
最外层电子数等于次外层电子数的3倍 O
最外层电子数等于次外层电子数的4倍 Ne
最外层电子数等于电子层数 H、Be、Al
最外层有1个电子 H、Li、Na、K
3 / 21最外层有2个电子 He、Be、Mg、Ca
内层电子数之和是最外层电子数2倍的元素 Li、P
电子总数为最外层电子数2倍的元素 Be
2.推断元素的性质
最外层电子
元素 得失电子能力 化学性质 主要化合价
数
稀 有 气 体 8 ( He 为 一般不易得失 较稳定,一般不参与化
-
元素 2) 电子 学反应
只有正价,一般是+
金属元素 <4 易失电子 金属性
1→+3
非 金 属 元
≥4 易得电子 非金属性 既有正价又有负价
素
特别提醒:通常把最外层有8个电子(K层为最外层时电子数是2个)的结构,称为相对
稳定结构。稀有气体的原子就是上述结构,一般不与其他物质发生化学反应。当元素的原子
最外层电子数小于8(K层小于2)时是不稳定结构。在化学反应中,不稳定结构总是通过各
种方式如得失电子、共用电子等趋向达到相对稳定结构。
重难点2:“10电子”“18电子”的等电子粒子
1.利用元素排布寻找“10电子”微粒的方法
2.利用元素排布寻找“18电子”微粒的方法
3.与OH-具有相同质子数和电子数的粒子是( )
A.H O
2
B.F-
C.Na+
D.NH
3
答案:B
解析:OH-具有9个质子,10个电子;H O具有10个质子,10个电子;F-具有9个质子,
2
10个电子;Na+具有11个质子,10个电子;NH 具有10个质子,10个电子。
3
4 / 214.用A+、B-、C2-、D、E、F和G分别表示含有18个电子的七种微粒(离子或分子),
请回答:
(1)A元素是________,B元素是________,C元素是________(用元素符号表示)。
(2)D是由两种元素组成的双原子分子,其分子式是________。
解析:常见的18e-微粒有:阳离子:K+、Ca2+;阴离子:P3-、S2-、HS-、Cl-;分子有
Ar、HCl、H S、PH 、SiH 、F 、H O 等。结合题目所给条件可确定答案。
2 3 4 2 2 2
答案:(1)K;Cl;S
(2)HCl
【第二课时】
(一)基础知识填充
一、元素周期表的编排原则
1.元素周期表的出现与演变
2.原子序数
(1)含义:按照元素在周期表中的顺序给元素的编号。
(2)原子序数与原子结构的关系:
原子序数=核电荷数=质子数=核外电子数。
二、元素周期表的结构
1.编排原则
5 / 212.元素周期表的结构
3.常见族的别称
族 别名
第 Ⅰ A 族 ( 除 氢
碱金属元素
外)
第ⅦA 卤族元素
0族 稀有气体元素
4.元素周期表中的方格中的符号的意义
思考:(1)元素周期表中所含元素种类最多的族是哪一族?
提示:ⅢB族。
(2)最外层电子数是2的元素都是第ⅡA族吗?
提示:不一定,0族的He原子最外层也是两个电子。
三、核素
1.核素
把具有一定数目质子和一定数目中子的一种原子叫做核素。如 12C、13C、14C就是碳元素
的三种不同核素。
2.同位素
(1)定义:质子数相同而中子数不同的同一元素的不同原子互称为同位素。即同一元素
的不同核素之间互为同位素,如三种核素均是氢元素的同位素。
6 / 21(2)实例——氢元素的同位素:1H、2H、3H
氢元素的原子核 原子
原子名称
质子数(Z) 中子数(N) 符号(X)
1 0 氕 H
1 1 氘 H或D
1 2 氚 H或T
(3)同位素的特征
①同一种元素的各种同位素的化学性质几乎完全相同;物理性质略有差异。
②在天然存在的某种元素里,不论是游离态还是化合态,同位素相互之间保持一定的比
率,即各种同位素所占的原子个数百分比是相同的。
(4)同位素的用途
①C在考古工作中用于测定文物的年代。
②H、H用于制造氢弹。
③利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病等。
思考:(1)C与N的质量数相等,是否互为同位素?
提示:质子数相同,中子数不同的同一元素的不同原子互称为同位素。C与N的质量数
相等,但质子数分别为6和7,属于不同的元素,故不是同位素。
(2)核素种类与质子数、中子数和质量数有何关系?
提示:核素是具有一定数目质子和一定数目中子的一种原子,因此核素种类由质子数、
中子数共同决定。质量数=质子数+中子数,故不同的核素也可能具有相同的质量数,如 C
和N,故核素种类与质量数无直接关系。
(3)结合核外电子排布讨论:互称同位素的不同核素为什么具有几乎完全相同的化学性
质?
提示:同种元素的不同核素核内质子数相同,具有完全相同的核外电子排布,因此化学
性质几乎完全相同。
(二)自学检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)现行元素周期表的编排依据是相对原子质量( )
(2)一个横行即是一个周期,一个纵列即是一个族( )
(3)最外层电子数相同的元素一定是同族元素( )
(4)每一周期都是碱金属元素开始,稀有气体元素结束( )
答案:(1)×(2)×(3)×(4)×
2.下列有关钯原子(Pd)的说法错误的是( )
7 / 21A.原子序数为46
B.质子数为46
C.电子数为46
D.中子数为46
答案:D
解析:由Pd可知,钯的原子序数为46,核外电子数=原子序数=质子数=46;核内中子
数为106-46=60,D选项错误。
3.在Li、N、Na、Mg、Li、C中:
(1)________和________互为同位素。
(2)________和________质量数相等,但不能互称同位素。
(3)________和________的中子数相等,但质子数不相等,所以不是同一种元素。
解析:质子数相同,中子数不同的同一元素的不同原子互称为同位素,故 Li与Li互为同
位素;N与C质量数相等,但因质子数不同,不能互称同位素;Na和Mg的中子数均是12,
但质子数不相等,所以不是同一种元素。
答案:(1)Li;Li
(2)N;C
(3)Na;Mg
(三)重难点突破
重难点1:认识元素周期表
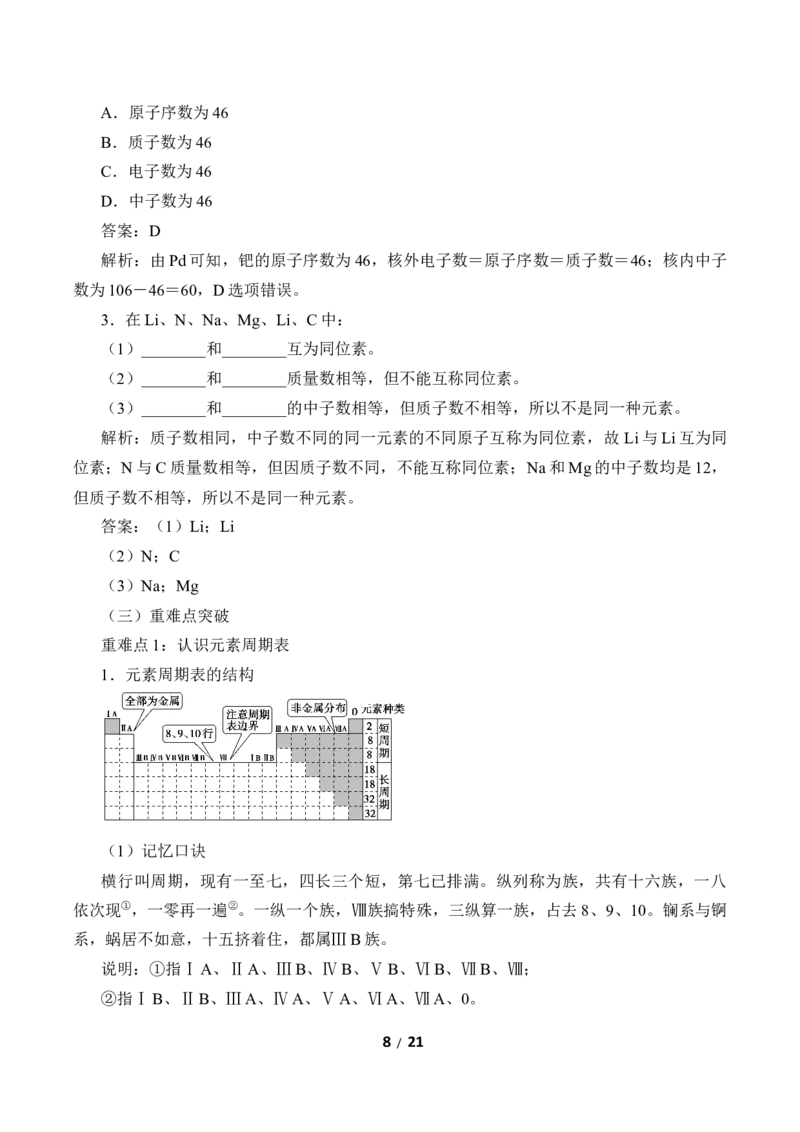
1.元素周期表的结构
(1)记忆口诀
横行叫周期,现有一至七,四长三个短,第七已排满。纵列称为族,共有十六族,一八
依次现①,一零再一遍②。一纵一个族,Ⅷ族搞特殊,三纵算一族,占去8、9、10。镧系与锕
系,蜗居不如意,十五挤着住,都属ⅢB族。
说明:①指ⅠA、ⅡA、ⅢB、ⅣB、ⅤB、ⅥB、ⅦB、Ⅷ;
②指ⅠB、ⅡB、ⅢA、ⅣA、ⅤA、ⅥA、ⅦA、0。
8 / 21(2)列序数与族序数的关系
①列序数<8,主族和副族的族序数=列序数;
②列序数=8或9或10,为第Ⅷ族;
③列序数>10,主族和副族的族序数=列序数-10(0族除外)。
(3)过渡元素
元素周期表中从ⅢB到ⅡB共10个纵列,包括了第Ⅷ族和全部副族元素,共60多种元
素,全部为金属元素,统称为过渡元素。
2.元素原子序数差的确定方法
(1)同周期第ⅡA族和第ⅢA族元素原子序数差
(2)同主族相邻两元素原子序数的差的情况
①若为ⅠA、ⅡA族元素,则原子序数的差等于上周期元素所在周期的元素种类数。
②若为ⅢA族至0族元素,则原子序数的差等于下周期元素所在周期的元素种类数。
典例:1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的
内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是( )
A.元素周期表含元素最多的族是第ⅢB族
B.元素周期表有18个族
C.第ⅠA族的元素全部是金属元素
D.短周期是指第一、二、三、四周期
答案:A
解析:第ⅢB族中包含锕系与镧系元素,共有32种元素,A项正确;元素周期表中共有
18个纵列,16个族,B项错误;第ⅠA族中H为非金属元素,C项错误;短周期包括第一、
二、三周期,D项错误。
重难点2:元素、核素、同位素、同素异形体的区别和联系
1.区别
名称
内容 元素 核素 同位素 同素异形体
项目
本质 质子数相同的一 质子数、中子数 质子数相同、中 同种元素形成的
9 / 21类原子的总称 都一定的原子 子数不同的核素 不同单质
范畴 同类原子 原子 原子 单质
只有种类,没有 化学反应中的最 化学性质几乎完 元素相同、性质
特性
个数 小微粒 全相同 不同
决定因素 质子数 质子数、中子数 质子数、中子数 组成元素、结构
H、C、O三种 H、H、H三种 H、H、H互称 O 与O 互为同
举例 2 3
元素 核素 同位素 素异形体
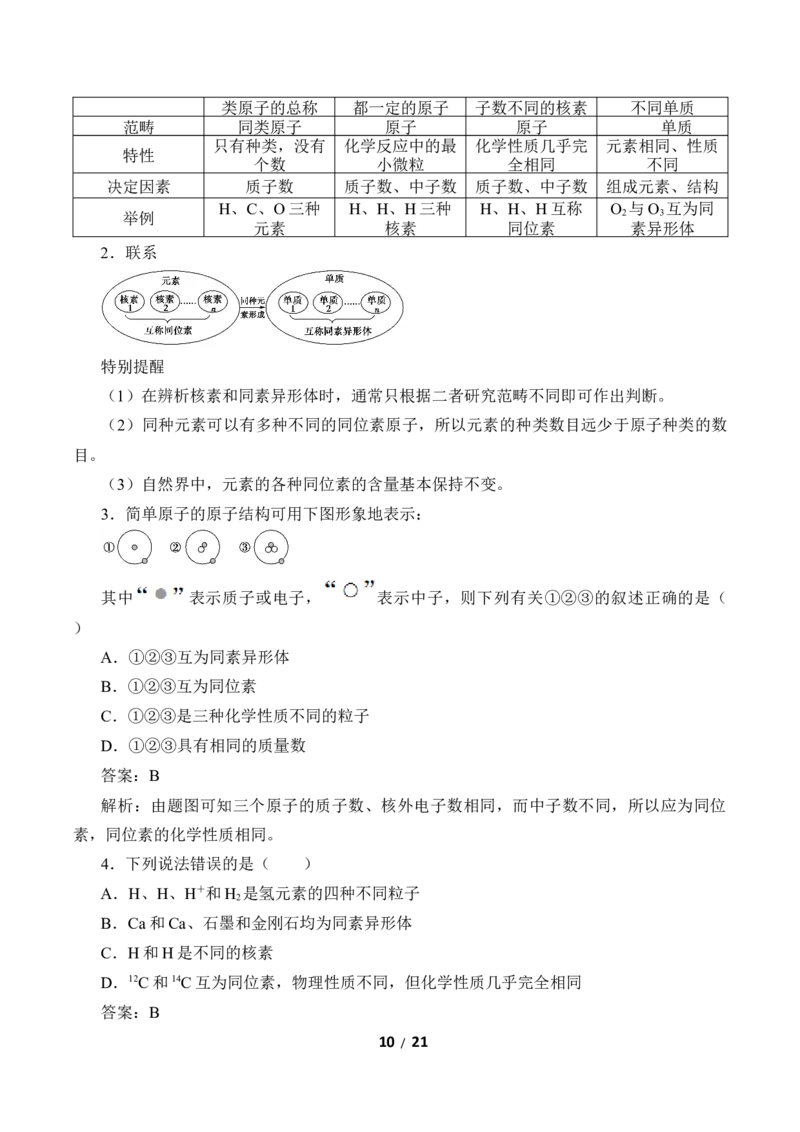
2.联系
特别提醒
(1)在辨析核素和同素异形体时,通常只根据二者研究范畴不同即可作出判断。
(2)同种元素可以有多种不同的同位素原子,所以元素的种类数目远少于原子种类的数
目。
(3)自然界中,元素的各种同位素的含量基本保持不变。
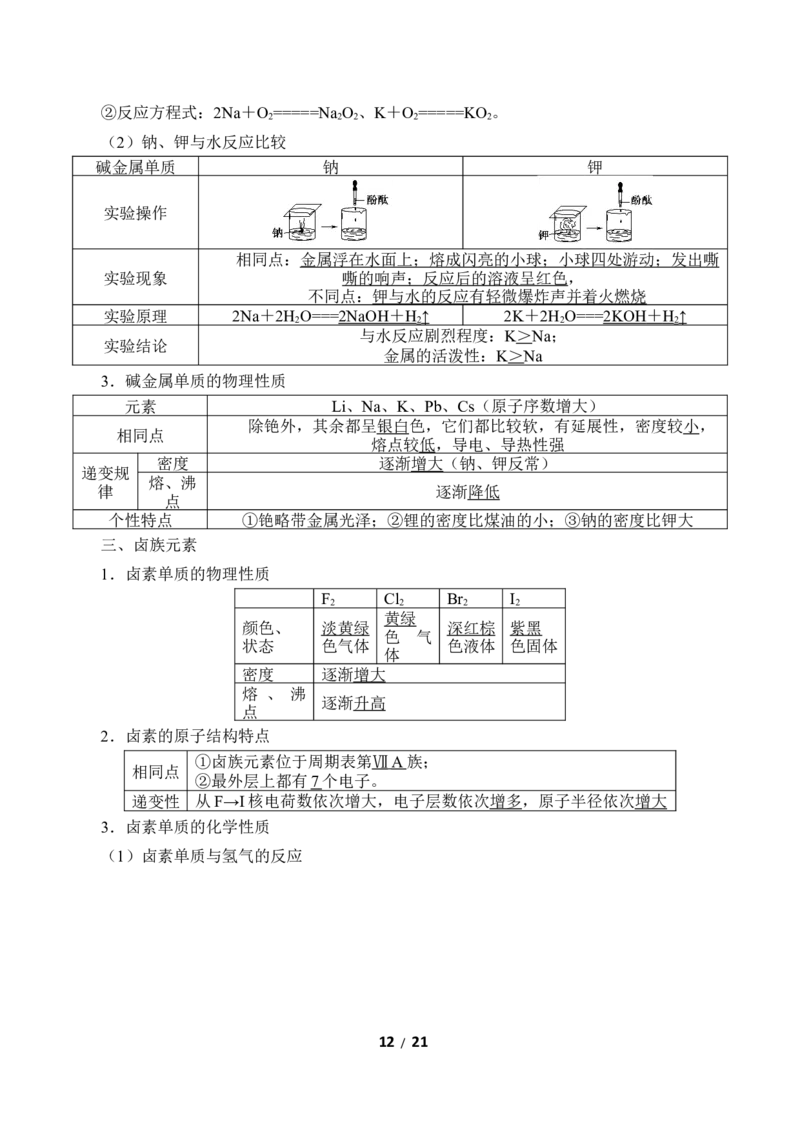
3.简单原子的原子结构可用下图形象地表示:
其中 表示质子或电子, 表示中子,则下列有关①②③的叙述正确的是(
)
A.①②③互为同素异形体
B.①②③互为同位素
C.①②③是三种化学性质不同的粒子
D.①②③具有相同的质量数
答案:B
解析:由题图可知三个原子的质子数、核外电子数相同,而中子数不同,所以应为同位
素,同位素的化学性质相同。
4.下列说法错误的是( )
A.H、H、H+和H 是氢元素的四种不同粒子
2
B.Ca和Ca、石墨和金刚石均为同素异形体
C.H和H是不同的核素
D.12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同
答案:B
10 / 21解析:元素的存在形式有游离态和化合态两种,A项中的四种微粒是氢元素的四种不同
粒子,H和H是质子数均为1,中子数不等的不同的氢原子,它们是不同的核素;12C和14C
由于其质子数均为6,而中子数分别为6和8,故它们互为同位素,同理,Ca和Ca互为同位
素其物理性质不同但化学性质几乎完全相同;金刚石与石墨是由碳元素组成的不同的单质,
它们互为同素异形体。
【第三课时】
(一)基础知识填充
一、原子结构与元素性质的关系
1.金属元素:原子最外层电子一般少于4 个,在化学反应中容易失去电子,具有金属性。
2.非金属元素:原子最外层电子一般多于 4 个,在化学反应中容易得到电子,具有非金
属性。
二、碱金属元素
1.碱金属元素的原子结构
元素名 元素符 核电荷 最外层电 电子层 原子 半径 /
原子结构示意图
称 号 数 子数 数 nm
锂 Li 3 1 2 0.152
钠 Na 11 1 3 0.186
碱 金 属
钾 K 19 1 4 0.227
元素
铷 Rb 37 1 5 0.248
铯 Cs 55 1 6 0.265
结论:碱金属元素原子结构的共同点是 最外层电子数均为 1,不同点是电子层数和原子
半径不同,其变化规律是随着核电荷数的增加,电子层数逐渐增多,原子半径逐渐增大
2.碱金属单质的化学性质
(1)钠、钾与氧气反应比较
①实验现象:都能在空气中燃烧,钠产生黄色火焰(透过蓝色钴玻璃观察),钾产生紫
色火焰,钾燃烧更剧烈。
11 / 21②反应方程式:2Na+O =====Na O 、K+O =====KO 。
2 2 2 2 2
(2)钠、钾与水反应比较
碱金属单质 钠 钾
实验操作
相同点:金属浮在水面上;熔成闪亮的小球;小球四处游动;发出嘶
实验现象 嘶的响声;反应后的溶液呈红色,
不同点:钾与水的反应有轻微爆炸声并着火燃烧
实验原理 2Na+2H O=== 2NaOH + H ↑ 2K+2H O=== 2KOH + H ↑
2 2 2 2
与水反应剧烈程度:K>Na;
实验结论
金属的活泼性:K>Na
3.碱金属单质的物理性质
元素 Li、Na、K、Pb、Cs(原子序数增大)
除铯外,其余都呈银白色,它们都比较软,有延展性,密度较小,
相同点
熔点较低,导电、导热性强
密度 逐渐增大(钠、钾反常)
递变规
熔、沸
律 逐渐降低
点
个性特点 ①铯略带金属光泽;②锂的密度比煤油的小;③钠的密度比钾大
三、卤族元素
1.卤素单质的物理性质
F Cl Br I
2 2 2 2
黄绿
颜色、 淡黄绿 深红棕 紫黑
色 气
状态 色气体 色液体 色固体
体
密度 逐渐增大
熔 、 沸
逐渐升高
点
2.卤素的原子结构特点
①卤族元素位于周期表第 Ⅶ A 族;
相同点
②最外层上都有7 个电子。
递变性 从F→I核电荷数依次增大,电子层数依次增多,原子半径依次增大
3.卤素单质的化学性质
(1)卤素单质与氢气的反应
12 / 21(2)卤素单质之间的置换反应
实验操作 实验现象 化学方程式
静置后,液体分层,上层接近无色,下层呈 Cl + 2NaBr===2NaCl +
2
橙红色 Br
2
静置后,液体分层,上层接近无色,下层呈
Cl + 2KI===2KC l + I
紫红色 2 2
静置后,液体分层,上层接近无色,下层呈
Br + 2KI===2KB r + I
紫红色 2 2
结论 Cl →I 氧化性逐渐减弱,相应卤素离子还原性逐渐增强
2 2
点拨:因为F 能与H O发生反应(2F +2H O===4HF+O ),所以F 不能从其他卤化物
2 2 2 2 2 2
的盐溶液中置换出卤素单质。
13 / 21(二)自学检测
1.判断正误(正确的打“√”,错误的打“×”)
(1)碱金属元素即ⅠA元素( )
(2)K比Na活泼,故K可以从钠盐溶液中置换出Na( )
(3)卤素单质与水反应均可用X +H O===HXO+HX表示( )
2 2
(4)HX都极易溶于水,它们的热稳定性随核电荷数增加而增强( )
答案:(1)×(2)×(3)×(4)×
2.下列金属与水反应最剧烈的是( )
A.Li
B.K
C.Rb
D.Cs
答案:D
解析:在碱金属中,随着元素原子电子层数的增多,碱金属的金属活动性增强,四个选
项中与水反应最剧烈的应是Cs。
3.铯单质与水剧烈反应,放出________色气体,向溶液中滴入紫色石蕊溶液,显
________色,因为_________________(写出化学方程式)。
答案:无;蓝;2Cs+2H O===2CsOH+H ↑
2 2
(三)重难点突破
重难点1:碱金属元素性质的相似性和递变性
1.相似性(R表示碱金属元素)
原子都容易失去最外层的一个电子,化学性质活泼,它们的单质都具有较强的还原性,
它们都能与氧气等非金属单质及水反应。碱金属与水反应的通式为 2R+2H O===2ROH+
2
H ↑。
2
2.递变性
随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,碱金
属元素的原子失电子能力逐渐增强,金属性逐渐增强。
(1)
(2)与O 的反应越来越剧烈,产物更加复杂,如Li与O 反应只能生成Li O,Na与O
2 2 2 2
反应还可以生成Na O ,而K与O 反应能够生成KO 等。
2 2 2 2
14 / 21(3)与H O的反应越来越剧烈,如K与H O反应可能会发生轻微爆炸,Rb与Cs遇水发
2 2
生剧烈爆炸。
(4)最高价氧化物对应水化物的碱性逐渐增强,CsOH的碱性最强。
典例:下列各组比较不正确的是( )
A.锂与水反应不如钠与水反应剧烈
B.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠
C.熔、沸点:Li>Na>K
D.碱性:LiOH<NaOH<KOH
答案:B
解析:A中锂的活泼性比钠弱,与水反应不如钠剧烈;B中还原性,K>Na>Li,但K不
能置换出NaCl溶液中的Na,而是先与H O反应;C中碱金属元素从Li到Cs,熔、沸点逐渐
2
降低,即Li>Na>K>Rb>Cs;D中从Li到Cs,碱金属元素的金属性逐渐增强,对应最高
价氧化物的水化物的碱性依次增强,即碱性:LiOH<NaOH<KOH<RbOH<CsOH。
思考:(1)碱金属单质的化学性质为什么具有相似性?
提示:结构决定性质,碱金属元素的原子结构相似,最外层均有一个电子,均易失电子,
化学性质活泼,故他们的单质具有较强的还原性,能与氧气等非金属及水、酸反应。
(2)碱金属单质的化学性质为什么具有递变性?
提示:碱金属原子结构存在递变性。从Li到Cs,随核电荷数的增加,电子层数逐渐增多,
原子半径逐渐增大,原子核对最外层电子的引力逐渐减弱,元素金属性逐渐增强;故单质的
还原性逐渐增强,离子的氧化性逐渐减弱。
重难点2:卤素的原子结构与化学性质的关系
1.相似性(X表示卤素元素)
卤素原子都容易得到一个电子使其最外层达到8个电子的稳定结构,它们的单质都是活
泼的非金属单质,都具有较强的氧化性。
(1)与H 反应:X +H ========2HX。
2 2 2
(2)与活泼金属(如Na)反应:2Na+X =====2NaX。
2
(3)与H O反应
2
①X +H O===HX+HXO(X=Cl、Br、I);
2 2
②2F +2H O===4HF+O 。
2 2 2
(4)与NaOH溶液反应
X +2NaOH===NaX+NaXO+H O(X=Cl、Br、I)。
2 2
15 / 212.递变性(X表示卤素元素)
随着原子序数的递增,原子半径逐渐增大,原子核对最外层电子的引力逐渐减小,卤素
原子得电子的能力逐渐减弱,非金属性逐渐减弱。
(1)
(2)与H 反应越来越难,对应氢化物的稳定性逐渐减弱,还原性逐渐增强,即:稳定性:
2
HF>HCl>HBr>HI;还原性:HF<HCl<HBr<HI。
(3)卤素单质与变价金属(如Fe)反应时,F 、Cl 、Br 生成高价卤化物(如FeX ),
2 2 2 3
而I 只能生成低价卤化物(如FeI )。
2 2
(4)氢化物都易溶于水,其水溶液酸性依次增强,氢化物中 HCl、HBr、HI的熔、沸点
依次升高,HF的熔、沸点最高。
(5)最高价氧化物的水化物的酸性逐渐减弱,即酸性:HClO >HBrO >HIO ,HClO 是
4 4 4 4
已知含氧酸中酸性最强的酸。
3.卤素的特性
(1)氟元素无正价,无含氧酸。F-的还原性极弱。
(2)X +H O===HX+HXO而2F +2H O===4HF+O 。
2 2 2 2 2
(3)Br 在常温下是唯一的一种液态非金属单质。
2
(4)碘为紫黑色固体,易升华,淀粉遇I 变蓝色。
2
(5)氢氟酸为弱酸,而盐酸、氢溴酸、氢碘酸为强酸。
【反馈检测】
第一课时
1.在化学变化过程中,原子中的下列粒子数可能发生改变的是( )
A.质子数
B.中子数
C.质量数
D.电子数
答案:D
解析:化学反应中原子的种类不变,质子数、中子数、质量数不变,电子数可能改变。
2.下列叙述正确的是( )
A.电子的能量越低,运动区域离核越远
16 / 21B.核外电子的分层排布即是核外电子的分层运动
C.稀有气体元素原子的最外层都排有8个电子
D.当M层是最外层时,最多可排布18个电子
答案:B
解析:电子的能量越低,运动区域离核越近,A错误;氦最外层只有2个电子,C错误;
当M层是最外层时,最多可排布8个电子,D错误。
3.核电荷数小于或等于18的元素中,原子的最外层电子数是其余电子总数一半的元素
种类有( )
A.1种
B.2种
C.3种
D.4种
答案:B
解析:在1号~18号元素中,符合题给要求的元素是Li和P。
4.下图微粒的结构示意图,正确的是( )
答案:A
解析:B中微粒结构示意图是Cl-而不是Cl,C中Ar的原子结构示意图应为 ,
D中K的原子结构示意图应为 。
5.(1)某元素原子的核电荷数是电子层数的5倍,其质子数是最外层电子数的3倍,该
元素的原子结构示意图是________。
(2)已知某粒子的结构示意图为 ,试回答:
①当x-y=10时,该粒子为________(填“原子”“阳离子”或“阴离子”)。
②当 y=8 时,粒子可能为(填名称)________、________、________、________、
17 / 21________。
解析:(1)设:核电荷数=质子数=a,元素原子的电子层数为x,最外层电子数为y,
依题意:a=5x,a=3y,则5x=3y,x=3y/5。因原子的最外层电子数不超过8,即y为1~8
的正整数,故仅当y=5,x=3合理,该元素的核电荷数为15。
(2)①当x-y=10时,x=10+y,说明核电荷数等于核外电子数,所以该粒子应为原子;
②当y=8时,应有18个电子的粒子,所以可能为氩原子、氯离子、硫离子、钾离子、钙离
子。
答案:(1)
(2)①原子;②氩原子;氯离子;硫离子;钾离子;钙离子
第二课时
1.下列说法正确的是( )
A.常用元素周期表中元素排序的依据是原子的核电荷数
B.元素周期表有十六个纵列,也就是十六个族
C.原子的最外层电子数相同的元素,一定属于同一族
D.电子层数相同的粒子,对应元素一定属于同一周期
答案:A
解析:元素周期表中有18个纵列,16个族,第Ⅷ族占三个纵列;Be和He的最外层电子
数都是2,但不属于同一族;Ne和Na+的电子层数都是2,但不属于同一周期。
2.下列各图若为元素周期表的一部分(表中数字代表原子序数),其中合理的是
( )
A B C D
答案:D
解析:本题要求熟记周期表的结构,知道1~18号元素在周期表中的具体位置。解题时
可根据稀有气体2号、10号元素应在周期表的最右端和3号元素在周期表的最左端排除A、
B、C三项。
3.俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成
功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙
18 / 21述正确的是( )
A.115号元素在第六周期
B.113号元素在第七周期ⅢA族
C.115号和113号元素都是非金属元素
D.镅元素和115号元素不在同一周期
答案:B
解析:95号元素镅、115号元素、113号元素,原子序数都大于 86而小于118,所以都在
第七周期;115号比118号原子序数少3,应在第ⅤA族,113号元素在第ⅢA族;113号元
素和115号元素都是金属元素。
4.Ne是最早发现的Ne元素的稳定同位素,汤姆孙(J.J.Thomson)和阿斯通(F.
W.Aston)在1913年发现了Ne。下列有关说法正确的是( )
A.Ne和Ne是同素异形体
B.Ne和Ne属于不同的核素
C.Ne和Ne的性质完全相同
D.Ne转变为Ne为化学变化
答案:B
解析:Ne和Ne的质子数相同,中子数不同,互为同位素,A错误;Ne和Ne的质子数相
同,中子数不同,属于不同的核素,B正确;Ne和Ne的化学性质完全相同,物理性质不同,
C错误;Ne转变为Ne中没有新物质生成,不是化学变化,D错误。
5.据短周期元素的信息回答问题。
元素信息
A 第三周期第ⅥA族
B 族序数是周期数的3倍
C 原子序数是11
D D3+与Ne电子数相同
(1)写出 A、B 的元素符号________、________,C、D 元素的名称________、
________。
(2)写出B、C单质在加热时的反应的化学方程式______________________________。
(3)从原子结构的角度分析A与B的____________相同,C与D的_____________相同。
解析:短周期是第一、二、三周期(前18号元素),据“周期序数=电子层数,主族序
数=最外层电子数”“原子序数=核电荷数=质子数=核外电子数”可推出A是硫,B是氧,
C 是钠,D3+与 Ne 电子数相同,即 D 是 13 号元素铝。钠与氧气在加热时的反应为 2Na+
O =====Na O ,从原子结构的角度分析硫与氧的最外层电子数相同,钠与铝的电子层数相同。
2 2 2
19 / 21答案:(1)S;O;钠;铝
(2)2Na+O =====Na O
2 2 2
(3)最外层电子数 电子层数相同
第三课时
1.我国西部地区蕴藏着丰富的锂资源,开发锂的用途是一个重要的科学课题。关于锂的
叙述不正确的是( )
A.锂是较轻的金属
B.LiOH的碱性比NaOH弱
C.锂的金属性比钠强
D.锂在空气中燃烧生成Li O
2
答案:C
解析:锂比钠的活泼性弱,在空气中燃烧只生成Li O,LiOH的碱性比NaOH弱,锂的金
2
属性比钠弱,C项错误。
2.按氟、氯、溴、碘顺序,下列说法不正确的是( )
A.它们的单质的熔、沸点逐渐升高
B.原子半径逐渐增大,单质氧化性逐渐增强
C.单质的颜色逐渐加深
D.它们气态氢化物的稳定性逐渐减弱
答案:B
解析:氟、氯、溴、碘的单质的熔、沸点逐渐升高,A正确;氟、氯、溴、碘同为第ⅦA
族元素,同主族从上到下,原子半径逐渐增大,非金属性逐渐减弱,因此单质氧化性逐渐减
弱,B错误;氟、氯、溴、碘的单质的颜色逐渐加深,C正确;非金属性F>Cl>Br>I,非
金属性越强,氢化物越稳定,则它们气态氢化物的稳定性逐渐减弱,D正确。
3.下列有关碱金属元素的叙述正确的是( )
A.碱金属单质均为银白色,密度均小于水
B.碱金属单质从Li到Cs,熔点依次升高
C.氢氧化铯碱性强于氢氧化钠
D.碱金属元素形成的阳离子,从Li+到Cs+氧化性依次增强
答案:C
解析:碱金属单质中除了Rb、Cs,其他的密度均小于水,Cs略带金属光泽,其他的都是
银白色的,A错误;碱金属单质从Li到Cs,熔点依次降低,还原性依次增强,形成的阳离子
20 / 21的氧化性依次降低,对应的氢氧化物碱性依次增强,C正确,B、D错误。
4.向含有NaBr和KI的混合溶液中通入过量Cl ,充分反应后将溶液蒸干并灼烧所得物
2
质,最后剩余的固体是( )
A.NaCl和KI
B.NaCl、KCl、I
2
C.KCl和NaBr
D.KCl和NaCl
答案:D
解析:过量的Cl 将I-、Br-从溶液中完全置换出来,在蒸干、灼烧过程中溴挥发、碘升
2
华,所得固体为NaCl和KCl。此题也可利用Cl 、Br 、I 活泼性强弱用排除法选出D项。
2 2 2
5.(1)卤素氢化物中最不稳定的是________(写化学式)。
(2)下列两个元素族,单质熔、沸点随原子序数递增而升高的是________(填序号)。
A.碱金属 B.卤素
(3)下列反应中,更剧烈的是________(填序号)。
A.钠与水反应 B.钾与水反应
(4)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静
置后,四氯化碳层显紫红色的是________(填序号)。
A.溴化钠溶液 B.碘化钾溶液
解析:卤素中碘元素的非金属性最弱,氢化物最不稳定的是 HI;碱金属元素单质熔、沸
点随原子序数递增而降低,卤素单质熔、沸点随原子序数递增而升高;钾比钠活泼,与水反
应更剧烈;氯水与NaBr、KI溶液分别生成Br 、I ,而二者的四氯化碳溶液分别为橙色、紫
2 2
红色。
答案:(1)HI
(2)B
(3)B
(4)B
21 / 21