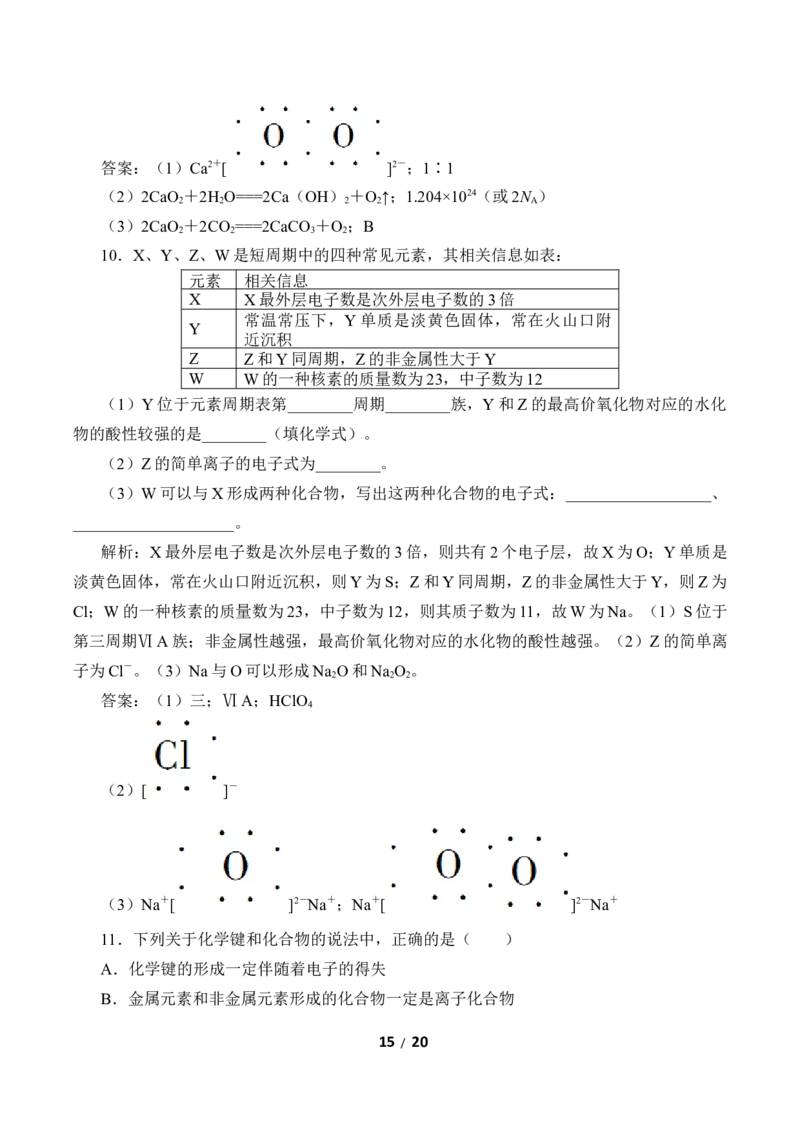
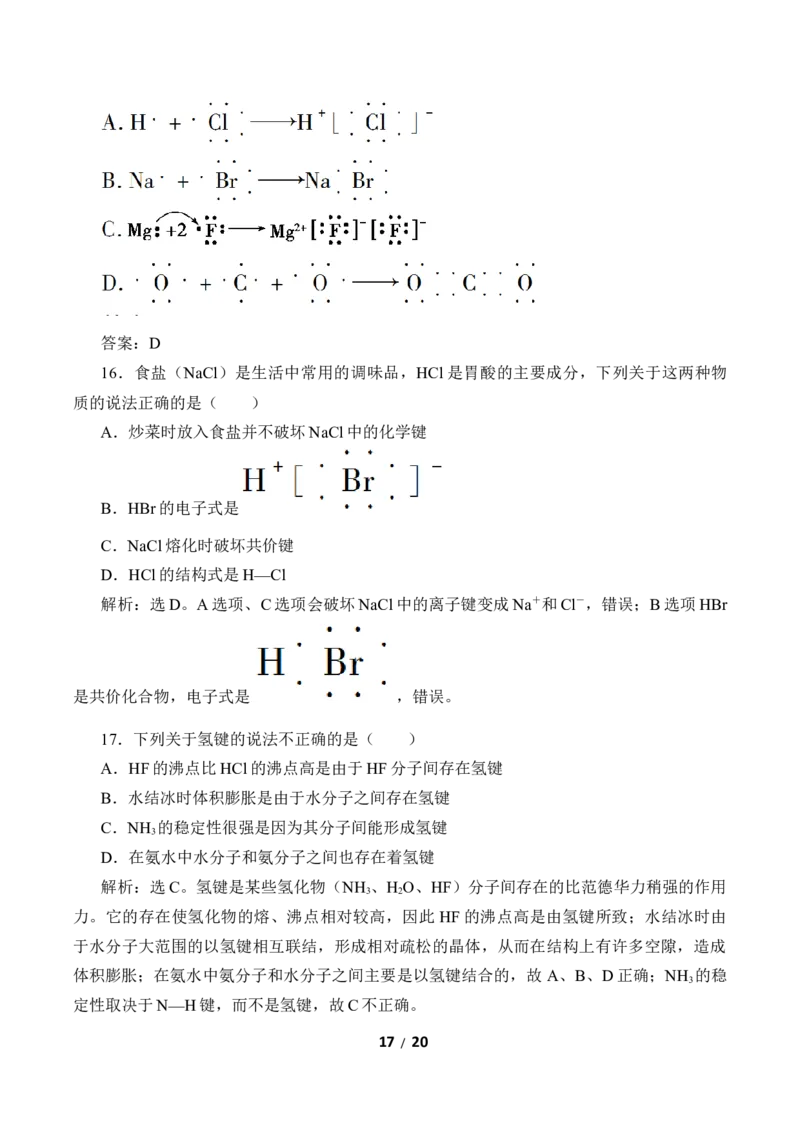
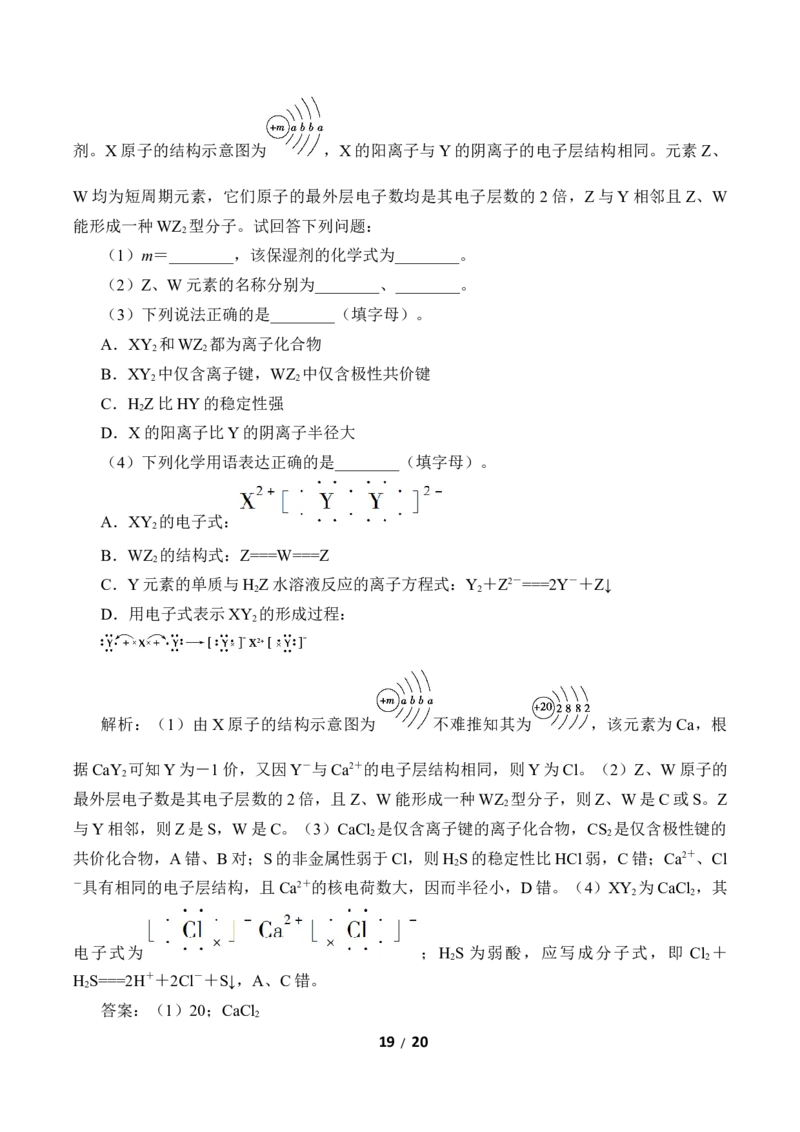
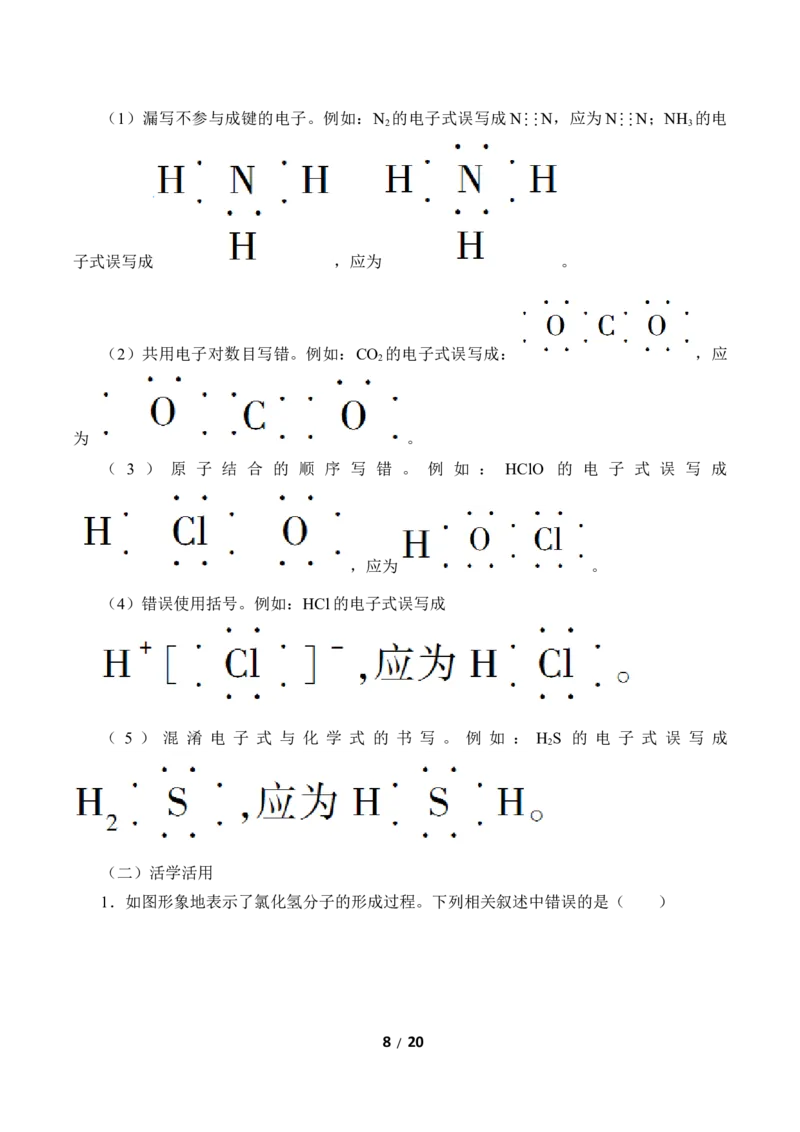文档内容
化学键
【学习目标】
1.宏观辨识:能运用模型、符号等多种方式对物质的结构及其变化进行综合表征。
2.变化观念:能运用宏观、微观、符号等方式描述、说明物质转化的本质和规律。
【学习重难点】
1.认识构成物质的微粒之间存在相互作用,认识共价键的形成,建立化学键概念。
2.能判断简单离子化合物、简单共价化合物中的化学键类型。
3.认识化学键的断裂和形成是化学反应中物质变化的实质。
【学习过程】
知识点1:离子键和离子化合物
一、自主学习
1.离子键
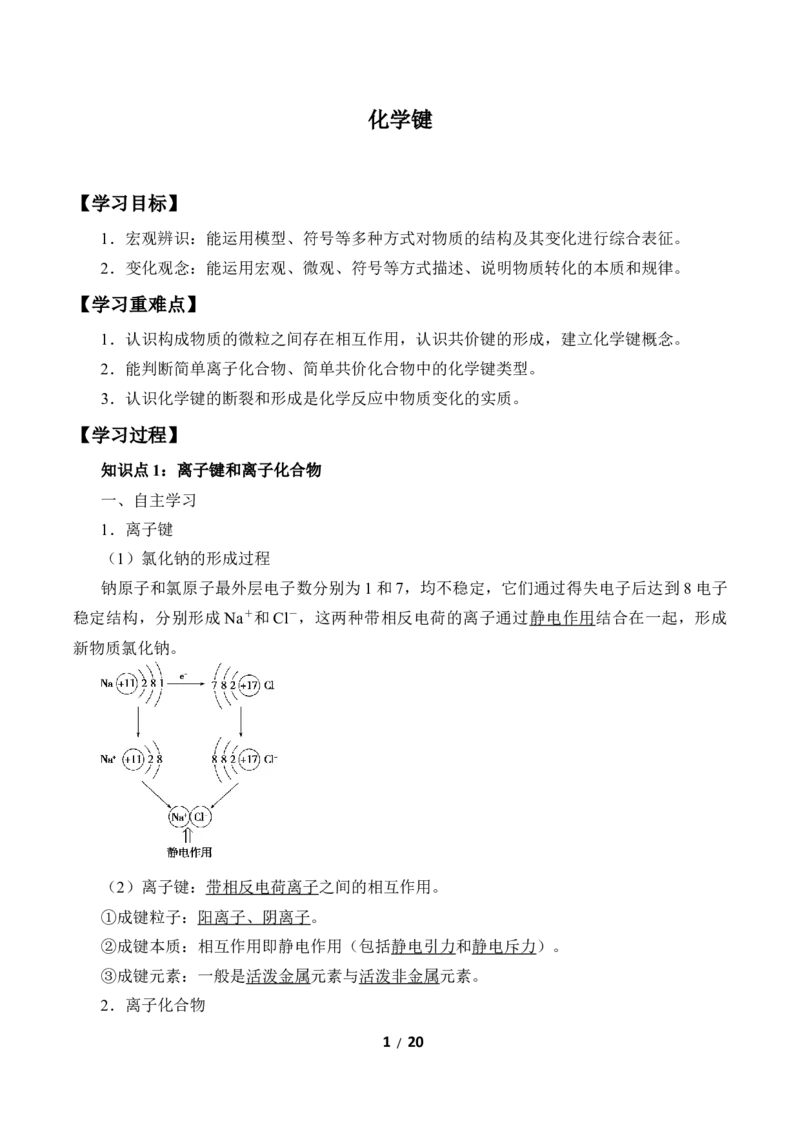
(1)氯化钠的形成过程
钠原子和氯原子最外层电子数分别为1和7,均不稳定,它们通过得失电子后达到8电子
稳定结构,分别形成 Na+和Cl-,这两种带相反电荷的离子通过静电作用结合在一起,形成
新物质氯化钠。
(2)离子键:带相反电荷离子之间的相互作用。
①成键粒子:阳离子、阴离子。
②成键本质:相互作用即静电作用(包括静电引力和静电斥力)。
③成键元素:一般是活泼金属元素与活泼非金属元素。
2.离子化合物
1 / 20(1)概念:由离子键构成的化合物。
(2)常见类型
①强碱,如NaOH、KOH等。
②绝大多数盐,如NaCl、K SO 等。
2 4
③活泼金属氧化物,如K O、Na O、MgO等。
2 2
(3)性质
①离子化合物中离子键一般比较牢固,破坏它需要很高的能量,所以离子化合物的熔点
一般较高,常温下为固体。
②离子化合物在溶于水或受热熔化时,离子键被破坏,形成自由移动的阴、阳离子,能
够导电。
二、重难点点拨
(一)关于离子键和离子化合物的误区提醒
(1)离子化合物中一定含有阴离子和阳离子。
(2)离子化合物中一定含有离子键,含有离子键的物质一定是离子化合物。
(3)铵根离子与酸根离子之间形成离子键,铵盐都是离子化合物。
(4)活泼金属(如第ⅠA、ⅡA族的金属)与活泼非金属(如第ⅥA、ⅦA族的非金
属)原子之间通常形成离子键。
(二)活学活用
1.如图形象地表示了氯化钠的形成过程。下列相关叙述中不正确的是( )
A.钠原子易失去一个电子,氯原子易得到一个电子
B.钠离子与钠原子有相似的化学性质
C.钠原子与氯原子作用生成NaCl后,其结构的稳定性增强
D.氯化钠是离子化合物
2 / 20解析:选B。钠原子最外层有一个电子,易失电子,有较强的还原性,而钠离子最外层
已经达到“8e-”稳定结构,故二者化学性质不同。
2.下列关于离子键和离子化合物的说法正确的是( )
A.阴、阳离子间通过静电引力形成离子键
B.阴、阳离子间通过离子键一定能形成离子化合物
C.离子化合物一定能导电
D.只有活泼金属元素和活泼非金属元素化合时,才能形成离子键
解析:选B。A项,离子键是阴、阳离子间的静电作用,包括静电引力和静电斥力;B项,
阴、阳离子间通过离子键形成的化合物只能是离子化合物;C项,离子化合物在水溶液或熔
融状态下才能导电;D项,NH与酸根离子之间也能形成离子键。
3.下列哪一组元素的原子间反应容易形成离子键( )
元素 a b c d e f g
M层电子数 1 2 3 4 5 6 7
A.a和c
B.a和f
C.d和g
D.c和g
解析:选B。由原子a~g的M层电子数可知,M层即为原子的最外层,元素 a~g均为
第三周期元素,a为活泼的金属元素,f、g为活泼的非金属元素,所以a与f、a与g形成的化
学键为离子键。
知识点2:电子式
一、自主学习
1.定义
在元素符号周围用“·”或“×”来表示原子的最外层电子(价电子),这种式子叫作电子式。
2.电子式的书写
原子
钠原子:Na×;氧原子:
简单阳离
Na+、Mg2+、Al3+
子
简单阴离
子
3 / 20复杂阴、
阳离子
离子化合
物
(1)
物质形成
过程
( 2 )
二、重难点点拨
(一)电子式书写中的常见错误
(1)漏标阴离子的括号,如将S2-的电子式错写为
( 2 ) 给 阳 离 子 多 标 电 子 和 括 号 , 如 将 Al3 + 的 电 子 式 错 写 为
(3)漏标或错标离子的电荷,如将S2-的电子式错写为
( 4 ) 将 多 个 相 同 的 离 子 归 在 一 起 , 如 将 K S 的 电 子 式 错 写 为
2
(二)活学活用
4 / 201.下列物质的电子式正确的是( )
解析:选C。A项,应为
2.用电子式表示下列离子化合物的形成过程:
(1)BaCl __________________________________________________________________;
2
( 2 )
NaF____________________________________________________________________;
( 3 )
MgS___________________________________________________________________;
( 4 )
K O____________________________________________________________________。
2
解析:书写电子式和用电子式表示离子化合物的形成过程时,一定要注意规范表达。
答案:(1)
(2)
(3)
5 / 20(4)
知识点3:共价键和共价化合物
一、自主学习
1.共价键
(1)形成过程
①氯分子的形成过程
→→→
用电子式表示其形成过程: 。
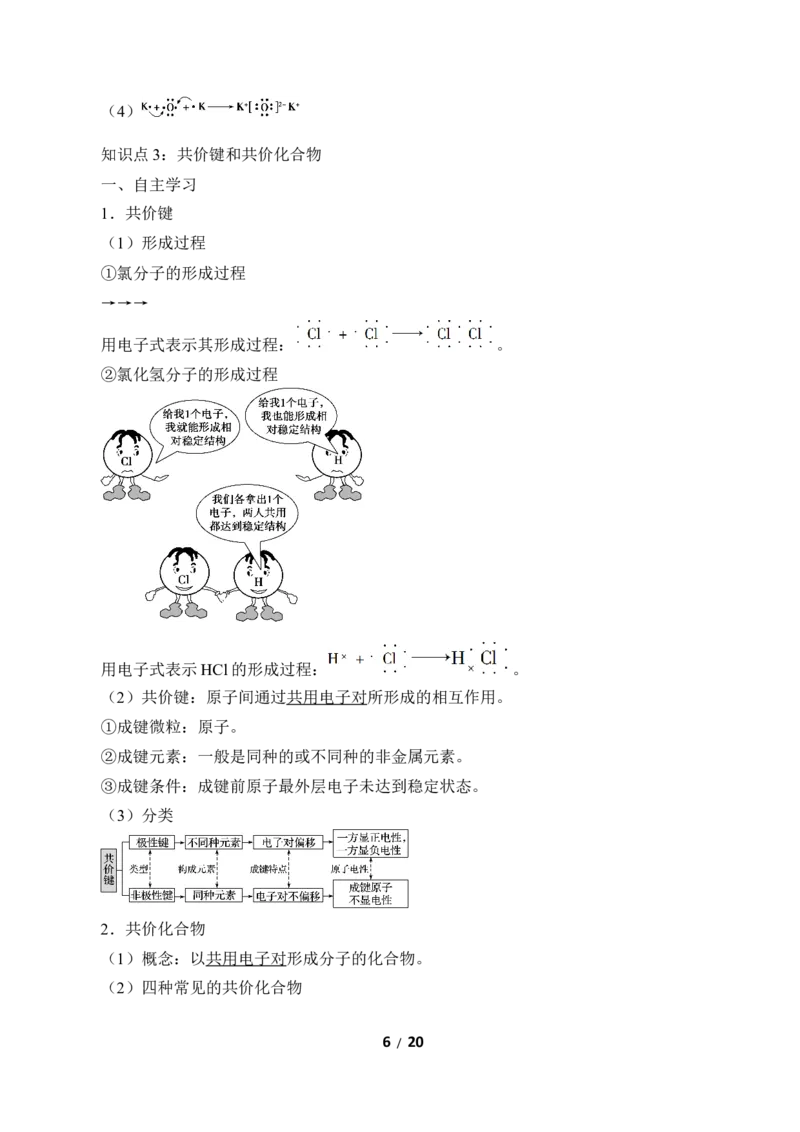
②氯化氢分子的形成过程
用电子式表示HCl的形成过程: 。
(2)共价键:原子间通过共用电子对所形成的相互作用。
①成键微粒:原子。
②成键元素:一般是同种的或不同种的非金属元素。
③成键条件:成键前原子最外层电子未达到稳定状态。
(3)分类
2.共价化合物
(1)概念:以共用电子对形成分子的化合物。
(2)四种常见的共价化合物
6 / 20①非金属氢化物,如NH 、H S、H O等。
3 2 2
②非金属氧化物,如CO、CO 、SO 等。
2 2
③含氧酸,如H SO 、HNO 等。
2 4 3
④大多数有机化合物,如CH 、CH CH OH等。
4 3 2
3.共价分子的表示方法及形成过程
(1)常见分子的电子式、结构式及结构模型
分子 H HCl CO H O CH
2 2 2 4
电子式 H:H
H:
结构式 H—H H—Cl O===C===O
分子结构模型
(2)用电子式表示共价分子的形成过程
二、重难点点拨
(一)误区提醒和常见错误
1.关于共价键和共价化合物的误区提醒
(1)含有共价键的分子不一定是共价化合物,如H 、O 等单质。
2 2
(2)含有共价键的化合物不一定是共价化合物,如NaOH、Na O 等。
2 2
(3)离子化合物中可能含有共价键,共价化合物中一定不含离子键,只有共价键。
(4)非金属元素组成的化合物不一定是共价化合物,如NH Cl等。
4
(5)由活泼金属元素和活泼非金属元素形成的化合物不一定是离子化合物,如 AlCl 是
3
共价化合物。
2.共价化合物(或单质)电子式书写的常见错误
7 / 20(1)漏写不参与成键的电子。例如:N 的电子式误写成N⋮⋮N,应为N⋮⋮N;NH 的电
2 3
子式误写成 ,应为 。
(2)共用电子对数目写错。例如:CO 的电子式误写成: ,应
2
为 。
( 3 ) 原 子 结 合 的 顺 序 写 错 。 例 如 : HClO 的 电 子 式 误 写 成
,应为 。
(4)错误使用括号。例如:HCl的电子式误写成
( 5 ) 混 淆 电 子 式 与 化 学 式 的 书 写 。 例 如 : H S 的 电 子 式 误 写 成
2
(二)活学活用
1.如图形象地表示了氯化氢分子的形成过程。下列相关叙述中错误的是( )
8 / 20A.氯化氢是共价化合物
B.氯化氢分子中所有原子最外层都有8个电子
C.氯化氢分子比氯原子和氢原子都稳定
D.氯化氢分子中含有1对共用电子对
解析:选B。氯化氢分子中的氢原子最外层有2个电子,B项错误。
2.下列叙述中,不正确的是( )
A.含有共价键的物质一定是共价化合物
B.H O 中既含有极性键又含有非极性键
2 2
C.CaO和NaCl晶体熔化时要破坏离子键
D.纯硫酸不导电
解析:选A。部分非金属单质如O 、N 中含有共价键,但不属于化合物;某些离子化合
2 2
物如NaOH中既含有离子键又含有共价键。
3.下列分子的电子式书写正确的是( )
答案:C
知识点4:化学键与分子间作用力
一、自主学习
1.化学键
9 / 20(1)概念:相邻的原子之间强烈的相互作用。
(2)分类
2.化学反应:反应物中的原子重新组合为产物分子的一种过程。在化学反应过程中,包
含着反应物分子内化学键的断裂和产物分子中化学键的形成。
化学反应的过程,本质上就是旧化学键断裂和新化学键形成的过程。
3.分子间作用力
(1)分子之间存在一种把分子聚集在一起的作用力,叫作分子间作用力。最初也将分子
间作用力称为范德华力。
(2)范德华力比化学键弱得多,主要影响物质的熔、沸点等。
4.氢键
(1)氢键也是一种分子间作用力,比化学键弱,但比范德华力强。
(2)氢键会使物质的熔点和沸点升高,这是因为固体熔化或液体汽化时必须破坏分子间
的氢键,消耗较多能量。
二、重难点点拨
(一)化学键、范德华力和氢键的比较
相互作用 化学键 范德华力 氢键
某些含强极性键的
氢化物分子之间
存在范围 相邻原子之间 分子之间
(如 HF、H O、
2
NH 等)
3
比化学键弱,比范
作用力大小 强 很弱
德华力强
物质的物理性质及
影响范围 物质的物理性质 物质的物理性质
化学性质
(二)活学活用
1.下列关于共价键的说法正确的是( )
A.金属原子在化学反应中只能失去电子,因而不能形成共价键
B.由共价键形成的分子可以是单质分子,也可以是化合物分子
C.共价键只能在不同原子之间形成
D.稀有气体分子中只存在共价键
解析:选B。金属和非金属化合时也能形成共价键,如 AlCl 分子中的Al—Cl键是共价键;
3
10 / 20在H 、O 、N 、HCl、NH 分子中均存在共价键;H 、Cl 分子中的H—H键和Cl—Cl键都是
2 2 2 3 2 2
共价键;稀有气体分子是单原子分子,本身就已达到8电子或2电子稳定结构,不存在共用
电子对,所以无共价键。
2.下列过程没有发生化学键变化的是( )
A.生石灰投入水中
B.氯化氢气体通入水中
C.冰融化成水
D.高锰酸钾固体受热分解
解析:选C。生石灰投入水中生成氢氧化钙,有化学键的断裂和形成,A项错误;氯化氢
气体通入水中电离出氢离子和氯离子,共价键断裂,B项错误;冰融化成水是状态的变化,
化学键不变,C项正确;高锰酸钾固体受热分解发生化学变化,有化学键的断裂和形成,D
项错误。
3.下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是( )
A.液溴和碘分别受热变为气体
B.干冰和碳酸氢钠分别受热得到气体
C.食盐和冰的熔化
D.食盐和葡萄糖分别溶解在水中
解析:选A。液溴和碘受热变成气体均需克服分子间作用力,A项正确;干冰受热得到气
体克服分子间作用力,碳酸氢钠受热得到气体破坏了化学键,B项错误;食盐熔化时,破坏
了离子键,冰熔化时破坏了分子间作用力和氢键,C项错误;食盐溶解在水中,破坏了离子
键,葡萄糖溶解在水中,破坏了分子间作用力,D项错误。
【反馈检测】
1.下列说法正确的是( )
A.离子键就是使阴、阳离子结合成化合物的静电引力
B.所有金属与所有非金属原子之间都能形成离子键
C.在化合物CaCl 中,两个氯离子之间存在共价键
2
D.含有离子键的化合物一定是离子化合物
解析:选D。离子键是使阴、阳离子结合成化合物的静电作用,要注意区别静电作用和
静电引力,A项错误;金属与非金属原子之间不一定形成离子键,B项错误;由CaCl 的电子
2
式 可以看出,CaCl 中只存在离子键,C项错误;含
2
11 / 20有离子键的化合物一定是离子化合物,D项正确。
2.下列关于离子化合物的叙述正确的是( )
A.离子化合物中都含有离子键
B.离子化合物中的阳离子只能是金属离子
C.离子化合物溶于水时化学键仍完好
D.溶于水可以导电的化合物一定是离子化合物
解析:选A。A项,离子化合物的构成粒子为阴、阳离子,一定含有离子键,正确;B项,
离子化合物中的阳离子可以全部由非金属元素构成,如铵盐,错误;C项,离子化合物溶于
水时离子键一定被破坏,错误;D项,溶于水可以导电的化合物不一定为离子化合物,如
HCl等,错误。
3.下列各数值表示有关元素的原子序数,其所表示的各原子组中能以离子键相互结合生
成稳定化合物的是( )
A.6与16
B.8与14
C.10与19
D.11与17
解析:选D。两种元素化合时,一般来说,活泼金属元素与活泼非金属元素化合形成离
子键。原子序数为6、8、14、16的元素都是非金属元素,10号元素是稀有气体元素,故A、
B、C选项中的元素不可能以离子键相互结合生成稳定化合物。11号元素是活泼金属元素钠,
17号元素是活泼非金属元素氯,它们能以离子键相互结合生成稳定化合物NaCl。
4.Y元素最高正价与最低负价的绝对值之差是4;Y元素与M元素形成离子化合物,并
在水中电离出电子层结构相同的离子,该化合物是( )
A.KCl
B.Na S
2
C.Na O
2
D.K S
2
解析:选D。由信息“Y元素最高正价与最低负价的绝对值之差是4”,可确定Y元素位
于第ⅥA族且不是氧元素;K S电离出的K+与S2-具有相同的电子层结构。
2
5.下列有关电子式的叙述正确的是( )
A.H、He、Li的电子式分别为H、He、Li
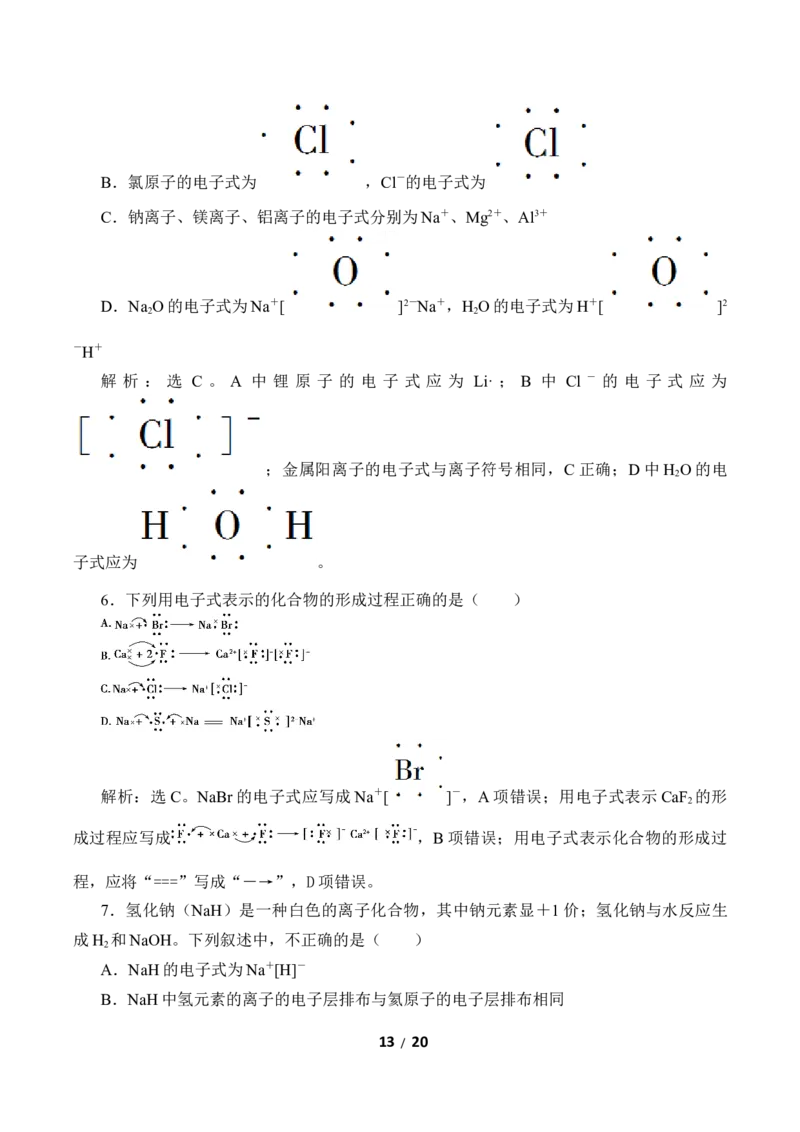
12 / 20B.氯原子的电子式为 ,Cl-的电子式为
C.钠离子、镁离子、铝离子的电子式分别为Na+、Mg2+、Al3+
D.Na O的电子式为Na+[ ]2-Na+,H O的电子式为H+[ ]2
2 2
-H+
解 析 : 选 C 。 A 中 锂 原 子 的 电 子 式 应 为 Li· ; B 中 Cl - 的 电 子 式 应 为
;金属阳离子的电子式与离子符号相同,C正确;D中H O的电
2
子式应为 。
6.下列用电子式表示的化合物的形成过程正确的是( )
解析:选C。NaBr的电子式应写成Na+[ ]-,A项错误;用电子式表示CaF 的形
2
成过程应写成 ,B项错误;用电子式表示化合物的形成过
程,应将“===”写成“―→”,D项错误。
7.氢化钠(NaH)是一种白色的离子化合物,其中钠元素显+1价;氢化钠与水反应生
成H 和NaOH。下列叙述中,不正确的是( )
2
A.NaH的电子式为Na+[H]-
B.NaH中氢元素的离子的电子层排布与氦原子的电子层排布相同
13 / 20C.微粒半径H-<Li+
D.NaH与H O反应时,H O做氧化剂
2 2
解析:选C。氢化钠(NaH)是一种白色的离子化合物,NaH的电子式为Na+[H]-,A正
确;NaH中氢元素的化合价为-1价,其离子的电子层排布与氦原子的电子层排布相同,B
正确;锂离子和H-的电子层排布相同,但是锂离子的核电荷数比 H-多,所以微粒半径H->
Li+,C错误;NaH与H O反应生成氢气和NaOH,在这个反应中只有氢元素的化合价发生了
2
变化,NaH中H元素的化合价升高做还原剂,被氧化,H O中H元素的化合价降低做氧化剂,
2
被还原,D正确。
8.X、Y、Z、W是原子序数依次增大的不同主族的短周期元素,X、Y的简单离子的核
外电子数相同,Y的原子半径是短周期主族元素原子中最大的,Z原子最外层电子数是K层
的3倍。下列说法正确的是( )
A.简单离子半径:Y>Z
B.X只能形成HXO 型的酸
3
C.气态氢化物的热稳定性:W