文档内容
实验活动 1 配制一定物质的量浓度的溶液
课题 配制一定物质的量浓度的 单元 2 学科 化学 年级 高一
溶液
宏观辨识与微观探析:从宏观上观察化学物质的质量、体
积、状态,从微观上学习化学物质的物理量——物质的量,体
会宏观物质与微观粒子间的联系。
证据推理与模型认知:通过化学仪器分类的基本方法,理解
容量瓶、烧杯等化学仪器的区别,通过结合理论与实际感知化
学学习的魅力,为后续的化学知识的学习奠定坚实的方法基
教学目标与核心
础。
素养
科学探究与创新意识:熟悉掌握多种化学仪器的使用方法,
熟练掌握通过实验分析不同化合物的性质和用途的能力,体会
化学研究过程中的科学方法。
科学精神与社会责任:通过对配置一定物质的量浓度的实验
探究和学习,掌握更高效的学习方法,建立高效学习的科学精
神。
学习容量瓶相关概念以及容量瓶的使用方法;掌握溶液的配
教学重点难点
制方法;学习和掌握稀释浓溶液的方法和步骤。
教学过程
教学环节 教师活动 学生活动 设计意图
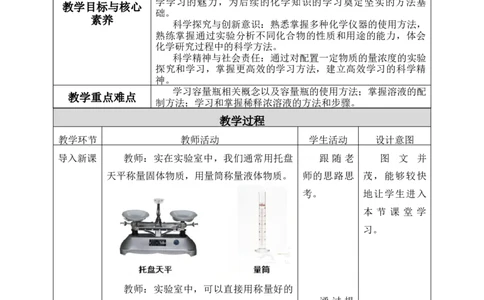
导入新课 教师:实在实验室中,我们通常用托盘 跟 随 老 图 文 并
天平称量固体物质,用量筒称量液体物质。 师的思路思 茂,能够较快
考。 地让学生进入
本 节 课 堂 学
习。
教师:实验室中,可以直接用称量好的
通 过 提
固体或液体试剂来配制一定物质的量浓度的
问,引出今 通 过 思
溶液。但如果要求比较精确,就需要使用容
天学习的新 考,打开同学
积精确的仪器,如容量瓶。容量瓶是什么?
内容。 们的思路。
容量瓶长什么样?
教师:引出本节课学习内容
1 / 8讲授新课 教师利用多媒体设备向学生投影出下面
新课讲解:容量瓶
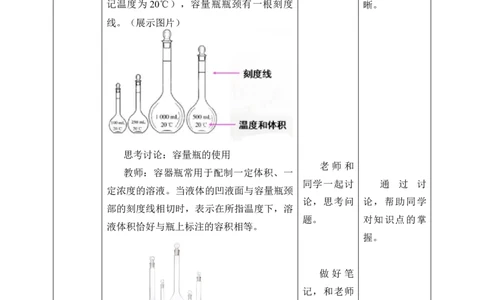
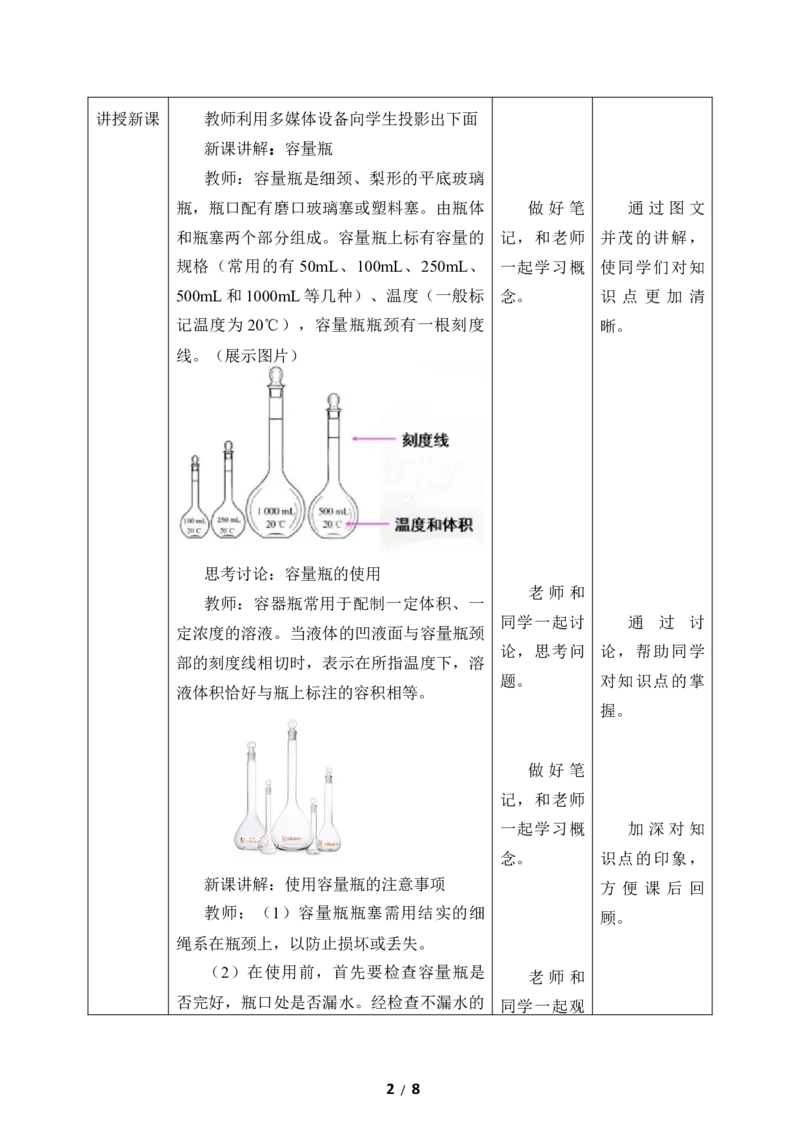
教师:容量瓶是细颈、梨形的平底玻璃
瓶,瓶口配有磨口玻璃塞或塑料塞。由瓶体 做 好 笔 通 过 图 文
和瓶塞两个部分组成。容量瓶上标有容量的 记,和老师 并茂的讲解,
规格(常用的有 50mL、100mL、250mL、 一起学习概 使同学们对知
500mL和1000mL等几种)、温度(一般标 念。 识 点 更 加 清
记温度为 20℃),容量瓶瓶颈有一根刻度 晰。
线。(展示图片)
思考讨论:容量瓶的使用
老 师 和
教师:容器瓶常用于配制一定体积、一
同学一起讨 通 过 讨
定浓度的溶液。当液体的凹液面与容量瓶颈
论,思考问 论,帮助同学
部的刻度线相切时,表示在所指温度下,溶
题。 对知识点的掌
液体积恰好与瓶上标注的容积相等。
握。
做 好 笔
记,和老师
一起学习概 加 深 对 知
念。 识点的印象,
新课讲解:使用容量瓶的注意事项 方 便 课 后 回
教师:(1)容量瓶瓶塞需用结实的细
顾。
绳系在瓶颈上,以防止损坏或丢失。
(2)在使用前,首先要检查容量瓶是
老 师 和
否完好,瓶口处是否漏水。经检查不漏水的 同学一起观
2 / 8容量瓶才能使用。 察、讨论实
(3)容量瓶使用完毕,应洗净、晾 验内容和过 通 过 讨
干。(玻璃磨口瓶塞应在瓶塞与瓶口处垫一 程。 论,帮助同学
张纸条,以免瓶塞与瓶口粘连。) 对知识点的掌
思考讨论:制 100mL1.00mol/LNaCl 溶 握。
液。
(1)计算需要 NaCl 固体的质量:
________g。
答案:利用物质的量浓度的定义,根据
n =c ·V 计算出所需要的 NaCl 物质的量:
B B
0.1L×1mol/L=0.1mol;然后通过质量与物质
的量的关系,根据m=n·M,求得NaCl的质
量:0.1mol×58.5g/mol=5.85g。
(2)根据计算结果称量NaCl固体。
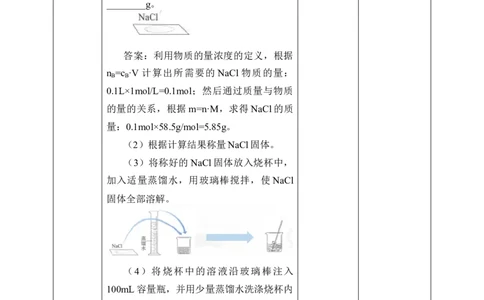
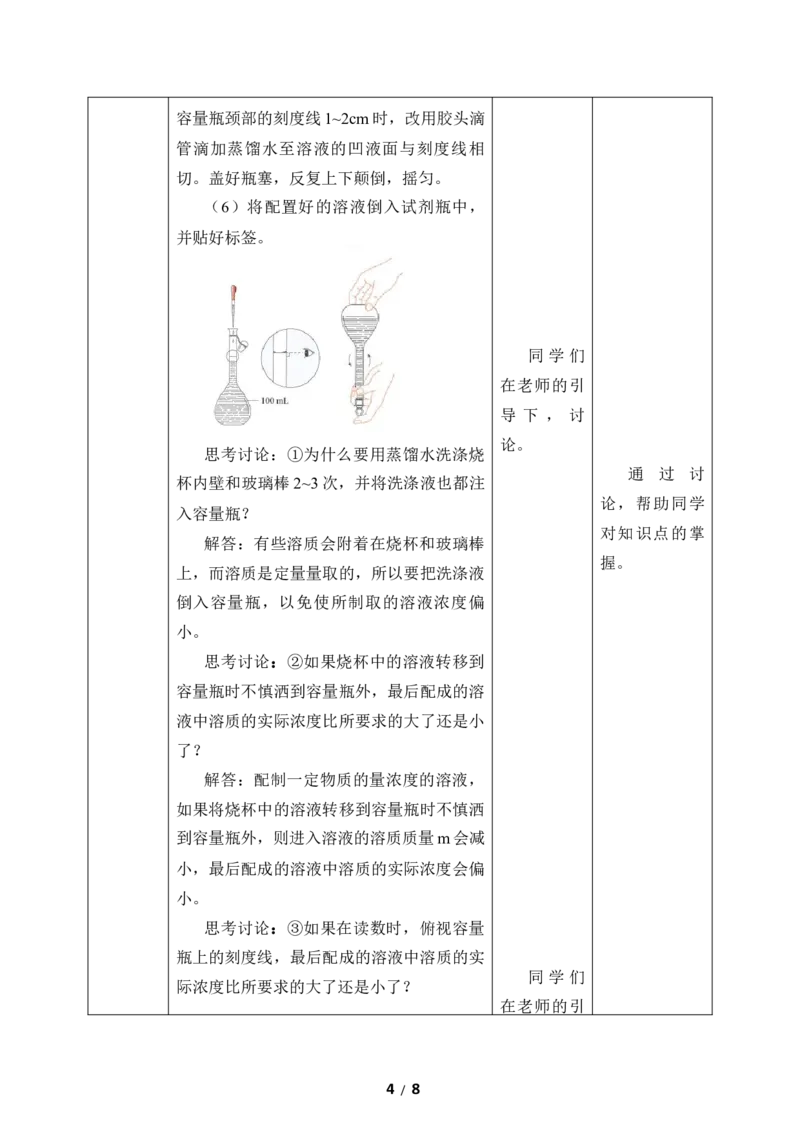
(3)将称好的NaCl固体放入烧杯中,
加入适量蒸馏水,用玻璃棒搅拌,使 NaCl
固体全部溶解。
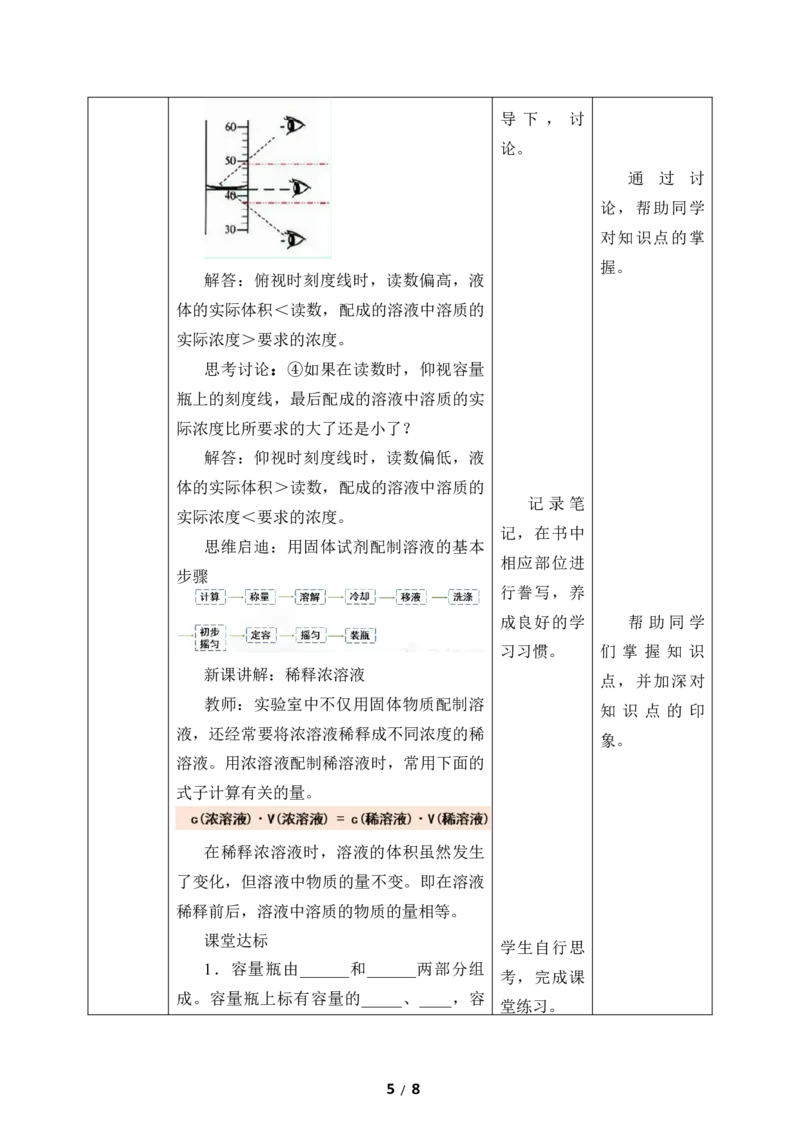
(4)将烧杯中的溶液沿玻璃棒注入
100mL容量瓶,并用少量蒸馏水洗涤烧杯内
壁和玻璃棒2~3次,将洗涤液也都注入容量
瓶。轻轻摇动容量瓶,使溶液混合均匀。
(5)将蒸馏水注入容量瓶,当液面离
3 / 8容量瓶颈部的刻度线1~2cm时,改用胶头滴
管滴加蒸馏水至溶液的凹液面与刻度线相
切。盖好瓶塞,反复上下颠倒,摇匀。
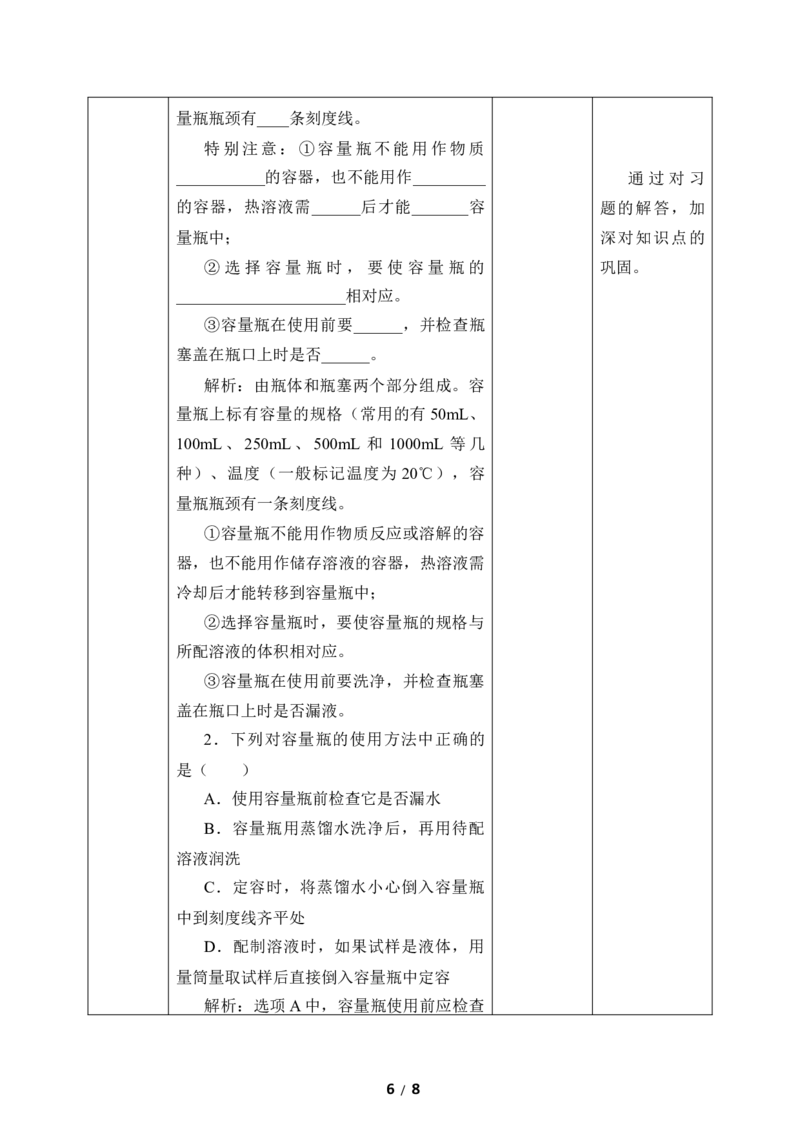
(6)将配置好的溶液倒入试剂瓶中,
并贴好标签。
同 学 们
在老师的引
导 下 , 讨
论。
思考讨论:①为什么要用蒸馏水洗涤烧
通 过 讨
杯内壁和玻璃棒2~3次,并将洗涤液也都注
论,帮助同学
入容量瓶?
对知识点的掌
解答:有些溶质会附着在烧杯和玻璃棒
握。
上,而溶质是定量量取的,所以要把洗涤液
倒入容量瓶,以免使所制取的溶液浓度偏
小。
思考讨论:②如果烧杯中的溶液转移到
容量瓶时不慎洒到容量瓶外,最后配成的溶
液中溶质的实际浓度比所要求的大了还是小
了?
解答:配制一定物质的量浓度的溶液,
如果将烧杯中的溶液转移到容量瓶时不慎洒
到容量瓶外,则进入溶液的溶质质量m会减
小,最后配成的溶液中溶质的实际浓度会偏
小。
思考讨论:③如果在读数时,俯视容量
瓶上的刻度线,最后配成的溶液中溶质的实
同 学 们
际浓度比所要求的大了还是小了?
在老师的引
4 / 8导 下 , 讨
论。
通 过 讨
论,帮助同学
对知识点的掌
握。
解答:俯视时刻度线时,读数偏高,液
体的实际体积<读数,配成的溶液中溶质的
实际浓度>要求的浓度。
思考讨论:④如果在读数时,仰视容量
瓶上的刻度线,最后配成的溶液中溶质的实
际浓度比所要求的大了还是小了?
解答:仰视时刻度线时,读数偏低,液
体的实际体积>读数,配成的溶液中溶质的
记 录 笔
实际浓度<要求的浓度。
记,在书中
思维启迪:用固体试剂配制溶液的基本
相应部位进
步骤
行誊写,养
成良好的学 帮 助 同 学
习习惯。 们 掌 握 知 识
新课讲解:稀释浓溶液
点,并加深对
教师:实验室中不仅用固体物质配制溶
知 识 点 的 印
液,还经常要将浓溶液稀释成不同浓度的稀
象。
溶液。用浓溶液配制稀溶液时,常用下面的
式子计算有关的量。
在稀释浓溶液时,溶液的体积虽然发生
了变化,但溶液中物质的量不变。即在溶液
稀释前后,溶液中溶质的物质的量相等。
课堂达标
学生自行思
1.容量瓶由______和______两部分组
考,完成课
成。容量瓶上标有容量的_____、____,容
堂练习。
5 / 8量瓶瓶颈有____条刻度线。
特别注意:①容量瓶不能用作物质
___________的容器,也不能用作_________ 通 过 对 习
的容器,热溶液需______后才能_______容 题的解答,加
量瓶中; 深对知识点的
② 选 择 容 量 瓶 时 , 要 使 容 量 瓶 的 巩固。
_____________________相对应。
③容量瓶在使用前要______,并检查瓶
塞盖在瓶口上时是否______。
解析:由瓶体和瓶塞两个部分组成。容
量瓶上标有容量的规格(常用的有50mL、
100mL、250mL、500mL 和 1000mL 等几
种)、温度(一般标记温度为 20℃),容
量瓶瓶颈有一条刻度线。
①容量瓶不能用作物质反应或溶解的容
器,也不能用作储存溶液的容器,热溶液需
冷却后才能转移到容量瓶中;
②选择容量瓶时,要使容量瓶的规格与
所配溶液的体积相对应。
③容量瓶在使用前要洗净,并检查瓶塞
盖在瓶口上时是否漏液。
2.下列对容量瓶的使用方法中正确的
是( )
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配
溶液润洗
C.定容时,将蒸馏水小心倒入容量瓶
中到刻度线齐平处
D.配制溶液时,如果试样是液体,用
量筒量取试样后直接倒入容量瓶中定容
解析:选项A中,容量瓶使用前应检查
6 / 8它是否漏水,A正确;选项B中,容量瓶用
蒸馏水洗净后,不能用待配溶液润洗,会使
配制的溶液浓度偏大,B错误;选项C中,
定容时,将蒸馏水小心倒入容量瓶中到距离
刻度线1-2cm处,再改用胶头滴管逐滴加入
至凹液面最低处与视线相平为止,C错误;
选项D中,如果试样是液体,用哪个量筒量
取试样后倒入烧杯中加水稀释,再转移到容
量瓶中定容,D错误。故应选A。
3.实验室中需要配制2mol/L的NaCl溶
液950mL,配制时应选用的容量瓶的规格和
称取的NaCl质量分别是( )
A.950mL,111.2g
B.500mL,117g
C.1000mL,117g
D.任意规格,111.2g
解析:配制溶液时,只能配制容量瓶上
规定体积的溶液,不能配制任意体积的一定
物质的量浓度的溶液。计算时也要按配制的
体积来计算所需溶质。与 950mL 最接近容
量瓶的体积是1000mL,因此配制2mol/L的
NaCl 溶液 1000mL 需氯化钠的质量为:
2mol/L×1L×58.5g/mol=117.0g。故应选C。
4.在 10mL2.4mol·L-1的 NaOH 溶液中
加入50mL水,下列说法正确的是( )
A.稀释后溶液的浓度是0.4mol·L-1
B.稀释后溶液的体积是60L
C.稀释后溶液的浓度为0.33mol·L-1
D.以上答案均不正确
解析:分子中间有空隙,所以混合后的
液体体积小于 10ml+50ml=60ml,故选项 A
7 / 8和 B 都错误;实际的溶液浓度应该略大于
0.4mol/L,所以C错误。故应选D。
容量瓶:由瓶体和瓶塞两个部分组成。 学 生 和 通 过 对 课
容量瓶上标有容量的规格(常用的有 老师一起快 堂学习知识的
50mL、100mL、250mL、500mL和1000mL 速回顾本次 总结,帮助同
等 几 种 ) 、 温 度 ( 一 般 标 记 温 度 为 课的学习内 学 们 加 深 印
20℃),容量瓶瓶颈有一根刻度线。 容。 象。
容量瓶的使用:①瓶塞用结实的细绳系
课堂小结
在瓶颈上,以防止损坏或丢失。
②使用前检查容量瓶是否完好,瓶口处
是否漏水。
③使用完毕,应洗净、晾干。
稀释浓溶液:c(浓溶液)·V(浓溶
液) =c(稀溶液)·V(稀溶液)
学 生 在 方 便 学 生
笔记本上对 课后回顾。
板书 板书进行誊
写。
8 / 8