文档内容
课时素养评价 九
氧化钠和过氧化钠
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·聊城高一检测)某同学将Na、Na O、Na O 、Na CO 分别投入盛有足量
2 2 2 2 3
盐酸的1号、2号、3号、4号四支试管中,结果他不会观察到有气泡生成的是
( )
A.1号 B.2号 C.3号 D.4号
2.(2019·南宁高一检测)Na O和Na O 在下列哪一点性质上是相似的( )
2 2 2
A.颜色 B.水溶液的酸碱性
C.氧化性 D.漂白性
3.向装有Na O 的试管中加入一定量水,再滴入2滴酚酞试液,振荡,下列叙述正
2 2
确的是 ( )
A.加水后,用燃着的木条放到试管口,燃着的木条熄灭
B.滴入酚酞溶液先变红,振荡后褪色
C.滴入酚酞溶液,溶液仍为无色D.因为Na O 与酚酞发生氧化还原反应使溶液变为红色
2 2
4.下列反应中,Na O 只表现出氧化性的是 ( )
2 2
A.2Na O +2H O 4NaOH+O ↑
2 2 2 2
B.2Na O +2H SO 2Na SO +2H O+O ↑
2 2 2 4 2 4 2 2
C.Na O +SO Na SO
2 2 2 2 4
D.5Na O +2KMnO +8H SO 5Na SO +K SO +2MnSO +5O ↑+8H O
2 2 4 2 4 2 4 2 4 4 2 2
5.某化工厂突发火灾,仓库内储存的17吨金属钠变成“定时炸弹”,东侧相距
200米的村庄近千人的居民区受到重大威胁。消防官兵到达现场,初步侦察发现,
一栋地上单层砖结构仓库内储存的金属钠起火。金属钠着火时,消防官兵可以
用来灭火的是 ( )
A.水 B.湿抹布盖灭
C.干沙 D.干粉灭火器
6.Na O 具有漂白性,下列关于Na O 的叙述中正确的是 ( )
2 2 2 2
A.Na O 是淡黄色固体,久置于空气中变成Na O
2 2 2
B.Na O 与水的反应中,Na O 只作氧化剂
2 2 2 2C.用Na O 漂白过的织物、麦秆等日久又渐渐变成黄色
2 2
D.Na O 放入饱和NaOH溶液中,放出大量的O ,并有白色固体析出
2 2 2
7.某无色溶液,加入Na O 时有无色无味气体放出,并有白色沉淀生成,该无色溶
2 2
液中含有的物质可能是 ( )
A.CuSO B.MgCl
4 2
C.BaCl D.Fe (SO )
2 2 4 3
8.(2019·长春高一检测)下列各组中的两种物质相互作用时,反应条件(温度、
反应物用量比)改变,不会引起产物的种类改变的是 ( )
A.Na和O B.NaOH和CO
2 2
C.Na O 和CO D.C和O
2 2 2 2
9.向含有HC 、C 、N 、Na+的溶液中加入一定量Na O 后,下列离子的浓度
2 2
减小的是 ( )
A.HC B.C
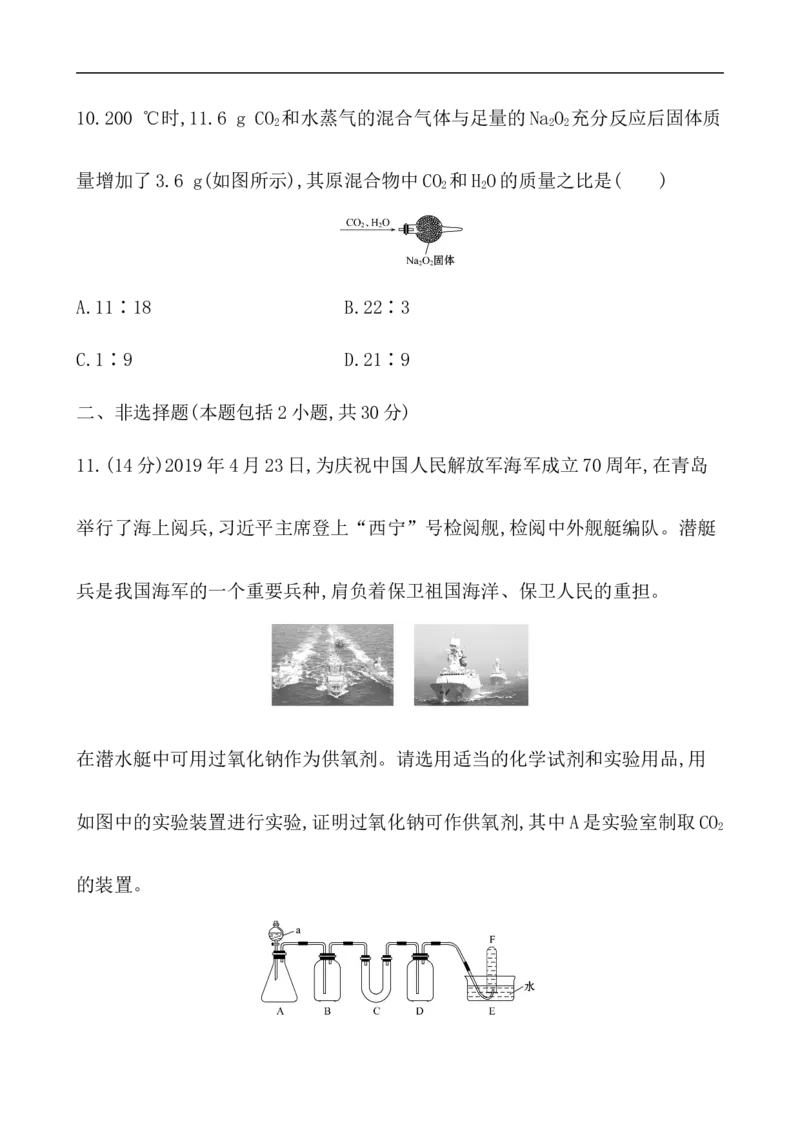
C.N D.Na+10.200 ℃时,11.6 g CO 和水蒸气的混合气体与足量的Na O 充分反应后固体质
2 2 2
量增加了3.6 g(如图所示),其原混合物中CO 和H O的质量之比是( )
2 2
A.11∶18 B.22∶3
C.1∶9 D.21∶9
二、非选择题(本题包括2小题,共30分)
11.(14分)2019年4月23日,为庆祝中国人民解放军海军成立70周年,在青岛
举行了海上阅兵,习近平主席登上“西宁”号检阅舰,检阅中外舰艇编队。潜艇
兵是我国海军的一个重要兵种,肩负着保卫祖国海洋、保卫人民的重担。
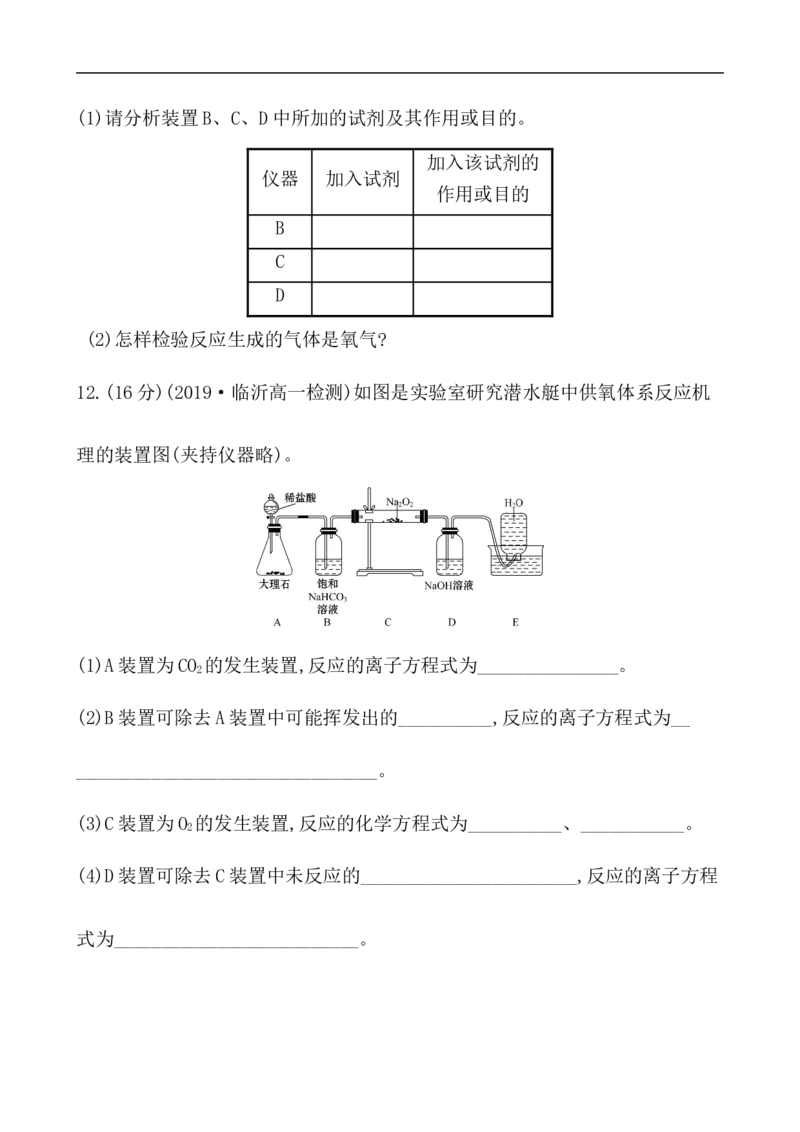
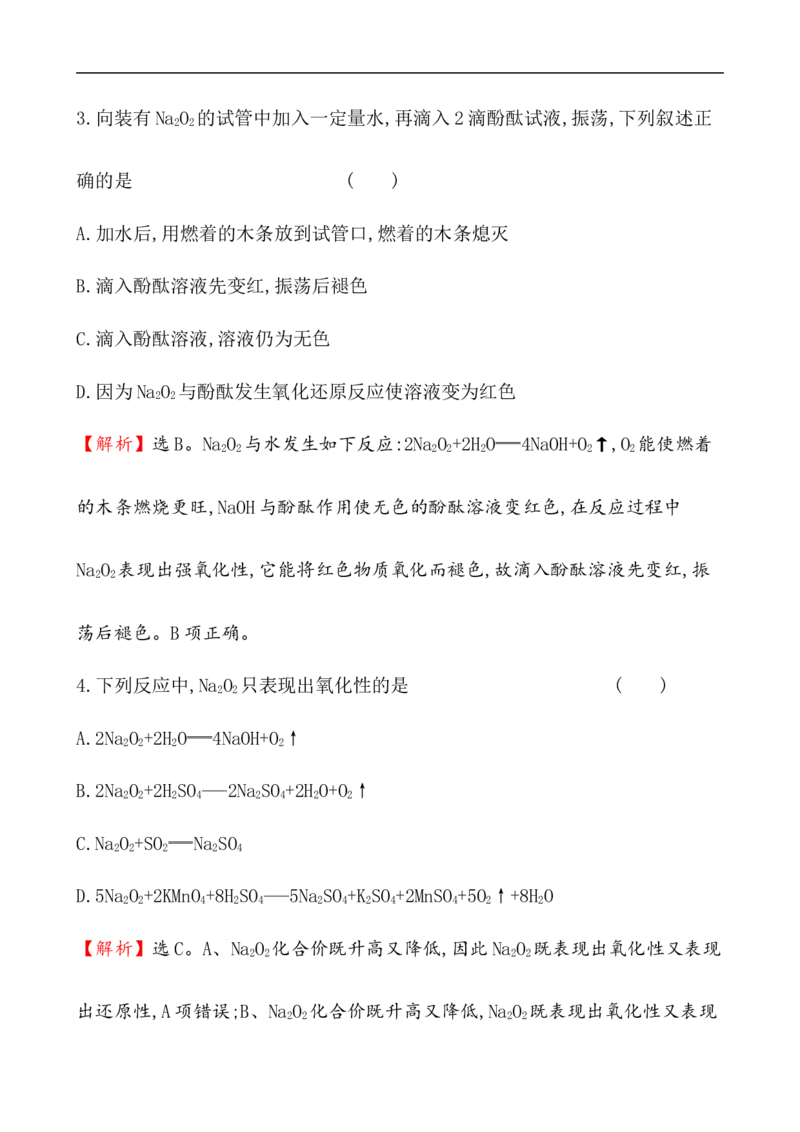
在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用
如图中的实验装置进行实验,证明过氧化钠可作供氧剂,其中A是实验室制取CO
2
的装置。(1)请分析装置B、C、D中所加的试剂及其作用或目的。
加入该试剂的
仪器 加入试剂
作用或目的
B
C
D
(2)怎样检验反应生成的气体是氧气?
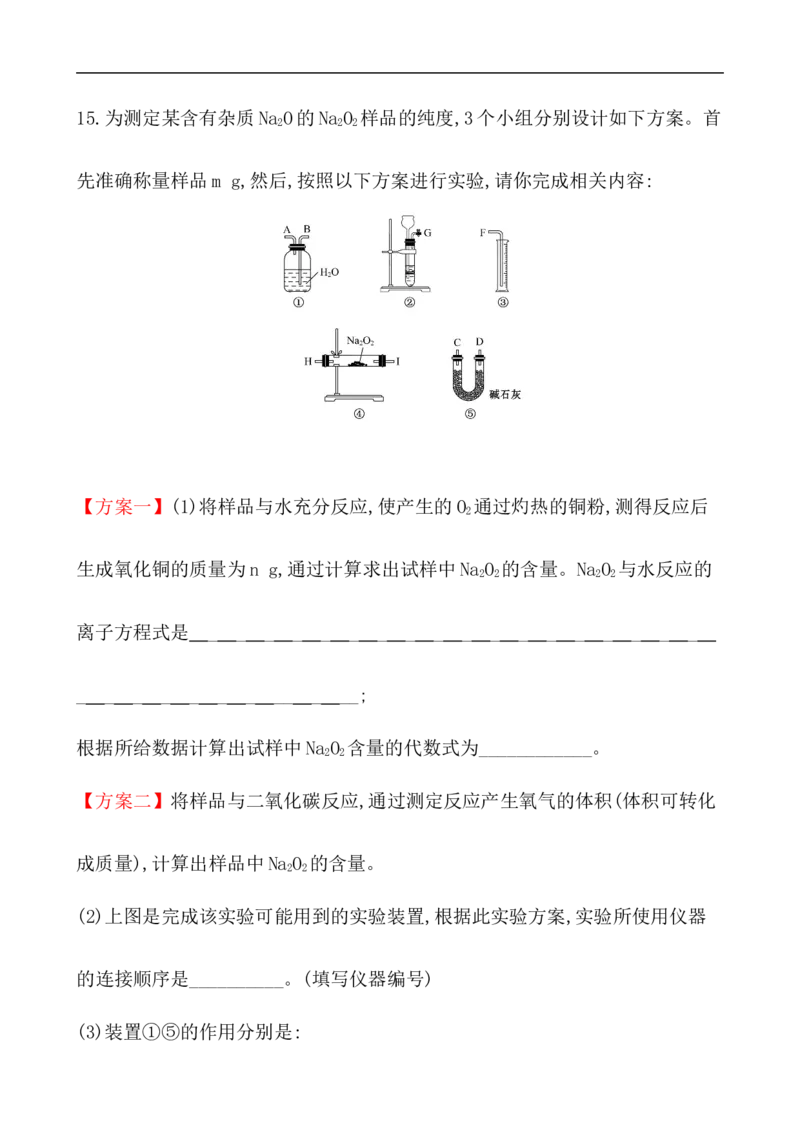
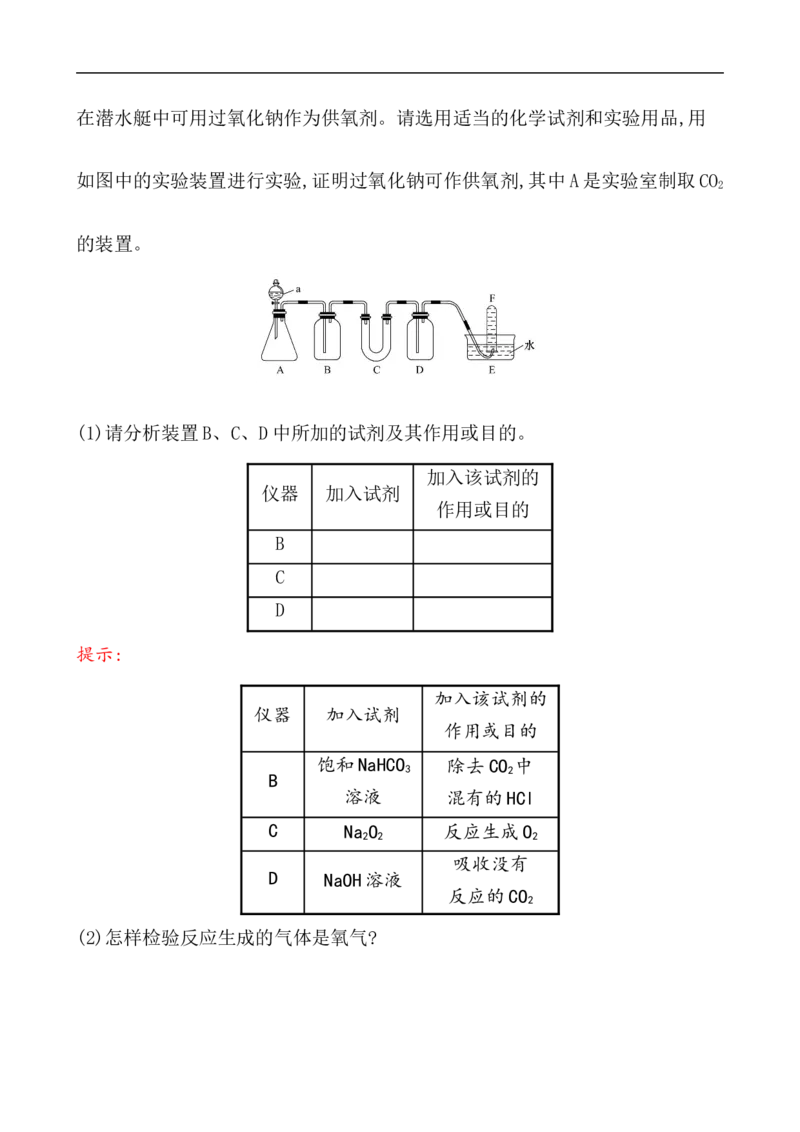
12.(16分)(2019·临沂高一检测)如图是实验室研究潜水艇中供氧体系反应机
理的装置图(夹持仪器略)。
(1)A装置为CO 的发生装置,反应的离子方程式为_______________。
2
(2)B装置可除去A装置中可能挥发出的__________,反应的离子方程式为__
________________________________。
(3)C装置为O 的发生装置,反应的化学方程式为__________、___________。
2
(4)D装置可除去C装置中未反应的_______________________,反应的离子方程
式为__________________________。(5)E装置为排水法收集O 的装置,检验所收集的气体为O 的方法为 _ _ _
2 2
__。
(6)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C
装置中反应后的固体溶于水,向溶液中滴入过量________溶液,若有白色沉淀生
成,则证明固体中含有________;过滤,向滤液中滴入几滴酚酞试液,若________
且不褪色,则证明固体中含有_ _ _ _ _ _ _ _ _ _ _ _ _ _ _
__。
【补偿训练】
兴趣是最好的老师。过氧化钠与水反应的滴水生火实验引起同学们的兴趣,大
家主动探究着火原因。
【猜想】(1)根据燃烧条件,知道脱脂棉是可燃物,小新认为过氧化钠(Na O )与
2 2
水反应生成了可以支持燃烧的物质;小海又进行了补充:此反应还会
________(填“吸收”或“放出”)很多热量,进而满足了燃烧的另一个条件是
____________。
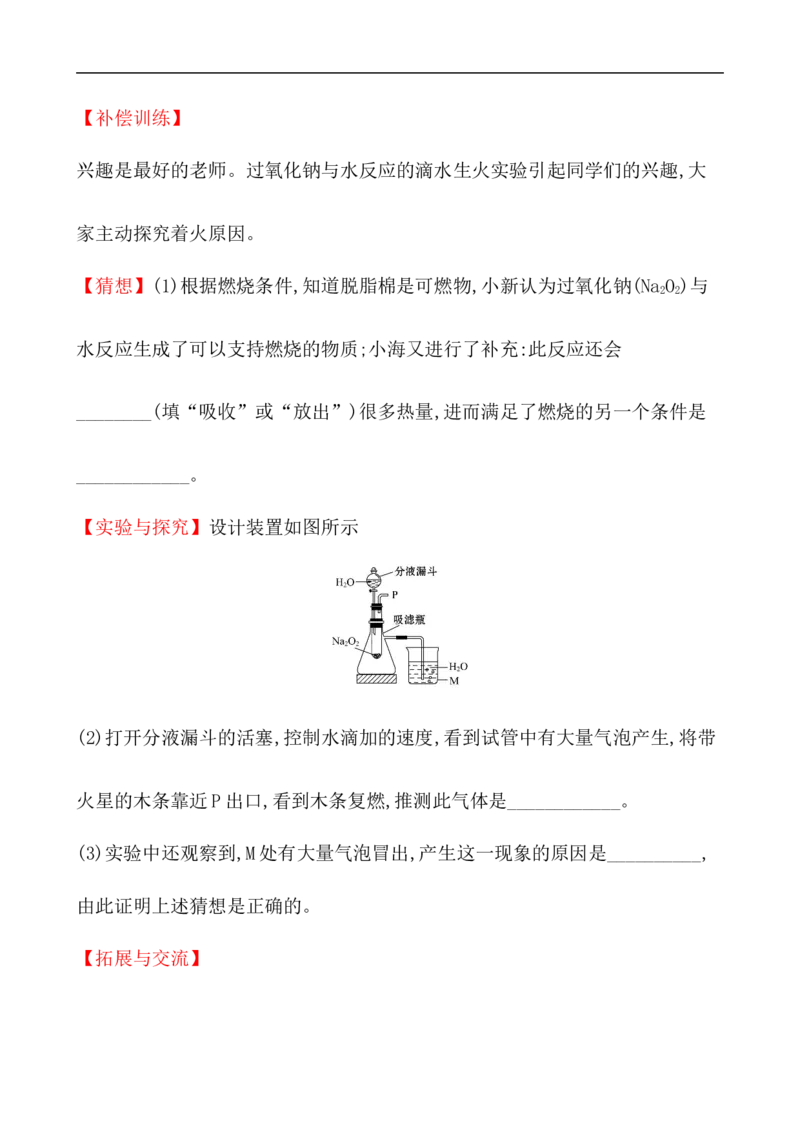
【实验与探究】设计装置如图所示(2)打开分液漏斗的活塞,控制水滴加的速度,看到试管中有大量气泡产生,将带
火星的木条靠近P出口,看到木条复燃,推测此气体是____________。
(3)实验中还观察到,M处有大量气泡冒出,产生这一现象的原因是__________,
由此证明上述猜想是正确的。
【拓展与交流】
(4)完成了以上实验,同学们又进一步探究过氧化钠(Na O )与水反应后生成的另
2 2
一种物质是什么?小新认为是NaOH,小华认为是NaOH和Na CO 的混合物。大家
2 3
经过讨论认为小新的猜想是正确的,不可能生成碳酸钠,判断依据是
____________
______。
(5)根据以上探究,要保证“滴水生火”魔术成功,从燃烧的条件考虑,滴入水的
量要适量,不能太多,也不能太少,则必须做到_________________________。
(20分钟 30分)一、选择题(本题包括2小题,每小题7分,共14分)
13.现将Na O 与过量NaHCO 混合固体在密闭容器中充分加热反应(已知:2NaHCO
2 2 3 3
Na CO +CO ↑+H O),排出气体后最终剩余固体是 ( )
2 3 2 2
A.NaOH和Na O B.NaOH和Na CO
2 2 2 3
C.Na CO D.Na O
2 3 2 2
14.(2019·成都高一检测)过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。
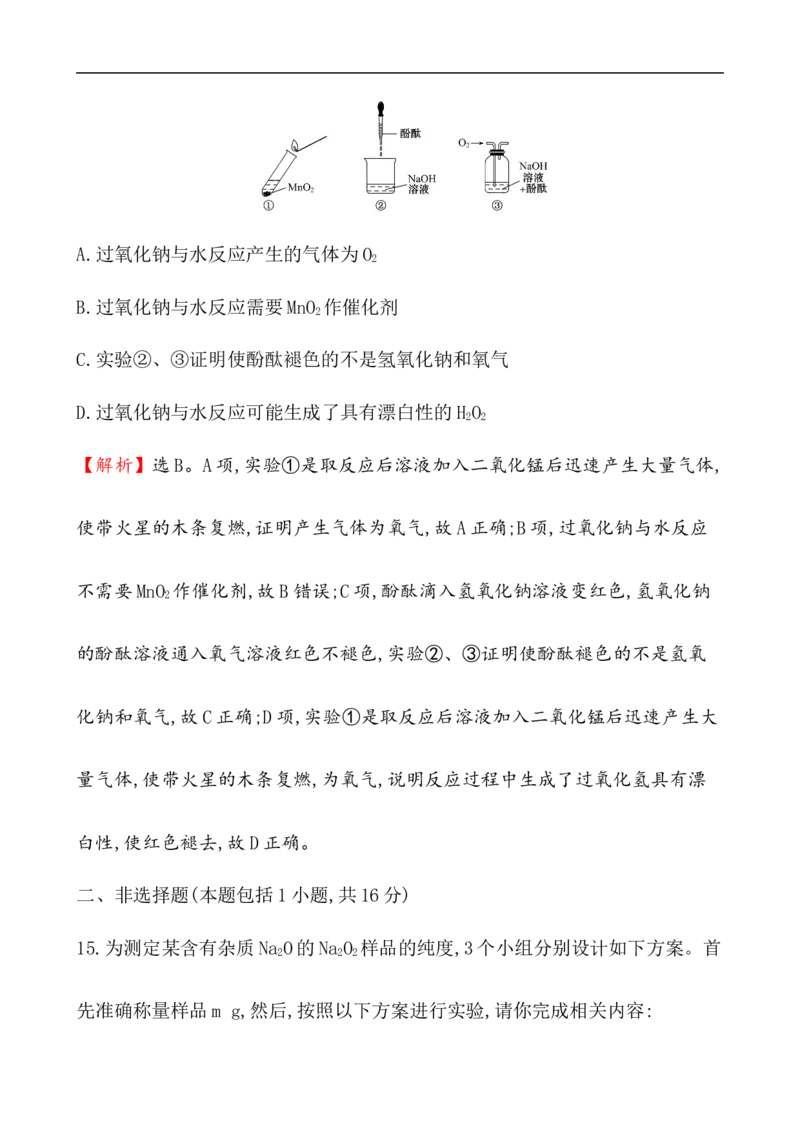
某小组欲探究其原因,进行以下实验:①取反应后溶液加入二氧化锰后迅速产生
大量气体;②、③中红色均不褪去。下列分析错误的是 ( )
A.过氧化钠与水反应产生的气体为O
2
B.过氧化钠与水反应需要MnO 作催化剂
2
C.实验②、③证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的H O
2 2
二、非选择题(本题包括1小题,共16分)15.为测定某含有杂质Na O的Na O 样品的纯度,3个小组分别设计如下方案。首
2 2 2
先准确称量样品m g,然后,按照以下方案进行实验,请你完成相关内容:
【方案一】(1)将样品与水充分反应,使产生的O 通过灼热的铜粉,测得反应后
2
生成氧化铜的质量为n g,通过计算求出试样中Na O 的含量。Na O 与水反应的
2 2 2 2
离子方程式是 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _
_ _ _ _ _ _ _ __ _ __;
根据所给数据计算出试样中Na O 含量的代数式为____________。
2 2
【方案二】将样品与二氧化碳反应,通过测定反应产生氧气的体积(体积可转化
成质量),计算出样品中Na O 的含量。
2 2
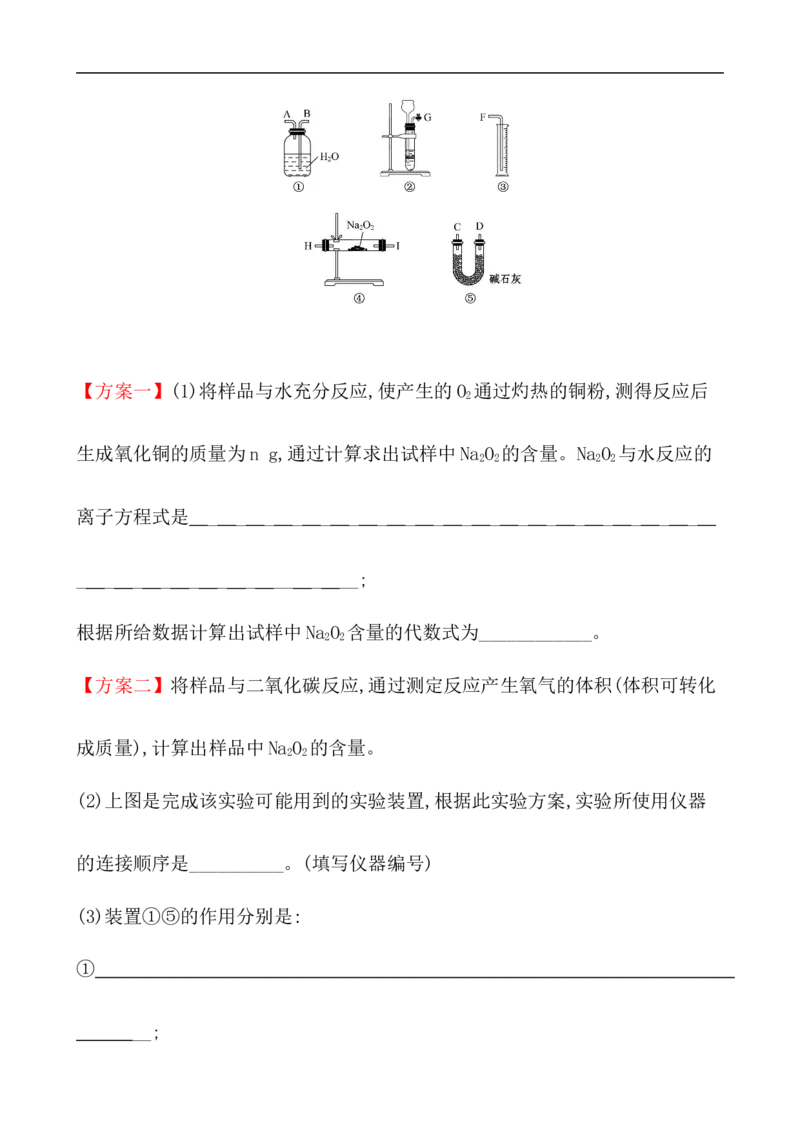
(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器
的连接顺序是__________。(填写仪器编号)
(3)装置①⑤的作用分别是:①
__;
⑤ _
_。课时素养评价 九
氧化钠和过氧化钠
(40分钟 70分)
一、选择题(本题包括10小题,每小题4分,共40分)
1.(2019·聊城高一检测)某同学将Na、Na O、Na O 、Na CO 分别投入盛有足量
2 2 2 2 3
盐酸的1号、2号、3号、4号四支试管中,结果他不会观察到有气泡生成的是
( )
A.1号 B.2号 C.3号 D.4号
【解析】选B。Na、Na O 、Na CO 和盐酸反应分别生成H 、O 和CO 。
2 2 2 3 2 2 2
2.(2019·南宁高一检测)Na O和Na O 在下列哪一点性质上是相似的( )
2 2 2
A.颜色 B.水溶液的酸碱性
C.氧化性 D.漂白性
【解析】选B。Na O为白色固体,无氧化性和漂白性,Na O 为淡黄色固体,具有很
2 2 2
强的氧化性和漂白性,故A、C、D不正确;Na O+H O 2NaOH,2Na O +2H O
2 2 2 2 2
4NaOH+O ↑,两者的水溶液最终都是强碱溶液,故B正确。
23.向装有Na O 的试管中加入一定量水,再滴入2滴酚酞试液,振荡,下列叙述正
2 2
确的是 ( )
A.加水后,用燃着的木条放到试管口,燃着的木条熄灭
B.滴入酚酞溶液先变红,振荡后褪色
C.滴入酚酞溶液,溶液仍为无色
D.因为Na O 与酚酞发生氧化还原反应使溶液变为红色
2 2
【解析】选B。Na O 与水发生如下反应:2Na O +2H O 4NaOH+O ↑,O 能使燃着
2 2 2 2 2 2 2
的木条燃烧更旺,NaOH与酚酞作用使无色的酚酞溶液变红色,在反应过程中
Na O 表现出强氧化性,它能将红色物质氧化而褪色,故滴入酚酞溶液先变红,振
2 2
荡后褪色。B项正确。
4.下列反应中,Na O 只表现出氧化性的是 ( )
2 2
A.2Na O +2H O 4NaOH+O ↑
2 2 2 2
B.2Na O +2H SO 2Na SO +2H O+O ↑
2 2 2 4 2 4 2 2
C.Na O +SO Na SO
2 2 2 2 4
D.5Na O +2KMnO +8H SO 5Na SO +K SO +2MnSO +5O ↑+8H O
2 2 4 2 4 2 4 2 4 4 2 2
【解析】选C。A、Na O 化合价既升高又降低,因此Na O 既表现出氧化性又表现
2 2 2 2
出还原性,A项错误;B、Na O 化合价既升高又降低,Na O 既表现出氧化性又表现
2 2 2 2出还原性,B项错误;C、Na O 化合价降低,所以只表现出氧化性,C项正确;D、
2 2
Na O 化合价只升高,只表现出还原性,D项错误。
2 2
5.某化工厂突发火灾,仓库内储存的17吨金属钠变成“定时炸弹”,东侧相距
200米的村庄近千人的居民区受到重大威胁。消防官兵到达现场,初步侦察发现,
一栋地上单层砖结构仓库内储存的金属钠起火。金属钠着火时,消防官兵可以
用来灭火的是 ( )
A.水 B.湿抹布盖灭
C.干沙 D.干粉灭火器
【解析】选C。钠着火生成Na O ,因为Na O 可以和H O、CO 反应生成氧气,会使
2 2 2 2 2 2
火势更大。湿抹布含H O,干粉灭火器的成分是CO ,均会与Na O 反应。
2 2 2 2
6.Na O 具有漂白性,下列关于Na O 的叙述中正确的是 ( )
2 2 2 2
A.Na O 是淡黄色固体,久置于空气中变成Na O
2 2 2
B.Na O 与水的反应中,Na O 只作氧化剂
2 2 2 2
C.用Na O 漂白过的织物、麦秆等日久又渐渐变成黄色
2 2
D.Na O 放入饱和NaOH溶液中,放出大量的O ,并有白色固体析出
2 2 2【解析】选D。Na O 久置空气中变成Na CO ;Na O 与水反应时,Na O 既是氧化剂
2 2 2 3 2 2 2 2
又是还原剂;利用Na O 的强氧化性漂白过的织物不具有可逆性;Na O 与H O反应
2 2 2 2 2
消耗NaOH溶液中的水,同时生成溶液中的溶质,故有NaOH固体析出。
7.某无色溶液,加入Na O 时有无色无味气体放出,并有白色沉淀生成,该无色溶
2 2
液中含有的物质可能是 ( )
A.CuSO B.MgCl
4 2
C.BaCl D.Fe (SO )
2 2 4 3
【解析】选B。溶液中CuSO 和 Fe (SO ) 有颜色,故A、D两项错误;2Na O +
4 2 4 3 2 2
2H O 4NaOH+O ↑ ,NaOH与MgCl 反应产生白色沉淀,与BaCl 溶液不反应,故
2 2 2 2
B项正确,C项错误。
8.(2019·长春高一检测)下列各组中的两种物质相互作用时,反应条件(温度、
反应物用量比)改变,不会引起产物的种类改变的是 ( )
A.Na和O B.NaOH和CO
2 2
C.Na O 和CO D.C和O
2 2 2 2
【解析】选C。Na和O 反应在常温下产物是Na O,在加热时产物是Na O ,产物与
2 2 2 2
条件有关;NaOH和CO 反应,CO 过量时产物是NaHCO ,CO 少量时产物是Na CO ,产
2 2 3 2 2 3物与用量有关;Na O 和CO 的产物和温度、用量无关;C和O 反应,C过量时产物
2 2 2 2
是CO,C少量时产物是CO ,产物与用量有关。
2
9.向含有HC 、C 、N 、Na+的溶液中加入一定量Na O 后,下列离子的浓度
2 2
减小的是 ( )
A.HC B.C
C.N D.Na+
【解析】选A。由于2Na O +2H O 4NaOH+O ↑,HC 可与OH-发生反应HC +OH-
2 2 2 2
C +H O,因此HC 的浓度减小。
2
【规律方法】Na O 溶于水后生成NaOH,离子共存时考虑与OH-的反应。
2 2
10.200 ℃时,11.6 g CO 和水蒸气的混合气体与足量的Na O 充分反应后固体质
2 2 2
量增加了3.6 g(如图所示),其原混合物中CO 和H O的质量之比是( )
2 2
A.11∶18 B.22∶3
C.1∶9 D.21∶9【解析】选A。向足量的固体Na O 中通入11.6 g CO 和H O,固体只增加3.6 g,
2 2 2 2
令混合物中CO 和水蒸气的质量分别为m(CO )、m(H O),则:
2 2 2
所以m(CO )+m(H O)=11.6 g、 m(CO )+ m(H O)=3.6 g;
2 2 2 2
解得:m(CO )=4.4 g,m(H O)=7.2 g,故原混合物中CO 和H O的质量比为4.4
2 2 2 2
g∶7.2 g=11∶18。
二、非选择题(本题包括2小题,共30分)
11.(14分)2019年4月23日,为庆祝中国人民解放军海军成立70周年,在青岛
举行了海上阅兵,习近平主席登上“西宁”号检阅舰,检阅中外舰艇编队。潜艇
兵是我国海军的一个重要兵种,肩负着保卫祖国海洋、保卫人民的重担。在潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用
如图中的实验装置进行实验,证明过氧化钠可作供氧剂,其中A是实验室制取CO
2
的装置。
(1)请分析装置B、C、D中所加的试剂及其作用或目的。
加入该试剂的
仪器 加入试剂
作用或目的
B
C
D
提示:
加入该试剂的
仪器 加入试剂
作用或目的
饱和NaHCO 除去CO 中
3 2
B
溶液 混有的HCl
C Na O 反应生成O
2 2 2
吸收没有
D NaOH溶液
反应的CO
2
(2)怎样检验反应生成的气体是氧气?提示:将试管F从水槽中取出,用带火星的木条伸入试管F内,木条复燃,则证明
该气体是氧气。
12.(16分)(2019·临沂高一检测)如图是实验室研究潜水艇中供氧体系反应机
理的装置图(夹持仪器略)。
(1)A装置为CO 的发生装置,反应的离子方程式为_______________。
2
(2)B装置可除去A装置中可能挥发出的__________,反应的离子方程式为__
________________________________。
(3)C装置为O 的发生装置,反应的化学方程式为__________、___________。
2
(4)D装置可除去C装置中未反应的_______________________,反应的离子方程
式为__________________________。
(5)E装置为排水法收集O 的装置,检验所收集的气体为O 的方法为 _ _ _
2 2
__。
(6)C装置中固体由淡黄色完全变为白色,检验固体成分的实验方案为取少量C
装置中反应后的固体溶于水,向溶液中滴入过量________溶液,若有白色沉淀生成,则证明固体中含有________;过滤,向滤液中滴入几滴酚酞试液,若________
且不褪色,则证明固体中含有_ _ _ _ _ _ _ _ _ _ _ _ _ _ _
__。
【解析】(1)实验室用稀盐酸与大理石反应制取CO 。(2)制得的CO 中混有
2 2
HCl,通过饱和NaHCO 溶液除去CO 中的HCl。(3)从B装置中出来的CO 中含有水
3 2 2
蒸气,通过C装置时CO 、H O均能与Na O 反应产生氧气。(4)D装置中NaOH溶液
2 2 2 2
的作用是除去CO 。(5)利用带火星的木条检验氧气。(6)C装置中反应后的固体
2
可能含有NaOH、Na CO ,先加入过量CaCl 溶液检验并除去Na CO ,过滤后加入酚
2 3 2 2 3
酞溶液检验NaOH。
答案:(1)CaCO +2H+ Ca2++H O+CO ↑
3 2 2
(2)HCl HC +H+ H O+CO ↑
2 2
(3)2Na O +2CO 2Na CO +O
2 2 2 2 3 2
2Na O +2H O 4NaOH+O ↑ (4)CO 2OH-+CO C +H O (5)取出集气瓶正放
2 2 2 2 2 2 2
于桌面上,将一根带火星的木条伸入集气瓶中,若木条复燃,证明所收集的气体
为O (6)CaCl Na CO 溶液变红 NaOH
2 2 2 3【补偿训练】
兴趣是最好的老师。过氧化钠与水反应的滴水生火实验引起同学们的兴趣,大
家主动探究着火原因。
【猜想】(1)根据燃烧条件,知道脱脂棉是可燃物,小新认为过氧化钠(Na O )与
2 2
水反应生成了可以支持燃烧的物质;小海又进行了补充:此反应还会
________(填“吸收”或“放出”)很多热量,进而满足了燃烧的另一个条件是
____________。
【实验与探究】设计装置如图所示
(2)打开分液漏斗的活塞,控制水滴加的速度,看到试管中有大量气泡产生,将带
火星的木条靠近P出口,看到木条复燃,推测此气体是____________。
(3)实验中还观察到,M处有大量气泡冒出,产生这一现象的原因是__________,
由此证明上述猜想是正确的。
【拓展与交流】(4)完成了以上实验,同学们又进一步探究过氧化钠(Na O )与水反应后生成的另
2 2
一种物质是什么?小新认为是NaOH,小华认为是NaOH和Na CO 的混合物。大家
2 3
经过讨论认为小新的猜想是正确的,不可能生成碳酸钠,判断依据是
____________
______。
(5)根据以上探究,要保证“滴水生火”魔术成功,从燃烧的条件考虑,滴入水的
量要适量,不能太多,也不能太少,则必须做到_________________________。
【解析】(1)根据物质燃烧的条件:脱脂棉是可燃物,小新认为过氧化钠(Na O )
2 2
与水反应生成了可以支持燃烧的物质,棉花要燃烧还需达到其着火点,据此分析。
(2)用带火星的木条靠近P出口,木条复燃,说明该气体具有助燃性,是氧气。
(3)M处有大量气泡冒出,可能生成了气体,也可能气体的温度升高,通过分析没
有生成气体,只能是锥形瓶中的气体温度升高,故可知过氧化钠与水反应放热使
锥形瓶内压强增大。
(4)过氧化钠(Na O )与水反应后生成的另一种物质不可能是NaOH和Na CO 的混
2 2 2 3
合物,根据质量守恒定律,反应物中不含有碳元素,故不可能生成碳酸钠。
(5)水不能太多,因为水能灭火,所以要使魔术成功必须控制反应物用量。答案:(1)放出 温度达到着火点 (2)氧气 (3)过氧化钠与水反应放热使锥形
瓶内压强增大 (4)质量守恒定律 (5)控制反应物的用量
(20分钟 30分)
一、选择题(本题包括2小题,每小题7分,共14分)
13.现将Na O 与过量NaHCO 混合固体在密闭容器中充分加热反应(已知:2NaHCO
2 2 3 3
Na CO +CO ↑+H O),排出气体后最终剩余固体是 ( )
2 3 2 2
A.NaOH和Na O B.NaOH和Na CO
2 2 2 3
C.Na CO D.Na O
2 3 2 2
【解析】选C。加热时碳酸氢钠分解生成二氧化碳和水,二氧化碳和水与过氧化
钠反应,当碳酸氢钠过量时,生成二氧化碳、水均过量,则反应后生成的固体中
不可能存在过氧化钠,可以为过氧化钠先与二氧化碳反应,后与水反应,因CO 过
2
量,故NaOH不一定存在。
14.(2019·成都高一检测)过氧化钠与水反应后滴加酚酞,酚酞先变红后褪色。
某小组欲探究其原因,进行以下实验:①取反应后溶液加入二氧化锰后迅速产生
大量气体;②、③中红色均不褪去。下列分析错误的是 ( )A.过氧化钠与水反应产生的气体为O
2
B.过氧化钠与水反应需要MnO 作催化剂
2
C.实验②、③证明使酚酞褪色的不是氢氧化钠和氧气
D.过氧化钠与水反应可能生成了具有漂白性的H O
2 2
【解析】选B。A项,实验①是取反应后溶液加入二氧化锰后迅速产生大量气体,
使带火星的木条复燃,证明产生气体为氧气,故A正确;B项,过氧化钠与水反应
不需要MnO 作催化剂,故B错误;C项,酚酞滴入氢氧化钠溶液变红色,氢氧化钠
2
的酚酞溶液通入氧气溶液红色不褪色,实验②、③证明使酚酞褪色的不是氢氧
化钠和氧气,故C正确;D项,实验①是取反应后溶液加入二氧化锰后迅速产生大
量气体,使带火星的木条复燃,为氧气,说明反应过程中生成了过氧化氢具有漂
白性,使红色褪去,故D正确。
二、非选择题(本题包括1小题,共16分)
15.为测定某含有杂质Na O的Na O 样品的纯度,3个小组分别设计如下方案。首
2 2 2
先准确称量样品m g,然后,按照以下方案进行实验,请你完成相关内容:【方案一】(1)将样品与水充分反应,使产生的O 通过灼热的铜粉,测得反应后
2
生成氧化铜的质量为n g,通过计算求出试样中Na O 的含量。Na O 与水反应的
2 2 2 2
离子方程式是 _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _
_ _ _ _ _ _ _ __ _ __;
根据所给数据计算出试样中Na O 含量的代数式为____________。
2 2
【方案二】将样品与二氧化碳反应,通过测定反应产生氧气的体积(体积可转化
成质量),计算出样品中Na O 的含量。
2 2
(2)上图是完成该实验可能用到的实验装置,根据此实验方案,实验所使用仪器
的连接顺序是__________。(填写仪器编号)
(3)装置①⑤的作用分别是:
①
__;⑤ _
_。
【解析】(1)根据:2Cu+O 2CuO
2
及2Na O +2H O 4NaOH+O ↑
2 2 2 2
得关系式:Na O ~ CuO
2 2
78 g 80 g
m(Na O ) n g
2 2
解得:m(Na O )= g,则样品中Na O 的含量= ×100%或 ×100%。
2 2 2 2
(2)测定某含有杂质Na O的Na O 样品的纯度,方法是利用装置②制备二氧化碳
2 2 2
气体,把生成的二氧化碳气体通过装置④与过氧化钠充分反应,生成的气体通过
装置⑤盛碱石灰的干燥管,除去二氧化碳,用装置①③排水法测量氧气的体积,
根据氧气的体积便可知样品中过氧化钠的质量,综上所述,装置的连接顺序是
②④⑤①③。
(3)应用排水法测定氧气的体积。氧气中混有二氧化碳气体,为准确测量生成的
氧气的体积,应用碱石灰吸收二氧化碳。
答案:(1)2Na O +2H O 4Na++4OH-+O ↑ ×100%或 ×100%
2 2 2 2(2)②④⑤①③
(3)①排水法收集O ⑤除去O 中混有的CO 气体
2 2 2