文档内容
课时素养评价 十
碳酸钠和碳酸氢钠 焰色试验
(40分钟 70分)
一、选择题(本题包括8小题,每小题5分,共40分)
1.某物质灼烧时焰色试验为黄色,下列判断正确的是 ( )
A.该物质一定是钠的化合物
B.该物质一定含钠元素
C.该物质一定是金属钠
D.该物质中一定含钠离子
2.(2019·昆明高一检测)焰色试验实验过程中铂丝的清洗和灼烧与钾焰色试验
的观察两项操作如图所示:
下列叙述中不正确的是 ( )
A.每次实验中都要先将铂丝灼烧至与原来的火焰颜色相同,再蘸取被检验物质
B.钾的焰色试验要透过蓝色钴玻璃观察C.实验时最好选择本身颜色较深的火焰
D.没有铂丝可用无锈铁丝代替进行实验
3.(2019·衡阳高一检测)我国医学家通过研究发现小苏打可去除肿瘤内的氢离
子,从而快速有效地杀死处于葡萄糖饥饿或缺乏状态的肿瘤细胞,为治疗原发性
肝癌开辟了新路径。下列有关小苏打的说法错误的是 ( )
A.可用于制备苏打
B.可用于糕点生产中
C.与H+作用易产生CO
2
D.可用饱和食盐水与CO 反应制得
2
4.下列有关NaHCO 与Na CO 的说法中,正确的是 ( )
3 2 3
A.分别加热两种样品,没有残留物质的是NaHCO
3
B.分别配成溶液,再加入澄清石灰水,无白色沉淀生成的是NaHCO
3
C.分别与完全相同的盐酸反应,产生CO 的速率Na CO NaHCO ,故C正确;由反应Na CO +Ca(OH) CaCO ↓+2NaOH、
2 3 3 2 3 2 3
2NaHCO +Ca(OH) Na CO +CaCO ↓+2H O可知,澄清的石灰水与碳酸钠、碳酸氢
3 2 2 3 3 2
钠反应都生成白色沉淀碳酸钙,故D错误。
二、非选择题(本题包括2小题,共30分)
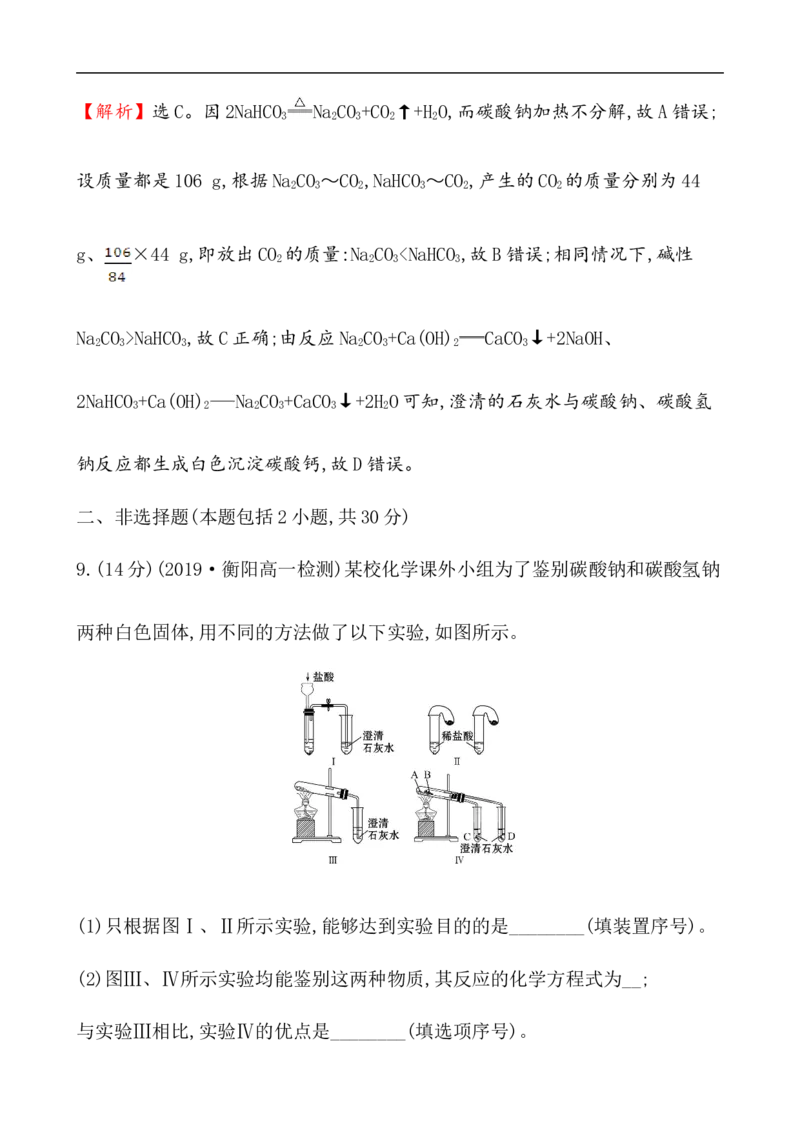
9.(14分)(2019·衡阳高一检测)某校化学课外小组为了鉴别碳酸钠和碳酸氢钠
两种白色固体,用不同的方法做了以下实验,如图所示。
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是________(填装置序号)。
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为__;
与实验Ⅲ相比,实验Ⅳ的优点是________(填选项序号)。A.Ⅳ比Ⅲ复杂
B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便
D.Ⅳ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是
________(填化学式)。
【解析】(1)Na CO 、NaHCO 均能与盐酸反应生成使澄清石灰水变浑浊的CO 气
2 3 3 2
体,但等质量的Na CO 与NaHCO 跟过量盐酸反应时,NaHCO 与盐酸反应更剧烈且
2 3 3 3
产生气体的量多,故实验Ⅰ不能鉴别Na CO 与NaHCO ,而实验Ⅱ可以。
2 3 3
(2)NaHCO 受热易分解:2NaHCO Na CO +CO ↑+H O,Na CO 受热不分解,可用加热
3 3 2 3 2 2 2 3
方法鉴别,对比实验Ⅲ,实验Ⅳ可以同时进行两个对比实验,现象明显。
(3)将NaHCO 置于小试管B中,Na CO 置于大试管A中,加热时D中澄清石灰水不
3 2 3
变浑浊,C中变浑浊,说明Na CO 比NaHCO 稳定。
2 3 3
答案:(1)Ⅱ
(2)2NaHCO Na CO +CO ↑+H O D
3 2 3 2 2
(3)NaHCO
310.(16分) (2019·福州高一检测)某校课外小组为测定某碳酸钠和碳酸氢钠混
合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验。
方案Ⅰ:甲组同学用质量法,按如图所示的实验流程进行实验:
称量样品 加入适量盐酸 蒸发结晶 称量固体
(1)实验时,蒸发结晶操作中,除了酒精灯外,还要用到的仪器是________。
(2)有同学认为“加入适量盐酸”不好操控,应改为“过量盐酸”,便于操作且
不影响测定的准确性,该观点_______________(填“正确”或“不正确”),其
原因是__ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ _ __。
(3)若实验中测得样品质量为46.4 g,固体质量为40.95 g,则碳酸钠的质量分数
为________(保留3位有效数字)。
(4)蒸发结晶过程中若有固体飞溅,测得碳酸钠的质量分数________(填“偏
大”“偏小”或“无影响”)。
方案Ⅱ:乙组同学的主要实验流程如下。
按如图所示装置进行实验:(5)在装置C中装碱石灰来吸收净化后的气体,装置D的作用是____________。
(6)有的同学认为为了减少实验误差,应在反应前后都通入N ,反应后通入N 的
2 2
目的是 _________________________。
【解析】(1)蒸发结晶操作中用到的仪器为酒精灯、蒸发皿、玻璃棒。(2)改为
“过量盐酸”正确,因盐酸易挥发,过量的盐酸在加热过程中挥发,不影响结果。
(3)设碳酸钠的质量为x g,碳酸氢钠的质量为y g,
则x+y=46.4
由Na CO ~2NaCl NaHCO ~NaCl
2 3 3
x+ y=40.95
x=21.2 y=25.2;碳酸钠的质量分数为
×100%≈45.7%。
(4)由于碳酸钠中钠的质量分数大于碳酸氢钠,所以蒸发结晶过程中若有固体飞
溅,测得碳酸钠的质量分数偏小。(5)方案Ⅱ是根据二氧化碳的质量测碳酸钠的
质量分数的,D装置的作用是吸收空气中的水蒸气和二氧化碳,以确保U形管中质量增加的准确性。(6)反应后通入N 的目的是将A、B装置中残留的CO 全部
2 2
赶入C装置的碱石灰中,减小实验误差。
答案:(1)蒸发皿、玻璃棒
(2)正确 盐酸易挥发,过量的盐酸在加热过程中挥发,不影响结果 (3)45.7%
(4)偏小
(5)吸收空气中的水蒸气和二氧化碳,以确保U形管中质量增加量的准确性
(6)将A、B装置中残留的CO 全部赶入C装置的碱石灰中,减小实验误差
2
(20分钟 30分)
一、选择题(本题包括2小题,每小题7分,共14分)
11.有两个无标签的试剂瓶,分别装有Na CO 和NaHCO 固体,有4位同学为鉴别它
2 3 3
们采用了以下不同的方法,其中不可行的是 ( )
A.分别配成溶液,再加入澄清石灰水
B.分别配成溶液,再加入CaCl 溶液
2
C.分别加热,再检验是否有使澄清石灰水变浑浊的气体产生
D.分别取固体样品,滴加同浓度盐酸,观察产生气泡的快慢【解析】选A。A中的石灰水与Na CO 和NaHCO 皆能发生反应产生CaCO 沉淀;B
2 3 3 3
中CaCl 与NaHCO 不反应,与Na CO 反应产生CaCO 沉淀;C中加热时,只有NaHCO
2 3 2 3 3 3
受热分解,2NaHCO Na CO +H O+CO ↑,产生的CO 能使澄清石灰水变浑浊,故可
3 2 3 2 2 2
用来鉴别;D中NaHCO 与盐酸反应速率比Na CO 快。
3 2 3
【补偿训练】
(2019·温州高一检测)下列有关纯碱和小苏打的叙述中,正确的是 ( )
A.Na CO 和NaHCO 都既能与盐酸反应,又能与氢氧化钠溶液反应
2 3 3
B.等质量的Na CO 、NaHCO 分别与相同浓度的盐酸反应,NaHCO 消耗的盐酸体积
2 3 3 3
少
C.向NaHCO 溶液中滴入Ba(OH) 溶液无沉淀,而向Na CO 溶液中加入Ba(OH) 溶
3 2 2 3 2
液出现白色沉淀
D.个数相同的Na CO 、NaHCO 分别与足量稀硫酸反应,NaHCO 产生的CO 多
2 3 3 3 2
【解析】选B。Na CO 与盐酸反应生成二氧化碳,不与氢氧化钠反应,NaHCO 属于
2 3 3
弱酸弱碱盐,既能与盐酸反应生成CO 气体,又能与氢氧化钠反应生成盐,故A错
2
误;由方程式Na CO +2HCl 2NaCl+CO ↑+H O,NaHCO +HCl NaCl+CO ↑+H O可
2 3 2 2 3 2 2知,等质量的Na CO 、NaHCO 分别与相同浓度的盐酸反应,NaHCO 消耗的盐酸体
2 3 3 3
积少,故B正确;Na CO 和NaHCO 都与Ba(OH) 溶液反应生成沉淀:Ba(OH) +Na CO
2 3 3 2 2 2 3
BaCO ↓+2NaOH,2NaHCO +Ba(OH) BaCO ↓+Na CO +2H O(NaHCO 足量),故C
3 3 2 3 2 3 2 3
错误;分别与足量稀硫酸反应,反应的离子方程式为:C +2H+ CO ↑+H O、HC
2 2
+H+ H O+CO ↑,所以个数相同的Na CO 、NaHCO 分别与足量稀硫酸反应,产
2 2 2 3 3
生的CO 一样多,故D错误。
2
12.(2019·郑州高一检测)将NaHCO 置于干燥的试管中加热,并使放出的气体依
3
次通过盛有足量过氧化钠和碱石灰的干燥管,最后得到的气体有 ( )
A.CO 、H O B.H O、O
2 2 2 2
C.CO 、O D.O
2 2 2
【解析】选D。2NaHCO Na CO +CO ↑+H O,所以分解产生CO 和水蒸气,依次通
3 2 3 2 2 2
过盛有足量过氧化钠和碱石灰的干燥管,CO 与水蒸气都与足量过氧化钠反应产
2
生氧气,故最终是氧气。
【补偿训练】加热10.0 g碳酸钠和碳酸氢钠的固体混合物至质量不再发生变化,剩余固
体的质量为8.45 g,则混合物中碳酸钠的质量分数为( )
A.42% B.58% C.36% D.64%
【解析】选B。由NaHCO 受热分解的化学方程式可知:
3
2NaHCO Na CO +CO +H O 质量减轻
3 2 3 2 2
168 62
m(NaHCO ) (10.0-8.45) g
3
则 = ,解得m(NaHCO )=4.2 g。
3
则Na CO 的质量分数= ×100%=58%。
2 3
【规律方法】“差量法”在解题中的应用
根据化学反应前后物质的有关物理量发生的变化,找出所谓“理论差量”,如反
应前后的质量、气体体积的差量等。该差量的大小与反应物质的有关量成正比。
差量法就是借助这种比例关系,解决一定量变的计算题的方法。
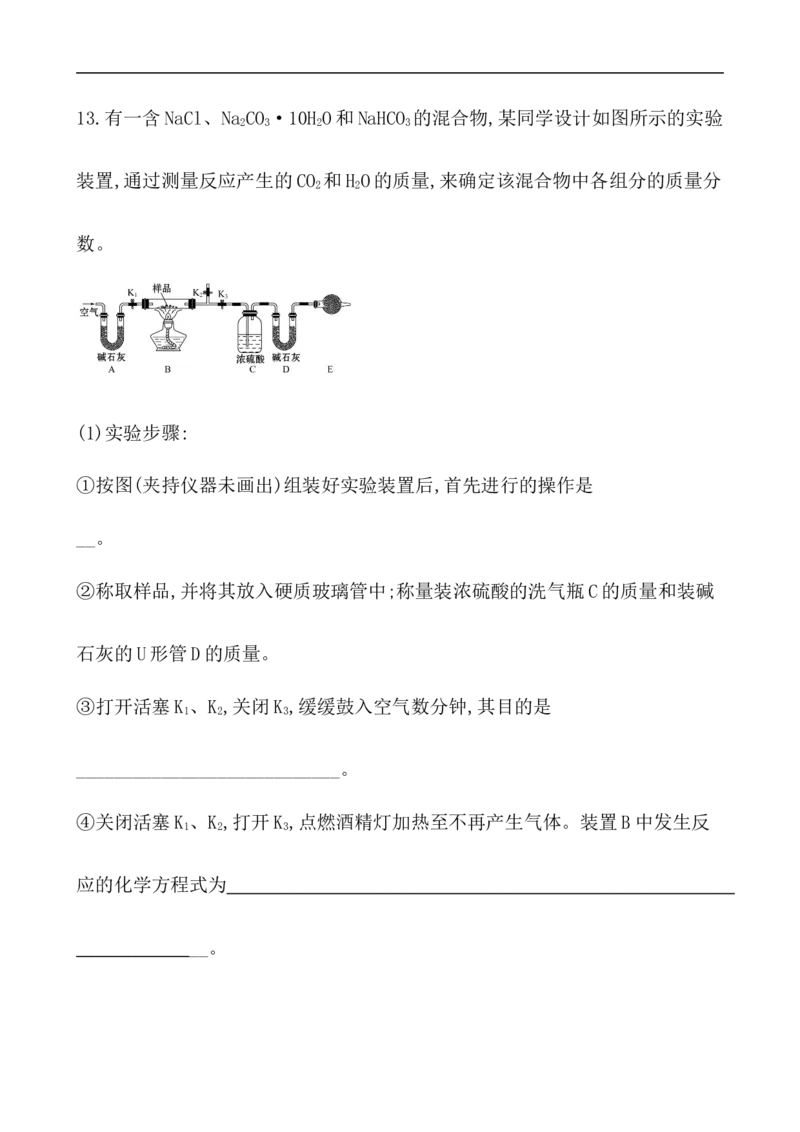
二、非选择题(本题包括1小题,共16分)13.有一含NaCl、Na CO ·10H O和NaHCO 的混合物,某同学设计如图所示的实验
2 3 2 3
装置,通过测量反应产生的CO 和H O的质量,来确定该混合物中各组分的质量分
2 2
数。
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是
__。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱
石灰的U形管D的质量。
③打开活塞K 、K ,关闭K ,缓缓鼓入空气数分钟,其目的是
1 2 3
____________________________。
④关闭活塞K 、K ,打开K ,点燃酒精灯加热至不再产生气体。装置B中发生反
1 2 3
应的化学方程式为
__。⑤打开活塞K ,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和
1
U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是
__。
②E处干燥管中盛放的药品是碱石灰,其作用是____________________,如果实
验中没有该装置,则会导致测量结果NaHCO 的质量____________________
3
(填“偏大”“偏小”或“无影响”)。
③若样品质量为w g,反应后C、D装置增加的质量分别为m g、m g,则混合物
1 2
中Na CO ·10H O的质量分数为________(用含w、m 、m 的代数式表示)。
2 3 2 1 2
【解析】(1)①组装好实验装置后首先应检查装置气密性。③由于装置中存在
CO 和水蒸气,应先除去装置中的CO 和水蒸气。④由物质的性质可知,在加热时
2 2
该装置中发生的反应为2NaHCO Na CO +H O+CO ↑、Na CO ·10H O
3 2 3 2 2 2 3 2
Na CO +10H O↑。
2 3 2
(2)①加热后有部分CO 和水蒸气会残留在装置中,必须鼓入空气使其完全被吸
2
收,若不鼓入空气,则测得的NaHCO 和Na CO ·10H O的质量分数偏小,NaCl的质
3 2 3 2量分数偏大。②装置E是防止空气中的CO 和水蒸气进入装置D,如果没有该装
2
置,会使测得的NaHCO 的质量偏大。③由题目信息知,反应放出的CO 的质量为
3 2
m g,根据反应的化学方程式2NaHCO Na CO +H O+CO ↑,可计算出该反应中产
2 3 2 3 2 2
生的水的质量为 g,从而计算出Na CO ·10H O分解产生水的质量为(m -
2 3 2 1
) g,再根据Na CO ·10H O Na CO +10H O↑,计算出Na CO ·10H O的质量,
2 3 2 2 3 2 2 3 2
最后计算出混合物中Na CO ·10H O的质量分数。
2 3 2
答案:(1)①检查装置气密性 ③除去装置中的水蒸气和二氧化碳
④2NaHCO Na CO +H O+CO ↑,
3 2 3 2 2
Na CO ·10H O Na CO +10H O↑
2 3 2 2 3 2
(2)①Na CO ·10H O和NaHCO 的质量分数测定结果偏小,NaCl的质量分数测定结
2 3 2 3
果偏大
②防止空气中的CO 和水蒸气进入D中影响测定结果 偏大 ③
2
×100%