文档内容
键的极性和分子的极性
重难点 题型 分值
1. 了解极性共价键和非极性共价键、极性
分子和非极性分子的概念;
2. 了解化学键的极性与分子的极性的关
重点
系;
3. 结合常见物质分子立体结构,判断极性
选择题 2-4分
分子和非极性分子;
1. 掌握化学键的极性与分子的极性的关
系;
难点
2. 结合常见物质分子立体结构,判断极性
分子和非极性分子;
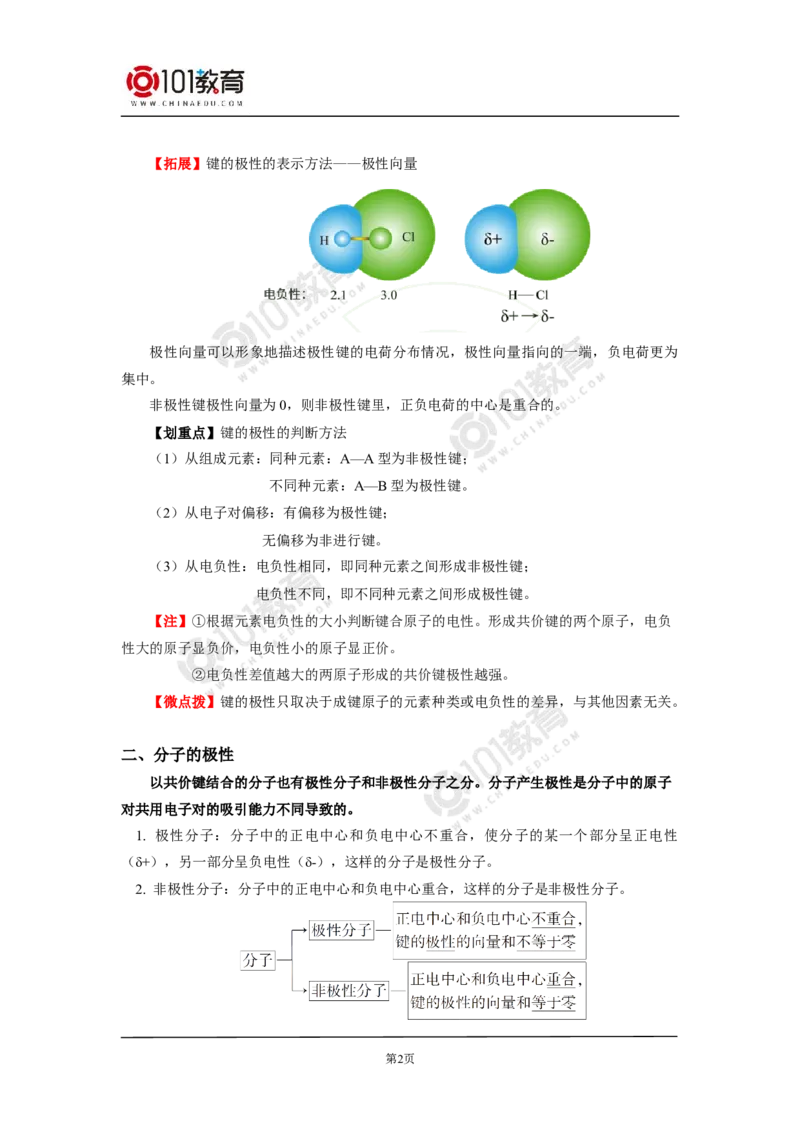
一、键的极性
分类 极性共价键 非极性共价键
成键原子 不同种原子 同种原子
电子对 发生偏移 不发生偏移
成键原子 一个原子呈正电性(δ+) 呈电中性
的电性 一个原子呈负电性(δ-)
示例 H—Cl、N—H等 H—H、O—O 等
第1页【拓展】键的极性的表示方法——极性向量
极性向量可以形象地描述极性键的电荷分布情况,极性向量指向的一端,负电荷更为
集中。
非极性键极性向量为0,则非极性键里,正负电荷的中心是重合的。
【划重点】键的极性的判断方法
(1)从组成元素:同种元素:A—A型为非极性键;
不同种元素:A—B型为极性键。
(2)从电子对偏移:有偏移为极性键;
无偏移为非进行键。
(3)从电负性:电负性相同,即同种元素之间形成非极性键;
电负性不同,即不同种元素之间形成极性键。
【注】①根据元素电负性的大小判断键合原子的电性。形成共价键的两个原子,电负
性大的原子显负价,电负性小的原子显正价。
②电负性差值越大的两原子形成的共价键极性越强。
【微点拨】键的极性只取决于成键原子的元素种类或电负性的差异,与其他因素无关。
二、分子的极性
以共价键结合的分子也有极性分子和非极性分子之分。分子产生极性是分子中的原子
对共用电子对的吸引能力不同导致的。
1. 极性分子:分子中的正电中心和负电中心不重合,使分子的某一个部分呈正电性
(δ+),另一部分呈负电性(δ-),这样的分子是极性分子。
2. 非极性分子:分子中的正电中心和负电中心重合,这样的分子是非极性分子。
第2页【典型例子】极性分子:①不同元素的双原子分子:H-Cl,H-F等。
②折线形分子:HS、HO等。
2 2
③三角锥形分子:NH 等。
3
非极性分子:①同种元素的双原子分子:H、Cl,N 等。
2 2 2
②只含极性键但空间构型对称的多原子分子:CO、CS、BF、CH、CCl 等。
2 2 3 4 4
③同时含有极性键、非极性键的对称分子:CH=CH 、CH CH、 。
2 2
三、分子极性的判断
要对分子极性进行判断,也可用极性向量。分子的极性是分子中化学键的极性的向量
和。极性向量的矢量和指向的一端,负电荷更为集中。若分子中各个键的极性的向量和为
零,为非极性分子,否则为极性分子。例如,HC1分子中,共用电子对偏向Cl原子,所以
Cl原子一端相对显负电性,H原子一端相对显正电性,极性向量矢量和指向Cl原子,整个
分子的电荷分布不均匀,所以HC1为极性分子。这样以极性键结合的双原子分子为极性分
子。
再如,Cl 分子中,共用电子对不偏向,电荷分布均匀,为非进行分子。这样以非极性
2
键结合的双原子分子均为非极性分子。
【拓展】CO 分子极性的判断
2
C=O键是极性键,C呈正电性,O呈负电性;根据VSEPR理论,可得出CO 是直线形
2
分子,两个C=O键对称排列,两键的极性的向量和为零,意味着键的极性互相抵消;整个
分子没有极性,电荷分布均匀,因此CO 是非极性分子。
2
【想一想】已知HO 的分子空间结构可在二面角中表示,如图所示:
2 2
(1)分析HO 分子中共价键的种类有哪些?
2 2
第3页【提示】HO 分子中H—O为极性共价键,O—O为非极性共价键。
2 2
(2)HO 属于极性分子还是非极性分子?
2 2
【提示】HO 分子中正电、负电中心不重合。HO 属于极性分子。
2 2 2 2
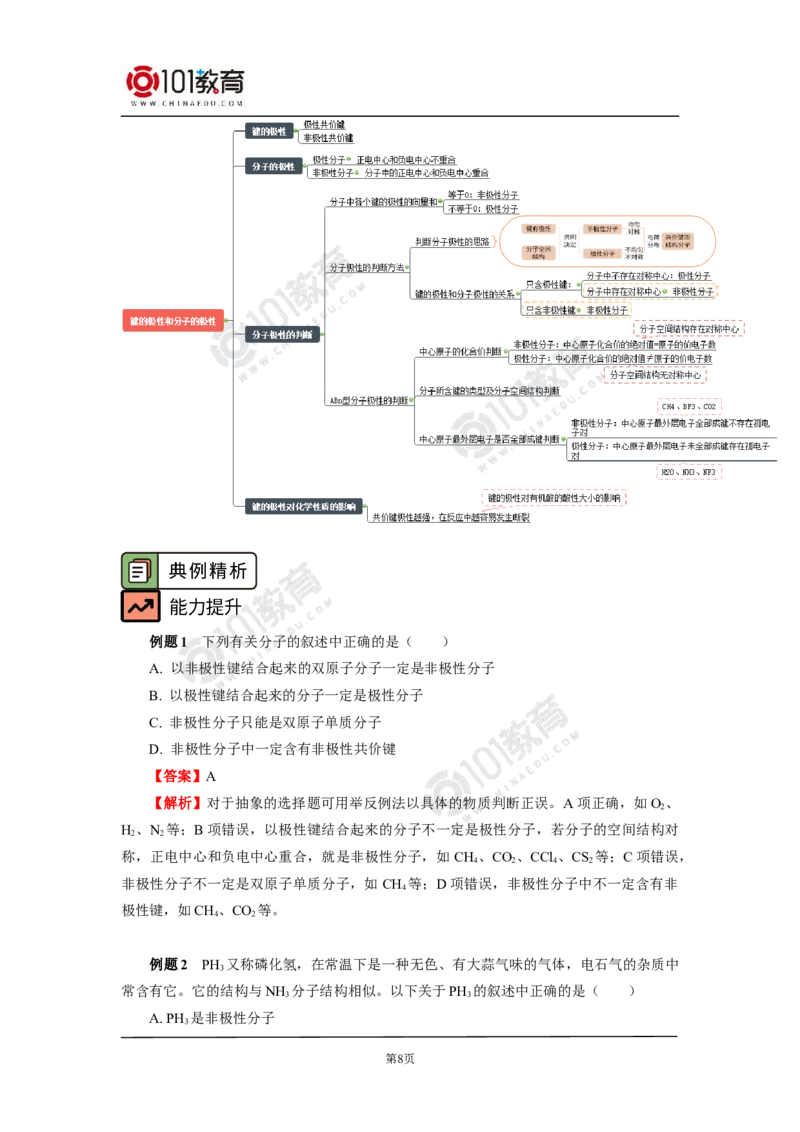
1. 分子的极性的判断方法
分子的极性是由分子中含共价键的极性和分子的空间结构两方面共同决定的。判断分
子极性时,可根据以下方法进行:
(1)判断分子极性的一般思路
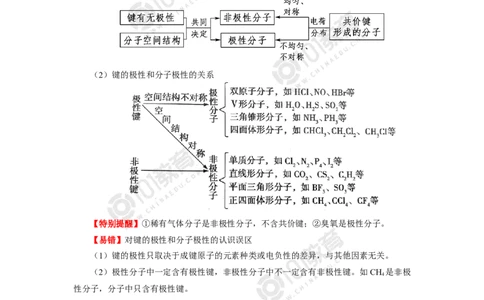
(2)键的极性和分子极性的关系
【特别提醒】①稀有气体分子是非极性分子,不含共价键;②臭氧是极性分子。
【易错】对键的极性和分子极性的认识误区
(1)键的极性只取决于成键原子的元素种类或电负性的差异,与其他因素无关。
(2)极性分子中一定含有极性键,非极性分子中不一定含有非极性键。如CH 是非极
4
性分子,分子中只含有极性键。
(3)含有非极性键的分子不一定为非极性分子,如HO 是含有非极性键的极性分子。
2 2
【即时练】回答下列问题
① H ② O ③ HCl ④ P ⑤ C ⑥ CO ⑦ CH==CH ⑧ HCN ⑨ HO
2 2 4 60 2 2 2 2
⑩NH
3
BF ⑫CH ⑬SO ⑭CHCl ⑮Ar ⑯HO
3 4 3 3 2 2
(1)只含非极性键的是________;只含极性键的是______,既含极性键又含非极性键
⑪
的是________。
第4页(2)属于非极性分子的是__________,属于极性分子的是________。
【答案】(1) ①②④⑤ ③⑥⑧⑨⑩⑪⑫⑬⑭ ⑦⑯
(2)①②④⑤⑥⑦⑪⑫⑬⑮ ③⑧⑨⑩⑭⑯
2. AB 型分子极性的判断
n
(1)根据中心原子的化合价判断:AB 型分子中,中心原子的化合价的绝对值等于该
n
元素的价电子数时,该分子为非极性分子,此时分子的空间结构对称;若中心原子的化合
价的绝对值不等于其价电子数,则分子的空间结构不对称,其分子为极性分子,具体实例
如下:
分子 BF CO PCl SO HO NH SO
3 2 5 3 2 3 2
中心原子化
3 4 5 6 2 3 4
合价绝对值
中心原子价电子数 3 4 5 6 6 5 6
分子极性 非极性 非极性 非极性 非极性 极性 极性 极性
(2)根据分子所含键的类型及分子空间结构判断:
分子 键的极性 键角 立体构型 分子极性
单原子分子 He、Ne - - - 非极性分子
H 非极性键 - 直线形 非极性分子
2
双原子分子
HCl 极性键 - 直线形 极性分子
HO 极性键 105° V形 极性分子
2
三原子分子
CO 极性键 180° 直线形 非极性分子
2
BF 极性键 120° 平面三角形 非极性分子
3
四原子分子
NH 极性键 107° 三角锥形 极性分子
3
CH 极性键 109°28′ 正四面体形 非极性分子
4
五原子分子
CHCl 极性键 - 四面体形 极性分子
3
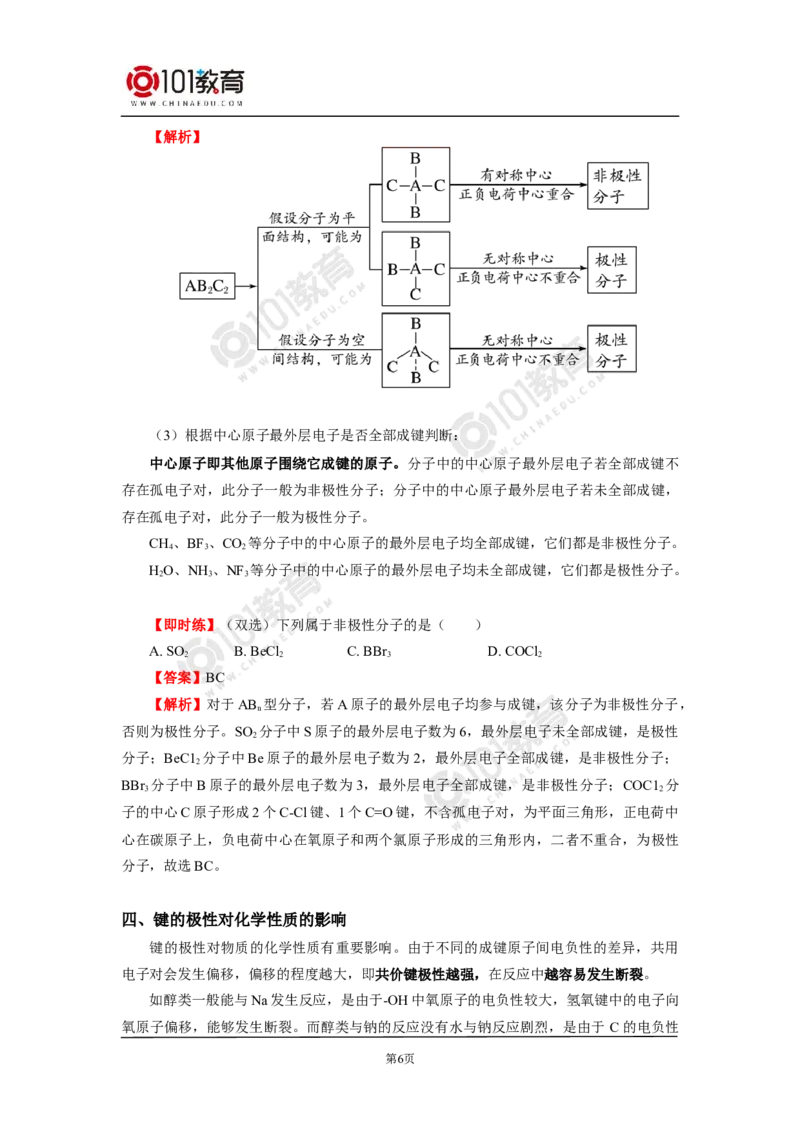
【即时练】有一种AB C 型分子,在该分子中A为中心原子。下列关于该分子的空间
2 2
结构和极性的说法中,正确的是( )
A. 假设为平面四边形,则该分子一定为非极性分子
B. 假设为四面体形,则该分子一定为非极性分子
C. 假设为平面四边形,则该分子可能为非极性分子
D. 假设为四面体形,则该分子可能为非极性分子
【答案】C
第5页【解析】
(3)根据中心原子最外层电子是否全部成键判断:
中心原子即其他原子围绕它成键的原子。分子中的中心原子最外层电子若全部成键不
存在孤电子对,此分子一般为非极性分子;分子中的中心原子最外层电子若未全部成键,
存在孤电子对,此分子一般为极性分子。
CH、BF、CO 等分子中的中心原子的最外层电子均全部成键,它们都是非极性分子。
4 3 2
HO、NH 、NF 等分子中的中心原子的最外层电子均未全部成键,它们都是极性分子。
2 3 3
【即时练】(双选)下列属于非极性分子的是( )
A. SO B. BeCl C. BBr D. COCl
2 2 3 2
【答案】BC
【解析】对于AB 型分子,若A原子的最外层电子均参与成键,该分子为非极性分子,
n
否则为极性分子。SO 分子中S原子的最外层电子数为6,最外层电子未全部成键,是极性
2
分子;BeC1 分子中Be原子的最外层电子数为2,最外层电子全部成键,是非极性分子;
2
BBr 分子中B原子的最外层电子数为3,最外层电子全部成键,是非极性分子;COC1 分
3 2
子的中心C原子形成2个C-Cl键、1个C=O键,不含孤电子对,为平面三角形,正电荷中
心在碳原子上,负电荷中心在氧原子和两个氯原子形成的三角形内,二者不重合,为极性
分子,故选BC。
四、键的极性对化学性质的影响
键的极性对物质的化学性质有重要影响。由于不同的成键原子间电负性的差异,共用
电子对会发生偏移,偏移的程度越大,即共价键极性越强,在反应中越容易发生断裂。
如醇类一般能与Na发生反应,是由于-OH中氧原子的电负性较大,氢氧键中的电子向
氧原子偏移,能够发生断裂。而醇类与钠的反应没有水与钠反应剧烈,是由于 C的电负性
第6页略大于H,烃基是推电子基团,使醇分子中的氢氧键的极性小于水分子中氢氧键的极性。
键的极性对有机酸的酸性大小的影响
羧酸的酸性可用pK 的大小来衡量,pK 越小,酸性越强。羧酸的酸性大小与其分子的
a a
组成和结构有关,如下表所示。
羧酸 pK
a
丙酸(C HCOOH) 4. 88
2 5
乙酸(CHCOOH) 4. 76
3
甲酸(HCOOH) 3. 75
氯乙酸(CHClCOOH) 2. 86
2
二氯乙酸(CHCl COOH) 1. 29
2
三氯乙酸(CCl COOH) 0. 65
3
三氟乙酸(CFCOOH) 0. 23
3
【思考】1 为什么甲酸、乙酸、丙酸的酸性逐渐减弱?
【提示】烃基(R-)是推电子基团,烃基越长推电子效应越大,使羧基中的烃基的极
性越小,羧酸的酸性越弱。所以,甲酸的酸性大于乙酸的,乙酸的酸性大于丙酸的,随着
烃基加长,酸性的差异越来越小。
【思考】2 为什么三氟乙酸、三氯乙酸、乙酸的酸性逐渐减弱?
为什么三氯乙酸、二氯乙酸、氯乙酸的酸性逐渐减弱?
【提示】与羧基(-COOH)相连的C-X(X为卤素原子)的极性越大,羧酸的酸性越
大;C-X的数量越多,羧酸的酸性越大,如酸性:CFCOOH>CCl COOH>CH COOH;
3 3 3
CCl COOH>CHCl COOH>CH ClCOOH。
3 2 2
第7页例题1 下列有关分子的叙述中正确的是( )
A. 以非极性键结合起来的双原子分子一定是非极性分子
B. 以极性键结合起来的分子一定是极性分子
C. 非极性分子只能是双原子单质分子
D. 非极性分子中一定含有非极性共价键
【答案】A
【解析】对于抽象的选择题可用举反例法以具体的物质判断正误。A项正确,如O 、
2
H 、N 等;B项错误,以极性键结合起来的分子不一定是极性分子,若分子的空间结构对
2 2
称,正电中心和负电中心重合,就是非极性分子,如 CH 、CO 、CCl 、CS 等;C项错误,
4 2 4 2
非极性分子不一定是双原子单质分子,如 CH 等;D项错误,非极性分子中不一定含有非
4
极性键,如CH、CO 等。
4 2
例题2 PH 又称磷化氢,在常温下是一种无色、有大蒜气味的气体,电石气的杂质中
3
常含有它。它的结构与NH 分子结构相似。以下关于PH 的叙述中正确的是( )
3 3
A. PH 是非极性分子
3
第8页B. PH 分子中有未成键的电子对
3
C. PH 是一种强氧化剂
3
D. PH 分子中的P—H是非极性键
3
【答案】B
【解析】PH 与NH 分子的结构相似,因此在P原子的最外层有一对孤电子对未成键。
3 3
P—H是由不同种原子形成的共价键,属于极性键。根据PH 的分子结构可知该分子的正电
3
中心和负电中心不重合,故分子有极性。PH 中P呈-3价,具有很强的还原性。
3
例题3 在HF、HS、NH 、CO、CCl 、N、C 、SO 分子中:
2 3 2 4 2 60 2
(1)以非极性键结合的非极性分子是___________
(2)以极性键相结合,具有直线型结构的非极性分子是___________
(3)以极性键相结合,具有正四面体结构的非极性分子是___________
(4)以极性键相结合,具有三角锥型结构的极性分子是___________
(5)以极性键相结合,具有V型结构的极性分子是___________
(6)以极性键相结合,而且分子极性最大的是___________
【答案】N、C CO CCl NH HS、SO HF
2 60 2 4 3 2 2
1
【解析】HF以极性键形成的极性分子;HS中中心原子S上的孤电子对数为 ×(6-2
2 2
×1)=2,成键电子对数为2,价层电子对数为4,VSEPR模型为四面体型,S上有两对孤
电子对,HS为V型结构,HS以极性键形成的极性分子;NH 中中心原子N上的孤电子
2 2 3
1
对数为 ×(5-3×1)=1,成键电子对数为3,价层电子对数为4,VSEPR模型为四面体型,
2
N上有一对孤电子对,NH 为三角锥型结构,NH 以极性键形成的极性分子;CO 中中心原
3 3 2
1
子C上的孤电子对数为 ×(4-2×2)=0,成键电子对数为2,价层电子对数为2,VSEPR
2
模型为直线型,C上没有孤电子对,CO 为直线型结构,CO 以极性键形成的非极性分子;
2 2
1
CCl 中中心原子C上的孤电子对数为 ×(4-4×1)=0,成键电子对数为4,价层电子对数
4 2
为4,VSEPR模型为四面体型,C上没有孤电子对,CCl 为正四面体结构,CCl 以极性键
4 4
形成的非极性分子;N 以非极性键形成的非极性分子;C 以非极性键形成的非极性分子;
2 60
1
SO 中中心原子S上的孤电子对数为 ×(6-2×2)=1,成键电子对数为2,价层电子对数
2 2
为3,VSEPR模型为平面三角型,S上有一对孤电子对,SO 为V型结构,SO 以极性键形
2 2
成的极性分子。
第9页(答题时间:40分钟)
一、选择题
1. 分子有极性分子和非极性分子之分。下列对极性分子和非极性分子的认识正确的是(
)
A. 只含非极性键的分子一定是非极性分子
B. 含有极性键的分子一定是极性分子
C. 非极性分子一定含有非极性键
D. 极性分子一定含有极性键
2. 下列说法正确的是( )
A. 含有非极性键的分子一定是非极性分子
B. 是由极性键构成的极性分子
C. 由极性键形成的双原子分子一定是极性分子
D. 键的极性与分子的极性无关
3. 已知BeCl 为共价化合物,两个Be—Cl键间的夹角为180°,则BeCl 属于( )
2 2
A. 由极性键构成的极性分子 B. 由极性键构成的非极性分子
C. 由非极性键构成的极性分子 D. 由非极性键构成的非极性分子
4. 用一带静电的玻璃棒靠近A、B两种纯液体流,根据图分析,这两种液体分子的极性
正确的是( )
A. A是极性分子,B是非极性分子
B. A是非极性分子,B是极性分子
C. A和B都是极性分子
D. A和B都是非极性分子
5. 下列说法中正确的是( )
A. 极性分子组成的溶质一定易溶于极性分子组成的溶剂之中,非极性分子组成的溶质
一定易溶于非极性分子组成的溶剂中
B. 溴分子和水分子是极性分子,四氯化碳分子是非极性分子,所以溴难溶于水而易溶
于四氯化碳
第10页C. 白磷分子是非极性分子,水分子是极性分子,而二硫化碳是非极性分子,所以白磷
难溶于水而易溶于二硫化碳
D. 水分子是极性分子,二氧化碳可溶于水,因此二氧化碳是极性分子
6. 下列叙述中正确的是( )
A. 卤化氢分子中,卤素的非金属性越强,共价键的极性越大,稳定性也越强
B. 以极性键结合的分子,一定是极性分子
C. 判断AB或AB 型分子是否是极性分子的依据是看分子中是否含有极性键
2 2
D. 非极性分子中,各原子间都应以非极性键结合
7. 实验测得CO 为共价化合物,两个C=O键间的夹角为180°,以下判断正确的是(
2
)
A. 由极性键构成的极性分子 B. 由极性键构成的非极性分子
C. 由非极性键构成的极性分子 D. CO 中C采取sp2杂化
2
8. 三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构
中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
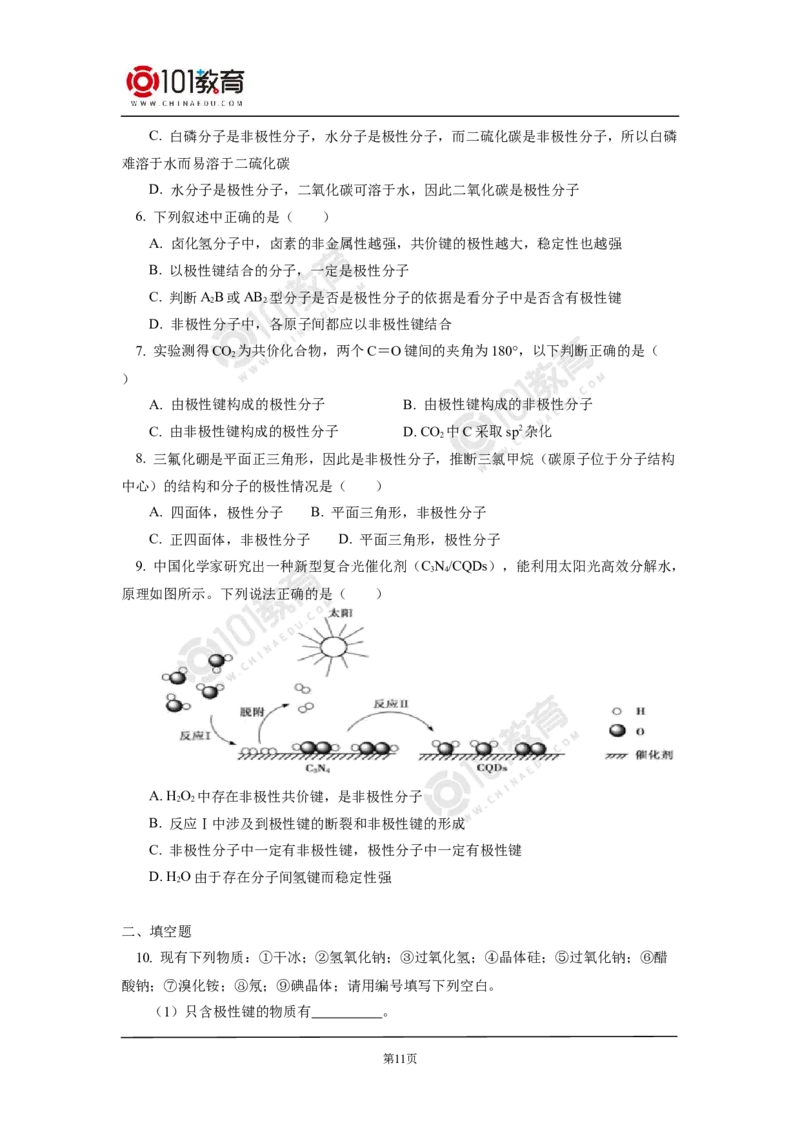
9. 中国化学家研究出一种新型复合光催化剂(C N/CQDs),能利用太阳光高效分解水,
3 4
原理如图所示。下列说法正确的是( )
A. H O 中存在非极性共价键,是非极性分子
2 2
B. 反应Ⅰ中涉及到极性键的断裂和非极性键的形成
C. 非极性分子中一定有非极性键,极性分子中一定有极性键
D. H O由于存在分子间氢键而稳定性强
2
二、填空题
10. 现有下列物质:①干冰;②氢氧化钠;③过氧化氢;④晶体硅;⑤过氧化钠;⑥醋
酸钠;⑦溴化铵;⑧氖;⑨碘晶体;请用编号填写下列空白。
(1)只含极性键的物质有 。
第11页(2)只含非极性键的物质有 。
(3)只含极性键和非极性键的物质有 。
(4)只含离子键和极性键的物质有 。
(5)只含离子键和非极性键的物质有 。
(6)既含离子键,又含极性键和非极性键的物质有 。
(7)不含化学键的物质有 。
第12页1. 【答案】D
【解析】键的极性是由组成共价键的原子是否相同决定,而分子的极性由键的极性和
分子的空间构型共同决定。只含非极性键的分子不一定是非极性分子(O 为极性分子)、
3
极性分子一定含有极性键,而含有极性键的分子、当空间构型非常对称时也可能为非极性
分子,例如CH。
4
故选D。
2. 【答案】C
【解析】A. 含有非极性键的分子不一定是非极性分子,如 ,选项A错误;
B. 是由极性键构成的非极性分子,选项B错误;
C. 由极性键形成的双原子分子,分子中正负电荷中心不重合,从整个分子来看,电荷
的分布是不均匀的,不对称的,所以是极性分子,选项C正确;
D. 分子的极性除与键的极性有关外,还与分子的空间构型有关,选项D错误。
3. 【答案】B
【解析】BeCl 中Be-Cl键是不同元素形成的共价键,为极性键,两个Be-Cl键间的夹
2
角为180°,说明分子是对称的,正电荷中心与负电荷的中心重合,BeCl 属于非极性分子,
2
故BeCl 由极性键形成的非极性分子,故答案为B。
2
4. 【答案】B
【解析】根据实验现象可知,A液体不偏转,说明A是非极性分子。B液体偏转,说
明B是极性分子,答案选B。
5. 【答案】C
【解析】A、很多有机物分子都是极性分子,但因为极性很弱,所以大部分难溶于水,
而有机物之间的溶解度却很大,选项A错误;
B、溴分子是非极性分子,选项B错误;
C、白磷分子是非极性分子,水分子是极性分子,而二硫化碳是非极性分子,所以白
磷难溶于水而易溶于二硫化碳,选项C正确;
D、二氧化碳是非极性分子,选项D错误;
6. 【答案】A
【解析】A、卤素中非金属性越强,键的极性越大,故A项正确;
B、以极性键结合的双原子分子一定是极性分子,但以极性键结合形成的多原子分子,
也可能是非极性分子,如CO,故B项错误;
2
C、AB型如HO、HS等,AB 型如CO、CS 等,判断其是否是极性分子的依据是看
2 2 2 2 2 2
分子中是否含有极性键及分子的立体构型是否对称。如CO、CS 为直线形,分子的立体构
2 2
第13页型对称,为非极性分子;如HO,有极性键,分子的立体构型不对称,为极性分子,故C
2
项错误;
D、多原子分子,其分子的立体构型对称,这样的非极性分子中可能含有极性键,故
D项错误;
7. 【答案】B
【解析】A、由于二氧化碳是对称结构,分子是非极性的,故A错误;B、碳原子和氧
原子的电负性不同,所以共价键是极性的,但分子是非极性的;C、错误;D、C是sp杂化。
8. 【答案】A
【解析】三氯甲烷(CHCl )中C形成1个碳氢σ键和3个碳氯σ键,碳上没有孤对电
3
子,三氯甲烷为四面体结构,由于碳氢键和碳氯键不同,三氯甲烷中正电中心、负电中心
不重合,三氯甲烷为极性分子,答案选A。
9. 【答案】B
【解析】A. H O 是极性分子,A错误;
2 2
B. 反应Ⅰ是在催化剂作用下HO生成H 和HO,涉及到极性键H-O键的断裂和非极
2 2 2 2
性键H-H键、O-O键的形成,B正确;
C. 分子的极性与分子内共价键的极性和分子的空间构型密切相关,是分析分子中的正
负电荷重心是否重合,重心重合是非极性分子,不重合是极性分子,C错误;
D. H O分子间氢键影响的是物理性质,而稳定性是化学性质,D错误。
2
10. 【答案】(1)① (2)④⑨ (3)③ (4)②⑦ (5)⑤ (6)⑥ (7)
⑧
【解析】(1)只含极性键的物质应为不同元素形成的化合物,干冰符合,故选①;
(2)只含非极性键的物质一般为单质,晶体硅、碘晶体符合,故选④⑨;(3)只含极性
键和非极性键的物质,过氧化氢中含H-O、O-O,故选③;(4)只含离子键和极性键的物
质,氢氧化钠中含离子键和H-O极性键,溴化铵中含离子键和N-H极性键,故选②⑦;
(5)只含离子键和非极性键的物质,过氧化钠中含离子键和O-O非极性键,故选⑤;
(6)既含离子键,又含极性键和非极性键的物质,醋酸钠含离子键、C-H极性键、H-O极
性键、C=O极性键、C-C非极性键,故选⑥;(7)不含化学键的物质,Ne为单原子分子,
不含化学键,故选⑧
第14页分子间的作用力 分子的手性
重难点 题型 分值
1. 范德华力、氢键及其对物质性质的影响
2. 能举例说明化学键和分子间作用力的区
从分子结构的角度,认识“相似相溶”规
重点
律。
选择题 2-4分
3. 了解“手性分子”在生命科学等方面的
应用。
难点 范德华力、氢键及其对物质性质的影响
一、范德华力及其对物质性质的影响
1. 概念:对气体加压降温,可使其液化;对液体降温,可使其凝固,这表明分子之间存
在着相互作用力。范德华是最早研究分子间普遍存在作用力的科学家,因此把这类分子间
作用力称为范德华力。范德华力是分子之间普遍存在的一种相互作用力,它使得许多物质
能以一定的凝聚态存在。
第15页2. 特征:
(1)范德华力广泛存在于分子之间(存在于固体、液体和气体中),只有分子间充分
接近时才有范德华力。
(2)范德华力很弱,比化学键的键能小1~2个数量级。每摩尔分子只有几到几十 。
(3)范德华力无方向性和饱和性。只要分子周围空间允许,分子总是尽可能多地吸引
其他分子。
3. 决定范德华力大小的因素
①一般来说,组成和性质相似的物质,相对分子质量越大,范德华力越大。如相对分
子质量:Br >Cl,因此,范德华力:Br >Cl。
2 2 2 2
②相对分子质量相同或相近时,分子的极性越大,范德华力也越大。如CO为极性分
子,N 为非极性分子,范德华力:CO>N。
2 2
③分子组成相同但结构不同的物质,分子的对称性越强,范德华力越小,如 对二甲苯
< 间二甲苯 < 邻二甲苯。
4. 范德华力对物质性质的影响
(1)对物质溶、沸点的影响
一般来说,分子晶体中范德华力越大,物质的熔、沸点越高。具体如下:
①组成和结构相似的物质,随着相对分子质量的增大,分子间的范德华力逐渐增大,
它们的熔、沸点逐渐升高。如图中的曲线所示:
【想一想】范德华力是怎样影响分子的物理性质(如熔、沸点)的?
物质发生固体→液体→气体的转化过程,熵值增大,分子间的距离不断被拉大,这个
过程中分子吸收外界能量,克服范德华力。分子间的范德华力越大,克服它需要吸收外界
的能量越多,因此只有外界温度较高时,分子才能顺利克服范德华力,实现固体→液体→
气体的三态变化。即范德华力越大,分子的熔、沸点越高。
②分子组成相同但结构不同的物质(即互为同分异构体),分子对称性越好,范德华
力越小,物质的熔、沸点越低,如熔、沸点;新成烷 < 异成烷 < 正戊烷。
第16页③一般,相对分子质量相近的物质,分子的极性越小、范德华力越小,物质的熔、沸
点越低,如熔、沸点:N氢键>范德华力
①随着分子极性的增
大而增大 成键原子半径越
对于X—H…Y,X、Y的
②组成和结构相似的 小,键长越短,键
影响因素 电负性越大,Y原子的半
分子构成的物质,相 能越大,共价键越
径越小,作用越强
对分子质量越大,范 稳定
德华力越大
影响物质的物理性质
①分子间氢键的存在,使
(如熔、沸点等)
物质的熔、沸点升高,在
组成和结构相似的物
对物质性 水中的溶解度增大。如 共价键键能越大,
质,相对分子质量越
质的影响 熔、沸点:HO>HS 分子稳定性越强
2 2
大,物质的熔、沸点
②分子内存在氢键时,降
升高。如
低物质的熔、沸点。
CF