文档内容
金属晶体与离子晶体同步练习
(答题时间:45分钟)
一、选择题
1. 金属的下列性质中和金属晶体的结构无关的是( )
A. 良好的导电性 B. 反应中易失电子
C. 良好的延展性 D. 良好的导热性
2. 下列关于金属键的叙述中,不正确的是( )
A. 金属键是金属阳离子和自由电子这两种带异性电荷的粒子间的强烈相互作用,其实
质与离子键类似,也是一种电性作用
B. 金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所以与共价键
类似,也有方向性和饱和性
C. 金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键无饱和性和
方向性
D. 构成金属键的自由电子在整个金属内部的三维空间中做自由运动
3. 下图是金属晶体内部电子气理论图
电子气理论可以用来解释金属的性质,其中正确的是( )
A. 金属能导电是因为金属阳离子在外加电场作用下定向移动
B. 金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C. 金属具有延展性是因为在外力的作用下,金属阳离子各层间会出现相对滑动,但自
由电子可以起到润滑的作用,使金属不会断裂
D. 合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金
的延展性比纯金属强,硬度比纯金属小
4. 在金属晶体中,如果金属原子的价电子数越多,金属阳离子的半径越小,自由电子与
金属阳离子间的作用力越大,金属的熔点越高。由此判断下列各组金属熔点的高低顺序,
其中正确的是( )
A. Mg>Al>Ca B. Al>Na>Li
C. Al>Mg>Ca D. Mg>Ba>Al
5. 自然界中的CaF 又称萤石,是一种难溶于水的固体,属于典型的离子晶体。下列一定
2
能说明CaF 是离子晶体的实验是( )
2
第1页A. CaF 难溶于水,其水溶液的导电性极弱
2
B. CaF 的熔、沸点较高,硬度较大
2
C. CaF 固体不导电,但在熔融状态下可以导电
2
D. CaF 在有机溶剂(如苯)中的溶解度极小
2
6. 石墨晶体是层状结构(如图)。以下有关石墨晶体的说法正确的一组是( )
①石墨中存在两种作用力;②石墨是混合晶体;③石墨中的C为sp2杂化;④石墨熔点、
沸点都比金刚石低;⑤石墨中碳原子数和C—C键数之比为1∶2;⑥石墨和金刚石的硬度
相同;⑦石墨层内导电性和层间导电性不同;⑧每个六元环完全占有的碳原子数是2
A. 全对 B. 除⑤外
C. 除①④⑤⑥外 D. 除⑥⑦⑧外
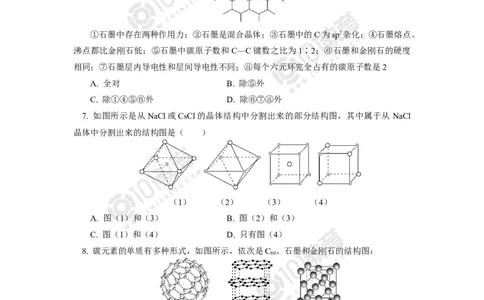
7. 如图所示是从NaCl或CsCl的晶体结构中分割出来的部分结构图,其中属于从 NaCl
晶体中分割出来的结构图是( )
(1) (2) (3) (4)
A. 图(1)和(3) B. 图(2)和(3)
C. 图(1)和(4) D. 只有图(4)
8. 碳元素的单质有多种形式,如图所示,依次是C 、石墨和金刚石的结构图:
60
回答下列问题:
(1)金刚石、石墨、C 、碳纳米管等都是碳元素的单质形式,它们互为________。
60
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C 属于________晶体,石墨属于________晶体。
60
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154
pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存
在________共价键,还有________键。
第2页第3页金属晶体与离子晶体同步练习参考答案
1.【答案】B
【解析】金属的物理性质是由金属晶体结构所决定的,A、C、D三项都是金属共有的
物理性质,这些性质都是由金属晶体结构所决定的。B项,金属易失电子是由金属原子的
结构决定的,和晶体结构无关。
2.【答案】B
【解析】从基本构成粒子的性质看,金属键与离子键的实质类似,都属于电性作用,
特征都是无方向性和饱和性;自由电子是由金属原子提供的,并且在整个金属内部的三维
空间内运动,为整个金属的所有阳离子所共有,从这个角度看,金属键与共价键有类似之
处,但两者又有明显的不同,如金属键无方向性和饱和性。
3.【答案】C
【解析】金属能导电是因为自由电子在外加电场作用下定向移动,A项错误;金属能
导热是因为自由电子在热的作用下与金属阳离子碰撞,从而发生热的传导,B项错误;合
金与纯金属相比,由于增加了不同的金属或非金属,相当于填补了金属阳离子之间的空隙
所以一般情况下合金的延展性比纯金属弱,硬度比纯金属大,D项错误。
4.【答案】C
【解析】金属原子的价电子数:Al>Mg=Ca=Ba>Li=Na,金属阳离子的半径:r(Ba2
+)>r(Ca2+)>r(Na+)>r(Mg2+)>r(Al3+)>r(Li+),则C正确。
5.【答案】C
【解析】离子晶体中含有离子键,离子键在熔融状态下被破坏,电离出自由移动的阴、
阳离子,所以离子晶体在熔融状态下能够导电,这是判断某晶体是否为离子晶体的依据。
6.【答案】C
【解析】①不正确,石墨中存在三种作用力,一种是范德华力,一种是共价键,还有
一种是金属键;②正确;③正确,石墨中的C为sp2杂化;④不正确,石墨熔点比金刚石高;
⑤不正确,石墨中碳原子数和C—C键数之比为2∶3;⑥不正确,石墨质软,金刚石的硬
度大;⑦正确;⑧正确,每个六元环完全占有的碳原子数是6×1/3=2。
7.【答案】C
【解析】本题考查了离子晶体的代表物质NaCl、CsCl的晶体结构。NaCl晶体中,每
个Na+周围最邻近的Cl-有6个,构成正八面体,同理,每个Cl-周围最邻近的6个Na+也
构成正八面体,由此可知图(1)和(4)是从NaCl晶体中分割出来的结构图,C项正确。
8.【答案】(1)同素异形体 (2)sp3 sp2 (3)分子 混合 (4)σ σ π(或大
π或ppπ)
【解析】(1)金刚石、石墨、C 、碳纳米管都是由同种元素形成的不同单质,故它
60
第4页们互为同素异形体。(2)在金刚石中,每个碳原子都形成四个共价单键,故碳原子的杂化
方式为sp3;石墨烯中碳原子采用sp2杂化。(3)一个“C ”就是一个分子,故C 属于分
60 60
子晶体;石墨层与层之间是范德华力,而同一层中碳原子之间是共价键,故形成的晶体为
混合晶体。(4)在金刚石晶体中,碳原子之间只形成共价单键,全部为σ键;在石墨层内
的碳原子之间既有σ键又有π键。
第5页配合物与超分子同步练习
(答题时间:45分钟)
一、选择题
1. 若X、Y两种粒子之间可形成配位键,则下列说法正确的是( )
A. X、Y只能是分子
B. X、Y只能是离子
C. 若X提供空轨道,则Y至少要提供一对孤电子对
D. 若X提供空轨道,则配位键表示为X→Y
2. 下列粒子中含配位键的是( )
+ +
①NH5 ②CH ③OH- ④NH4 ⑤Fe(CO)
2 4 3
⑥Fe(SCN) ⑦HO+ ⑧Ag(NH )OH
3 3 3 2
A. ①②④⑦⑧ B. ③④⑤⑥⑦
C. ①④⑤⑥⑦⑧ D. 全部
3. 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶
解得到深蓝色的透明溶液。下列对此现象的说法正确的是( )
A. 沉淀溶解后,生成深蓝色的配合离子[Cu(NH )]2+
3 4
B. [Cu(HO)]2+比[Cu(NH )]2+中的配位键稳定
2 4 3 4
C. 用硝酸铜溶液代替硫酸铜溶液进行实验,不能观察到同样的现象
D. 在[Cu(NH )]2+中,Cu2+给出孤电子对,NH 提供空轨道
3 4 3
4. 下列有关超分子的说法错误的是( )
A. 超分子是由两种或多种分子形成的聚集体
B. 分子形成超分子的作用可能是分子间作用力
C. 超分子具有分子识别的特性
D. 分子以共价键聚合形成超分子
5. (1)在[Ni(NH ) ]2+中Ni2+与NH 之间形成的化学键称为________,提供孤电子对
3 6 3
的成键原子是________。
(2)CaF 难溶于水,但可溶于含Al3+的溶液中,原因是_________。(用离子方程式
2
3−
表示,已知AlF6 在溶液中可稳定存在)。
(3)配合物[Cr(HO) ]3+中,与Cr3+形成配位键的原子是___________(填元素符
2 6
号)。
6. 碳元素的单质有多种形式,如图所示,依次是C 、石墨和金刚石的结构图:
60
第6页回答下列问题:
(1)金刚石、石墨、C 、碳纳米管等都是碳元素的单质形式,它们互为________。
60
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C 属于________晶体,石墨属于________晶体。
60
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154
pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存
在________共价键,还有________键。
第7页配合物与超分子同步练习参考答案
1. 【答案】C
【解析】形成配位键的两种粒子可以均是分子或者均是离子,还可以一种是分子、一
种是离子,但必须是一种粒子提供空轨道、另一种粒子提供孤电子对,A、B项错误,C项
正确;配位键中箭头应该指向提供空轨道的X,D项错误。
2. 【答案】C
【解析】形成配位键的条件是一个原子(或离子)有孤电子对,另一个原子(或离
子)有空轨道。在②CH 、③OH-中,中心原子碳和氧的价电子已完全成键,没有孤电子
4
对。
3. 【答案】A
【解析】从实验现象分析可知,Cu2+与NH ·H O反应生成Cu(OH) 沉淀。继续添加
3 2 2
氨水,由于Cu2+更易与NH 结合,生成更稳定的[Cu(NH ) ]2+。上述现象是Cu2+的性质
3 3 4
2−
与SO4 无关,故换用Cu(NO ) 溶液仍可观察到同样的现象,C项错误;在[Cu(NH )
3 2 3
]2+中,Cu2+提供空轨道,NH 给出孤电子对,属于配位体,D项错误。
4 3
4. 【答案】D
【解析】分子以非共价键或仅以分子间作用力形成超分子。
3−
5. 【答案】(1)配位键 N (2)3CaF +Al3+===3Ca2++AlF6 (3)O
2
【解析】(1)Ni2+与NH 之间形成共价键时Ni2+提供空轨道,N提供孤电子对,形成
3
配位键。(2)CaF 中存在沉淀溶解平衡:CaF (s) Ca2+(aq)+2F-(aq),溶液
2 2
3−
中的F-与Al3+形成配位离子AlF6 ,使沉淀溶解平衡向右移动,导致氟化钙溶解。(3)
HO分子中的O原子有孤电子对,能与Cr3+形成配位键。
2
6. 【答案】(1)同素异形体 (2)sp3 sp2 (3)分子 混合 (4)σ σ π(或
大π或ppπ)
【解析】(1)金刚石、石墨、C 、碳纳米管都是由同种元素形成的不同单质,故它
60
们互为同素异形体。(2)在金刚石中,每个碳原子都形成四个共价单键,故碳原子的杂化
方式为sp3;石墨烯中碳原子采用sp2杂化。(3)一个“C ”就是一个分子,故C 属于分
60 60
子晶体;石墨层与层之间是范德华力,而同一层中碳原子之间是共价键,故形成的晶体为
混合晶体。(4)在金刚石晶体中,碳原子之间只形成共价单键,全部为σ键;在石墨层内
的碳原子之间既有σ键又有π键。
第8页