文档内容
铁及其化合物(2)
重难点 题型 分值
重点 1. 掌握铁的化学性质及化学方程式;了解几种铁的 填空、选择 6-8分
氧化物和氢氧化物的主要性质及其应用;掌握 Fe
(OH)、Fe(OH) 的制备方法。
3 2
2. 以Fe2+、Fe3+的相互转化为例,理解变价金属元素
的氧化还原反应;能鉴别溶液中的Fe2+、Fe3+。
难点 以Fe2+、Fe3+的相互转化为例,理解变价金属元素的
氧化还原反应;能鉴别溶液中的Fe2+、Fe3+。
核心知识点一:
一、铁的氢氧化物的制备与性质
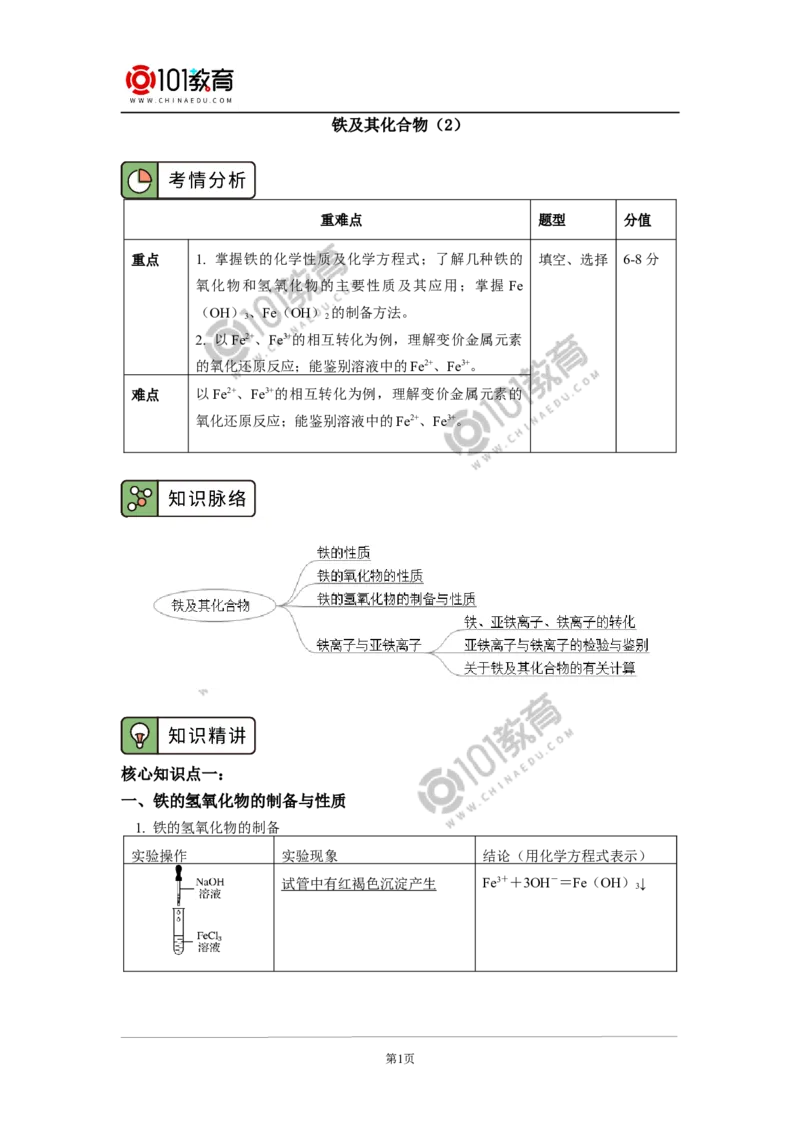
1. 铁的氢氧化物的制备
实验操作 实验现象 结论(用化学方程式表示)
试管中有红褐色沉淀产生 Fe3++3OH-=Fe(OH)↓
3
第1页试管中先生成白色沉淀,迅速 Fe2++2OH-= Fe(OH) ↓
2
变成灰绿色,最后变成红褐色 (白色)、4Fe(OH)+O+
2 2
2HO=4Fe(OH)
2 3
2. 氢氧化铁和氢氧化亚铁都为不溶性碱,由此可推测它们具有的性质是
(1)都能与酸反应生成相应的盐和水,它们分别与盐酸反应的离子方程式是①Fe
(OH)+3H+=Fe3++3HO,②Fe(OH)+2H+=Fe2++2HO。
3 2 2 2
(2)不稳定,受热易分解,其化学方程式分别为
①Fe(OH):2Fe(OH) Fe O+3HO,
3 3 2 3 2
②Fe(OH):Fe(OH) FeO+HO。
2 2 2
【归纳总结】
铁的氢氧化物的性质及制取
(1)氢氧化铁和氢氧化亚铁的物质类别是不溶性碱,其主要化学性质为都能与酸反应
生成盐和水,不稳定,受热易分解。
(2)铁的氢氧化物的制取方法是相应盐和碱反应,制取氢氧化亚铁时,常得到红褐色
沉淀是因为Fe(OH) 极易被空气中的O 氧化成Fe(OH) ,所以为了防止NaOH溶液加
2 2 3
入时带入空气,可将吸有NaOH溶液的长胶头滴管伸入到FeSO 液面下,再挤出NaOH溶
4
液。
核心知识点二
二、亚铁盐和铁盐
1. 亚铁盐和铁盐的性质
(1)亚铁盐
含有Fe2+的溶液,呈浅绿色,既有氧化性,又有还原性。
①氧化性:
Fe2+与Zn反应的离子方程式:Zn+Fe2+=Fe+Zn2+。
②还原性:
Fe2+与Cl 反应的离子方程式:2Fe2++Cl=2Fe3++2Cl-。
2 2
Fe2+在酸性条件下被HO 氧化的反应的离子方程式:
2 2
2Fe2++HO+2H+=2Fe3++2HO。
2 2 2
− −
【注意】Fe2+与MnO4 、NO3 (H+) 、ClO-等因发生氧化还原反应而不共存。Fe2
2−
+与OH-、S2-、CO3 等因发生沉淀反应而不共存。
(2)铁盐
第2页①氧化性:含Fe3+的溶液,呈黄色,Fe3+具有较强的氧化性。Fe3+与Cu、I-反应的离
子方程式:2Fe3++Cu=Cu2++2Fe2+,2Fe3++2I-=2Fe2++I。
2
②特性:含有Fe3+的盐溶液遇到KSCN时变成血红色。
③FeCl 将其饱和溶液滴入沸水中制备胶体的化学方程式为FeCl +3HO Fe(OH)
3 3 2
2−
(胶体)+3HCl。Fe3+与S2-、HS-、I-、SO3 等还原性离子因发生氧化还原反应而不能
3
共存,Fe3+与SCN-因发生络合反应而不共存,Fe3+与OH-因发生沉淀反应而不共存。
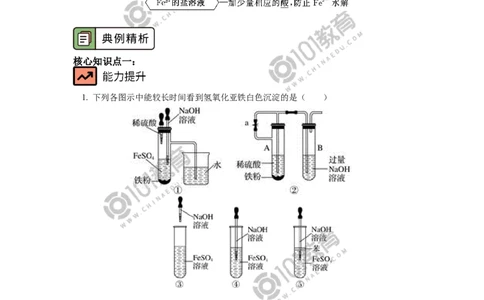
(3)Fe、Fe2+、Fe3+三者之间的相互转化关系
2. Fe2+、Fe3+的检验
(1)Fe2+的检验
①样品溶液 无现象 溶液变红色,证明含有Fe2+
②样品溶液 白色絮状沉淀,迅速变成灰绿色,最终变为红褐色,
证明有Fe2+
(2)Fe3+的检验
①样品溶液 溶液变红色,证明含有Fe3+
②样品溶液 产生红褐色沉淀,证明有Fe3+存在
(3)含Fe2+、Fe3+的混合溶液中Fe3+、Fe2+的检验
Fe3
方法1:混合溶液 溶液变红色,说明含有Fe3+
+的检验
方法2:混合溶液 试纸变蓝色,说明含有Fe3+
Fe2
方法1:混合溶液 酸性KMnO 溶液紫红色褪去,说明
+的检验 4
含有Fe2+
方法2:混合溶液 溴水褪色,说明含有Fe2+
【】
第3页(1)检验Fe2+时不能先加氯水后加KSCN溶液,也不能将加KSCN后的混合溶液加
入到足量的新制氯水中(新制氯水可能氧化SCN-)。
(2)Fe3+、Fe2+、Cl-同时存在时不能用酸性 KMnO 溶液检验Fe2+(Cl-能还原酸性
4
KMnO ,有干扰)。
4
3. 亚铁盐和铁盐溶液的配制与保存方法
核心知识点一:
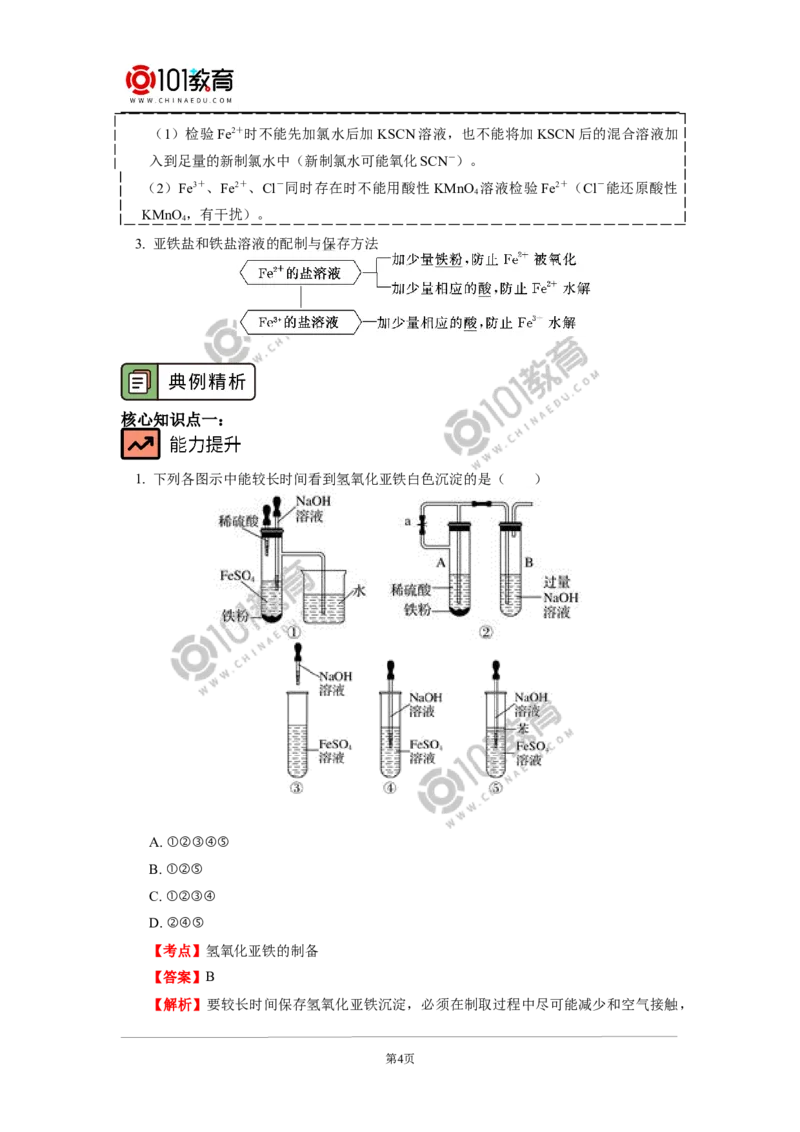
1. 下列各图示中能较长时间看到氢氧化亚铁白色沉淀的是( )
A. ①②③④⑤
B. ①②⑤
C. ①②③④
D. ②④⑤
【考点】氢氧化亚铁的制备
【答案】B
【解析】要较长时间保存氢氧化亚铁沉淀,必须在制取过程中尽可能减少和空气接触,
第4页防止氧化。①盛有氢氧化钠溶液的滴管伸入溶液中,能减少与氧气接触;溶液中加入铁粉,
可将氧化形成的铁盐重新还原为亚铁盐,符合题意。②打开止水夹,铁与稀硫酸生成氢气,
能排出装置中的空气,并作亚铁盐的保护气;关闭止水夹时,左管中积聚的氢气将亚铁盐
溶液压入B中,与碱反应生成氢氧化亚铁,符合题意。③滴加的氢氧化钠溶液会带进空气,
加速氢氧化亚铁的氧化,不符合题意。④能有效避免混合过程中带进氧气,但溶液仍与空
气有接触,生成的氢氧化亚铁久置时还能被氧化,不合题意。⑤能有效避免混合过程中带
进氧气,且加入的有机物作隔离层,不和空气接触,留存时间就长,符合题意。
2. 关于氢氧化铁和氢氧化亚铁的下列叙述中错误的是( )
A. 都是不溶于水的固体
B. 都能与酸反应生成盐和水
C. 不稳定,受热都能分解
D. 在空气中都容易被氧化
【考点】氢氧化铁和氢氧化亚铁的性质
【答案】D
【解析】氢氧化铁和氢氧化亚铁都不溶于水,都能与酸反应生成盐和水,受热都能分
解生成相应的氧化物和水;氢氧化亚铁具有还原性,在空气中易被氧化为氢氧化铁,氢氧
化铁在空气中不能被氧化。
核心知识点二:
1. 下列离子方程式正确的是( )
A. 将氨水滴入到FeCl 溶液中:Fe3++3OH-=Fe(OH)↓
3 3
B. 氧化铁与盐酸反应:Fe O+6H+=2Fe3++3HO
2 3 2
C. 向FeCl 溶液中加入铁粉:Fe+Fe3+=2Fe2+
3
D. 向氯化亚铁溶液中通入Cl:Fe2++Cl=Fe3++2Cl-
2 2
【考点】与铁及其化合物相关离子方程式的考查
【答案】B
【解析】弱电解质NH ·H O不能拆写成离子的形式,A错误;离子方程式中除遵循原
3 2
子守恒外,电荷也必须守恒,正确的离子方程式应为Fe+2Fe3+=3Fe2+,C错误。只符合
原子守恒,不符合电荷守恒,正确的离子方程式应为2Fe2++Cl=2Fe3++2Cl-,D错误。
2
第5页2. 为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,下
列物质中最好选用( )
A. HO 溶液
2 2
B. KMnO 溶液
4
C. 氯水
D. HNO 溶液
3
【考点】铁离子和亚铁离子之间的氧化还原反应
【答案】A
【解析】A项,HO +2Fe2++2H+=2Fe3++2HO,不会引入杂质;B、C和D选项,
2 2 2
能将Fe2+氧化为Fe3+,但引入新的杂质,故只选A。
(答题时间:25分钟)
一、选择题:本题包括12小题,每小题4分,共48分。
1. 将下列四种化合物溶于稀盐酸,滴加硫氰化钾溶液,没有颜色变化,再加氯水即呈现
红色的是( )
A. FeO B. Fe O C. Fe O D. Fe (SO )
2 3 3 4 2 4 3
2. 向某溶液中加入含Fe2+的溶液后,无明显变化。当再滴入几滴新制氯水后,混合溶液
变成红色,则下列结论错误的是( )
A. 该溶液中一定含有SCN-
B. 氧化性:Cl>Fe3+
2
C. Fe2+与SCN-能形成红色物质
D. Fe2+被氧化为Fe3+
3. 把铁粉、铜粉置于FeCl 溶液中,充分反应后加入KSCN不显红色,下列情况不能成
3
立的是( )
A. 铁不剩余,Cu剩余
B. 铁、铜均剩余
C. 铁剩余,含Cu2+
D. 铜剩余,含Fe2+
4. 有NaCl、FeCl 、FeCl 、CuCl 、AlCl 五种溶液,用一种试剂就可把它们鉴别开来,
2 3 2 3
这种试剂是( )
A. 盐酸 B. 烧碱溶液 C. 氯水 D. KSCN溶液
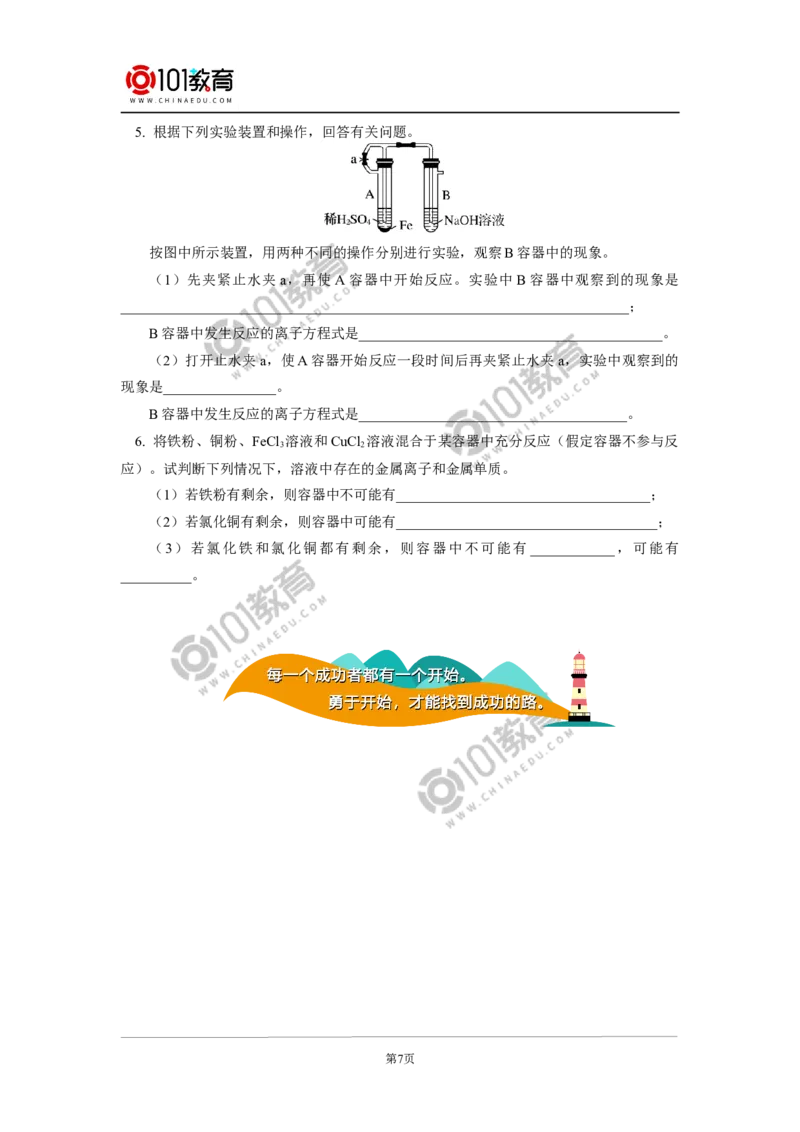
第6页5. 根据下列实验装置和操作,回答有关问题。
按图中所示装置,用两种不同的操作分别进行实验,观察B容器中的现象。
(1)先夹紧止水夹a,再使A容器中开始反应。实验中 B容器中观察到的现象是
________________________________________________________________________;
B容器中发生反应的离子方程式是___________________________________________。
(2)打开止水夹a,使A容器开始反应一段时间后再夹紧止水夹a,实验中观察到的
现象是________________。
B容器中发生反应的离子方程式是______________________________________。
6. 将铁粉、铜粉、FeCl 溶液和CuCl 溶液混合于某容器中充分反应(假定容器不参与反
3 2
应)。试判断下列情况下,溶液中存在的金属离子和金属单质。
(1)若铁粉有剩余,则容器中不可能有____________________________________;
(2)若氯化铜有剩余,则容器中可能有_____________________________________;
(3)若氯化铁和氯化铜都有剩余,则容器中不可能有____________,可能有
__________。
第7页1. 【答案】A
【解析】Fe O 与HCl反应,既有FeCl 生成,又有FeCl 生成。
3 4 3 2
2. 【答案】C
【解析】溶液中的Fe2+与加入的新制氯水发生反应:2Fe2++Cl =2Fe3++2Cl-,故氧
2
化性:Fe3+