文档内容
化学反应与能量变化(1)
重难点 题型 分值
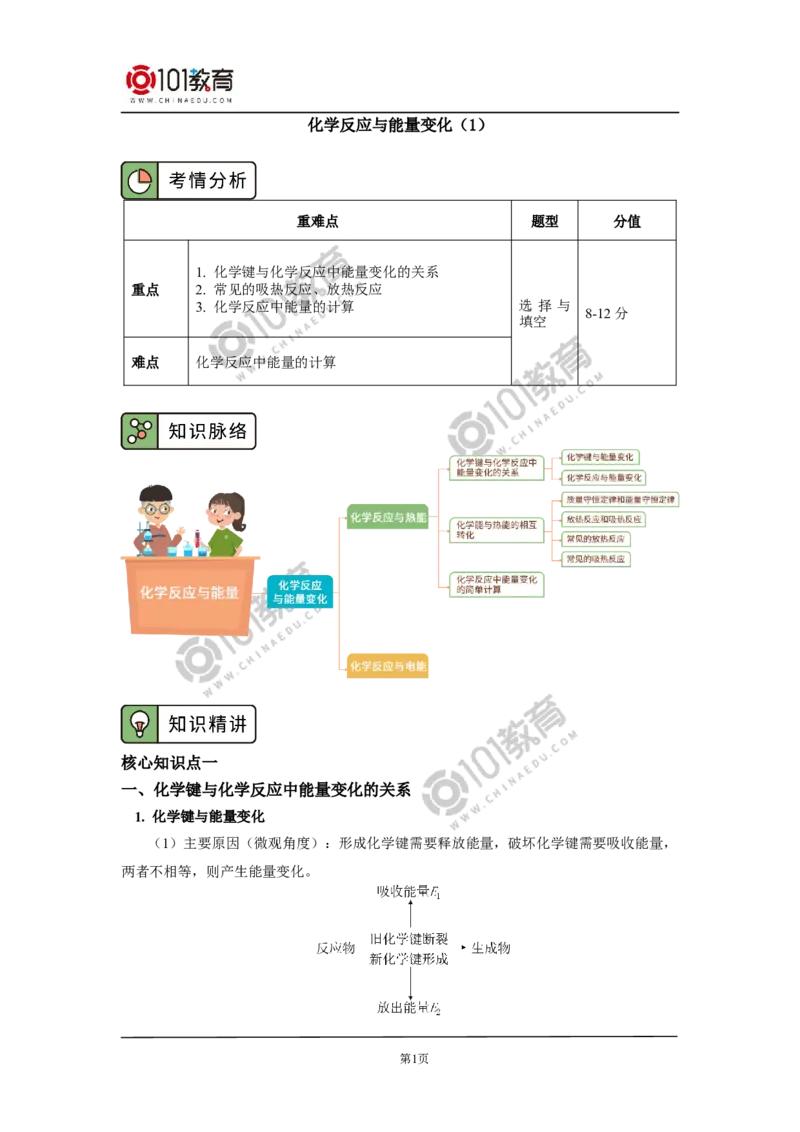
1. 化学键与化学反应中能量变化的关系
重点 2. 常见的吸热反应、放热反应
3. 化学反应中能量的计算 选 择 与
8-12分
填空
难点 化学反应中能量的计算
核心知识点一
一、化学键与化学反应中能量变化的关系
1. 化学键与能量变化
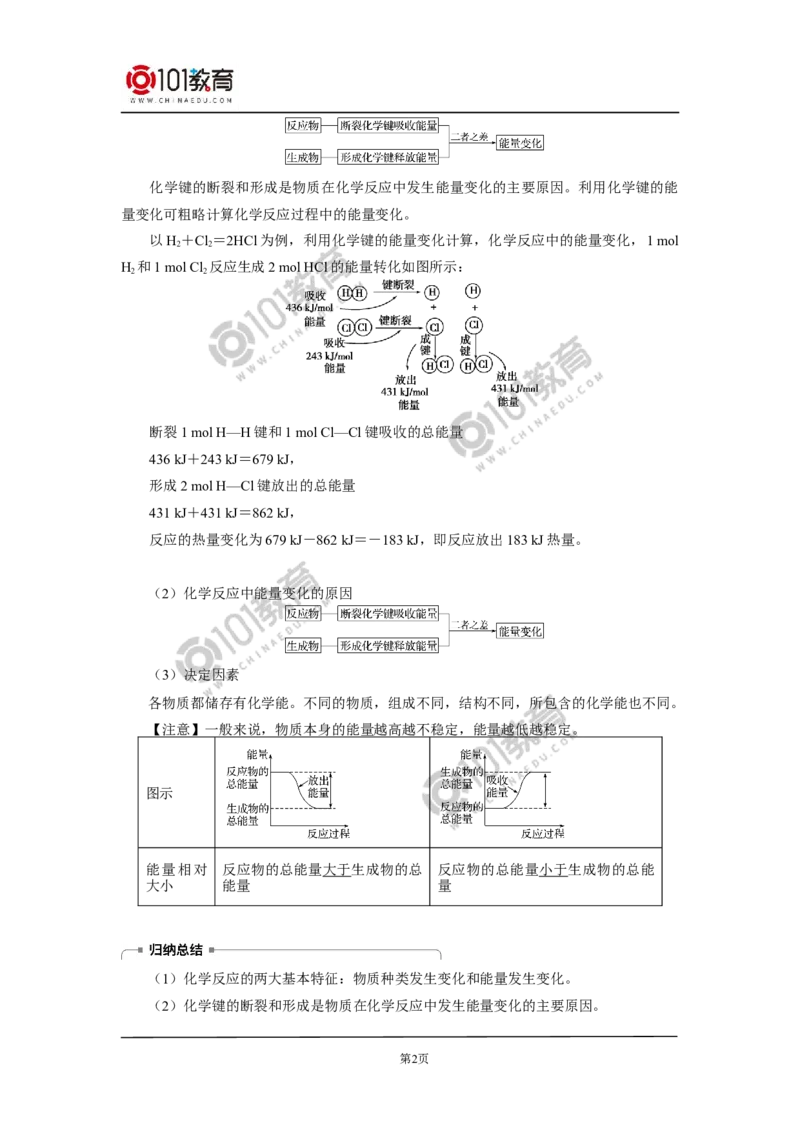
(1)主要原因(微观角度):形成化学键需要释放能量,破坏化学键需要吸收能量,
两者不相等,则产生能量变化。
第1页化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因。利用化学键的能
量变化可粗略计算化学反应过程中的能量变化。
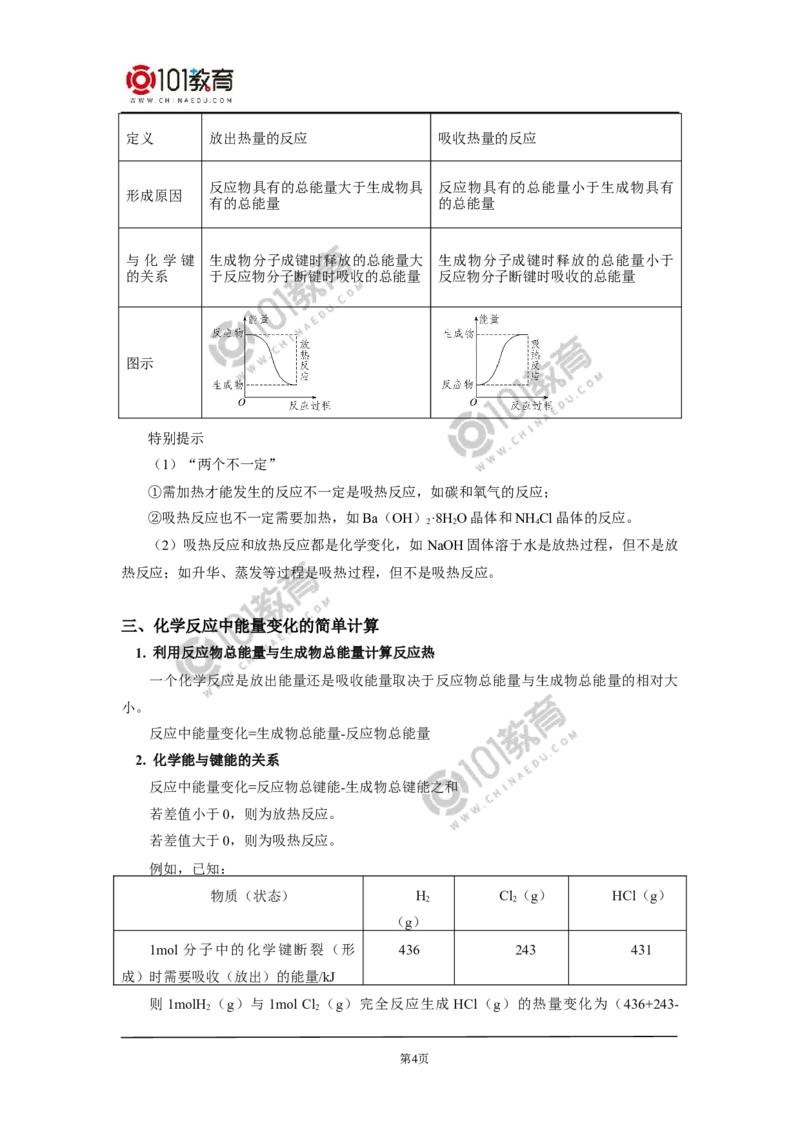
以H +Cl =2HCl为例,利用化学键的能量变化计算,化学反应中的能量变化,1 mol
2 2
H 和1 mol Cl 反应生成2 mol HCl的能量转化如图所示:
2 2
断裂1 mol H—H键和1 mol Cl—Cl键吸收的总能量
436 kJ+243 kJ=679 kJ,
形成2 mol H—Cl键放出的总能量
431 kJ+431 kJ=862 kJ,
反应的热量变化为679 kJ-862 kJ=-183 kJ,即反应放出183 kJ热量。
(2)化学反应中能量变化的原因
(3)决定因素
各物质都储存有化学能。不同的物质,组成不同,结构不同,所包含的化学能也不同。
【注意】一般来说,物质本身的能量越高越不稳定,能量越低越稳定。
图示
能量相对 反应物的总能量大于生成物的总 反应物的总能量小于生成物的总能
大小 能量 量
(1)化学反应的两大基本特征:物质种类发生变化和能量发生变化。
(2)化学键的断裂和形成是物质在化学反应中发生能量变化的主要原因。
第2页2. 化学反应与能量变化
(1)一个化学反应是吸收能量还是放出能量,决定于反应物总能量与生成物总能量的
相对大小。
(2)旧键断裂所吸收的能量与新键形成所释放的能量相对大小决定了一个化学反应是
吸收能量还是放出能量。
二、化学能与热能的相互转化
1. 两条基本的自然定律
(1)质量守恒定律:自然界的物质发生转化时,总质量不变。(即反应前后原子个数、
元素种类、原子质量不变)。
(2)能量守恒定律:一种形式的能量可以转化为另一种形式的能量,但是体系包含的
总能量不变。
2. 放热反应和吸热反应
(1)概念
①放出热量的化学反应为放热反应。
②吸收热量的化学反应为吸热反应。
(2)常见的吸热反应和放热反应
①常见的放热反应有:
a. 可燃物燃烧反应(甲烷在氧气中燃烧,氢气在氯气中燃烧);
b. 铝热反应(铝和氧化铁在高温下的反应);
c. 金属与水(钠与水)或酸(铁与盐酸)的反应;
d. 酸碱中和反应(氢氧化钠和盐酸);
e. 大多数化合反应(氧化钙和水,三氧化硫和水)。
②常见的吸热反应有:
a. 大多数分解反应、
b. 铵盐和碱(Ba(OH)•8H O + 2NH Cl =BaCl + 2NH ↑ + 10H O)
2 2 4 2 3 2
高温
c. C+HO(g) CO+H
2 2
高温
d. C+CO 2CO、等。
2
放热反应与吸热反应比较
类型
放热反应 吸热反应
比较
第3页定义 放出热量的反应 吸收热量的反应
反应物具有的总能量大于生成物具 反应物具有的总能量小于生成物具有
形成原因
有的总能量 的总能量
与化学键 生成物分子成键时释放的总能量大 生成物分子成键时释放的总能量小于
的关系 于反应物分子断键时吸收的总能量 反应物分子断键时吸收的总能量
图示
特别提示
(1)“两个不一定”
①需加热才能发生的反应不一定是吸热反应,如碳和氧气的反应;
②吸热反应也不一定需要加热,如Ba(OH)·8H O晶体和NH Cl晶体的反应。
2 2 4
(2)吸热反应和放热反应都是化学变化,如NaOH固体溶于水是放热过程,但不是放
热反应;如升华、蒸发等过程是吸热过程,但不是吸热反应。
三、化学反应中能量变化的简单计算
1. 利用反应物总能量与生成物总能量计算反应热
一个化学反应是放出能量还是吸收能量取决于反应物总能量与生成物总能量的相对大
小。
反应中能量变化=生成物总能量-反应物总能量
2. 化学能与键能的关系
反应中能量变化=反应物总键能-生成物总键能之和
若差值小于0,则为放热反应。
若差值大于0,则为吸热反应。
例如,已知:
物质(状态) H Cl(g) HCl(g)
2 2
(g)
1mol 分子中的化学键断裂(形 436 243 431
成)时需要吸收(放出)的能量/kJ
则1molH (g)与1mol Cl (g)完全反应生成 HCl(g)的热量变化为(436+243-
2 2
第4页431×2)kJ=-183kJ,即放出183kJ热量。
{ΔQ<0,为放热反应
¿¿¿¿
(1)ΔQ=Q(吸)-Q(放)
(2)ΔQ=Q(吸)-Q(放)=反应物的总键能-生成物的总键能。
Q(吸)指反应物断键吸收的总能量,Q(放)指生成物形成化学键释放的总能量,
ΔQ表示化学反应吸收或放出能量的多少。
物质的稳定性与物质具有的能量的关系
(1)物质的能量越低越稳定,参加反应时,化学键断裂吸收的能量就越多;而如果是
通过新化学键形成而生成该物质时,放出的能量就越多。
(2)物质的能量越高越不稳定,参加反应时,化学键断裂吸收的能量就越少;该物质
化学性质活泼,而形成该物质时,放出的能量就越少。
核心知识点一:
最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的
过程。反应过程的示意图如图所示:
下列说法正确的是( )
A. CO和O生成CO 是吸热反应
2
B. 在该过程中,CO断键形成C和O
C. CO和O生成了具有极性共价键的CO
2
D. 状态Ⅰ→状态Ⅲ表示CO与O 反应的过程
2
【答案】C
【解析】C项,在该反应中,CO与O在催化剂的作用下生成了CO,而CO 中含有极
2 2
性共价键,故C项正确;A项,由图像可知,从起始状态到最终状态,总能量降低,故该
反应为放热反应,故A项错误;B项,由图可知在该过程中,CO的键并没有发生断裂,
故B项错误;D项,状态Ⅰ→状态Ⅲ表示的过程是CO与O的反应,而不是其与O 的反应,
2
第5页故D项错误。
【考点】化学键与化学反应中的能量关系
已知反应A + B = C+D的能量变化如图所示,下列说法正确的是( )
A. 铝与稀盐酸的反应符合该图示
B. 该反应为吸热反应
C. A的能量一定低于C的能量
D. 该反应只有在加热条件下才能进行
【答案】B
【解析】A. 根据图象分析,反应物的总能量低于生成物的总能量,所以反应是吸热反
应,而铝与稀盐酸的反应为放热反应,故A错误;B. 根据图象分析,反应物的总能量低于
生成物的总能量,所以反应是吸热反应,所以B选项是正确的;C. 反应物的总能量小于生
成物的总能量,但是A物质能量不一定低于C物质能量,故C错误;D. 有的吸热反应常
温下也能发生,如碳酸氢铵的分解,所以该反应常温下也能发生,故D错误;所以B选项
是正确的。
【考点】化学键与化学反应中的能量关系
核心知识点二
金刚石与石墨是碳元素的两种结构不同的单质,彼此互称同素异形体。在100 kPa时,
1 mol石墨转化为金刚石要吸收1. 895 kJ的热能。据此判断在100 kPa压强下,下列说法正
确的是( )
A. 金刚石比石墨更稳定
B. 石墨比金刚石更稳定
C. 1 mol金刚石比1 mol石墨的总能量低
D. 1 mol金刚石转变为石墨需要吸收1. 895 kJ能量
【答案】B
【解析】1 mol石墨转化为金刚石吸收1. 895 kJ的热能,说明金刚石的能量高于石墨,
石墨更稳定,A项不正确,B项正确,C项不正确;1 mol金刚石转变为石墨时要放出1.
第6页895 kJ的能量,D项不正确。
【考点】化学能与热能的转化
NF 是一种温室气体,其存储能量的能力是CO 的12 000~20 000倍,在大气中的寿
3 2
命可长达740年,如表所示是几种化学键的键能:
化学键 N≡N F—F N—F
键能(kJ·mol-1) 946 154. 8 283. 0
下列说法中正确的是( )
A. 过程N(g)―→2N(g)放出能量
2
B. 过程N(g)+3F(g)→NF (g)放出能量
3
C. 反应N(g)+3F(g)=2NF(g)为吸热反应
2 2 3
D. NF 吸收能量后如果没有化学键的断裂与生成,仍可能发生化学反应
3
【答案】B
【解析】N (g)―→2N(g)为化学键的断裂过程,应该吸收能量,A错误;N(g)
2
+3F(g)―→NF (g)为形成化学键的过程,放出能量,B正确;反应N (g)+3F
3 2 2
(g)=2NF (g)的ΔH=(946+3×154. 8-283. 0×6)kJ·mol-1=-287. 6 kJ·mol-1,ΔH
3
<0,属于放热反应,C错误;化学反应的实质是旧键的断裂和新键的形成,NF 吸收能量
3
后如果没有化学键的断裂与生成,则不能发生化学反应,D错误。
【考点】化学反应中能量变化的简单计算
(答题时间:25分钟)
一、选择题
1. 如图是化学反应中物质变化和能量变化的示意图。若 E>E ,则下列反应符合该示意
1 2
图的是( )
A. NaOH溶液与稀盐酸的反应
B. 锌与稀盐酸的反应
第7页C. 氢氧化钡与氯化铵固体的反应
D. 一氧化碳在空气中的燃烧反应
2. CH 在O 中燃烧生成CO 和气态HO的反应是一个放热反应,在反应过程中( )
4 2 2 2
A. 核能转化成热能
B. 化学能转化成热能
C. 生成物的总能量等于反应物的总能量
D. 生成物的总能量大于反应物的总能量
3. 已知反应A+B=C+D为放热反应,对该反应的下列说法中正确的是( )
A. A的能量一定高于C
B. B的能量一定高于D
C. A和B的总能量一定高于C和D的总能量
D. 该反应为放热反应,故不必加热就一定能发生
4. 已知断开1 mol H—H键吸收的能量为436 kJ,形成1 mol H—N键放出的能量为391
kJ,根据化学方程式N+3H 2NH ,反应完1 mol N 放出的能量为92. 4 kJ,则断开1
2 2 3 2
mol N≡N键需吸收的能量是( )
A. 431 kJ B. 945. 6 kJ C. 649 kJ D. 869 kJ
5. 将铁粉和硫粉混合后加热,待反应一发生即停止加热,反应仍可持续进行,直至反应
完全生成新物质硫化亚铁。这现象说明了( )
A. 该反应是吸热反应
B. 该反应是放热反应
C. 铁粉和硫粉在常温下可以发生反应
D. 硫化亚铁的总能量高于铁粉和硫粉的总能量
6. 如图表示化学反应过程中的能量变化,据图判断下列说法中合理的是( )
A. 500 mL 2. 0 mol·L-1 HCl 溶液和 500 mL 2. 0 mol·L-1 NaOH 溶液的反应符合图
(a),且放出热量为ΔE
1
B. 500 mL 2. 0 mol·L-1 HSO 溶液和500 mL 2. 0 mol·L-1 Ba(OH) 溶液的反应符合
2 4 2
图(b),且吸收热量为ΔE
2
C. 发生图(a)能量变化的任何反应,一定不需要加热即可发生
D. CaO、浓硫酸分别溶于水时的能量变化均符合图(a)
第8页7. 已知2 mol H 完全燃烧生成水蒸气放出热量484 kJ,且1 mol H—H键断裂时吸收热量
2
为436 kJ,水蒸气中1 mol H—O键形成时放出热量463 kJ,则O 中1 mol O=O键完全断
2
裂时吸收热量( )
A. 496 kJ B. 188 kJ
C. 557 kJ D. 920 kJ
二、非选择题
8. 如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入粉末状的二
氧化锰,再用胶头滴管滴入5 mL 10%的过氧化氢溶液于试管中。试回答下列问题:
(1)实验中观察到的现象_________________________________________________。
(2)产生上述现象的原因是_______________________________________________。
(3)写出反应的化学方程式_______________________________________________。
(4)由实验推知,O 和HO的总能量________(填“大于”“小于”或“等于”)
2 2
HO 的总能量。
2 2
第9页1.【答案】C
【解析】由于吸收的能量大于反应放出的能量,故反应总的能量变化为吸收能量,
A、B、D三项的三个反应为放热反应;C项反应为吸热反应,故选C项。
2.【答案】B
【解析】CH 在O 中燃烧生成CO 和气态HO的反应为放热反应,在放热反应过程中
4 2 2 2
化学能转化成热能,反应物的总能量大于生成物的总能量,B正确。
3.【答案】C
【解析】放热反应说明A和B的总能量一定高于C和D的总能量,选C项。
4.【答案】B
【解析】设断开1 mol N≡N键需吸收的能量为x,根据反应放出的能量=形成新键放
出的能量-断开旧键吸收的能量,代入数据:92. 4 kJ=6×391 kJ-3×436 kJ-x,x=945. 6
kJ。
5.【答案】B
【解析】反应发生后停止加热,反应仍可持续进行说明反应为放热反应,A错误,B
正确;反应需要加热才能发生,常温下不能进行,C错误;反应是放热反应,所以反应物
的总能量高于生成物的总能量,D错误。
6.【答案】A
【解析】图(a)表示放热反应,选项A是放热反应,A项正确;图(b)表示吸热反
应,选项B是放热反应,B项错误;一些放热反应需加热才能发生,C项错误;浓硫酸溶
于水虽然会放出热量,但不属于化学反应,D项错误。
7.【答案】A
【解析】根据反应方程式2H (g)+O (g)=2HO(g),可知2 mol H 完全燃烧生
2 2 2 2
成2 mol H O(g)放出热量484 kJ,可设1 mol O=O键完全断裂吸收的热量为Q,则ΔQ
2
=Q(吸)-Q(放)=2×436 kJ+Q-4×463 kJ=-484 kJ,解得Q=496 kJ。
8、【答案】(1)试管内有气泡冒出,烧杯内溶液变浑浊
(2)HO 分解放出O ,该反应放热,使烧杯中饱和石灰水的温度升高而析出氢氧化
2 2 2
MnO
钙晶体 (3)2HO 2 2HO+O↑ (4)小于
2 2 2 2
【解析】双氧水在二氧化锰的催化作用下分解生成氧气和水,化学方程式为 2HO
2 2
MnO
2 2HO+O↑,该反应是放热反应,所以O 和HO的总能量小于HO 的总能量;由
2 2 2 2 2 2
于Ca(OH) 的溶解度随温度的升高而降低,所以烧杯中的溶液变浑浊。
2
第10页